что делать если у человека 45 хромосом
Что делать если у человека 45 хромосом
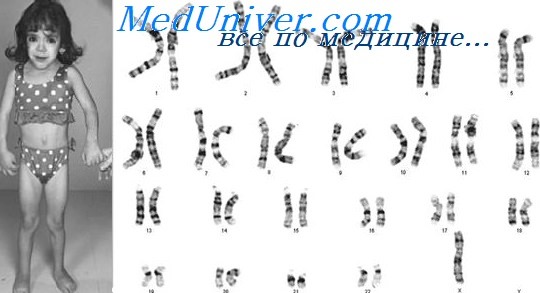
В отличие от пациентов с другими половыми хромосомными анеуплоидиями, девочек с синдромом Тернера часто идентифицируют при рождении или до половой зрелости из-за отчетливых фенотипических признаков. Синдром Тернера значительно более редкий, чем другие анеуплоидии по половым хромосомам. Встречаемость фенотипа синдрома Тернера — приблизительно 1 на 4000 новорожденных девочек, хотя в некоторых исследованиях приведены значительно более высокие цифры.
Наиболее частая хромосомная конституция при синдроме Тернера — 45,Х (иногда неправильно записываемая 45,Х0), без второй половой хромосомы. Тем не менее до 50% случаев имеет другие кариотипы. Около четверти случаев синдрома Тернера — мозаичные кариотипы, в которых только часть клеток содержит 45,Х. Наиболее частые кариотипы и их приближенные относительные частоты следующие:
1) 45,Х: 50%
2) 46,X,i(Xq): 15%
3) Мозаики 45,Х/46, XX: 15%
4) Мозаики 45,X/46,X,i (Xq): около 5%
5) 45,Х, другая аномалия X: около 5%
6) Другие мозаики 45,Х/?: около 5%
Состав хромосом клинически значим. Например, пациентки с i(Xq) подобны женщинам с классическим 45,Х, пациентки с делецией Хр имеют низкий рост и врожденные пороки развития, а с делецией Xq часто имеют только дисфункцию гонад.
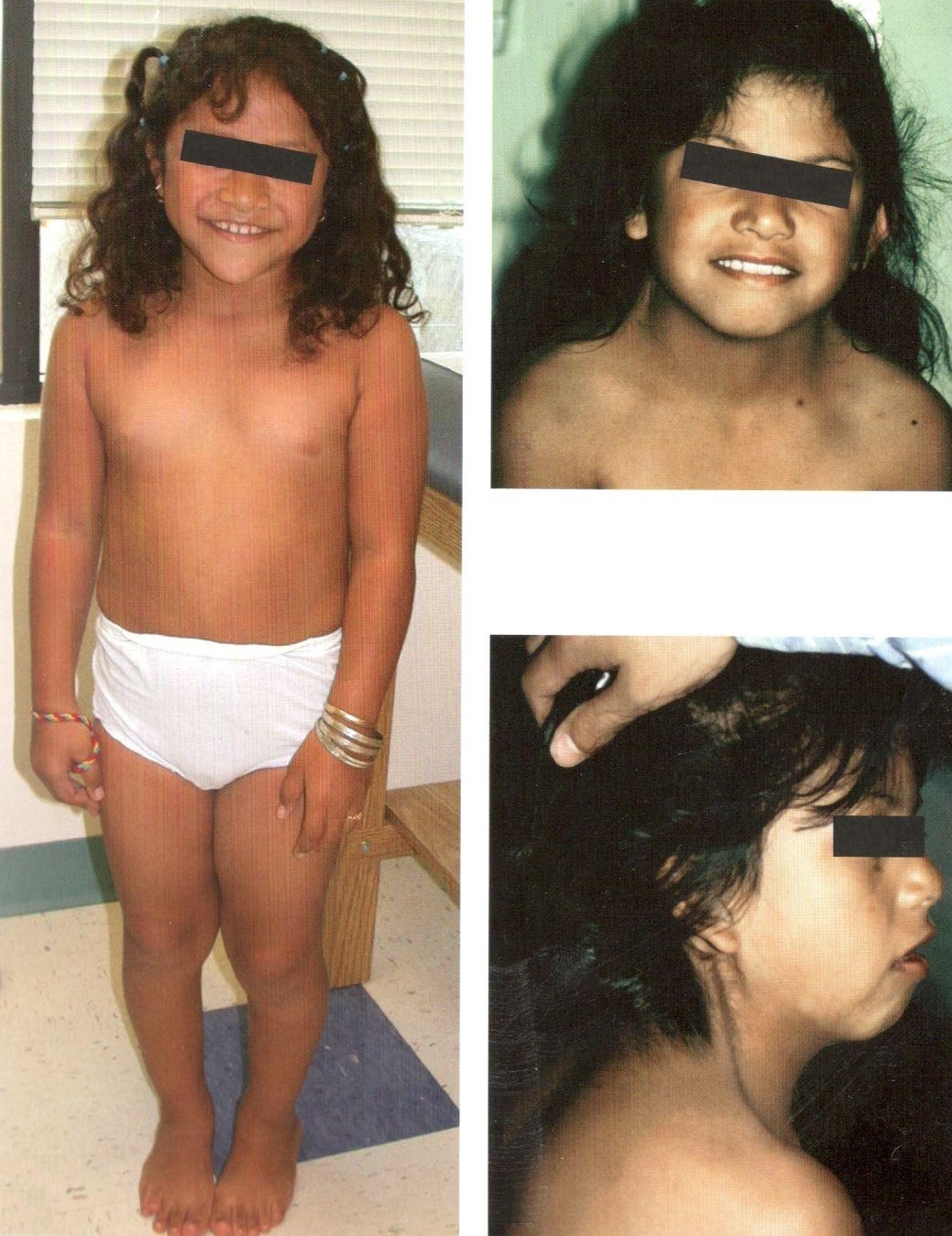
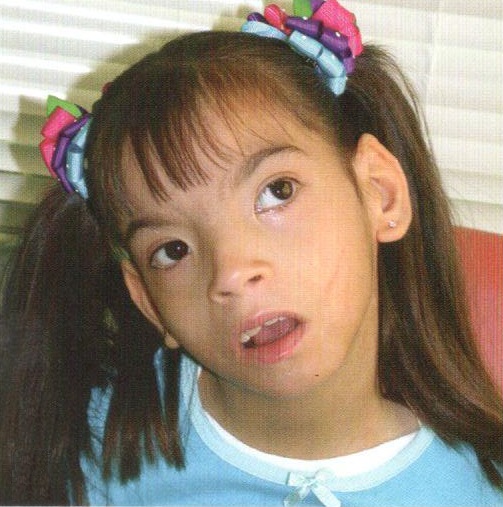
Типичные аномалии при синдроме Тернера включают низкий рост, дизгенезию гонад (в результате нарушения их формирования яичники обычно представлены соединительнотканными полосками), характерное необычное лицо, складчатую шею, низкий рост волос на затылке, широкую грудную клетку с широко расположенными сосками и высокую частоту почечных и сердечно-сосудистых аномалий.
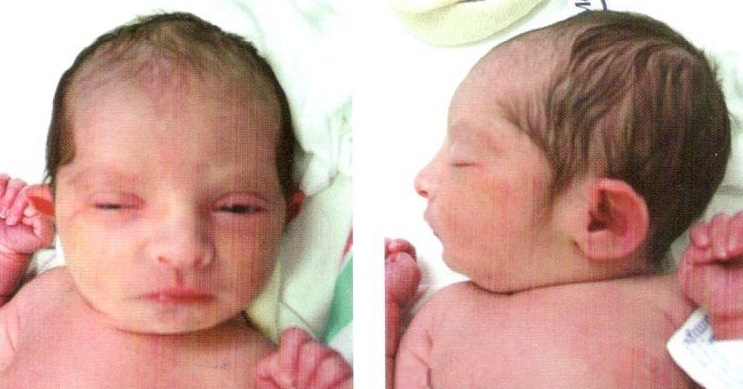
При рождении младенцы с этим синдромом часто имеют важный диагностический признак — отек тыльной стороны стоп и кистей.
У многих пациентов обнаруживают коарктацию аорты, женщины с синдромом Тернера имеют повышенный риск сердечно-сосудистых аномалий. Лимфоотек может проявляться во внутриутробном периоде, вызывая кистозную гигрому плода (обнаруживаемую при ультразвуковом исследовании — УЗИ), вызывающую видимые после родов шейные складки.
Синдром Тернера следует заподозрить у любой новорожденной девочки с отеком кистей и стоп или с гипоплазией левых отделов сердца или коарктацией аорты. Возможность этого диагноза нужно также учитывать в подростковом периоде у девушек с первичной или вторичной аменореей, особенно если они низкого роста. Терапия гормоном роста показана для всех девушек с синдромом Тернера и позволяет прибавить от 6 до 12 см роста.
Обычно считают, что интеллект у женщин с синдромом Тернера будет нормальным, хотя приблизительно 10% пациенток имеют значимую задержку развития, требующую специального образования. Даже среди тех, кто имеют нормальный интеллект, тем не менее, часто выявляют недостаточность в пространственном восприятии, двигательной и тонкой моторике.
Как следствие, невербальная оценка IQ значительно ниже вербальной, и большинство пациенток нуждается в педагогической поддержке, особенно по математике. Женщины с синдромом Тернера имеют высокий риск низкой социальной адаптации. Сравнение девушек 45,Х с материнским и отцовским происхождением Х-хромосомы показало значительно худшие социальные навыки при материнской Х-хромосоме. Поскольку эффект родительского происхождения может объясняться импринтингом, такую возможность исследуют для генов Х-хромосомы, которые влияют на фенотип.
Высокая встречаемость кариотипа 45,Х при спонтанных абортах уже упоминалась. Аномалия присутствует предположительно в 1-2% всех зачатий; выживание до срока родов — редкое явление, и более чем 99% таких беременностей спонтанно прерывается. Единственная Х-хромосома примерно в 70% случаев имеет материнское происхождение; другими словами, хромосомная ошибка, ведущая к потере половой хромосомы, обычно происходит у отца.
Основа для необыкновенно высокой частоты утраты Х- или Y-хромосомы неизвестна. Кроме того, неясно, почему кариотип 45,Х, столь часто летальный внутриутробно, очевидно полностью совместим с жизнью после родов. Утраченные гены, ответственные за фенотип синдрома Тернера, должны находиться как в Х-, так и Y-хромосоме. Предполагают, что эти гены входят в число генов, избегающих Х-инактивации, в частности, находящихся на коротком плече, включая псевдоаутосомную область.
Иногда у пациентов с низким ростом, дизгенезией гонад и умственной отсталостью выявляют небольшие кольцевые Х-хромосомы. Поскольку задержка умственного развития нетипична для синдрома Тернера, наличие такой задержки с другими аномалиями у больных с кариотипом 46,Х,r(Х) связывают с тем, что небольшие кольцевые Х-хромосомы утрачивают центр Х-инактивации.
Невозможность инактивировать кольцевую Х-хромосому приводит к избыточной экспрессии генов, в норме подлежащих инактивации. Обнаружение кольцевой Х-хромосомы при пренатальной диагностике может вести к большой неопределенности, в таком случае показано исследование экспрессии гена XIST. Большие кольца, содержащие центр Х-инактивации и экспрессирующие ген XIST, приводят к развитию фенотипа синдрома Тернера; при небольших кольцевых хромосомах без экспрессии гена XIST можно предполагать более серьезный фенотип.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Хромосомные нарушения
Хромосомные нарушения — это клинические синдромокомплексы, в основе которых лежат нарушения числа или структуры хромосом, то есть избыток или нехватка генетического материала, локализованного в той или иной хромосоме.
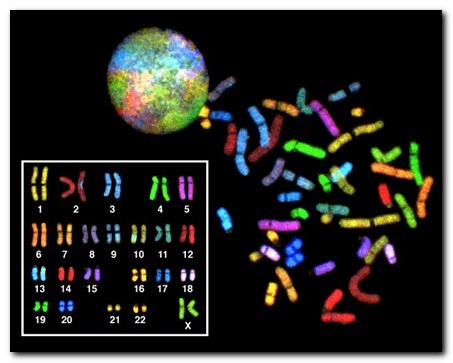
В норме у человека число хромосом равно 46, из которых 23 ребенок получает от матери и 23 аналогичные хромосомы от отца. В этом наборе гентического материала есть 2 особые хромосомы, которые были названы «половыми». Они определяют пол ребенка и ряд других важных признаков.
Таким образом, изменения числа хромосом (больше или меньше 46), а также изменение структуры хромосом (например, выпадение или удвоение даже небольшого кусочка хромосомы) получили название «хромосомные мутации».
Наиболее часто из них встречаются изменения модального числа хромосом — это отсутствие в хромосомном наборе какой-либо хромосомы (моносомия) или появление добавочной хромосомы (трисомия, тетрасомия и т.д.).
Число возможных изменений структуры хромосомы неисчислимое множество. К примеру, транслокации (обмен сегментами между разными хромосомами), делеции (выпадение участка хромосомы), дупликации (удвоение части хромосомы), инверсии (переворот сегмента хромосомы на 180 градусов) и т.д.
Хромосомные мутации, возникшие в половых клетках (сперматозоидах или яйцеклетках) или на первых этапах деления клеток зародыша, как правило, передаются большинству клеток развивающегося организма, вызывая множественные аномалии развития, а многие хромосомные изменения плода могут стать причиной спонтанных абортов и выкидышей, что важно учитывать в семьях, воспитывающих детей с задержками развития.
К факторам риска, способствующим их возникновению, относят ионизирующую радиацию, инфекции и интоксикации матери, эндокринные нарушения, психические травмы, воздействие ряда лекарственных препаратов и некоторых физиотерапевтических методов лечения.
Наиболее точно установлено, что причиной появления ребенка с хромосомными мутациями является не молодой возраст матерей (свыше 40 лет).
В последнее время очень большое значение придается факту скрытого носительства хромосомных нарушений у родителей родившегося ребенка (сбалансированные транслокации, мозаицизм). Изучение данного вопроса позволяет предотвратить риск повторного рождения ребенка с аналогичной формой заболевания.
Различают хромосомные синдромы, обусловленные изменением половых хромосом, и синдромы, вызванные аномалиями аутосом (любой из 44 неполовых хромосом).
Основными клиническими проявлениями аутосомных аномалий являются признаки психического и физического недоразвития, дисплазии (неправильное развитие), врожденные пороки развития (аномалии) и умственная отсталость различной степени тяжести. К врожденным порокам можно отнести: аномалии развития сердца, удвоение почки, расщелина неба, особенности строения кистей и стоп и многие другие. При заболеваниях, обусловленных нарушениями в системе половых хромосом, как правило, более характерны недоразвитие половых желез и аномалии развития вторичных половых признаков, также с симптомами задержки психо-речевого развития.
Различные хромосомные синдромы встречаются с разной частотой. По сводным данным многих исследований, распространенность наиболее частых из них среди новорожденных следующая:
трисомия по 21 хромосоме (синдром Дауна) 1:500
XXX (трисомия-Х) 1:1000 (девочек)
ХYY (синдром дубль-Y) 1:1000 (мальчиков)
ХХY (синдром Клайнфелтера) 1:1400 (мальчиков)
Х0 (синдром Шерешевского-Тернера) 1:3300 (девочек)
46,5р del (синдром «кошачьего крика») 1:4000
трисомия по 18 хромосоме (синдром Эдвардса) 1: 6800
трисомия по 13 хромосоме (синдром Патау) 1:7600
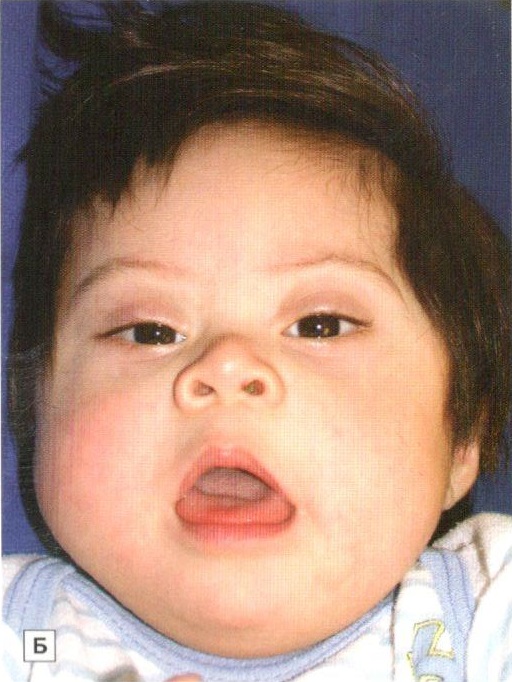
Установлено, что для синдрома Дауна характерно уменьшение размеров и веса головного мозга, а также аномалии развития мозга и мозговых сосудов. Отмечаются также структурные изменения в железах внутренней секреции, печени и сердце. Клиническая картина синдрома Дауна характеризуется проявлениями симптомов умственной отсталости. Характерен также и внешний вид таких больных: косо расположенные глазные щели, широкая уплощенная переносица, дополнительная кожная складка у внутреннего угла глаз, высокое стояние твердого неба (признаки эмбриональной задержки в развитии лицевого скелета), полуоткрытый рот, увеличенный высунутый язык с выраженными сосочками и глубокими бороздами (признаки дисфункции щитовидной железы), выпадение волос (дисфункция надпочечников), низкий рост, короткая шея, укороченные кисти и стопы, искривление мизинца, на ладонях имеется поперечная складка, на стопах увеличен промежуток между 1 и 2 пальцами, выражены внешние проявления гипогенитализма.
В клинической картине заболевания доминируют симптомы неврологической патологии, диффузная мышечная гипотония (снижение мышечного тонуса), благодаря чему больные гибки и иногда могут складываться как «перочинный ножик», расстройства координации движений, косоглазие, выраженные вегетососудистые нарушения.
Особенностью психического дефекта является относительная сохранность эмоциональной сферы по сравнению с тяжестью интеллектуального недоразвития. Так, больные ласковы, добродушны, послушны. Характерной особенностью таких детей является повышенная внушаемость, что является положительным фактором при проведении коррекционной работы и отрицательным при их развитии.
Уровень социального развития больных с синдромом Дауна зависит от степени и формы заболевания. Так, дети с более легкими формами умственной отсталости, хотя и медленно, но развиваютя, приобретая определенные навыки, знания, осваивая программу нескольких классов вспомогательной школы. Однако, как правило, большинство из них не достигают удовлетворительного уровня социальной адаптации и нуждаются в постоянной опеке. Им может быть оформлена инвалидность детства с момента точной диагностики заболевания. Особенностью возрастной динамики синдрома Дауна является позднее половое созревание и раннее появление признаков инволюции (25—30 лет). Мужчины с синдромом Дауна бесплодны, женщины могут давать потомство, половина которого также страдает синдромом Дауна.
Впервые заболевание описано отечественным эндокринологом Н.А. Шерешевским (1925), а более подробно — американским эндокринологом Н. Тернером (N.H. Terner) л 1938 г. В основе заболевания лежит отсутствие одной хромосомы (половой Х-хромосомы) (45 вместо 46).
Клиническая картина синдрома характеризуется разной степенью умственной отсталости и ЗПРР, низким конечным ростом (135—145 см), замедлением полового развития, недоразвитием половых желез, аменореей, бесплодием и отсутствием грудных желез. Диспластические расстройства проявляются в виде короткой шеи и особых кожных складок, идущих от затылка к надплечью, укорочением 4 пальцев на руках и искривлением мизинцев, выраженной деформацией ушных раковин, наличием множественных пигментных родинок. Преимущественно данным синдромом страдают лица женского пола.
Клинические проявления синдрома Клайнфельтера варьируют от внешне нормального и интеллектуального развития до выраженного евнухоидизма и умеренной умственной отсталости. Однако в ряде случаев уже в раннем возрасте у больных отмечаются характерные своеобразные симптомы физического развития: низкий и узкий лоб, густые и жесткие волосы, высокое стояние таза, короткая, плоская и узкая грудная клетка, недоразвитие половых органов. Более отчетливо вышеперечисленные симптомы начинают обнаруживаться в подростковом, пубертатном возрасте. Характерен внешний вид взрослого больного с синдромом Клайнфельтера: высокий рост, астеническое сложение, узкие плечи, широкий таз, удлиненные конечности, слаборазвитая мускулатура, скудная растительность на лице и в подмышечных впадинах, ожирение и оволосение по женскому типу, сутулость, выраженные евнухоидные пропорции и гинекомастия (набухание грудных желез). Постоянными признаками синдрома Клайнфельтера являются недоразвитие половых органов и бесплодие.
Степень интеллектуального недоразвития у больных выражена тем глубже, чем больше дополнительных половых хромосом обнаруживается в кариотипе (46 или 49). Так, умеренная умственная отсталость зачастую приближается к психическому инфантилизму, что клинически проявляется недостаточностью внимания, восприятия, памяти, абстрактного мышления, чрезмерной внушаемостью, подражательностью, подчиняемостью, несамостоятельностью, чрезмерной привязанностью к близким, нередко с элементом назойливости. Глубокая незрелость эмоционально-волевой сферы проявляется в виде повышенного настроения, с эйфорическим оттенком, склонностью к эксплозивным аффективным вспышкам, неспособностью к длительному волевому усилию и напряженной деятельности. У больных, как правило, отсутствуют чувство долга и ответственности. При легких формах заболевания больные осознают свою неполноценность, что приводит к внутреннему конфликту и возникновению у них невротических реакций. Данным синдромом страдают лица мужского пола.
Синдром ломкой Х-хромосомы (Fragile X syndrome, FraХ). Начиная с 1980 года большое значение придают синдрому ломкой Х-хромосомы (Хq27.3) – именно с ним связывают развитие более чем 50 наследственных расстройств, включая ранний детский аутизм и 30% случаев умственной отсталости у мальчиков. Хрупкий участок Х-хромосомы впервые обнаружил Labs (1969).
Полная мутация в Х-хромосоме возникает только у женщин, и происходит это в процессе гаметогенеза, поэтому почти всегда страдают мальчики, получившие единственную Х-хромосому от матери. У девочек, получивших вторую Х-хромосому от отца, также могут быть нарушения развития, но они менее выражены, а тяжелые патологии встречаются много реже, чем у мальчиков. В отдельных случаях девочки могут получить обе ломкие хромосомы от матери, в этом случае частота и тяжесть патологии будет одинаковой с мальчиками.
Клиническую триаду синдрома ломкой Х-хромосомы образуют:
1) умеренная до степени тяжелой умственная отсталость. Лишь 30% лиц мужского пола имеют интеллект, стремящийся к нижней границе нормы, а среди женщин – носительниц такой хромосомной патологии примерно у 30% обнаруживаются признаки умственного недоразвития;
2) характерные особенности строения лица и черепа: выдающийся вперед высокий лоб, прогнатизм и удлиненные уши;
3) мальчики имеют увеличенные в размерах тестикулы (макроорхидизм).
Наблюдаются, кроме того, эпилептические припадки, синдром гиперактивности с дефицитом внимания, у более чем половины мальчиков аутизм и подобные аутизму расстройства, различные нарушения развития речи, персеверации, эхолалия, другие отклонения.
Женщины, унаследовавшие ломкую Х-хромосому с полной мутацией от своих матерей, могут быть склонны к развитию атипической депрессии, а также шизофреноподобного заболевания.
Синдром Вольфа—Хиршхорна.
В основе синдрома лежит изменение длины хромосомы из четвертой пары. Основные признаки заболевания у новорожденных: большое туловище, клювовидный нос и выступающее надпереносье, деформированные ушные раковины со складками, пучеглазие и колобома радужной оболочки (ее частичное отсутствие), общее недоразвитие во время беременности. Отмечается наличие четырех сгибательных складок на пальцах верхних конечностей.
Клиническая картина характеризуется микроцефалией, расщелиной лица, двусторонним расщеплением верхней губы, полным расщеплением неба, маленькими глазными яблоками либо полным их отсутствием, короткой шеей, маленькими деформированными низко расположенными ушами, полидактилией, дистрофическими изменениями ногтей и костного скелета. Отмечаются также пороки развития сердца, желудка, кишечника и других органов.
Синдром трисомии-Х впервые описан в 1959 г. Частота данной патологии составляет среди новорожденных 0,1%, а среди умственно отсталых — 0,6%. Большинство лиц женского пола с трисомией-Х выявляется среди больных психиатрических лечебниц. Клиническая картина характеризуется аномалиями развития скелета, внутренних органов, различными психическими проявлениями и интеллектуальной недостаточностью. Среди полиморфизма признаков трисомии-Х наиболее характерными являются: низкий рост, аномалии ушей, прикуса, высокое стояние твердого неба, короткие пальцы, искривленный мизинец, широкий промежуток между 1 и 2 пальцами на стопах, синдактилия, недоразвитие половых функций.
Умственная отсталость проявляется в виде легкой или умеренной степени. Характерны эмоциональные расстройства (вспыльчивость, агрессивность, неустойчивость настроения и немотивированные поступки). Девочки с синдромом трисомии-Х с трудом, но в большинстве случаев (легкая степень умственной отсталости) обучаются в массовых школах.
К хромосомным синдромам, помимо вышеописанных, относится большая группа так называемых семейных форм умственной отсталости, когда совершенно точно доказано наличие данной патологии у близких родственников.
Синдром Аперта (акроцефалосиндактилия) — наследственное заболевание, характеризующееся умеренной или тяжелой умственной отсталостью, экзофтальмом, деформацией зубов и синдактилиями. Синдром описан французским педиатром Апертом (Е. Apert) в 1906 г.
Синдром Крузона — наследственное заболевание, характеризующееся умеренной или тяжелой умственной отсталостью, преждевременным срастанием швов черепа, уменьшением мозгового вещества, экзофтальмом, вторичной атрофией зрительных нервов, прямоугольным расположением большого пальца к кисти. Впервые синдром описан французским врачом Крузоном (О. Crouson) в 1912 г.
Синдром Берьесона—Форсмана—Лемана — синдром характеризующийся умственной отсталостью в сочетании с избыточным весом. Впервые описан американскими врачами Берьесоном (М. Berjeson) Форсманом (Н. Foreman) и Леманом (О. Lehman) в 1963 г. Клиническая картина заболевания проявляется выраженным ожирением и прогрессирующей умственной отсталостью. Ожирение носит не равномерный характер. Жир откладывается преимущественно на бедрах, груди и лице, что придает своеобразный вид такому больному (бочкообразная карликовая фигура с заплывшим лицом, большими ушами и узкими разрезами глаз). У больных часто отмечаются эпилептические припадки. Умственная отсталость колеблется от умеренной до тяжелой степени. Данная патология встречается только у лиц мужского пола, но носителями патологического гена являются женщины.
Синдром Прадера—Вилли — наследственное заболевание, характеризующееся глубокой умственной отсталостью, низким ростом, гипогенитализмом, ожирением, резко выраженной мышечной гипотонией.
Синдром Книппеля—Фейля (синдром короткой шеи) — наследственное семейное заболевание, обусловленное врожденными аномалиями развития скелета и внутренних органов в сочетании с тяжелой степенью умственной отсталости. Клиника синдрома подробно описана французскими врачами Клиппелем Фейлем в 1912 г.
Аномалия развития характеризуется следующими проявлениями: короткой шеей как результат количественного уменьшения шейных позвонков, ограничением подвижности головы, расщеплением твердого неба, бочкообразной грудной клеткой, врожденными пороками сердца, добавочными долями или отсутствием отдельных долей легких, синдактилиями (сращение пальцев конечностей), глухотой вследствие заращения наружных слуховых проходов, сужением анального отверстия и многими другими симптомами. Интеллектуальная недостаточность является результатом тяжелой умственной отсталости
Лечение ЗПРР при хромосомных заболеваниях.
Исследования последних десятилетий выявили, что у большинства детей с речевыми и поведенческими проблемами в различной степени нарушены функции мозжечка и базальных ганглиев. Именно функционирование мозжечка определяет успешность ребенка в обучении. С этой целью применяется уникальная разработка Центра авиакосмической медицины — подошвенный имитатор опорной нагрузки «Корвит», применяемый для нейрофизиологической регуляции стато-кинетической функции ЦНС. В основе терапевтического воздействия аппарата «Корвит» лежит процесс активации опорной афферентации, отвечающей за нормализацию процессов возбуждения и торможения в центральной нервной системе, что приводит к уменьшению спастичности мышц, развитию и закреплению функциональных связей в головном мозге, способствующих восстановлению координации движений, и, опосредованно, улучшению речи и мышления.
Обязательным звеном в лечебном комплексе у детей с наличием речевых расстройств является занятия с клиническим психологом, а также логопедическая коррекция, которая включает диагностику степени нарушений, ежедневные занятия, направленные на улучшение речевой функции и логопедический массаж для коррекции различных видов дизартрии и дисфагии.
На фоне сочетания проведения биофизической активации со вспомогательными методиками лечения наблюдаются положительные изменения, которые могут быть видны уже через несколько процедур, но максимальный эффект развивается через полтора-три месяца после курса. Как правило, для закрепления полученных результатов и дальнейшего развития двигательных и когнитивных навыков специалистами центра рекомендуется повторный курс лечения через 5-6 месяцев.
Причины генетического бесплодия
Согласно оценкам экспертов Всемирной организации здравоохранения, около 50 миллионов супружеских пар во всем мире (что составляет примерно 7% от их общего количества) не могут завести ребенка из-за мужского и/или женского бесплодия. На данный момент считается, что в 50% случаев причиной являются генетические нарушения.
Современная наука достигла больших успехов в изучении причин генетического бесплодия, особенно с появлением метода секвенирования нового поколения (next generation sequencing, NGS), позволяющего быстро и с минимальными трудозатратами «читать» последовательность ДНК. Тем не менее, этот вопрос остается сложным, и в имеющихся на данный момент знаниях остается еще немало пробелов.
Существует множество генов, влияющих на мужскую и женскую репродуктивную функцию. Например, в одних только яичках мужчины экспрессируется около 2300 генов. Наука продолжает развиваться, и список доступных анализов ежегодно пополняется новыми генетическими тестами.
Генетические изменения, способные приводить к невозможности зачатия и вынашивания беременности, бывают разными:
Хромосомные аномалии
Хромосомные нарушения представляют большой интерес в аспекте вопросов бесплодия, так как они ответственны более чем за половину всех выкидышей в первом триместре беременности. В большинстве случаев хромосомные аномалии не наследуются – они возникают случайно в половых клетках или клетках эмбриона. При этом происходят выкидыш, мертворождение, либо ребенок рождается с серьезными пороками развития.
В каждой клетке человеческого тела содержится 46 хромосом. В яйцеклетке и сперматозоиде их по 23 – соответственно, ребенок получает половину набора от матери и половину от отца. Состояние, при котором меняется количество хромосом, называется анеуплоидией. Некоторые примеры, связанные с бесплодием:
Помимо изменений количества хромосом, встречаются нарушения их структуры – аберрации.
Их основные разновидности:
Моногенные заболевания
Моногенные заболевания характеризуются возникновением мутации в одном гене, отвечающем за синтез определенного белка. Эти патологии передаются от родителей детям, причем типы наследования бывают разными.
В настоящее время известно много моногенных мутаций, связанных с бесплодием. Их список постоянно пополняется.
Мультифакториальные заболевания
Мультифакториальные, или полигенные заболевания имеют сложный патогенез. В их развитии принимают участие генетические нарушения (как наследственные, так и приобретенные), образ жизни, воздействия внешней среды. На «неправильные» гены накладываются такие факторы, как особенности питания, уровень физической активности, экологическая обстановка, вредные привычки, стрессы, прием различных лекарственных препаратов и пр.
Типичные примеры мультифакториальных заболеваний – сахарный диабет и сердечно-сосудистые патологии. Среди причин женского бесплодия важное значение имеют следующие заболевания:
Эпигенетические изменения
Эпигенетические изменения возникают в результате различных процессов, когда последовательность ДНК остается нормальной, но меняется активность генов. Например, это происходит в результате метилирования – прикрепления особых метильных групп к определенным участкам ДНК. Некоторые научные исследования показали, что эпигенетические механизмы играют роль в развитии бесплодия.
В каких случаях рекомендуется пройти генетическое тестирование?
Обычно врачи направляют пациентов на консультации к клиническим генетикам в следующих случаях:
Генетик собирает семейный анамнез, анализирует родословную и при необходимости назначает анализы. Для диагностики причин генетического бесплодия применяют разные методы: цитогенетический анализ, полимеразную цепную реакцию (ПЦР), флуоресцентную гибридизацию in situ (FISH), микрочипирование, секвенирование нового поколения.
Чтобы выявить распространенные аномалии у плода, на 16–20-й неделях беременности проводят тройной тест. По показаниям выполняют различные инвазивные исследования. Более современный и точный метод диагностики – неинвазивное пренатальное тестирование (НИПТ), во время которого изучают ДНК плода в крови матери.
Если у одного или обоих партнеров из пары, страдающей бесплодием, выявляют генетические нарушения, в ряде случаев могут помочь различные методы лечения или вспомогательные репродуктивные технологии (ЭКО, ИКСИ). Но иногда проблему не удается решить. В таких ситуациях врач предложит рассмотреть возможность использования донорских яйцеклеток или сперматозоидов.
С возрастом репродуктивные возможности уменьшаются, а в клетках накапливаются мутации, которые могут помешать наступлению и вынашиванию беременности, вызвать тяжелые патологии у ребенка. Поэтому женщинам, которые планируют забеременеть после 35 лет, стоит подумать о возможности сохранить свои яйцеклетки в криобанке. В дальнейшем ими можно воспользоваться в любое время – это будет своего рода «страховка» репродуктивной функции.
Если вы решили сохранить собственные половые клетки или воспользоваться донорскими, важно подобрать надежный банк половых клеток. На данный момент Репробанк является одним из крупнейших на территории России и СНГ. Наше криохранилище оснащено новейшим оборудованием, а в каталоге представлено большое количество доноров, среди которых любая пара наверняка сможет подобрать подходящего.
Зиновьева Юлия Михайловна
Ведёт генетическое обследование доноров Репробанка, осуществляет подбор доноров для пар, имеющих ранее рождённых детей с установленной генетической патологией.