что такое стирол в химии
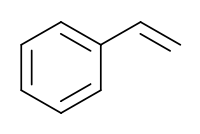
Стирол
| Стирол | |
 | |
 | |
| Общие | |
|---|---|
| Химическая формула | C8H8 |
| Физические свойства | |
| Молярная масса | 104.15 г/моль |
| Плотность | 0.909 г/см³ |
| Термические свойства | |
| Температура плавления | -30 °C |
| Температура кипения | 145 °C |
| Классификация | |
| Рег. номер CAS | 100-42-5 |
| SMILES | c1ccccc1C=C |
Стиро́л C8H8 (фенилэтилен, винилбензол, этиленбензол) — бесцветная жидкость со специфическим запахом. Стирол практически нерастворим в воде, хорошо растворим в органических растворителях, хороший растворитель полимеров. Стирол относится ко второму классу опасности.
Содержание
Получение
Большую часть стирола (около 85 %) в промышленности получают дегидрированием этилбензола при температуре 600—650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3 — 10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздухом.
Разрабатываются альтернативные способы получения стирола. Каталитическая циклодимеризация бутадиена в винилциклогексен, с его последующим дегидрированием. Окислительное сочетание толуола с образованием стильбена; метатезис стильбена с этиленом приводит к стиролу. Взаимодействием толуола с метанолом также может быть получен стирол. Кроме того, активно разрабатывались способы выделения стирола из жидких продуктов пиролиза. На сегодняшний день, ни один из этих процессов не является экономически выгодным и в промышленном масштабе не реализован.
В лабораторных условиях может быть получен нагреванием до 320 °С полистирола с его моментальным отведением.
Свойства
Стирол легко окисляется, присоединяет галогены, полимеризуется (образуя твердую стекловидную массу — полистирол) и сополимеризуется с различными мономерами. Полимеризация происходит уже при комнатной температуре (иногда со взрывом), поэтому при хранении стирол стабилизируют антиоксидантами (например, третбутилпирокатехином, гидрохиноном). Галогенирование, например, в реакции с бромом, в отличие от анилина идёт не по бензольному кольцу, а по виниловой группе с образованием 1,2-дибромэтилфенила.
Применение
Стирол применяют почти исключительно для производства полимеров. Многочисленные виды полимеров на основе стирола включают полистирол, пенопласт (вспененный полистирол), модифицированные стиролом полиэфиры, пластики АБС (акрилонитрил-бутадиен-стирол) и САН (стирол-акрилонитрил). Также стирол входит в состав напалма.
Токсичность
Средняя летальная доза составляет около 500-5000 мг/м³ (для крыс). Стирол относится ко второму классу опасности.
Литература
Примечания
Полезное
Смотреть что такое «Стирол» в других словарях:
СТИРОЛ — СТИРОЛ, стирола, мн. нет, муж. (от стиракс) (хим., тех.). 1. Жидкое ароматическое вещество желтоватого цвета, добываемое из смолы некоторых тропических деревьев и употр. в парфюмерном и мыловаренном производстве. 2. Небьющаяся пластическая масса … Толковый словарь Ушакова
стирол — сущ., кол во синонимов: 3 • винилбензол (2) • углеводород (77) • церин (2) … Словарь синонимов
СТИРОЛ — (винилбензол C6H5CH = CH2) бесцветная жидкость, легко полимеризуется. Получают дегидрированием этилбензола. Применяют для синтеза полистирола, бутадиен стирольных каучуков, ионообменных смол и как компонент полиэфирных смол. См. также… … Российская энциклопедия по охране труда
Стирол — фенилэтилен, винилбензол, бесцветная жидкость со специфическим запахом; tпл 30,6 °С, tкип145,2 °С, плотность 0,906 г/см3 (20 °С); практически нерастворима в воде, смешивается с большинством органических растворителей. С. легко окисляется … Большая советская энциклопедия
стирол — а; м. Бесцветная ароматическая жидкость со сладковатым запахом, содержащаяся в смоле некоторых тропических деревьев или получаемая синтетическим путём в промышленности (используется в основном для получения синтетических полимеров). ◁ Стироловый … Энциклопедический словарь
стирол — (стиракс + лат. ol(eum) масло) органическое соединение, углеводород ароматического ряда; бесцветная жидкость со сладковатым запахом; содержится в растительной смоле стиракс, в каменноугольной смоле, сланцевом масле и т. д.; в промышленности… … Словарь иностранных слов русского языка
стирол — stirenas statusas T sritis chemija formulė C₆H₅CH=CH₂ atitikmenys: angl. styrene; vinylbenzene rus. винилбензол; стирол ryšiai: sinonimas – vinilbenzenas sinonimas – feniletenas … Chemijos terminų aiškinamasis žodynas
Стирол — см. Углеводороды ароматические … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Что такое стирол в химии
Стирол (фенилэтилен, винилбензол) — бесцветная жидкость со специфическим запахом; практически нерастворима в воде, хорошо растворима в органических растворителях, хороший растворитель полимеров.
Стирол легко окисляется, присоединяет галогены, полимеризуется (образуя твердую стекловидную массу — полистирол) и сополимеризуется с различными мономерами. Полимеризация происходит уже при комнатной температуре (иногда со взрывом), поэтому при хранении стирол стабилизируют антиоксидантами (например, третбутилпирокатехином, гидрохиноном).
Опасность стирола для человека.
Вдыхание паров стирола грозит многочисленными острыми и хроническими заболеваниями. Это вещество отрицательно влияет на функцию печени и почек, на кровеносную и нервную системы. Длительное попадание стирола в организм человека грозит катарами дыхательных путей, раздражением кожи и слизистых оболочек, изменением состава крови, нарушениями функций вегетативной системы.
На предприятиях и в лабораториях, где производится работа со стиролом, меры безопасности предписывают обязательное использование резиновых перчаток, а в случаях особенно высокой концентрации ядовитых паров в воздухе – применение противогазов.
ПДК (Предельно-допустимая концентрация).
ПДК рабочей зоны = 30 мг/м³
ПДК среднесменная в рабочей зоне = 10 мг/м³
ПДК максимально разовая = 0,04 мг/м³
ПДК средне-суточная = 0,002 мг/м³
ПДК водных объектов = 0,02 мг/л
Токсикология.
Средняя летальная доза составляет около 500-5000 мг/м³ (для крыс). Стирол относится ко второму классу опасности.
Получение.
Большую часть стирола (около 85 %) в промышленности получают дегидрированием этилбензола при температуре 600—650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3 — 10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздухом.
другие статьи
Вентиляционные системы в медицинских учреждениях
Очистка воздуха от городского смога
Проектирование лечебно-профилактических учреждений
Стирол
Стирол представляет собой прозрачную жидкость.
Стирол практически нерастворим в воде, но хорошо растворим в органических растворителях, хороший растворитель полимеров.
Стирол относится ко 2-му классу опасности.
При хронической интоксикации поражаются центральная и периферическая нервная система, система кроветворения, пищеварительный тракт, нарушается азотисто-белковый, холестериновый и липидный обмен, у женщин происходят нарушения репродуктивной функции.
Стирол проникает в организм в основном ингаляционным путем.
При попадании на слизистые оболочки носа, глаз и глотки паров и аэрозоля стирол вызывает их раздражение.
Большую часть стирола (около 85%) в промышленности получают дегидрированием этилбензола при температуре 600-650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3-10 раз.
Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15%, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола.
Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздухом.
Разрабатываются альтернативные способы получения стирола.
Каталитическая циклодимеризация бутадиена в винилциклогексен, с его последующим дегидрированием.
Окислительное сочетание толуола с образованием стильбена; метатезис стильбена с этиленом приводит к стиролу; взаимодействие толуола с метанолом, выделение стирола из жидких продуктов пиролиза.
Ни один из этих процессов пока не является экономически выгодным.
В лабораторных условиях может быть получен нагреванием до 320 °С полистирола с его моментальным отведением.
Стирол легко окисляется, присоединяет галогены, полимеризуется,образуя полистирол, и сополимеризуется с различными мономерами.
Полимеризация происходит уже при комнатной температуре (иногда со взрывом), поэтому при хранении стирол стабилизируют антиоксидантами (например, третбутилпирокатехином, гидрохиноном).
Галогенирование, в реакции с бромом, в отличие от анилина идет не по бензольному кольцу, а по виниловой группе с образованием 1,2-дибромэтилфенила.
Применение стирола
Стирол применяют для производства разнообразных материалов:
Что такое стирол? состав, свойства, применение
Стирол в основном используется для производства термопластичного полимера под названием полистирол, а также ряда других пластмасс и синтетических каучуков. Этот легкий и недорогой материал обеспечивает высококачественный внешний вид, который можно разрезать на любую форму.
Профиль стирола
Стирол является членом углеводородной винильной группы (CH2=CH-), молекулы которой состоят из двойной связи между двумя атомами углерода.
Под действием инициаторов и катализаторов эта двойная связь может расщепляться на две одинарные связи, связывающие атом углерода другой молекулы стирола. Так образуется полистирол, в котором тысячи соединений стирола прикреплены вдоль углеродной основы.
Физические и химические свойства
Стирол представляет собой бесцветную маслянистую жидкость, которая легко испаряется. Старый образец может выглядеть слегка желтоватым. Хотя он имеет сладковатый запах, другие химические вещества могут придать ему резкий, неприятный привкус.
Хотя стирол плохо растворяется в воде, он хорошо растворяется в этаноле, эфире и ацетоне и слабо растворяется в четыреххлористом углероде. Также он образует однородную смесь с бензолом.
Стирол менее плотен, чем вода, но его пары тяжелее воздуха и раздражают глаза. Если он полимеризуется в закрытом контейнере, контейнер может разорваться на части.
Вязкость: 0,696 сП при 25 °C
Полимеризация: Постепенно при комнатной температуре и легко при температуре выше 65 °C.
Полимеризация также может происходить из-за присутствия пероксидов, окислителей или солнечного света. Чтобы предотвратить это, стирол обычно смешивают с ингибиторами. Однако это не препятствует стиролу разъедать медь и медные сплавы.
Как производится стирол?
Натуральный стирол содержится (в очень небольших количествах) в некоторых продуктах и растениях, таких как кофейные зерна, арахис, корица и бальзамические деревья. Он также содержится в каменноугольной смоле.
В настоящее время для производства стирола из этилбензола используются два процесса:
1. Дегидрирование этилбензола.
Около 75% стирола получают путем удаления водорода из этилбензола (C 6 H 5 CH 2 CH). Этот процесс включает нагревание этилбензола до 600 °C в присутствии катализатора, которым обычно является оксид железа (III).
Реакция поглощает значительное количество тепла (из внешней среды) и является обратимой. При этом выделяется 88-94% стирола, который затем очищается путем дистилляции.
Поскольку во время процесса стирол может подвергаться термической полимеризации, в систему постоянно добавляют ингибитор.
2. Обработка этилбензола кислородом
Реакция между этилбензолом и кислородом дает гидропероксид этилбензола. Затем этот продукт обрабатывают пропиленом для получения оксида пропилена и 1-фенилэтанола. Наконец, дегидратация 1-фенилэтанола дает стирол.
Более дешевая альтернатива
Стирол также можно получить, используя недорогое сырье: метанол (простейший спирт) и толуол (ароматический углеводород).
Реакция между этими соединениями при 425 °C и в присутствии цеолитного катализатора дает смесь стирола и этилбензола 9:1. Выход стирола более 60%.
Из коричной кислоты
Обычное использование
Ежегодно миллиарды килограммов стирола производятся промышленным способом для изготовления таких продуктов, как пищевые контейнеры, одноразовые стаканчики, пластик, резина, трубы, стекловолокно, автомобильные компоненты и различные химикаты.
Хотя стирол в основном используется для производства полистирольных пластиков и смол, он также служит промежуточным звеном в синтезе соединений, используемых для ионообменных смол.
В частности, стирол используется для производства:
Твердый полистирол, из которого делают жесткую тару для предприятий общественного питания, кухонную технику, игрушки, медицинские и оптические инструменты.
Полимерные композиты, армированные волокном, которые используются для производства коррозионно-стойких труб и резервуаров, спортивных товаров, компонентов ветряных турбин, военных и коммерческих самолетов и автомобильных запчастей.
Пенополистирол и пленки, которые используются для изготовления контейнеров для предприятий общественного питания, легкой защитной упаковки, а также для ламинирования и печати.
Самыми популярными материалами на основе стирола являются:
Токсичность
Стирол представляет опасность при хранении при температуре выше 32 °C. При разложении (при нагревании) он выделяет едкий дым и раздражающие испарения.
Пары стирола сильно раздражают горло, нос, глаза и легкие. У работников, подвергающихся воздействию высоких уровней паров стирола, могут развиться дегенеративные заболевания нервной системы.
Длительное воздействие может привести к усталости, потере слуха, ухудшению цветового зрения, снижению концентрации, замедлению реакции и психическим проблемам. У некоторых работников наблюдались астма, аллергические кожные реакции, изменения иммунной функции и даже свертываемость крови.
Размер рынка
В 2019 году мировой рынок стирола оценивался в 48 миллиардов долларов. Прогнозируется, что к 2026 году эта цифра достигнет 70 миллиардов долларов при среднегодовом темпе роста (CAGR) в 4,6% с 2020 по 2026 год.
Однако растущие проблемы со здоровьем и окружающей средой при использовании стирола будут тормозить рост рынка. За последнее десятилетие были зарегистрированы различные промышленные аварии. Недавно, в мае 2020 года, в результате утечки газообразного стирола погибли тринадцать рабочих на заводе LG Chem в Висакхапатнаме, Индия.
Несмотря на вредные последствия, стирол будет пользоваться значительным спросом благодаря применению полистирола. Азиатские страны будут продолжать доминировать на рынке в течение прогнозного периода.
В частности, ожидается, что в Китае в ближайшие годы будет наблюдаться устойчивый рост из-за растущего спроса на упакованные товары в продовольственном сегменте.
Часто задаваемые вопросы
Как люди подвергаются воздействию стирола?
Стирол может попасть в организм человека при дыхании (в виде пара) или при прямом контакте с кожей. Население в целом может подвергаться воздействию при употреблении питьевой воды, употребления пищи, курения сигарет, вдыхания воздуха в помещении или использования потребительских товаров, содержащих стирол.
При попадании в окружающую среду стирол попадает в воздух с поверхности воды и влажной почвы. Небольшие количества стирола были обнаружены как в организмах, дышащих воздухом (морские птицы, хищники, люди), так и в организмах, дышащих водой (хищные рыбы).
Насколько опасен стирол?
Оксид стирола может быть канцерогенным как для человека, так и для животных. У животных он вызывает рак печени. Безопасного уровня воздействия этого газа не существует, поэтому любой контакт с ним должен быть сведен к минимально возможному уровню.
Как быстро стирол попадает в организм?
Во многих контролируемых исследованиях было установлено, что стирол задерживается в легких до 70% от вдыхаемой дозы. В окружающем воздухе он может абсорбироваться через кожу на уровне 4% от дозы, поглощенной в дыхательных путях. Более того, жидкий стирол может проникать через кожу со скоростью 1 мкг/м2 в минуту.
Как защитить себя от газообразного стирола?
Работники могут использовать средства защиты и следовать аварийным процедурам, чтобы обезопасить себя. Это включает обеспечение достаточной вентиляции и устранение всех источников воспламенения на предприятии.
Не допускайте скопления паров в небольших помещениях и предотвращайте любые утечки или проливы. Также необходимо избегать выброса продукта в окружающую среду.
Cтирол
История стирола
Полистирол является полностью безвредным веществом. Тем не менее, при определенных условиях из него может выделяться стирол, который давно признали слабо токсичным веществом. Как известно, большие концентрации стирола приводят к возникновению раздражения слизистых оболочек верхних дыхательных путей, головной боли, расстройства центральной и вегетативной нервной системы.
Стирол является бесцветной жидкостью со специфическим запахом. Она практически не растворяется в воде, зато отлично растворяется в органических растворителях, и является хорошим растворителем полимеров.
Данное вещество с легкостью подвергается окислению, вступает в реакции присоединения с галогенами. Кроме того, он вступает в реакции полимеризации с образованием твердой стекловидной массы — полистирола, и сополимеризации с разными мономерами. Реакция полимеризации начинается еще при комнатной температуре (часто сопровождаясь взрывом), по этой причине во время хранения стирол должен быть стабилизирован антиоксидантами (например, третбутилпирокатехином, гидрохиноном).
Вдыхать пары стирола категорически запрещено. Кроме того, данное вещество оказывает отрицательное влияние на функцию печени и почек, на кровеносную и нервную системы.
Руководство предприятий и лабораторий, в которых ведется работа со стиролом, обязано обеспечить своих сотрудников резиновыми перчатками, а при очень высоких концентрациях ядовитых паров в воздухе – противогазами.
Стирол причислен к ядам общетоксического действия. В высоких дозах он характеризуется раздражающими, мутагенными и канцерогенными свойствами, а также источает резкий и неприятный запах. Вследствие хронической интоксикации у работников возможны заболевания центральной и периферической нервной систем, а также системы кроветворения, пищеварительного тракта, происходят нарушения азотисто-белкового, холестеринового и липидного обмена. Среди женщин отмечены случаи нарушений в репродуктивной системе.
Получение стирола
Долгие годы с момента открытия стирола ученые пытались ответить на вопрос: как получить стирол в больших объемах? В результате различных экспериментов ученые нашли несколько подходящих реакций синтеза. На сегодняшний день главным промышленным методом получения стирола является каталитическое дегидрирование этилбензола в токе водяного пара при 500-630 0С. По этой схеме производство стирола выглядит следующим образом:
Еще один промышленный метод заключается в окислении этилбензола в присутствии марганцового катализатора до ацетофенона, который далее гидрируют под давлением на медно-хромово-железном катализаторе до метилфенилкарбинола, с последующим дегидрированием на окиси алюминия или титана:
Сырьё для синтеза стирола – это этилбензол, получаемый алкилированием бензола:
Американским корпорациям UOP, Lummus Crest и Monsanto принадлежат самые новейшие разработки в сфере синтеза стирола. Технологию дегидрирования этилбензола в стирол стиро-плас (styro-plus) запатентовали ученые из фирмы UOP.
Данная реакция является классическим процессом дегидрирования этилбензола в присутствии высокотемпературного водяного пара в условиях вакуума. Обязательным условием является обработка смеси на специальном катализаторе между двумя стадиями дегидрирования. Специалисты UOP нашли наиболее подходящее соотношение между степенью перехода этилбензола в стирол и селективностью процесса. Вещество, которое получается вследствие реакции дегидрирования, подвергается фракционированию. Таким образом, синтезируется товарный стирол. Основным условием является разбавление ингибитором, чтобы минимизировать неконтролируемую полимеризацию.
Одним из ответвлений технологии фирм ABB Lummus Crest Inc. и UOP стала процедура дегидрирования smart (смарт). Такой синтез происходит в жидкой фазе на базе двухступенчатого реактора, в присутствии цеолитного катализатора. Стоит отметить, что большая часть существующих установок работает по схеме стиро-плас. Тем не менее, сегодня все чаще создают установки именно по жидкофазной схеме. Главная отличительная черта процесса smart заключается в том, что требуемое для реакции тепло подается при помощи селективного окисления водорода в прослойке катализатора.
В числе прочих методов синтеза стирола можно отметить реакцию совместного производства стирола и оксида пропилена. В тоже время, по уровню удельных капитальных вложений метод дегидрирования характеризуется определенными преимуществами. Легкость, довольно низкий уровень капиталоемкости, постоянно высокий спрос на стирол для синтеза полистирола и смол АБС стали движущей силой быстрого роста мощностей по выпуску стирола.
Среди самых крупных предприятий по выпуску стирола стоит отметить:
Наибольшие мощности по синтезу стирола в Российской Федерации расположены на Нижнекамском нефтехимическом комбинате, а также в Уфе, Салавате, Перми и Ангарске.
Основное направление использования стирола – это создание огромного количества полимеров. Среди них:
Кроме этого, стирол является составляющим компонентом напалма.
В результате реакции сополимеризации бутадиена и стирола получаются бутадиен-стирольные каучуки, которые активно применяют в шинном производстве, а также при изготовлении формовой и неформовой резиновой продукции. Вследствие высокого уровня радиационной стойкости, бутадиен-стирольные каучуки используют в процессе создания резин, которые противостоят гамма-излучению.
Если стружку из полистирола растворить в стироле, то получается отличный клеевой состав для полистирола. Тепло и остатки полимеризаторов действуют таким образом, что клеевой шов в короткие сроки полимеризуется и становится полностью незаметным. В конце получаем монолит из двух деталей.




