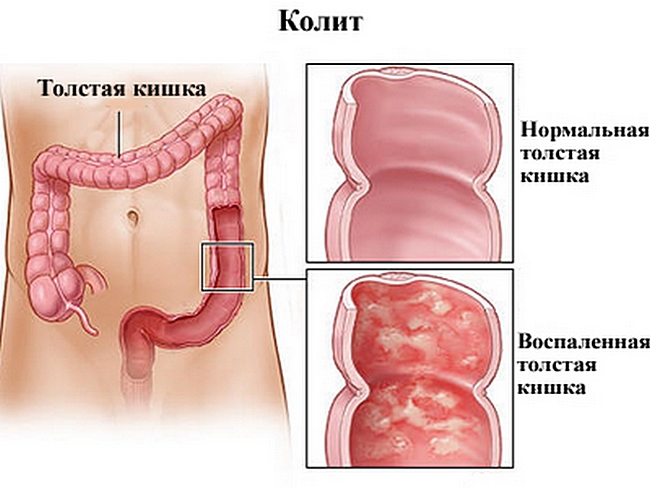
что такое слизистая гиперемирована кишечника
Хронические воспалительные заболевания кишечника
Что принято считать хроническим невоспалительным заболеванием кишечника? Какими методами можно подтвердить диагноз? Какая терапия наиболее эффективна? Рисунок 1. Слизистая кишечника при болезни Крона Хроническим воспалительным забо
Что принято считать хроническим невоспалительным заболеванием кишечника?
Какими методами можно подтвердить диагноз?
Какая терапия наиболее эффективна?
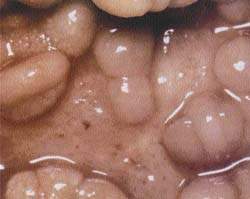 |
| Рисунок 1. Слизистая кишечника при болезни Крона |
Хроническим воспалительным заболеванием кишечника принято считать каждый длительный энтерит — как инфекционной, так и иммуноаллергической этиологии, который ведет к хроническому воспалительному процессу в кишечнике.
Помимо целиакии, эти заболевания включают в себя язвенный ректоколит, болезнь Крона и другие более редкие заболевания: колит при болезни Бехчета, некротизирующий энтероколит у детей младшего возраста. Все эти заболевания характеризуются:
— неизвестной этиологией (кроме целиакии);
— воспалительным характером поражений;
— хроническим течением и возможными рецидивами;
— ассоциацией с другими некишечными заболеваниями;
— хорошей реакцией на кортикостероидную терапию;
— возможностью хирургического разрешения (лечения).
В возникновении данных заболеваний большую роль играют как географический (встречаются чаще в Северной Европе), так и генетический факторы.
Болезнь Крона встречается чаще в западных странах и среди городского населения.
Этиология неизвестна, можно лишь предположить влияние инфекционных заболеваний и питания. Патогенез связан с нарушением ответной иммунной реакции со стороны слизистой кишечника, характер которой недостаточно изучен, известно лишь, что происходит активация Т- и В-лимфоцитов, увеличивается производство цитокинов и комплемента.
Гистопатологические наблюдения позволяют выявить два основных и множество промежуточных типов нарушений при хроническом воспалении кишечника.
Болезнь Крона. Характеризуется четко отграниченными трансмуральными сегментарными поражениями, разделенными между собой внешне неизмененной слизистой. Поражение распространяется на мезентериальные лимфоузлы. Может быть затронут любой участок желудочно-кишечного тракта, но чаще поражается кишечный отдел подвздошной кишки. Типично формирование стенозов, абсцессов и фистул. Характерны отек слизистой, изъязвления, атрофия и утолщение кишечной стенки, гиперплазия лимфоузлов.
Наблюдается гранулематозное поражение. В 60-70% случаев гранулема обнаруживается на хирургическом материале и лишь в 30-40% при биопсии. Гранулема состоит из эпителиоидных и гигантских клеток. Несмотря на тенденцию к некрозу, казеозного некроза не отмечается. Легко формируются язвы и фистулы.
Язвенный ректоколит. Это заболевание ободочной кишки. Начинается с ректального уровня и распространяется вверх. Процесс поверхностный, затрагивает подслизистую, слизистую и редко более глубокие слои. Для острой стадии характерны гиперемия слизистой, отек, легко кровоточащие эрозии и язвы. В промежутках между язвенными поражениями слизистая гипертрофирована, нередко образуются псевдополипы. Описанные поражения могут сочетаться с перианальными трещинами. Гистологически характерно образование крипт и абсцессов, в которых накапливаются лимфоциты, эозинофилы, нейтрофилы, плазматические клетки. Гранулематозная ткань отсутствует.
Варианты вышеописанных двух основных типов хронических воспалительных заболеваний кишечника:
1. Язвенный энтероколит. Некоторыми авторами считается врожденной формой болезни Крона. Поражения затрагивают весь пищеварительный тракт, но преимущественно локализуются в конечной части подвздошной кишки и в начальном участке ободочной кишки.
2. Синдром Бехчета, при котором к кишечным поражениям присоединяются ретинит, слепота, болезненные язвенные и некротические поражения слизистой рта и гениталий.
3. Некротизирующий энтероколит у грудных детей часто приводит к летальному исходу. Клинические проявления болезни приходятся на первую неделю жизни: диарея с примесью крови, признаки перитонита и шок. Характерны множественные язвенные поражения с перфорацией.
Классически хронические заболевания кишечника характеризуются как желудочно-кишечными (диарея, боли в животе, наличие крови в кале), так и общими (температура, потеря веса, задержка физического развития) симптомами.
Болезнь Крона: на фоне анорексии, типичной для этого заболевания, преобладают общие симптомы. Боли в животе напоминают приступы аппендицита. Кровь в кале обнаруживается редко. При осмотре отмечается болезненность в правой подвздошной области, там же иногда пальпируется масса.
Язвенный ректоколит: преобладают кишечные симптомы — тенезмы, диарея с примесью крови. При пальпации живота отмечается болезненность по ходу ободочной кишки.
Стенозы, абсцессы и фистулы, трещины, мегаколон, перфорации с массивным кровотечением, карцинома ободочной кишки, энтеропатия с потерей белка. Характерны такие общие осложнения, как воспаление радужки, сосудистой оболочки глаза, афтозный стоматит, артрит, перихолангит, склерозирующий холангит.
Хроническая диарея с болями в животе, кал с примесью крови позволяют думать о хроническом воспалительном заболевании кишечника.
Для подтверждения диагноза необходимо оценить данные лабораторного анализа: общий анализ крови; сидеремию; трансферинемию; иммуноглобулины; время свертываемости крови; содержание в крови кальция, фосфора, цинка, меди; костный возраст; С-реактивный белок, a1-антитрипсин; анализ кала. Особо важную роль для постановки диагноза приобрела контрастная рентгенография с барием. Широко используется рентгенография с двойным контрастированием, при которой отмечается:
— уменьшение просвета кишечной стенки;
— неоднородность рисунка;
— кистовидные участки.
Наличие этих трех признаков в терминальной части подвздошной кишки образует триаду Bodart, типичную для болезни Крона.
О распространении воспалительного процесса позволяют судить участки, заполненные лейкоцитами, меченными радиоактивным йодом I111. Компьютерная томография незаменима для выявления осложнений (фистул, абсцессов).
Окончательный диагноз ставится на основе биопсии.
Дифференциальный диагноз проводится с
— аллергическим колитом;
— узловой лимфоидной гиперплазией;
— хроническим гранулематозным заболеванием;
— аппендицитом;
— полипозом и лимфомой кишечника;
—болезнью Шенлейна — Геноха.
За последние годы значительно улучшился. Детская смертность практически исчезла (от 15 до 2%).
Большую тенденцию к рецидивам имеет язвенный ректоколит. Наблюдение за детьми заключается в
— контроле за ростом;
— контроле за показателями воспалительного процесса;
— за терапией [10].
Диетотерапия играет важную роль, особенно при болезни Крона, для которой характерна потеря веса и задержка роста [1, 2, 10, 15, 17].
Новый подход к терапии заключается в возможности достигнуть ремиссии с помощью диеты без гормональной терапии [1, 18, 21, 23, 24, 25].
Фармакотерапия основана на применении кортикостероидов [26], сульфасалазина, салазопирина [27, 28, 29], метронидазола [30]. Иммуносупрессоры малоприменимы из-за их токсичности.
Хирургическое лечение возможно при тяжелых осложнениях (мегаколон, стенозы, абсцессы, фистулы) и в случаях задержки роста в пубертатном и препубертатном периодах [13, 14].
Из клинической практики
Поражение печени, хотя и без явных клинических проявлений, встречается довольно часто при хронических заболеваниях кишечника. У взрослых в 70% случаев развивается перихолангит с портальной триадой. У 50% отмечаются жировые изменения печени. 10% приобретают заболевания печени. Цирроз печени развивается у 5%.
Другие, более тяжелые и редкие осложнения — это хронический активный гепатит, склерозирующий холангит и карцинома желчевыводящих путей.
Необходимо отметить, что у детей частым осложнением является хронический активный гепатит, в то время как перихолангит и склерозирующий холангит встречаются очень редко и протекают бессимптомно.
Представляем клинический случай язвенного колита у девочки трех лет. Начальная фаза заболевания протекала бессимптомно. Впоследствии развилась ярко выраженная гепатомегалия.
Девочка была госпитализирована в трехлетнем возрасте. За 8 месяцев до госпитализации отмечались раздражительность, потеря аппетита, непостоянные боли в животе, кал с примесью алой крови. С вышеописанной симптоматикой девочка была госпитализирована. При осмотре отмечалась значительная гепатомегалия (+4 см из-под реберной дуги по правой среднеключичной линии). В анализе крови СОЭ 104 мм в час; общий белок крови 9,9 гр%; альбумин 2,5 гр%; a1-глобулин 0,3; a2-глобулин 1,1; b-глобулин 1,0; g-глобулин 5,0; IgG 4810 мг%; щелочная фосфатаза 1273 МЕ; антитела противоядерные и против гладких мышц отсутствуют.
В период госпитализации девочка жаловалась на частые боли в животе. В кале примесь слизи и алой крови. При анализе слизи кала выявлено множество нейтрофильных лейкоцитов. Эндоскопически выявлен обширный воспалительный процесс по всей ободочной кишке с отеком слизистой. При контакте с инструментом слизистая легко кровоточила.
При множественных биопсиях проводился гистологический анализ, который выявил изрежение железистых протоков с моно- и полинуклеарной инфильтрацией.
Чрескожная печеночная биопсия выявила воспалительные и грануломатозные изменения преимущественно в портобилиарных пространствах. Более того, отмечался воспалительный процесс типа перихолангита и начального холангита в межлобулярных протоках.
Лечение преднизолоном в начальной стадии и далее салазопиридином (SAZP) привело к полной ремиссии кишечной симптоматики. Клиническая ремиссия с полной регрессией гепатомегалии (печень пальпировалась у реберной дуги) была подтверждена гистологически. Нормализовались и лабораторные показатели (IgG 997 мг%).
Известно, что язвенный колит нередко сопровождается непереносимостью белка коровьего молока, поэтому были проведены кожный тест и тест на определение специфичных IgE. IgE были значительно увеличены.
Быстрая клиническая ремиссия была обусловлена двумя факторами: назначением салазопиридина (SAZP) и одновременным исключением из диеты коровьего молока.
Chronic inflammatory bowel diseases
Summary
Chronic inflammatory bowel diseases are commonly believed to present in the form of two diseases with aetiologies of unknown origin, Ulcerative Rectocolitis and Chron’s Disease, which are characterised by important inflammatory events affecting the normal structure of the intestinal wall, with a tendency to relapse.
Both diseases share a variety of common characteristics and are thus considered by many as one single clinical entity.
The common features are the following:
— unknown aetiology
— inflammatory aspect of the lesions
— chronicity of the course of disease, with possible relapses
— association with extra-intestinal symptoms
— good response to corticosteroid therapy
— recourse to surgery (for a limited number of cases).
The aforenamed two paradigmatical pictures constitute the essentials of a spectrum comprising an indefinite number of intermediate pictures, for example Behcet’s Colitis, similar to Ulcerative Colitis but where ulcers can be found in the area of the mouth and the genitals, or Ulcerative Enterocolitis of the infant, thought to be a congenital form of Chron’s Disease.
Both pictures display gastrointestinal symptoms such as diarrhoea, tenesmus and bloody stools, usually prevailing in Ulcerative Colitis, and are accompanied by general symptoms such as fever and weight loss, usually found in Chron’s Disease.
One of the recent and most interesting aspects of Chron’s disease is the possibility to induce remission as well as restoration of the patient’s growth by administration of an elementary diet. The administration of a hypercaloric diet has also proved useful in correcting growth speed and in reducing the need of steroids, which also play an important role in inducing disease remission.
In order to further maintain remission, the administration of salazopirina (sulfosalazina) and corresponding salacylates, as well as of immunosoppressors such as azathioprine and cyclosporins, have proved useful. The administration of metronidazolo is indicated in the case of perineal injuries only. The use of surgery should be limited to complications and, in the presence of failure to thrive, only if the lesions are well delimited.
Колит
Хронический колит – это наследственное хроническое воспалительное поражение слизистой, подслизистой и мышечной оболочек толстой кишки, при тяжелом течении заболевания с дегенерацией собственных нервных волокон, являющееся одним из наиболее частых заболеваний системы пищеварения.
Заболевание имеет доминантный тип наследования, передается из поколения в поколение. В основе развития заболевания лежит информация закодированная в участке гена человека, с которого она списывается в определенный период его жизнедеятельности.
Под воздействием списанной с гена информации о заболевании, происходит переформирование нервнорефлекторной регуляции записанной в мозговом центре памяти в ее кольцевой цепи памяти. Происходит замещение в кольцевой цепи памяти существовавшего ранее физиологического безусловного рефлекса на новый вновь сформированный патологический доминирующий безусловный рефлекс.
Измененная нервнорефлекторная регуляция в мозговом центре памяти начинает переформировывать нервнорефлекторную регуляцию в кольцевой цепи памяти периферического центра автоматизма. Разное процентное преобладание патологического доминирующего безусловного рефлекса над физиологическим безусловным рефлексом приводит к разной степени разбалансированности взаимодействия симпатической и парасимпатической нервной системы.
Степень тяжести заболевания напрямую зависит от процентного преобладания доминирующего патологического безусловного рефлекса над существовавшим до возникновения болезни физиологическим безусловным рефлексом. Чем сильнее выражена разбалансированность симпатической и парасимпатической нервной системы под непосредственным влиянием вновь сформированного патологического доминирующего безусловного рефлекса, тем быстрее возникает и тяжелее протекает возникшее заболевание толстого кишечника.
В основе хронического колита лежит нервнорефлекторное нарушение взаимодействия симпатической и парасимпатической нервной системы, которые вызывают изменение трофики слизистой, подслизистого слоя и мышечной ткани, приводящее к ухудшению всасывающей, переваривающей и моторно-эвакуационной функций толстого кишечника. В следствии этого происходит изменение PH внутри толстого кишечника, который ухудшает условия для жизнедеятельности кишечной палочки, что приводит к автоматическому уменьшению ее количества, а следовательно, нарушает функцию переваривания а затем и функцию всасывания пищи.
Нарушение перистальтической функции толстого кишечника приводит к дополнительному нарушению функции переваривания, всасывания и эвакуации пищи, а также к еще одному фактору, влияющему на уменьшение количества жизнеспособной кишечной палочки. Все это вместе взятое приводит к вторичным гистологическим изменениям слизистого, подслизистого и мышечного слоев толстого кишечника.
Слизистая становится гиперемирована, клеточная инфильтрация ее резко выражена, поверхность слизистой покрыта слизью, местами эрозирована или изъязвлена, отмечается гиперплазия лимфатических фолликул. При более тяжелом и длительном протекании заболевания преобладают атрофические процессы в стенке толстой кишки: крипты становятся менее глубокими, их просвет неравномерно расширен, число их на единицу поверхности внутренней стенки кишки уменьшается, поверхностный цилиндрический эпителий слизистой оболочки уплощается.
Наблюдается утолщение и гомогенизация базальной мембраны эпителия, поражаются кровеносные капилляры и лимфатические сосуды стенки кишки, а также внутриклеточные нервные сплетения (наблюдается дистрофия и распад нервных волокон, гибель ганглиозных клеток), разрастание соединительной ткани в слизистом и подслизистом слоях толстой кишки. Присоединение к заболеванию толстого кишечника: различных инфекций, грибков и паразитов, интоксикаций различной этиологии, а также заболеваний желудка, печени и поджелудочной железы, безконтрольного применения антибиотиков и слабительных препаратов, только усугубляет клинику течения болезни и усиливает ее тяжесть.
При обострении процесса заболевания появляются ложные позывы на дефекацию, сопровождающиеся отхождением газа и отдельных комочков каловых масс, покрытых тяжами или хлопьями слизи, или слизи с прожилками крови. При спастическом колите, особенно при вовлечение в процесс дистальных отделов толстой кишки, каловые массы имеют фрагментированный вид («овечий кал»). Частым симптомом хронического колита являются тупые боли в животе, обычно локализующиеся в боковых или нижних отделах живота, усиливающиеся после приема пищи и перед дефекацией.
Иногда боли приобретают спастический характер (при «спастическом колите»), приступ болей может сопровождаться отхождением газов или возникновением позыва к дефекации. При обострении колита возникают болезненные тенезмы; боли могут сохраняться некоторое время после дефекации, возникать при проведении очистительной клизмы, стихать от применения тепла (грелка, компресс), после приема холино- и спазмолитиков.
При распространении воспалительного процесса на серозную оболочку толстой кишки (периколит) боли, имея постоянный характер, усиливаются во время ходьбы, тряски и уменьшаются в положении лежа. При периколите и возникновении мезаденита боли могут усиливаться от тепловых процедур; упорные ноющие боли по всему животу или локализующиеся преимущественно в подложечковой области, не связанные с приемом пищи, актом дефекации, трудно поддающиеся лечению, наблюдаются при сопутствующем ганглионите, особенно солярите. Метеоризм нередко наблюдается при колите, его причиной является нарушение переваривания пищи в толстой кишке и дисбактериоз.
Часто наблюдаются диспепсические жалобы: анорексия, подташнивание, отрыжка, ощущение горечи во рту, урчание в животе и т. д., во многих случаях эти явления связаны с сопутствующими заболеваниями пищеварительной системы (гастрит, холецистит, панкреатит). Общее состояние больных в большинстве случаев мало страдает, но могут наблюдаться слабость, общее недомогание, снижение трудоспособности, астеноневротический синдром. При длительно протекающем тяжелом колите может развиваться похудание, как следствие анорексии, сознательных ограничений в приеме пищи, вызванных боязнью болей, позывов к дефекации, а также неполноценной диетой.
При поверхностной пальпации нередко выявляются участки болезненности брюшной стенки, располагающейся по ходу толстой кишки. При глубокой пальпации пораженные участки толстой кишки обычно болезненны и спастически сокращены, может иметь место чередование спастически сокращенных и расширенных участков, наполненных плотным или жидким содержимым; в последнем случае определяется сильное урчание и даже «плеск» в соответствующем отделе кишки. Симптом умеренного урчания определяется только при ощупывании слепой кишки. При периколите, ганглионите и мезадените болезненность брюшной стенки не ограничена областью расположения толстой кишки, а может наблюдаться в подложечковой области и ниже по средней линии около пупка.
При копрологическом исследовании определяется большое количество: слизи и лейкоцитов, эритроцитов (при эрозивных и язвенных формах), перевариваемой клетчатки и внутриклеточного крахмала. Рентгенологическое исследование толстой кишки (иригоскопия), при хроническом колите, обнаруживает функциональные нарушения (ускорение перистальтики, усиленная гаустрация, спастическое сокращение или, наоборот, атония кишечной стенки).
При тяжелых формах колитов выявляются изменения рельефа слизистой оболочки за счет воспалительного отека и инфильтрации, а иногда и участки рубцововоспалительного сужения просвета кишки. Ректороманоскопия, сигмоидоскопия и колоноскопия, проводимые с помощью гибких эндоскопов, позволяют осмотреть слизистую оболочку толстой кишки и определить характер и степень морфологических изменений, выявить эрозии и язвы, взять биопсию слизистой для цитологической диагностики. Исследование крови позволяет выявить наличие гипохромной анемии, при обострении процесса – умеренный нейтрофильный лейкоцитоз со сдвигом влево, ускоренное СОЭ.
Сегментарные колиты. Хронические тифлиты протекают с упорными болями в правой подвздошной области, иррадиирующие в пах и поясницу; вздутием и урчанием правой половины живота, с выделением полужидкого стула (3-5 раз в сутки) – «коровий кал». При пальпации отмечается болезненность в области слепой и восходящего отдела ободочной кишки, отмечается сильное урчание и их спазм.
При перитифлите в период обострения воспалительного процесса может определяться нерезко выраженный симптом Щеткина – Блюмберга, который иногда сочетается с субфебрилитетом, повышением СОЭ может симулировать обострение хронического аппендицита.
Изолированный трансверзит возникает редко и во многих случаях сочетается с колоноптозом. Проявляется тупыми болями в эпигастральной области и левом подреберье, нередко усиливающимися после еды, метеоризмом, ощущением распирания живота, который облегчается после дефекации, нарушениями стула. При пальпации определяется болезненная, иногда опущенная и неравномерно спазмированная поперечная ободочная кишка. При выраженных явлениях процесса в области селезеночного изгиба могут возникнуть симптомы частичной, а в редких случаях и полной непроходимости кишечника.
Проктит и проктосигмоидит –это самые частые формы хронического колита. Они проявляются болями в левой подвздошной области и в области заднего прохода, болезненными тенезмами, метеоризмом; нередко наблюдаются запоры в сочетании с тенезмами, стул необильный, иногда типа «овечьего кала», содержит много видимой слизи, а нередко и кровь (при язвенном процессе) и гной.
При пальпации отмечается болезненность сигмовидной кишки, ее спастическое сокращение или урчание (при поносах). Иногда определяется дополнительная петля сигмовидной кишки – «долихосигма» (врожденная аномалия развития сигмовидной кишки), которая способствует задержке продвижения каловых масс и возникновению воспалительного процесса.
Осмотр и пальцевое исследование прямой кишки выявляют:
геморой, трещины заднего прохода, парапроктит, выпадение прямой кишки и т. д.. В диагностике хронического проктосигмоидита большое значение имеет ректороманоскопия.
Процесс излечивания хронического колита включает в себя:
1) – это прекращение развития заболевания,
2) – это восстановление в кольцевой цепи памяти периферического центра автоматизма и в мозговом центре памяти физиологического безусловного рефлекса, что восстанавливает уравновешенность взаимодействия симпатической и парасимпатической нервной системы, а это приводит к прекращению заболевания.
Уравновешенная и сбалансированная симпатическая и парасимпатическая нервная система восстанавливает жизнедеятельность и функционирование толстого кишечника, и приводит к постепенному восстановлению в нем концентрации кишечной палочки, что существенно улучшает процесс переваривания пищи, а следовательно, и ее всасывание слизистой.
Процесс излечивания хронического колита протекает волнообразно, с периодами улучшения и периодами ухудшения течения заболевания. Этот постепенный волнообразный тип излечивания заболевания и позволяет уравновесить симпатическую и парасимпатическую нервную систему, а через нее восстановить нормальное функционирование толстого кишечника. Встречаются случаи длительного, до трех и более месяцев, восстановительного периода излечивания хронического колита.
Это требует упорства и большого желания со стороны больного человека, а также правильного применения соответствующей методики лечение колита и строгого контролирования процесса выздоровления со стороны лечащего врача. При полном излечивании заболевания, рецидивов возникновения болезни не бывает.
Функция толстого кишечника, как правило, восстанавливается полностью. Иногда при поражении, тяжелым течением хронического колита, нервных окончаний в стенке толстой кишки, восстановление уравновешенного нервнорефлекторного взаимодействия симпатической и парасимпатической нервной системы, не приводит к излечиванию заболевания.
Это происходит из-за утраченной возможности влияния симпатической и парасимпатической нервной системы на жизнедеятельность толстого кишечника.
Воспалительные заболевания кишечника
Несмотря на очевидный прогресс в исследовании данной гастроэнтерологической проблемы все еще загадкой остается причина (этиология) происхождения данных болезней. Вне понимания исследователей остаются такие вопросы как особенности клинического течения и развитие резистентных к лечению форм болезни. Пока мы не можем прогнозировать ответ на лечение и предупреждение рецидивов у конкретного пациента. Не умеем предотвратить развития острых «молниеносных» форм заболевания и избежать необходимости прибегать к калечащим операциям (колэктомии).
Что же сегодня мы знаем об этих болезнях?
Не подвергая сомнению, факт самостоятельности нозологических форм язвенного колита и болезни Крона следует отметить ряд общих черт, позволяющих рассматривать их в рамках единого воспалительного заболевания толстой кишки (ВЗК):
Головенко Николай Олегович
Зубкова Галина Васильевна
Семейный врач, терапевт, гастроэнтеролог, ведущий специалист
Маевская Евгения Андреевна
Нурматов Шавкат Шарибжанович
Гастроэнтеролог, семейный врач, терапевт, эндоскопист
Сенча Александр Викторович
Сидорова Александра Владимировна
Хирург, онколог, колопроктолог
Фарбер Андрей Витальевич
Юнусов Булат Тимирзянович
Неспецифический язвенный колит (язвенный колит, НЯК)
Заболеваемость язвенным колитом колеблется в пределах 10-15 случаев на 100000 населения ежегодно, достигая в некоторых регионах до 200 случаев на 100000 населения в интервале двадцатилетия. Нередко, пациенты с легкими проктитами поздно обращаются к специалистам; привыкают к своему жидкому стулу, а появление крови в кале связывают с геморроем.
Язвенный колит встречается во всех возрастных группах, однако основной пик заболеваемости приходится на возраст 20-40 лет, а второй небольшой подъем заболеваемости наблюдается у лиц в возрасте 60-70 лет. Дети моложе 10 лет редко болеют язвенным колитом.
Половые различия выражены не ярко, хотя женщины болеют чаще (соотношение 1,5:1). Привычные и устоявшиеся представления о расовом различии в заболеваемости (евреи США в 3,5 раза чаще болели, чем черные) пересматриваются. Вероятно, имеют значение общие факторы внешней среды и единый иммунитет, противодействующие расовому и этническому фактору риска.
Этиология
До настоящего времени язвенный колит определяется как идиопатическое воспаление толстой кишки. Попытки связать происхождение ВЗТК с каким – либо единственным причинным фактором пока оказались безуспешными. Разные исследователи предлагают возникновение и развитие заболевания объяснять аномальным стресс-синдромом, действием бактериальных или вирусных агентов, аллергическими реакциями в слизистой оболочке, генетической предрасположенностью, нарушением иммунологического гемостаза. Причем, прямые и косвенные результаты проводимых исследований не позволяют игнорировать участие тех или иных факторов в качестве возможной причины для определенных больных.
Существование генетической предрасположенности, связывают с регистрацией семейных случаев язвенного колита, который среди ближайших родственников встречается в 15 раз чаще, чем в общей популяции. Отмечается высокая частота конкорданса среди монозиготных близнецов. Имеются данные о связи язвенного колита с геном DR2 и B27 комплекса гистосовместимости HLA.
Гипотеза аутоиммунного механизма развития язвенного колита подтверждается высокой частотой обнаружения антинейтрофильных цитотоксических антител, а также наличием специфического антигена – тропомиозина и выделения антител к нему из пораженной слизистой оболочки. Роль аутоиммунного процесса очевидна, однако значение аутоиммунных реакций, как причины патологического процесса, остаются дискутабельными.
Дефект в гликопротеинах кишечной слизи делает слизистую оболочку восприимчивой к повреждающему действию бактериальных энзимов и других медиаторов воспаления.
Факт взаимосвязи язвенного колита и курения пока трудно интерпретировать.
Морфология
Изменения кишечного эпителия возникают вторично в связи с воспалением, которое начинается в прямой кишке и распространяется проксимально, вовлекая в болезненный процесс различные отделы толстой кишки. Слизистая оболочка гиперемирована, отечна и изъязвлена. Размер и форма язв различна – от мелких поверхностных эрозий до обширных язвенных полей. Часто обнаруживаются воспалительные полипы (псевдополипы), как следствие разрастания грануляционной ткани, формируя нередко причудливые выросты. Микроскопические изменения зависят от фазы и степени активности воспалительного процесса и характеризуются инфильтрацией собственной пластинки плазматическими клетками, эозинофилами, лимфоцитами, тучными клетками и нейтрофилами. Изъявление крипт приводит к формированию интрамускулярных абсцессов ( крипт- абсцессы ), которые, вскрываясь, образуют язвы. Регенерирующие крипты становятся короткими и разветвленными. Форма и состояние крипт является важным диагностическим критерием язвенного колита при гистологической оценке воспаления.
Клиническая картина
Клиническая картина язвенного колита включает три основных признака:
Напротив, симптомами язвенного проктита являются ложные позывы на дефекацию и запоры. Течение заболевания обычно легкое, без существенных изменений общего состояния пациента и в показателях гемограммы.
При оформлении диагноза многие клиницисты указывают на особенности течения, выделяя рецидивирующее (редко рецидивирующее) и непрерывно-прогрессирующее течение болезни. Просматривается попытка подчеркнуть волнообразность течения (рецидивирующие формы) или рефрактерность к проводимой терапии (хронически не- прерывное). Данное деление во многом является условным и в большой степени зависит от опыта практикующего врача, выбранной им схемы лечения, применяемых доз, длительности терапии и т.п.
Диагноз
В типичных случаях поражения прямой кишки не представляет трудностей и легко устанавливается при первом посещении больного на основании данных эндоскопического исследования (ректоскопии, колоноскопии): выраженное покраснение слизистой оболочки, ее отечность, зернистость, отсутствие сосудистого рисунка, участки точечных геморрагий (кровоизлияний), характеризующих ранние изменения (1 степень эндоскопической активности). Позднее появляются мелкие абсцессы и поверхностные эрозии, местами сливающиеся между собой. Слизистая оболочка легко ранима и при контакте с тубусом ректоскопа кровоточит (2 степень активности). При тяжелом поражении на стенках кишки отмечаются наложения фибрина, покрывающего различных размеров язвы; слизистая спонтанно кровоточит (в просвете кровь и гной), на отдельных участках видны псевдополипы (3-4 степень активности). Во время ремиссии появляется сосудистый рисунок, хотя местами он деформирован. Часто сохраняются отдельные участки гиперемии с зернистостью слизистой, но нет кровоточивости, язв и фибринозно-гнойного налета на стенке кишки. При средне-тяжелом язвенном колите для определения протяженности поражения и получение биоптатов, используется фибросигмоскопия или колоноскопия.
Рентгенологический метод исследования с бариевой клизмой в настоящее время используется редко, хотя рентгенологические признаки язвенного колита хорошо разработаны в 70-80 гг. Сегодня, при формальных признаках тяжелой атаки язвенного колита эндоскопические и рентгенологические исследования противопоказаны. Рентгенологическое исследование должны быть ограничено обзорным снимком брюшной полости, позволяющим исключить токсический мегаколон и определить границы поражения. Редким показанием для ирригоскопии являются трудности исключения болезни Крона при доброкачественных сужениях толстой кишки, имеющих место при длительном течении язвенного колита.
Лабораторные исследования включают общий анализ крови, СОЭ, гемоглобин, С-реактивный протеин. Последние годы в качестве маркера воспаления исследуется фекальный калпротектин, величина которого коррелирует с активностью воспалительного процесса. Этот белок выделяется нейтрофилами, мигрирующими в очаг воспаления.
Дифференциальный диагноз
Дифференциальный диагноз при первой атаке язвенного колита проводят острыми инфекционными колитами, вызывающими кровянистый понос. Обязательное исследование испражнений с целью выявления культуры возбудителя позволяют диагностировать бактериальную дизентерию, сальмонеллезы, кампилобактерную инфекцию и эширихиоз. Амебный колит следует предположить в эндемических районах (Индия, Тайланд, Вьетнам, Малазия, страны Африки). При сигмоидоскопии можно обнаружить дискретные «штампованные» язвы на фоне малоизмененной слизистой оболочки.
Основным объектом для дифференциального диагноза является болезнь Крона. Различия базируются на таких признаках как прерывистость поражения (чередование зон поражения и нормальной слизистой оболочки), глубоких язв-трещин, афт, симптом «булыжной мостовой», наличия перианальных поражений, внутренних и наружных кишечных свищей, стриктур, редкое вовлечение в воспалительный процесс прямой кишки, наличие пальпируемых опухолевидных образований в брюшной полости. Имеются и гистологические отличия болезни Крона – наличие полных или незавершенных гранулем, однако поверхностная биопсия крайне редко позволяет их обнаружить. Следует отметить, что при длительном течении язвенного колита у 10% пациентов эти два заболевания трудно распознать даже на операционном материале, что послужило основанием для обозначения таких случаев как «недифференцируемый колит».
Псевдомембранозный колит, протекающий в тяжелых случаях с кровавым поносом, лихорадкой и болью в животе нередкая причина диагностических трудностей, особенно если в процесс вовлечена прямая кишка.
Во всех случаях хронической диареи должна быть выполнена колоноскопия и биопсия для исключения микроскопического (лимфоцитарного) или коллагенового колита, сходного по течению с легкими формами язвенного колита.
Лечение
У переживших без операции первую атаку колита болезнь принимает хроническое течение с чередованием периодов обострения и ремиссии. Тесная связь симптомов болезни с активностью воспалительного процесса делает лечение язвенного колита схематичным, почти постоянное поражение прямой кишки позволяет легко контролировать проводимую терапию сигмоидоскопией и оценивать ее состояние гистологически.
Диета при язвенном колите не имеет большого значения. Питание должно быть нормальным, полноценным и обогащено витаминами. Обычно назначают стол-4 (по Певзнеру). При проктите со склонностью к запору допустимо обогащать рацион пищевыми волокнами. Назначение каких-либо антидиарейных препаратов не показано из-за угрозы спровоцировать токсическую дилятацию и низкой терапевтической эффективности данных средств.
Успех медикаментозной терапии острых явлений колита зависит от правильной оценки степени активности и протяженности поражения, определяющих адекватную схему лечения. Протяженность поражения и активность определяется при колоноскопии, а степень тяжести по критериям Truelove и Witts – простых, доступных и пригодных для индивидуального подбора терапии.
Предметом дискуссии остается эффективность гепарина в практике лечения среднетяжелых и тяжелых форм язвенного колита. Большинство исследователей подчеркивают безопасность его применения, что касается эффективности то есть восторженные отзывы о применении низкомолекулярного гепарина, как и указание на бесполезность его использования.
При легких формах язвенного колита неплохие результаты получают при назначении пробиотиков в комплексе с месалазином. Другим экзотическим методом лечения явилось применение клизм с никотином, которые заметно уменьшали частоту ложных позывов на стул у пациентов с язвенном проктитом.
Хирургическое лечение
Вопрос о хирургическом лечении может возникнуть на любом этапе лечения и наблюдения за больными с распространенными формами язвенного колита. Тяжелая токсическая атака колита в 60% случаев заканчивается экстренной колэктомией. В целом около 30% больных с хроническим течением распространенной формы язвенного колита подвергаются хирургическому лечению. Показанием к операции служат не только жизненно опасные осложнения ( токсический мегаколон, перфорация и перитонит, кишечное кровотечение и рак толстой кишки), но и рефрактерное течение хронического непрерывного колита, протекающего с дефицитом массы тела, анемией. Среди показаний к операции может быть задержка развития у детей и осложнения стероидной терапии.
Операцией выбора обычно является колэктомия (субтотальная резекция толстой кишки) с наложением илеостомы и на втором этапе реконструктивная операция формирования резервуара из тонкой кишки и закрытия илеостомы, т.е. восстановление естественного пассажа по кишечнику.
Осложнения
Различают кишечные осложнения: токсическая мегаколон при острой тяжелой атаке. Перфорация и развитие перитонита, обычно наблюдается после токсической дилятации толстой кишки. Кишечное кровотечение, массивность которого подтверждается нарушением гемодинамики, резко выраженной анемией и выделением сгустков крови из прямой кишки. Рак толстой кишки встречается при длительном течение тотального язвенного колита, достигая 18% у лиц страдающих более 20-25 лет данным заболеванием.
Внекишечные осложнения (манифестации) выявляются у 25-30% пациентов и включают: артриты, узловатую эритему, гангренозную пиодермию, сакроилеит, увеит, эписклерит, первичный склерозирующий холангит, гепатиты, некротизирующий васкулит, амилоидоз печени и почек, задержку развития и роста у детей. Ряд осложнений ассоциированы с активностью воспаления, а ряд лишь ассоциированы с данным заболеванием, например первичный склерозирующий холангит.
Прогноз
В целом прогноз у большинства больных с дистальными и левосторонними формами язвенного колита относительно благополучный и они доживают до старости, хотя и с нарушением качества жизни. У больных тотальным колитом после 8-10 лет болезни растет риск развития рака толстой кишки, который достигает 13-18% после 20 лет болезни. Эти пациенты нуждаются в тщательном диспансерном наблюдении с ежегодной колоноскопией с множественной биопсией из различных участков толстой кишки, что позволяет выявить дисплазию. При высокой степени дисплазии необходимо рекомендовать колпроктэктомию. При умеренной дисплазии возможно дальнейшее наблюдение 1 раз в год, а при легкой степени дисплазии колоноскопию выполняют 1 раз в 2 года.
Полное излечение от язвенного колита возможно лишь с помощью радикальной операции – колпроктэктомии.
Болезнь Крона (гранулематозный колит)
Заболевание впервые описано в 1932 г как странная форма туберкулеза без казеозного поражения. Как и язвенный колит встречается чаще в экономически развитых странах (Северная Америка, страны Европы, особенно Скандинавия). Несколько чаще болеют женщины. В настоящее время (вероятно, это связано с лучшей диагностикой) сглаживается различие в частоте болезни Крона и язвенного колита и ежегодно регистрируется порядка 8-10 новых случаев на 100000 населения, а общая распространенность достигает более 100 на 100000 населения.
Причина
Причина болезни Крона до конца неизвестна. Как и в случаи с язвенным колитом, в качестве возможной причины рассматривается инфекция, диетические факторы, генетическая предрасположенность, дефекты иммунологической системы.
Вероятно, болезнь Крона является гетерогенным заболеванием, при котором в качестве гена восприимчивости был идентифицирован ген NOD2(CARD15). Причем мутация данного гена определяет фенотип болезни Крона. Связь с гаплотипом показали 6 клинических характеристик: фистулообразование, поражение подвздошной кишки, левостороннее или правостороннее поражение толстой кишки, стенозы и резекции.
Важную роль в регуляции иммунного ответа и воспалительной реакции играют цитокины. Характер иммунного ответа и выработка цитокинов регулируется генетически. Ведущую роль при болезни Крона играют провоспалительные цитокины: интерферон q, тумор-некротический фактор (TNF-a), IL-12. Генотип TNF-a 308 был связан с предрасположенностью к болезни Крона. Гомозиготы TNF-a – 308 демонстрировали более высокую частоту узловатой эритемы и артрита, толстокишечную локализацию и отсутствие абдоминальных хирургических вмешательств.
Предполагают, что микроорганизмы тонкой кишки участвуют в этиопатогенезе болезни Крона, но выделить в чистом виде бактерии и вирусы пока не удается. Вместе с тем были выделены бактериальные протеины – антигены (флагелины) способные активировать врожденный иммунитет через Toll-подобные рецепторы. Они стимулируют патогенетические иммунные реакции у генетически различных хозяев. Кроме того, были выделены две PDA-производные микробные последовательности (11 и 12), идентифицированные как новые гомологи бактериальной транскрипции. Оказалось, что у больных болезнью Крона (у 43-54%, против 9% у НЯК и 5% СРК) 12-генный преобладал в препаратах подвздошной кишки независимо от фазы заболевания. Это связывает болезнь Крона с новой бактериальной последовательностью и что микроорганизм, экспрессирующий 12-генный продукт имеет отношение к патогенезу болезни Крона.
Важно, что ген NOD2 в норме обеспечивает возможность ответа на бактериальные продукты, распознавая мурамид-дипептид (структура бактерии). Мутанты NOD2, ассоциированные с предрасположенностью к болезни Крона, лишены способности распознавать мурамид-дипептид у грамотрицательных бактерий, делая их ответственными за воспаление.
В качестве гипотезы рассматривалась роль некоторых гидротированных жиров, включаемых в состав маргарина. Согласно одной из недавних гипотез механизм развития болезни первично связан с васкулитом, а в качестве триггерных механизмов могут быть курение, прием оральных контрацептивов или каких-то агрессивных макромолекул, поступающих в кишку при питании. Аргументом в пользу данного предположения является отсутствие рецидива болезни в отключенной из пассажа части кишки, после операции.
Клиническая картина
Клиническая картина, в отличие от язвенного колита, весьма разнообразна, и во многом определяется местом локализации воспаления и глубиной поражения кишечной стенки. Болезнь Крона представляет собой хроническую не резко выраженную диарею с болью в животе, длительной лихорадкой, потерей массы тела. При поражении подвздошной кишки развиваются симптомы аппендицита или кишечной непроходимости. При вовлечении прямой кишки болезнь может начинаться с симптомов острого парапроктита или анальных трещин (перианальные проявления наблюдаются у 30% пациентов). При длительном течение заболевания даже у одного больного удается проследить практически все местные проявления (осложнения) этого тяжелого трансмурального воспаления: инфильтраты и абсцессы в брюшной полости, заканчивающиеся образованием наружных и внутренних кишечных свищей, стриктуры тонкой или толстой кишки с развитием кишечной непроходимости. Поражение тонкой кишки может сопровождаться синдромом мальсорбции, дефицитом витамина Д, нарушением кальциевого обмена и развитием тяжелого остеопороза со спонтанными переломами. Нередко болезни Крона сопутствует калькулезный холецистит, МКБ.
Согласно Венской классификации (1998 г.) выделяют следующие клинические формы болезни Крона:
Нужно отметить, что к пенетрирующей подгруппе относят свищи (наружные и внутренние), воспалительные инфильтраты и абсцессы брюшной полости, свищи прямой кишки. Свищи и абсцессы встречаются в 15-50% случаев, перианальные поражения у 30% пациентов. Наружные свищи, чаще бывают следствием хирургического вмешательства, открываются на переднюю брюшную стенку (после аппендэктомии) и внутренние свищи: межкишечные, кишечно-вагинальные, кишечно-пузырные.
К стриктурирующей подгруппе относят стриктуры кишки и кишечную непроходимость, как следствие трансмурального поражения и исхода воспаления в фиброз. Иногда пальпируются не воспалительные образований в брюшной полости ( inter abdominal masse).
Тяжесть клинической картины болезни может быть выражена специальным индексом активности (индекс Беста) болезни Крона: менее 150 баллов- ремиссия, 150-300 баллов легкая, 300-450 баллов среднетяжелая, свыше 450 баллов – тяжелая. Высокое бальное значение фактора самочувствия является слабым местом данного индекса в оценке активности, а следует расценивать его как индекс заболевания.
Диагноз
Диагностика болезни Крона основывается на данных клинического, рентгенологического (ирригоскопия и пассаж бария по тонкой кишке), эндоскопические исследования (ректоскопия, колоноскопия и гастроскопия), гистологические исследования. Следует отметить, что осмотр тонкой и подвздошной кишки может быть дополнен видео капсульной эндоскопией.
При проведении дифференциальной диагностики следует всегда помнить о йерсиниозе, амебной дизентерии, кишечной форме туберкулеза. Определенные трудности могут возникнуть при распознавании ишемического колита, лимфомы тонкой кишки, болезни Бехчета, колоректального рака.
Всегда проблема затрагивает распознавание болезни Крона и язвенного колита. Рентгеносимеотика и эндоскопическая картина в типичных случаях не представляет проблем для распознавания болезни Крона. Однако, банальные анальные трещины и парапроктит при язвенном колите, развитие доброкачественных стриктур ободочной кишки при длительном течении язвенного колита создают «диагностические ловушки» и могут трактоваться в пользу болезни Крона. Особенно сложная проблема возникает при колите Крона, который клинически и эндоскопически протекает как язвенный колит. Поэтому у 10% пациентов даже операционный материал не позволяет четко дифференцировать эти два заболевания и эти случаи определяются как «недифференцированный колит».
Критерии диагноза болезни Крона:
Достоверный диагноз болезни Крона устанавливают при наличии как минимум 3 относительных критериев (от 1 до 6), а при выявлении гранулемы – еще одного относительного критерия (от 1 до 7).
Лечение
Цель лечения болезни Крона:
Базисными средствами лечения являются кортикостероиды, производные 5-аминосалициловой кислоты, антибактериальные средства и иммунодепрессанты. Последние годы революцией в лечении гранулематозного колита стали биологические методы лечения: иммунотерапия моноклональными человеческими антителами. К сожалению, чрезвычайно высокая стоимость этих средств, сдерживает их включение в базисную терапию.
Салицилаты: мезакол, салофальк, пентаза эффективны лишь для купирования легкого рецидива болезни (4 г/сутки) и для поддержания клинической ремиссии (1,5-2 г/сутки). Салофальк начинает действовать в терминальном отделе подвздошной кишки и наиболее активен в толстой кишке. Напротив, пентаза начинает действовать в двенадцатиперстной кишке и на протяжении всей тонкой кишки.
Кортикостероиды (преднизолон, метипред) способны быстро и эффективно воздействовать на воспалительный процесс, локализуемый в глубоких слоях кишечной стенки. Обычно рекомендуемые дозы 40-60 мг/сутки достаточно эффективны при среднетяжелых формах поражения. Неплохо зарекомендовал себя будесонид (9-12 мг/сутки),препарат с быстрой метаболизацией в печени и имеющий значительно меньшие системных проявлений. При легких дистальных формах препарат вводится в виде ректальных клизм или пены.
Однако, для лечения тяжелого (ИАБК > 450 баллов) приходится прибегать к назначению преднизолона из расчета 1,5 мг/кг/веса (80-90 мг/сутки) со схемой быстрого ступенчатого снижения или начинать лечение с парантерального введения гидрокортизона в дозе 500 мг/сутки.
Метронидазол (1,0 г/сутки) включают в схему терапии с первых дней лечения, но продолжительностью не более 1,5 месяцев из-за возможного развития тяжелых парастезий (периферическая нейропатия). Лечение прерывают на 2 недели и затем вновь включают в схему лечения.
Имеются указания на положительный эффект антибиотиков (ципрофлоксацин, фрамицитин) как дополнение к схеме базисной терапии.
Иммунодепрессанты ( азатиоприн, 6-меркаптопурин, метотрексат) включают в схему лечения на ранних этапах среднетяжелого и тяжелого воспаления, учитывая, что действие препаратов начинается через 10-12 недель. Длительность терапии 3-4 месяца. Лечение иммунодепрессантами способно предотвратить развитие стероидной рефрактерности и преодолеть стероидную зависимость.
Иммунокоррегирующая терапия (биотехнологическая терапия) своим появлениям обязана расшифровки механизма патогенеза аутоиммунного воспаления. Клеточная ветвь воспалительного процесса запускается провоспалитальными цитокинами (интерлейкин 1,12, тумор-некротический фактор-альфа) и целью терапии является подавление Т-хелперов и восстановление Т-супрессоров. Собственно циклоспорин и другие цитостатики ингибируют ИЛ-2 –опосредованную деятельность Т-хелперов оставляя интактной деятельность Т-супрессоров.
Основой биологической терапии являются белки, включая рекомбинантные человеческие протеины с иммунорегуляторными эффектами, моноклональные антитела (химерные, полностью человеческие) и синтезированные протеины. Уже в течение 20 лет для лечения болезни Крона используется инфликсимаб (ремикейд), который связывается с человеческим тумор-некротическим фактором и блокирует его биологическую активность. Разработаны схемы лечения различных форм болезни Крона, особенно пенетрирующей с перианальными повреждениями.
С каждым годом расширяется число этих биологических препаратов, название которых перешагнуло десяток (талидомид, онерцепт, адалимумаб, натализумаб, базиликсимаб, фонтолизумаб и др.)
Последние годы появились сообщения о новых подходах к лечению болезни Крона с использованием яиц гельминтов, мотивируя такой выбор терапии редкостью болезни Крона у носителей гельминтов в некоторых регионах.
Имеются указания на определенный эффект гипербарической оксигенации, абсорбционном аферезе гранулоцитов и моноцитов.
Находит применение и трансплантация выделенных из костного мозга гемопоэтических стволовых клеток при рефрактерных формах болезни Крона.
Хирургическое лечение
Длительные наблюдения свидетельствуют о неуклонном прогрессировании симптомов болезни и развитии осложнений. К 10 годам болезни подвергаются операции 55-65% больных, а через 15-20 лет болезни 74-90%. Большинство больных положительно оценивают результаты хирургического лечения, отмечают улучшение самочувствия, качества жизни. Однако операция не предотвращает риска рецидивов болезни Крона, и уже в ближайшие 5 лет после операции 42% больных имеют один или несколько эпизодов обострения. У некоторых пациентов повторно развиваются осложнения, требующие новых хирургических вмешательств. Показания к операции многообразны, но наиболее частыми являются приступы кишечной непроходимости, внутренние и наружные кишечные свищи, абсцессы, перфорации, токсическая дилятация, кишечные кровотечения и рак.
Хирургическими пособиями могут быть резекция пораженных сегментов кишки с анастомозом, дренирование гнойных полостей и отключение кишки, формирование обходных анастомозов, колпроктэктомия, брюшно-анальная резекция прямой кишки. При коротких стриктурах тонкой кишки возможна стриктуропластика.
Осложнения
Осложнения – перфорация в свободную брюшную полость и разлитой перитонит, а также массивные кишечные кровотечения.
Внекишечные проявления болезни Крона аналогичны тем, что наблюдаются при язвенном колите: