что такое синдром циве
Что такое синдром циве
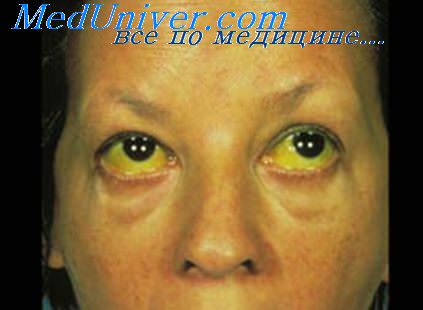
Синоним синдрома Циве. Гиперлипемия с гемолитической анемией и желтухой.
Определение синдрома Циве. Рецидивирующий гепатоз с желтухой, гемолитической анемией и гиперлипемией при алкоголизме.
Автор. Zieve Leslie — современный американский клиницист. Впервые синдром был описан в 1958 г.
Симптоматология синдрома Циве:
1. Приступообразное развитие желтухи и гемолитической анемии.
2. Гепатомегалия.
3. Рецидивирующие боли — эпигастральные или в правом верхнем квадранте живота.
4. Хронический рецидивирующий понос.
5. Ощущение общей слабости и недомогания, иногда тошнота или рвота, анорексия, потеря веса.
6. Часто в течение недель имеется субфебрильная температура, кашель и чувство зябкости.
7. Во время приступов функциональные пробы выявляют патологические изменения печени, которые, однако, обычно быстро нормализуются. Гиперлипемия, гиперхолестеринемия, интенсивность которых параллельна интенсивности желтухи.
8. Биопсия печени: жировая печень или разрастания соединительной ткани в перипортальной области (от умеренных до резко выраженных).
9. Часто имеются типичные «печеночные» телеангиэктазии на коже.
10. Тяжесть и частота приступов коррелируют с количеством потребляемого алкоголя. При воздержании от алкоголя обычно наступает быстрое клиническое улучшение.
Этиология и патогенез синдрома Циве. Нозологическая самостоятельность, а также механизм гемолиза не ясны, однако связь с алкоголизмом бесспорна. Zieve считает, что существует связь между гемолитическим процессом и гиперлипемией; он допускает также возможность наличия патологического липида. До сих пор не ясно, какую роль играют часто одновременно обнаруживаемые поражения поджелудочной железы.
Дифференциальный диагноз. Синдром Корсакова (см.). S. Dubin—Johnson (см.). S. Meulengracht (см.). S. Rotor (см.). Постгепатическая гемолитическая желтуха. Цирроз печени. S. Minkowski—Chauffard—Gansslen (см.). S. Loutit (см.).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Алкогольная болезнь печени
Согласно МКБ 10-го пересмотра выделяют следующие расстройства печени:
Болезни печени объединяет различные нарушения структуры паренхимы и функционального состояния гепатоцита, вызванные систематическим употреблением спиртных напитков. Алкогольные болезни печени относятся к токсическим.
Выделяют:
Жировой гепатоз печени. Симптомы и лечение
У 30% больных жировой дистрофией печени жалоб не наблюдается. Часто у 70% больных наблюдается гепатомегалия с гладкой поверхностью. Иктеричность, увеличение селезенки обнаруживаются редко.
В биоптатах определяют до 10% жира на влажный вес биопсионного материала, гепатоциты содержат крупные жировые капли.
У 1/3 больных жировой дистрофией печени имеет место гипербилирубинемия, гиперлипидемия, снижение поглотительно-экскреторной функции, установленное на основании бромсульфалеиновой пробы, нерезкое повышение аминотрансферазной активности и гаммаглютамилтранспептидазы. Жировая дистрофия печени подтверждается данными УЗИ на основании эхосимеотики, свойственной жировому гепатозу.
Разновидностью жирового гепатоза печени при хроническом алкоголизме является синдром Циве. Кровь характеризуется выраженным нарушением липидного зеркала (гиперхолестеринемия, гипертриглицеридемия, гиперфосфолипидемия). Наблюдается гемолиз крови (как результат снижения резистентности эритроцитов на фоне дефицита витамина Е), повышение уровня билирубина.
Жировой гепатоз печени, лечение
Жировая дистрофия печени без наличия фиброза не является предцирротическим состоянием. При прекращении употребления спиртных напитков структура органа обычно восстанавливается за 4-6 недель.
При жировом гепатозе печени назначается диета с достаточным количеством белка, полиненасыщенных жирных кислот (растительные масла, рыба), препараты, содержащие силимарин (гепатопротекторы-антиоксиданты), поливитаминные драже, содержащие микроэлементы, особенно важен цинк, так как он является составляющей ферментов алкогольдегидрогеназу, супероксид-дисмутазу (антиокислительная система организма), ферментов, стимулирующих иммунную систему.
Кроме диеты для лечения жирового гепатоза печени необходимы витамины. Непременно следует назначать альфа-токоферол либо витаминными препаратами, либо увеличить потребление витамин-Е-содержащих продуктов: преимущественно нерафинированные растительные масла, желток, орехи, гречка, петрушка, проросшие семена пшеницы.
Алкогольный фиброз печени
Клинические и функциональные проявления фиброза и жирового гепатоза идентичны. Отличительной особенностью первого является повышение в крови аминокислот пролина, оксипролина, являющихся крупной составляющей коллагена.
Перивенулярный фиброз может быть остановлен отказом от алкоголя, лечением как при жировой дистрофии печени. Хронический центролобулярный склероз трансформируется в цирроз даже при полной абстиненции, однако лечение, отказ от алкоголя задерживают развитие стадии цирроза.
Алкогольный гепатит и цирроз печени
Алкогольный гепатит соответственно Международным классификациям болезней печеночного органа делят на острый и хронический. Болезнь является одним из основных вариантов, наряду с алкогольным фиброзом, трансформируется в цирроз.
Установлена зависимость недостатка антигена гистосовместимости HLA В40 с развитием хронического активного гепатита с последующим переходом в цирроз.
Эта форма гепатита (острый некроз) может развиваться на фоне жировой дистрофии печени, острых гепатитов, фиброза или цирроза. При циррозе развитие острого гепатита (некрозов) очень часто приводит к распадной (паренхиматозной) и шунтовой (портокавальной) печеночной энцефалопатии, что чаще всего заканчивается летальным исходом.
Гистологически наблюдается перивенулярное поражение гепатоцитов, баллонная дистрофия, их некроз, алкогольный гиалин (тельца Мэллори), лейкоцитарная инфильтрация, перицеллюлярный фиброз и т.д. Некроз гепатоцитов центра печеночных гексагональных долек.
Острый гепатит часто развивается у лиц молодого, среднего возраста после запоя с предшествующим длительным употреблением алкоголя. Характерно острое появление болевого, диспепсического синдромов, однако у некоторых больных заболевание может развиваться постепенно.
Наиболее частый желтушный вариант: нарастает резкая слабость, отсутствие аппетита, тошнота, рвота, желтуха, диарея, резкая потеря массы тела. Боли локализуются у правого подреберья, подложечной области. Может быть лихорадка.
При обследовании выявляется желтуха, гепатомегалия, лихорадка. Область расположения органа болезненна при пальпации, гладкая. У части больных увеличивается селезенка, появляется ладонный рубероид (эритема), кожные сосудистые звездочки, тремор рук (астериксис), что является признаком печеночной энцефалопатии, нарушение психики (заторможенность, возбуждение, галлюцинации), асцит, устойчивый к диуретикам.
Отмечаются сопутствующие инфекции: пневмония, пиелонефрит, активный туберкулез. Холестатический вариант с кожным зудом, светлым калом, темной мочой встречаются редко. Кровь характеризует выраженная гипербилирубинемия, гиперхолестеринемия, повышение активности щелочной фосфатазы, гаммаглютамилтранспептидазы, незначительное повышение AST, ALT.
Выделяют молниеносный (фульминантный) острый алкогольный гепатит, который протекает тяжело, часто с неблагоприятным прогнозом, латентный вариант с бессимптомным течением. Всегда наблюдается лейкоцитоз со сдвигом влево, резкое увеличение СОЭ.
Прогностически неблагоприятными симптомами является печеночная энцефалопатия, гепаторенальный синдром, удлинение протромбинового времени более чем на 50%, рецидивы острого гепатита на стадии сформировавшегося цирроза. Прогноз наиболее благоприятен при латентной форме острого гепатита.
Выздоровление возможно при полном отказе от алкоголя, но это не всегда гарантирует отсутствие впоследствии цирроза.
Хронический гепатит делят на персистирующий и активный легкой, средней, тяжелой степени, чаще всего представляющие собой стадии прогрессирования острого гепатита.
Хронический персистирующий гепатит гистоморфологически проявляется перицеллюлярным и субсинусоидальным фиброзом, тельцами Мэллори, баллонной дистрофией гепатоцитов. Подобная картина без прогрессирования фиброза может сохраняться 5-10 лет даже при умеренном употреблении алкоголя.
Хронический персистирующий гепатит сопровождается умеренными болями живота, вздутием, анорексией, неустойчивым стулом, отрыжкой, изжогой. Печеночный орган увеличен незначительно, уплотнен. Диффузное уплотнение, увеличение подтверждается данными УЗИ. Умеренно повышается активность гаммаглютамилтранспептидазы, трансаминаз сыворотки крови, а иногда тимоловой пробы.
Хронический активный гепатит имеет вышеописанную гистоморфологическую картину алкогольного гепатита с наличием более или менее выраженным активным фиброзом, склерозирующим гиалиновым некрозом. Воздержание от алкоголя на протяжение 3-6 мес. приводит к улучшению морфологической картины по типу хронического неалкогольного гепатита. Для хронического активного гепатита при наличии аутоиммунной деструкции паренхимы характерно прогрессирование процесса с переходом к циррозу.
Клинические проявления более яркие, чем при персистируюшем гепатите. Чаще наблюдается желтуха, спленомегалия (при переходе в цирроз орган резко может уменьшиться). Значительно повышается билирубин, гаммаглютамилтранспептидаза, иммуноглобулин А, умеренно тимоловая проба, трансаминазная активность крови.
При электронно-микроскопическом исследовании биоптатов, взятых у больных хроническим алкоголизмом, алкогольный гиалин выявляется как фибриллярный или гранулярный материал. Фибриллы гиалина короче и толще нормальных тонофиламентов. Образование телец Мэллори в гепатоцитах описано при ряде заболеваний неалкогольной этиологии: сахарном диабете, индийском детском циррозе, болезни Вильсона-Коновалова, первичном билиарном циррозе, раке печени, после операции наложения кишечного анастомоза по поводу ожирения.
Характерные ультраструктурные изменения гепатоцитов и звездчатых ретикулоэндотелиоцитов отражают токсическое воздействие этанола на организм.
Изменения гепатоцитов представлены гиперплазией, вакуолизацией элементов гладкой цитоплазматической сети, образованием гигантских митохондрий, имеющих неправильную форму. Изменения звездчатых ретикулоэпителиоцитов свидетельствуют о несостоятельности их фагоцитарной функции: цитолемма их не образует выростов, единичные лизосомы с электронно-светлым содержанием.
Постоянно встречающимися морфологическими маркерами воздействия этанола на печень являются:
Важное диагностическое значение при хронических гепатитах (алкогольных, как любой другой этиологии) имеет проведение УЗИ органов брюшной полости (печени, селезенки и других органов), а также на предмет выявления асцита и размеров воротной вены. Ультразвуковая допплерография должна выполняться для исключения или установления степени выраженности портальной гипертензии. Традиционно продолжают применять при диагностическе радионуклидную гепатоспленосцинтиграфию.
Алкогольная жировая дистрофия печени [жирная печень] (K70.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Алкогольная жировая печень (стеатоз печени), согласно общей классификации алкогольных поражений печени (Логинов А.С., Джалалов К.Д., Блок Ю.Е.), разделяется на следующие формы:
1. Без фиброза.
2. С фиброзом.
3. В сочетании с острым алкогольным гепатитом.
4. С внутрипеченочным холестазом.
5. С гиперлипемией и гемолизом (синдром Циве).
Этиология и патогенез
Патоморфология
При внешнем осмотре печень большая, желтая с жирным блеском; гепатоциты нагружены жиром, признаков воспаления или фиброза не обнаруживается. Жировая дистрофия печени диагностируется, когда содержание жира в печени превышает 10% ее влажной массы, при этом более 50% печеночных клеток содержат жировые капли, размеры которых достигают величины ядра печеночной клетки или превышают его. Жировой дистрофии часто сопутствует умеренный сидероз звездчатых ретикулоэндотелиоцитов.
Эпидемиология
Признак распространенности: Распространено
Соотношение полов(м/ж): 0.5
Возраст: преимущественно 20-60 лет.
Раса: лица белой расы имеют статистически более низкую скорость развития всех форм алкогольной болезни печени.
Пол: считается, что женщины более подвержены риску заболевания. Имеется несколько гипотез на этот счет (гормональный фон, низкое содержание алкогольдегидрогеназы в слизистой желудка, высокое содержание аутоантител к слизистой желудка у пьющих женщин), но ни одна из них не нашла подтверждения.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Алкогольный стеатоз обычно протекает бессимптомно у амбулаторных больных.
Тщательный анамнез, особенно в отношении количества потребления алкоголя, имеет важное значение для определения роли алкоголя в этиологии ненормальных результаты тестов печени. Опрос членов семьи может выявить связанные с алкоголем проблемы в прошлом.
Американская ассоциация по изучению заболеваний печени (AASLD) в рекомендациях 2010 года акцентирует внимание на важность использования специальных опросников для выяснения анамнеза у пациентов, в отношении которых данные анамнеза, собранные обычными способами, кажутся недостоверными. Также применение опросника рекомендуется в случаях подозрительных (клинически, лабораторно, инструментально) на алкогольный стеатоз печени.
Диагностика
Критерием диагностики алкогольной жировой дистрофии печени является наличие алкогольного анамнеза и гистологическое исследование биоптата. Диагноз считается обоснованным, если не менее 50% гепатоцитов содержат крупные липидные вакуоли, оттесняющие ядро клетки к периферии цитоплазмы (см. раздел «Этиология и патогенез»). Однако на практике к биопсии прибегают довольно редко и ведущими методиками подтверждения диагноза являются методы визуализации.
1. УЗИ:
— различная эхогенность структуры паренхимы печени (при неалкологольном стеатозе, как правило, отмечаются только яркие гиперэхогенные изменения);
— для алкогольного стеатоза печени характерна сонографическая картина как очагового, так и диффузного поражения (на стадии алкогольного гепатита отмечается только диффузное поражение).
Алкогольный стеатоз печени, как и любой другой стеатоз, идентифицируется УЗИ только при наличии более 30% поражения ткани печени. Чувствительность метода около 75%.
2. Компьютерная томография, магнитно-резонансная томография являются чувствительными методами, однако не свидетельствуют в пользу именно алкогольной этиологии стеатоза.
Лабораторная диагностика
2. Возможно повышение уровня щелочной фосфатазы (около 20-40% пациентов) в диапазоне 200-300%.
3. Гипербилирубинемия (выявляется у 30-35% пациентов), связанная по-видимому с алкогольным гемолизом или сопутствующим холестазом.
Примечания
2. Изменения в определении натощак инсулина и уровня глюкозы должны насторожить врача относительно потенциального нарушения толерантности к глюкозе, которое нередко сопутствует стеатозу.
3. У большинства пациентов присутствует нерезкое снижение поглотительно-экскреторной функции печени по данным бромсульфалеиновой пробы (в настоящее время применяется редко).
Cемейные формы функциональных гипербилирубинемий в работе практического врача
Ребенок с синдромом Криглера — Найяра I типа Пациенты с функциональными гипербилирубинемическими состояниями длительное время (по нашим данным, от 6 месяцев до 3 лет и более) наблюдаются с первоначально ошибочными диагнозами. Таблица
 |
| Ребенок с синдромом Криглера — Найяра I типа |
Пациенты с функциональными гипербилирубинемическими состояниями длительное время (по нашим данным, от 6 месяцев до 3 лет и более) наблюдаются с первоначально ошибочными диагнозами.
Известно, что синдром желтух у детей представлен массой состояний. И если гемолитические, гепатитные и, реже встречающие в детском возрасте, механические (хирургические = подпеченочные) желтухи хорошо известны педиатрам и учитываются в дифференциальной диагностике, то так называемые семейные формы (функциональные гипербилирубинемические синдромы) чаще описываются в разделе казуистики [3, 4]. Но по мере изменения структуры заболеваемости на первый план выдвигаются наследственные синдромы. Пациенты с функциональными гипербилирубинемическими состояниями, прежде всего дети, длительное время (по нашим данным, от 6 мес. до 3 лет и более) наблюдаются с первоначально ошибочными диагнозами (гепатиты и т. п.). Между тем вспомнить о заболевании — это значит на 50% его диагностировать.
В связи с этим мы решили обобщить данные литературы и результаты собственных наблюдений.
По времени манифестации и тяжести проявлений одно из первых мест занимает синдром Криглера — Найяра [1].
Синдром Криглера — Найяра тип I — врожденная семейная негемолитическая желтуха с ядерной желтухой в результате полного отсутствия уридин-дифосфат-глюкоронилтрансферазы (УДФГТ) при нормальных функциях печени и отсутствии признаков гемолиза или резус-конфликта.
Патогенез заболевания заключается в отсутствии или резком снижении активности УДФГТ [6], в результате чего значительно повышается сывороточный уровень неконъюгированного жирорастворимого билирубина. Он связывается с альбумином, диффундирует через плацентарный и гематоэнцефалический барьеры (последнее — только у новорожденных). Связывающая (своеобразная буферная, компенсаторная емкость) альбумина уменьшается и соответственно клиническое течение синдрома ухудшается при гипоальбуминемии, ацидозе, увеличении концентрации органических ионов, назначении гепарина, салицилатов, сульфаниламидов, употреблении свободных жирных кислот. Проникновение несвязанного, неконъюгированного билирубина в клетки и митохондрии ведет к блокаде окислительно-фосфорилирующих реакций, особенно в гипоталамусе, хвостатом ядре, подкорковых ядрах, мозжечке.
| По частоте среди врожденных функциональных билирубинемий на первом месте стоит синдром Жильбера. Наш опыт работы в многопрофильных педиатрической и терапевтической клиниках показал, что в каждой из них за год выявляется порядка 10—20 случаев синдрома. |
Дифференциальная диагностика (ДД) проводится с синдромами Жильбера — Мойленграхта, Дабина — Джонса, Ротора, Люси — Дрисколла, ядерной желтухой новорожденных любой другой этиологии, врожденными циррозами печени и гепатитами, атрезией желчных ходов или тонкого кишечника (см. табл.).
Значительно благоприятней протекает синдром Криглера — Найяра типа II. Определение его [7] почти в точности повторяет синдром Криглера — Найяра типа I (врожденная семейная негемолитическая желтуха с ядерной желтухой при нормальных функциях печени), с той лишь разницей, что УДФГТ присутствует, хотя активность фермента значительно снижена. Уровень неконъюгированного билирубина может колебаться в пределах 60— 250 мг/л, фекального уробилиногена — 200—800 мг/л. Эффект от применения фототерапии и индукторов микросомальных ферментов хороший. Желтуха редко достигает степени ядерной, больные доживают до 50 и более лет, но в отделенном периоде, особенно при запоздалом лечении, нередки случаи глухоты, хореоатетоза, нейромышечных и личностых отклонений, гипоплазии зубов.
По частоте среди врожденных семейных функциональных билирубинемий на 1-м месте стоит синдром Жильбера. Наш опыт работы в многопрофильных — педиатрической и терапевтической — клиниках показал, что в каждой из них за год выявляется порядка 10 — 20 случаев синдрома. Но истинная частота, видимо, выше, поскольку диагностика заболевания строится главным образом на данных клиники и функциональной пробы с голоданием, а «клиническая мягкость» не привлекает внимание врача. Так, С. Д. Подымова [5] считает, что синдром Жильбера имеют не менее 1— 5% населения. Наблюдая таких больных, мы пришли к заключению, что синдром ассоциируется с генерализованной дисплазией соединительной ткани (особенно часто по типу синдромов Марфана и Элерса — Данлоса).
Патогенез синдрома неоднозначный. Обнаруживается небольшое снижение активности УДФГТ (на 10 — 30% по сравнению с нормой), однако основное значение придается нарушению захвата билирубина гепатоцитами. Последнее связывают с аномалией проницаемости мембран и с дефектом белка внутриклеточного транспорта. Эта гетерогенность клиренса билирубина проявляется также вариабельностью таких тест-субстратов, как бромсульфталеин и индоцианин зеленый.
Клинически для синдрома характерна субиктеричность различной степени выраженности. Чаще это выражается в иктеричности склер, матовой желтушности кожи, особенно лица, иногда частичном пожелтении стоп и ладоней, подмышечных впадин и носогубного треугольника. Нередко больные жалуются на общую слабость, подавленность, плохой сон, трудность концентрации внимания. Влияние голода на повышение содержания билирубина в сыворотке известно и для здоровых, но значительно выражено при синдроме Жильбера. С целью его выявления проводят пробу с голоданием. В течении 48 часов больной получает питание энергетической ценностью 400 ккал/сутки. В день начала пробы утром натощак и спустя 2 суток определяют билирубин сыворотки крови. При подъеме его на 50 — 100% проба считается положительной.
В последнее время многие специалисты полностью идентифицируют его с синдромом Мойленграхта, рассматривая их как одно состояние — синдром Жильбера — Мойленграхта — и определяют его как доброкачественную семейную конституциональную гибербилирубинемию в результате аномалии ферментов печени [7]. Большое значение для диагноза имеет семейный анамнез (легкая желтушность у членов семьи больного). Клиническая картина проявляется интермиттирующей мало выраженной желтухой, никогда не сопровождающейся ядерной. Желтуха усиливается при голодании, о чем говорилось выше, физических перегрузках, оперативных вмешательствах, употреблении алкоголя, инфекционных заболеваниях. Больных беспокоят тошнота, чувство переполнения желудка, тяжесть в эпигастрии, боли в правом подреберье, запоры или диспепсии. Почти у половины больных обнаруживается скрытый гемолиз (группа риска по холелитиазу!). Наряду с уже упомянутыми неврологическими расстройствами в рамках общей дисплазии соединительной ткани, свойственной этим больным, описывают и такие проявления, как пылающие и пигментные невусы, пигментация век, брадикардия и артериальная гипотония. Применение индукторов микросомальных ферментов очень эффективно. Прогноз хороший. Диагноз строится на клиническом исследовании и лабораторно-функциональных пробах. Гистологические находки (см. табл.) неспецифичны и обнаруживаются далеко не всегда. Поэтому ввиду общего нетяжелого состояния пациентов пункционная биопсия печени вряд ли оправданна (напомним, что риск обследования не должен превышать риска неустановленного диагноза и что прежде больные погибали от болезни, позже от лечения, а сейчас — от обследования).
ДД проводится со всеми типами неконъюгированной билирубинемии, синдромом Криглера — Найяра типа II, гемолитическими анемиями, шунтовыми гипербилирубинемиями (неэффективный гемопоэз с интрамедуллярным образованием значительного количества билирубина = талассемия, пернициозная анемия), постгепатической персистирующей гипербилирубинемией.
Синдром Дабина — Джонса — семейное нарушение выведения конъюгированного билирубина в желчные ходы, сочетающееся с отложением пигмента в печеночных клетках и умеренным увеличением печени («шоколадная печень»). При нем отсутствует нарушение глюкоронирования. Патогенез заключается в недостаточности транспорта конъюгированного билирубина внутрь и из гепатоцита. Билирубин попадает в кровь, его уровень в крови повышается, затем он усиленно выводится через почки. Заболевание может дебютировать в любом возрасте (разная пенетрантность гена?), но нередко проявляется после приема гормональных противозачаточных препаратов или при беременности.
| Влияние голода на повышение содержания билирубина в сыворотке известно и для здоровых людей, но значительно выражено при синдроме Жильбера. С целью его выявления проводят пробу с голоданием. В течение 48 часов больной получает питание энергетической ценностью 400 ккал/сутки. В первый день пробы натощак и спустя двое суток определяют билирубин сыворотки крови. При подъеме его на 50 — 100% проба считается положительной. |
Клинически ВВ проявляется в рецидивирующих периодах желтухи разной степени выраженности, но, как правило, не сопровождается зудом; увеличение размеров печени, а затем и селезенки умеренное. Функциональные печеночные пробы не изменены или изменены незначительно, однако наблюдается замедленное выведение контраста в желчный пузырь, повышение уровня копропорфирина I и снижение уровня копропорфирина III в моче. Гистологически в рибосомах печени откладывается меланиноподобный пигмент от желто-коричневого до черного цвета. Купферовские клетки остаются свободными, а соединительная ткань не разрастается.
ДД проводится со всеми формами конъюгированной и неконъюгированной гипербилирубинемии с желтухой: синдромы Жильбера — Мойленграхта, Ротора, Кароли (кистозное расширение внутрипеченочных желчных ходов), гепатиты, первичный билиарный цирроз, холестаз, синдром (симптомокомплекс) Циве. Синдром Циве — симптомокомплекс с гемолитической анемией, гиперлипидемией и желтухой, развивающийся у пациентов с неумеренным потреблением алкоголя. Он обусловлен увеличенным содержанием С16- и С18-жирных кислот в оболочке эритроцитов при уменьшении содержания длинноцепочечных ненасыщенных кислот. Провоцирующим фактором разрушения эритроцитов чаще является употребление алкоголя, после чего развиваются гемолиз и гиперлипидемия. Клинически синдром проявляется в основном после алкогольных эксцессов и сопровождается усиливающимися болями в правом подреберье и/или эпигастрии, лихорадкой, тошнотой, рвотой, потерей аппетита, увеличением размеров печени, а нередко и селезенки. При лабораторных исследованиях — повышение активности трансаминаз, щелочной фосфатазы, гамма-глютамилтрансферазы, анемия с манифестным или скрытым гемолизом, гиперхолестеринемия и/или гипертриглицеридемия. Гистологически — алкогольная жировая дистрофия печени с циррозом или без.
Формой синдрома Дабина — Джонса (или самостоятельной нозологической единицей?) является синдром Бюрка. При этом также обнаруживается липохромный гепатоз, но БЕЗ желтухи, хотя и СО ЗНАЧИТЕЛЬНОЙ гепатоспленомегалией.
Синдром Ротора — идиопатическая семейная доброкачественная гипербилирубинемия с адекватным повышением конъюгированного и неконъюгированного билирубина.
Патогенез заключается в нарушенном захвате неконъюгированного билирубина гепатоцитами, изменении его глюкоронирования и выведении с последующим рефлюксом билирубина в кровь.
Клинически синдром проявляется хронической желтухой (или субиктеричностью) кожи и слизистых. При этом ее интенсивность флюктуирует, увеличения размеров печени и селезенки не наблюдается. Гистологическая картина печени при световой микроскопии не изменена, при электронной микроскопии — митохондрии различных размеров, в фаголизосомах — пигментные тельца в виде решетчатообразных включений [8].
Диагнозы постгепатической доброкачественной гипербилирубинемии и физиологической желтухи новорожденных, постпрандиальных желтух (длительное употребление большого количества тугоплавких жиров), как прогностически благоприятные, строятся на принципе исключения более тяжелых вариантов гипербилирубинемий. Можно предположить, что подобные состояния связаны с маломанифестными ферментными аномалиями или аномалиями развития желчного пузыря (перетяжки, перегибы, особенно — в области сифона, сужения холедоха, приводящие к повышению давления в желчных ходах и избыточной нагрузке на гепатоцит).
| Синдром Дабина — Джонса может дебютировать в любом возрасте (разная пенетрантность гена?), но нередко проявляется после приема гормональных противозачаточных препаратов и при беременности. |
Семейный доброкачественный возвратный холестаз = синдром Аагенеса = Саммерскилла-Тигструппа = норвежский холестаз = холестаз с лимфедемами. Само обилие синонимов говорит о редкости синдрома: каждый вновь описываемый случай представляется авторам как открытие. Поскольку он редко встречается в литературе, определить истинную его распространенность весьма сложно. В основном он известен из описаний скандинавских авторов. Вероятно, патогенез заключается в гипоплазии лимфатических сосудов печени и других органов.
Клинически синдром проявляется как холестаз (наиболее чувствительный и специфический фермент холестаза — лейцин-аминопептидаза) уже в неонатальном периоде. Затем холестаз самостоятельно уменьшается, рецидивируя у взрослых. Медленно развиваются лимфатические отеки. Типичны гепатомегалия и нарушение функций печени. Гистологически он выражен внутрипеченочным холестазом с гигантоклеточной трансформацией.
Хронический холестаз сопровождается дефицитом жирорастворимых витаминов. Дефицит витамина Е приводит к прогрессирующей мозжечково-спинальной дегенерации (синдром Пермуттера).
ДД синдрома Аагенеса проводится со всеми синдромами холестаза и врожденных лимфатических отеков (синдромы Милроя, Вевера — Смита).
Злокачественный семейный холестаз (болезнь Байлера = синдром Клейтон — Юберга). В подавляющем большинстве случаев проявляется на 1-м году жизни [1]. Вначале холестаз (желтуха) самостоятельно разрешается через несколько недель или месяцев. Затем интенсивность желтухи нарастает, присоединяется мучительный зуд. Печень и селезенка существенно увеличиваются. В результате поражения паренхимы печени возникает геморрагический синдром. Эхографически печень выглядит плотной, напоминает цирротическую, в просвете желчного пузыря наблюдается густой застой. Прогноз плохой.
ДД проводят со всеми синдромами холестаза и синдромом Алажиль.
Синдром Люси — Дрисколл — аутосомно-рециссивно наследуемое редкое состояние, проявляющееся массивной гипербилирубинемией, развивающейся у всех детей, рожденных от одной матери страдающей этим заболеванием, в первые четыре дня их жизни.
Патогенез заключается в наличии фактора — ингибитора конъюгации билирубина в крови и моче матери и постнатально в крови и моче детей. Сыворотка таких матерей ингибирует in vitro конъюгацию билирубина в 5 — 7 раз сильнее, чем сыворотка женщин, не являющихся кондукторами данного синдрома. Вероятно, подобный фактор представлен стероидом, но он до сих пор не идентифицирован. Клиническая картина соответствует тяжелой гипербилирубинемии вплоть до ядерной желтухи.
ДД проводится с синдромами Криглера — Найяра типов I и II, новобиоциновой желтухой, эстрогеновой (транзиторная желтуха детей, вскармливаемых грудным молоком) и окситоциновой желтухой.
Лечение семейных функциональных гипербилирубинемий проводится по следующим принципам:
Литература
1. Алажиль Д., Одъевр М. Заболевания печени и желчных путей у детей. М.: Медицина, 1982. — 486 с.
2. Асоян А. В. Применение гипербарической оксигенации в комплексном лечении гипербилирубинемии у новорожденных с гемолитической болезнью. Автореф. дис. к. м. н. М., 1985. — 24 с.
3. Гасан Абу-Джабаль. Хронический гастродуоденит у детей на фоне дисплазии соединительной ткани. Автореф. дис. к. м. н. М., 1997. — 24 с.
4. Имамбаев С.Е. Эхография в диагностике заболеваний желчевыводящей системы у детей. Автореф. дис. к. м. н. М., 1986. — 24 с.
5. Подымова С. Д. Болезни печени. М.: Медицина, 1993. — 544 с.
6. Emery A., Rimoin D. (Ed.) Principles and practice of medical Genetics. London, Vv. 1, 2. — 1983.
7. Leiber B. Die klinischen Syndrome. Muenchen. — 1990.
8. Moelbert E., Marx R. Elektronenmikroskopiesche Untersuchungen am Lebergewebe beim Rotor-Syndrom. Acta hepato-splenoloy, 1966. — 13. — ss. 160 — 175.

