Что такое периодическая система менделеева
Что такое периодическая система менделеева
Выдающийся русский учёный, химик, физик и энергетик. Самым значимым его вкладом в науку стало открытие периодического закона, графическое выражение которого получило название Периодической системы химических элементов.
Периодический закон
К середине XIX века учёные располагали множеством сведений о физических и химических свойствах разных элементов и их соединений. Появилась необходимость упорядочить эти знания и представить их в наглядном виде. Исследователи из разных стран пытались создать классификацию, объединяя элементы по сходству состава и свойств веществ, которые они образуют. Однако ни одна из предложенных систем не охватывала все известные элементы.
Пытался решить эту задачу и молодой русский профессор Д.И. Менделеев. Он собирал и классифицировал информацию о свойствах элементов и их соединений, а затем уточнял её в ходе многочисленных экспериментов. Собрав данные, Дмитрий Иванович записал сведения о каждом элементе на карточки, раскладывал их на столе и многократно перемещал, пытаясь выстроить логическую систему. Долгие научные изыскания привели его к выводу, что свойства элементов и их соединений изменяются с возрастанием атомной массы, однако не монотонно, а периодически.
Так был открыт периодический закон, который учёный сформулировал следующим образом: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Своё открытие Менделеев совершил почти за 30 лет до того, как учёным удалось понять структуру атома. Открытия в области атомной физики позволили установить, что свойства элементов определяются не атомной массой, а зависят от количества электронов, содержащихся в нём. Поэтому современная формулировка закона звучит так:
Свойства химических элементов, а также формы и свойства образуемых ими веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов.
Этот принцип Менделеев проиллюстрировал в таблице, в которой были представлены все 63 известных на тот момент химических элемента. При её создании учёный предпринял ряд весьма смелых шагов.
Во-первых, многочисленные эксперименты позволили Менделееву сделать вывод, что атомные массы некоторых элементов ранее были вычислены неправильно, и он изменил их в соответствии со своей системой.
Во-вторых, в таблице были оставлены места для новых элементов, открытие которых учёный предсказал, подробно описав их свойства.
Мировое научное сообщество поначалу скептически отнеслось к открытию русского химика. Однако вскоре были открыты предсказанные им химические элементы: галлий, скандий и германий. Это разрушило сомнения в правильности системы Менделеева, которая навсегда изменила науку. Там, где раньше учёному требовалось провести ряд сложнейших (и даже не всегда возможных в реальности) опытов — теперь стало достаточно одного взгляда в таблицу.
Существует легенда, якобы знаменитая таблица явилась Менделееву во сне. Но сам Дмитрий Иванович эту информацию не подтвердил. Он действительно нередко засиживался над работой до поздней ночи и засыпал, продолжая размышлять над решением задачи, однако факт мистического озарения во сне учёный отрицал: «Я над ней, может быть, двадцать лет думал, а вы думаете, сел и вдруг — готово!».
Теперь расскажем, как устроена Периодическая таблица элементов Менделеева и как ею пользоваться.
Структура Периодической системы элементов
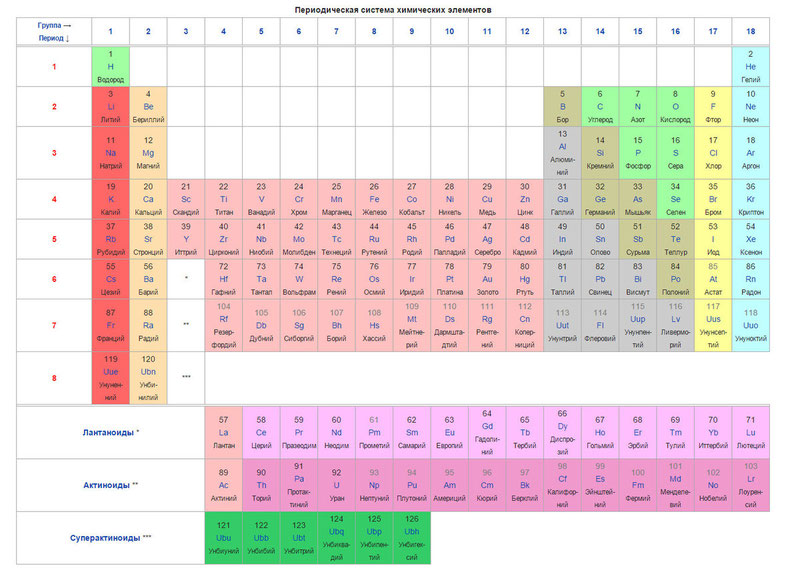
На настоящий момент Периодическая таблица Менделеева содержит 118 химических элементов. Каждый из них занимает своё место в зависимости от атомного числа. Оно показывает, сколько протонов содержит ядро атома элемента и сколько электронов в атоме находятся вокруг него. Атом каждого последующего элемента содержит на один протон больше, чем предыдущий.
Периоды — это строки таблицы. На данный момент их семь. У всех элементов одного периода одинаковое количество заполненных электронами энергетических уровней.
Группы — это столбцы. В группы в Периодической таблице объединяются элементы с одинаковым числом электронов на внешнем энергетическом уровне их атомов. В кратком варианте таблицы, используемой в школьных учебниках, элементы разделены на восемь групп. Каждая из них делится на главную (A) и побочную (B) подгруппы, которые объединяют элементы со сходными химическими свойствами.
Каждый элемент обозначается одной или двумя латинскими буквами. Порядковый номер элемента (число протонов в его ядре) обычно пишется в левом верхнем углу. Также в ячейке элемента указана его относительная атомная масса (сумма масс протонов и нейтронов). Это усреднённая величина, для расчёта которой используются атомные массы всех изотопов элемента с учётом их содержания в природе. Поэтому обычно она является дробным числом.
Чтобы узнать количество нейтронов в ядре элемента, необходимо вычесть его порядковый номер из относительной атомной массы (массового числа).
Свойства Периодической системы элементов
Расположение химических элементов в таблице Менделеева позволяет сопоставлять не только их атомные массы, но и химические свойства.
Вот как они изменяются в пределах группы (сверху вниз):
В пределах периодов (слева направо) свойства элементов меняются следующим образом:
Элементы Периодической таблицы Менделеева
По положению элемента в периоде можно определить его принадлежность к металлам или неметаллам. Металлы расположены в левом нижнем углу таблицы, неметаллы — в правом верхнем углу. Между ними находятся полуметаллы. Все периоды, кроме первого, начинается щелочным металлом. Каждый период заканчивается инертным газом.
Щелочные металлы
Первая группа главная подгруппа элементов (IA) — щелочные металлы. Это серебристые вещества (кроме цезия, он золотистый), настолько мягкие, что их можно резать ножом. Поскольку на их внешнем электронном слое находится только один электрон, они очень легко вступают в реакции. Плотность щелочных металлов меньше плотности воды, поэтому они в ней не тонут, а бурно реагируют с образованием щёлочи и водорода. Реакция идёт настолько энергично, что водород может даже загореться или взорваться. Эти металлы настолько активно реагируют с кислородом в воздухе, что их приходится хранить под слоем керосина (а литий — под слоем вазелина).
Учите химию вместе с домашней онлайн-школой «Фоксфорда»! По промокоду CHEMISTRY892021 вы получите бесплатный недельный доступ к курсам химии за 8 класс и 9 класс.
Щелочноземельные металлы
Вторая группа главная подгруппа (IIА) представлена щелочноземельными металлами с двумя электронами на внешнем энергетическом уровне атома. Бериллий и магний часто не относят к щелочноземельным металлам. Они тоже имеют серебристый оттенок и легко взаимодействуют с другими элементами, хотя и не так охотно, как металлы из первой группы главной подгруппы. Температура плавления щелочноземельных металлов выше, чем у щелочных. Ионы магния и кальция обусловливают жёсткость воды.
Лантаноиды и актиноиды
В третьей группе побочной подгруппе (IIIB) шестого и седьмого периодов находятся сразу несколько металлов, сходных по строению внешнего энергетического уровня и близких по химическим свойствам. У этих элементов электроны начинают заполнять третий по счёту от внешнего электронного слоя уровень. Это лантаноиды и актиноиды. Для удобства их помещают под основной таблицей.
Лантаноиды иногда называют «редкоземельными элементами», поскольку они были обнаружены в небольшом количестве в составе редких минералов и не образуют собственных руд.
Актиноиды имеют одно важное общее свойство — радиоактивность. Все они, кроме урана, практически не встречаются в природе и синтезируются искусственно.
Переходные металлы
Элементы побочных подгрупп, кроме лантаноидов и актиноидов, называют переходными металлами. Они вполне укладываются в привычные представления о металлах — твёрдые (за исключением жидкой ртути), плотные, обладают характерным блеском, хорошо проводят тепло и электричество. Валентные электроны их атомов находятся на внешнем и предвнешнем энергетических уровнях.
Неметаллы
Правый верхний угол таблицы до инертных газов занимают неметаллы. Неметаллы плохо проводят тепло и электричество и могут существовать в трёх агрегатных состояниях: твёрдом (как углерод или кремний), жидком (как бром) и газообразном (как кислород и азот). Водород может проявлять как металлические, так и неметаллические свойства, поэтому его относят как к первой, так и к седьмой группе Периодической системы.
Подгруппа углерода
Четвёртую группу главную подгруппу (IVА) называют подгруппой углерода. Углерод и кремний обладают всеми свойствами неметаллов, германий и олово занимают промежуточную позицию, а свинец имеет выраженные металлические свойства. Углерод образует несколько аллотропных модификаций — вариантов простых веществ, отличающихся по своему строению, а именно: графит, алмаз, фуллерит и другие.
Большинство элементов подгруппы углерода — полупроводники (проводят электричество за счёт примесей, но хуже, чем металлы). Графит, германий и кремний используют при изготовлении полупроводниковых элементов (транзисторы, диоды, процессоры и так далее).
Подгруппа азота
Пятую группу главную подгруппу (VA) называют пниктогенами или подгруппой азота. В ходе реакций эти элементы могут как отдавать электроны, так и принимать их, завершая внешний энергетический уровень.
Физические свойства элементов подгруппы азота различны. Азот является бесцветным газом. Фосфор, мягкое вещество, образует несколько вариантов аллотропных модификаций — белый, красный и чёрный фосфор. Мышьяк — твёрдый полуметалл, способный проводить электрический ток. Висмут — блестящий серебристо-белый металл с радужным отливом.
Азот — основное вещество в составе атмосферы нашей планеты. Некоторые элементы подгруппы азота токсичны для человека (фосфор, мышьяк, висмут). При этом азот и фосфор являются важными элементами почвенного питания растений, поэтому они входят в состав большинства удобрений. Азот и фосфор также участвуют в формировании важнейших молекул живых организмов — белков и нуклеиновых кислот.
Подгруппа кислорода
Халькогены или подгруппа кислорода — элементы шестой группы главной подгруппы (VIA). Для завершения внешнего электронного уровня атомам этих элементов не хватает лишь двух электронов, поэтому они проявляют сильные окислительные (неметаллические) свойства. Однако, по мере продвижения от кислорода к полонию они ослабевают.
Кислород образует две аллотропные модификации — кислород и озон — тот самый газ, который образует экран в атмосфере планеты, защищающий живые организмы от жёсткого космического излучения.
Кислород и сера легко образуют прочные соединения с металлами — оксиды и сульфиды. В виде этих соединений металлы часто входят в состав руд.
Галогены
Седьмая группа главная подгруппа (VIIA) представлена галогенами — неметаллами с семью электронами на внешнем электронном слое атома. Это сильнейшие окислители, легко вступающие в реакции. Галогены («рождающие соли») назвали так потому, что они реагируют со многими металлами с образованием солей. Например, хлор входит в состав обычной поваренной соли.
Самый активный из галогенов — фтор. Он способен разрушать даже молекулы воды, за что и получил своё грозное имя (слово «фтор» переводится на русский язык как «разрушительный»). А его «близкий родственник» — иод — используется в медицине в виде спиртового раствора для обработки ран.
Инертные газы
Инертные газы, расположенные в последней, восьмой группе главной подгруппе (VIIIA) — элементы с полностью заполненным внешним электронным уровнем. Они практически не способны участвовать в реакциях. Поэтому их иногда называют «благородными», проводя параллель с представителями высшего общества, которые брезгуют контактировать с посторонними.
У инертных газов есть удивительная способность: они светятся под действием электромагнитного излучения, поэтому используются для создания ламп. Так, неон используется для создания светящихся вывесок и реклам, а ксенон — в автомобильных фарах и фотовспышках.
Гелий обладает массой всего в два раза больше массы молекулы водорода, но, в отличие от последнего, не взрывоопасен и используется для заполнения воздушных шаров.
У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.

Интересное по рубрике
Найдите необходимую статью по тегам
Подпишитесь на нашу рассылку
Мы в инстаграм
Домашняя онлайн-школа
Помогаем ученикам 5–11 классов получать качественные знания в любой точке мира, совмещать учёбу со спортом и творчеством

Рекомендуем прочитать
Реальный опыт семейного обучения
Звонок по России бесплатный
Посмотреть на карте
Если вы не нашли ответ на свой вопрос на нашем сайте, включая раздел «Вопросы и ответы», закажите обратный звонок. Мы скоро свяжемся с вами.
Таблица Менделеева: что это такое и как ей пользоваться
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.

Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.

В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
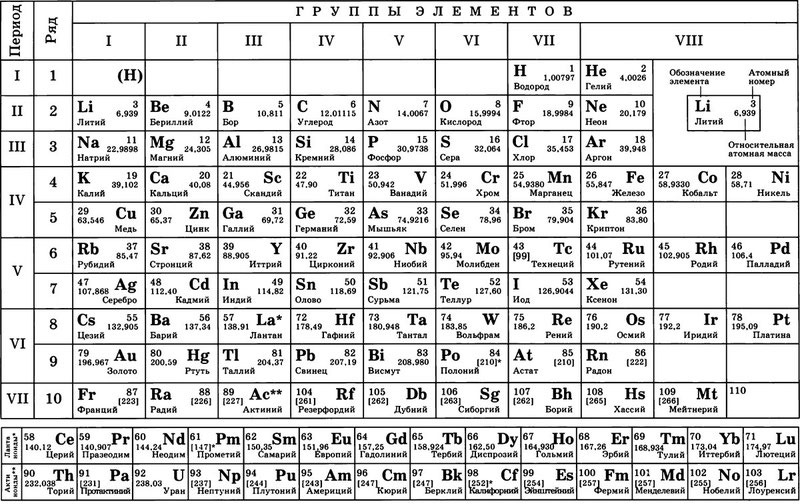
Ниже приведем саму таблицу
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.
Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс «Таблица Менделеева для чайников». В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе, который с радостью поделится с вами своими знаниями и опытом.
Иван Колобков, известный также как Джони. Маркетолог, аналитик и копирайтер компании Zaochnik. Подающий надежды молодой писатель. Питает любовь к физике, раритетным вещам и творчеству Ч. Буковски.
Периодическая система Менделеева
Если химические элементы расположить в порядке возрастания атомных номеров, то их химические свойства укладываются в определенную схему.
Дмитрий Иванович Менделеев любил рассказывать, что идея периодической системы пришла ему во сне. Как и многие химики середины XIX века, он пытался как-то систематизировать огромное количество открываемых химических элементов. Менделеев тогда работал над книгой «Основы химии», и ему все время казалось, что для веществ, которые он описывал, непременно должен существовать какой-то способ упорядочивания, который сделает их больше чем просто случайным набором элементов. Именно такой способ упорядочивания, такой закон он и увидел во сне.
В своей таблице (сегодня мы ее называем периодической таблицей, или системой, элементов) Менделеев расположил химические элементы по рядам в порядке возрастания их массы, подобрав длину рядов таким образом, чтобы химические элементы в одной колонке имели похожие химические свойства. Так, например, правая крайняя колонка таблицы содержит гелий, неон, аргон, криптон, ксенон и радон. Это благородные газы * — вещества, которые неохотно реагируют с другими элементами и проявляют низкую химическую активность. В противоположность этому, элементы самой левой колонки — литий, натрий, калий и др. — реагируют с другими веществами бурно, процесс носит взрывной характер. Аналогичные утверждения можно сделать и о химических свойствах элементов в других колонках таблицы — внутри колонки эти свойства подобны, но варьируются при переходе от одной колонки к другой.
Нельзя не отдать дань смелости мысли Менделеева, решившегося опубликовать свои результаты. С одной стороны, таблица в первоначальном виде содержала много пустых клеток. Элементы, о существовании которых мы сейчас знаем, тогда еще только предстояло открыть. (Действительно, открытие этих элементов, включая скандий и германий, стало одним из величайших триумфов периодической системы.) С другой стороны, Менделееву пришлось допустить, что атомные веса некоторых элементов были измерены неправильно, так как в противном случае они не вписались бы в систему. И опять оказалось, что он был прав.
Периодическая система в своем первом варианте просто отражала существующее в природе положение дел. Как и в случае с кеплеровскими законами движения планет, таблица никак не объясняла, почему это должно быть именно так. И только с появлением квантовой механики и, в особенности, принципа запрета Паули стал понятен истинный смысл расположения элементов в периодической таблице.
Сегодня мы смотрим на периодическую таблицу с точки зрения того, как электроны заполняют электронные слои в атоме (см. Принцип Aufbau). Химические свойства атома (то есть то, какого рода связи будут образованы с другими атомами) определяются числом электронов в наружном слое. Так, у водорода и лития только по одному внешнему электрону, поэтому в химических реакциях они ведут себя похоже. В свою очередь, гелий и неон оба имеют заполненные внешние оболочки, и тоже ведут себя похоже, но совершенно не так, как водород и литий.
Химические элементы вплоть до урана (содержит 92 протона и 92 электрона) встречаются в природе. Начиная с номера 93 идут искусственные элементы, созданные в лаборатории. Пока самый большой заявленный учеными номер — 118.
* Эти вещества назвали инертными газами, но название было изменено в 1962 году, когда было обнаружено, что ксенон может все-таки реагировать с фтором. — Прим. автора
Русский химик. Родился в Сибири, в городе Тобольске, в семье был младшим из 17 детей. Детство Менделеева было нелегким. Его отец, школьный учитель, ослеп, и матери, чтобы содержать семью, пришлось управлять стекольным заводом. Отец умер, когда Менделееву было 13 лет, затем сгорел завод, а после этого умерла мать. Свои научные знания мальчик почерпнул у мужа сестры.
Перед смертью мать определила Дмитрия в Педагогический институт в Санкт-Петербурге. Там Менделеев получил научную степень по химии и продолжил свое обучение во Франции и Германии. В Карлсруэ он встретил итальянского химика Станислава Канниццаро (Stanislao Cannizaro, 1826–1910), чья идея о разграничении понятий атомного и молекулярного веса произвела большое впечатление на русского ученого. Вернувшись в Санкт-Петербург, Менделеев в 1864 году стал профессором химии Технологического института.
Периодическая таблица, которую Менделеев составлял с конца 1860-х годов, не сразу получила признание, но впоследствии сделала его самым известным русским ученым. В 1890 году он высказался в поддержку студентов, выступавших за социальную реформу, за что был уволен из университета. Но больше всего судьба была несправедлива к Менделееву, когда в 1906 году ему не хватило всего одного голоса для получения Нобелевской премии в области химии. Премия досталась Анри Муассану (Henri Moissan, 1852–1907), которому удалось выделить фтор — всего лишь один химический элемент, в то время как Менделеев создал классификацию их всех.
Следующий грубейший научный промах Менделеева и его последователей: начало каждого периода щелочным металлом и окончание благородным газом. Ведь в первом периоде Периодической системы элементов в редакции Менделеева до 1902 года первым являлся не щелочной металл, а неметалл химически активный двух атомный газ водород, имеющий крайне низкую температуру кипения! В то время, как во всех последующих периодах первым был элемент группы щёлочноземельных металлов. Прокол в Периодической таблице элементов жутчайший! А в периодической таблице элементов в редакции Менделеева от 1902 и 1906 годов первым элементом в периодах являлся элемент группы благородных газов.
Тогда мировой науке официально следует принять то что первый правильный (естественный) период атомных уровней материи содержит 4 элемента, которые радикально отличаются друг от друга по физическим и химическим свойствам: водород (химический активный двух атомный газ), гелий (химически инертный одно атомный газ), литий (химически активный щелочной металл) и бериллий (химически активный щёлочноземельный металл-металлоид). Поэтому последние 4 элемента каждого последующего правильного (естественного) периода позиционно аналогичны неметаллу химически активному подобному галогенам двухатомному газу водороду, неметаллу химически инертному одноатомному газу гелию, химически активному щелочному металлу литию и химически активному щёлочноземельному металлу бериллию!
Смотрите подробности здесь:
Менделеева по справедливости не наградили Нобелевской Премией в 1906 году. Ведь его Периодическая таблица химических элементов грубо не верна в окончаниях всех периодов! Он даже не смог сформулировать ни одного настоящего периодического закона!
Теперь Комитет по присуждению Премии им. Альфреда Нобеля может с чистой душой, не опасаясь проявления со временем подвоха, присудить свою высокую Премию настоящему создателю Естественной системы элементов и открывателю целого пакета настоящих периодических законов россиянину Макееву Александру Константиновичу! Ау, нынешние Нобелевские Лауреаты, имеющие на то право, замолвите словечко в Нобелевский Комитет, пожалуйста!
Во всех школах и вузах России учат догматично, мировоззренчески-наркомански по таблице IUPAC от 1989 года и 2012 года. Эта таблица основана на таблице от 1905 года швейцарского химика Альфреда Вебера, где все периоды впервые на Земле были неправильно окончены на элементе группы благородных газов. Зато каждый из всех периодов, пусть и неправильных, представлялся одним рядом.
КАВЕРЗНЫЕ ГРАНИЦЫ ПЕРИОДОВ
Великий химик Менделеев
Всё призывал в науках мерить.
Без меры вся ж наука каша!
— Так изрекло светило наше.
Призвав других, он сам оплошал.
В Таблице периодов промах вдруг дал.
Элементы в ряды он построил,
И в группах столбцами достроил:
В начало строк – благородный газ,
Галогену в конец! – Был отдан приказ.
Поразмыслив всерьёз, диссидент
Изречёт: очень плох документ!
— Всяк период в конце с ошибкой!
Там на три элемента ошибка!
Ведь металлом щелочноземельным
Периодам быть завершеньем!
С наукой «Закон» стал в разладе.
– Себя не дал в цифирь приладить!
А раз формулы нет в цифири,
Не Закон он, как «мусор в квартире»!
Мы подводим всему делу итог,
Чему Светоч–Химик «царь» и «бог»:
Периодичности лишь Явление
Дмитрий открыл, без сомнения!
Но мир учёных незыблем,
Новатора довод не принял.
Как и прежде, Таблице молится,
А с диссидентами борется…
Мейер на восемь лет упредил,
Точно периоды нагородил,
Чарльз Жанет таблицу дополнил,
Но мало, кто сейчас это помнит…
Макеев Таблицу позже построил,
Все элементы на место пристроил.
По Жанету и Мейеру, которых не знал,
Но в границы периодов точно попал!

.jpg)

.jpg)

.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)