Что такое перекисное окисление липидов
Из липидов — в дирижеры клеточных реакций, или Как общаются клетки
Снимок конфокальной микроскопии эмбриональных фибробластов мыши, обработанных индуктором ферроптоза RSL3 (100 nM, 6h)
Авторы
Редакторы
Статья на конкурс «Био/Мол/Текст»: Задумывались ли вы когда-нибудь о том, что клетки общаются между собой? Ведь клеточный мир настолько многообразен и велик, что в нем без языка не обойтись! Всем известные гормоны — только один из диалектов такого «языка»! В этой статье мы расскажем о том, как липиды помогают клеткам «общаться». Почему такой, казалось бы, простой химический процесс, как окисление липидов, может приводить к гибели клетки? Как клетки понимают, когда пора заканчивать фазу воспаления и переходить к восстановлению? Что такое ферроптоз. Вы все еще читаете аннотацию? Давайте скорее окунемся в удивительный мир редокс-липидомики и взглянем на липиды по-новому!
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Давно известно, что без липидов человеческий организм не может существовать. Эта обширная группа природных органических соединений, включающая жиры и жироподобные вещества, необходима для построения клеточных мембран и регуляции обмена веществ. Изучением липидов занимается липидомика, а появление раздела «редокс-липидомика» (окислительно-восстановительная липидомика, часть липидомики, занимающаяся характеристикой окисленных липидов) позволило по-новому взглянуть на роль продуктов окисления липидов и оценить их влияние на ключевые процессы, происходящие в клетках.
О липидах в составе клеточных мембран читайте в статье «Липидный фундамент жизни» [1]. — Ред.
В дополнение к природному липидому (совокупности всех липидов организма), существуют виды липидов, полученные в результате ферментативных и неферментативных модификаций (эпилипидом), что делает общую картину еще более сложной, поскольку их функции все еще в значительной степени неизвестны. Окисленные липиды представляют собой фракцию эпилипидома, которая привлекла большое внимание ученых из-за их роли в возникновении и развитии многих заболеваний человека. Однако основной проблемой редокс-липидомики остается отсутствие оптимальных вычислительных инструментов для надежной, точной и специфической идентификации уже открытых и еще неизвестных модифицированных липидов. В настоящее время жидкостная хроматография и масс-спектрометрия являются основными методами, позволяющими определить количество липидов в клетке, оценить их участие в ряде физиологических механизмов и даже изучить структуру продуктов окисления этих веществ [2].
Знакомство с липидами
Молекулы липидов чрезвычайно разнообразны, их насчитывают более миллиона вариантов [3]! Впечатляющее количество, по сравнению с 70 000 выявленных белков и 30 000 генов! Для удобства химики разделили все липиды на две большие группы:
К первой группе относятся простые липиды, состоящие исключительно из спирта и жирных кислот (воски, триацилглицеролы, эфиры холестерола), и сложные липиды, в состав которых входят и другие компоненты (фосфолипиды, гликолипиды, сфинголипиды). К неомыляемым липидам относится большая группа стероидов, включающая холестерин и его производные: стероидные гормоны, витамины, желчные кислоты.
Большая роль маленьких молекул
Липиды, содержащие полиненасыщенные жирные кислоты (ПНЖК — кислоты, содержащие две и более двойных связей), являются важными сигнальными молекулами, регулирующими многие метаболические процессы и клеточные реакции, включая воспаление. Для выполнения этих функций они подвергаются реакциям окисления, то есть присоединяют кислородсодержащие группы.
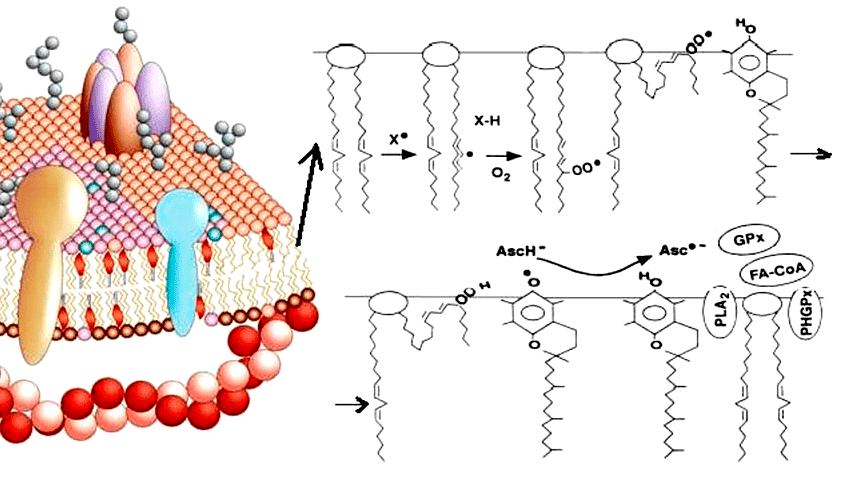
Окисление липидов происходит с помощью двух основных механизмов. Первый способ — неферментативное перекисное окисление. При этом липиды взаимодействуют с активными формами кислорода (АФК), в результате чего происходит накопление гидроперекисей липидов (LOOH) (рис. 1). В норме процессы перекисного окисления необходимы для поддержания структуры клеточных мембран, функционирования ионных каналов, рецепторов и ферментных систем. Их роль велика и в синтезе липидных медиаторов — биорегуляторов (простагландинов, тромбоксанов, лейкотриенов и др.). Однако неконтролируемое свободнорадикальное окисление липидов может приводить к изменению проницаемости мембраны, нарушению ее целостности, а это прямая угроза гибели клетки [3]!
Рисунок 1. Зарождение цепной реакции перекисного окисления липидов. Фосфолипиды клеточных мембран, взаимодействуя со свободными радикалами, превращаются в гидроперекиси липидов, что может влиять на функции мембраны клетки.
Второй путь окисления — ферментативные изменения, отличающиеся высокой селективностью и специфичностью. Ферментативное окисление происходит под действием металлопротеинов: липоксигеназы, циклооксигеназы, цитохрома Р450, пероксидазы. Продукты реакций окисления ПНЖК, выступая в качестве сигнальных молекул, координируют метаболизм и другие физиологические процессы, иными словами, управляют судьбой клетки [4]! Такие вещества носят название эйкозаноидов. Они принимают участие во многих важнейших процессах: росте мышечной ткани, реакциях иммунитета на токсины и патогены, выступают в роли нейромедиаторов и даже гормонов!
К сожалению, человеческий организм не научился синтезировать все необходимые ПНЖК. Возникает вопрос: можно ли их получить извне? Разумеется! Пищевыми источниками полиненасыщенных жирных кислот являются растительные масла, рыбий жир и препараты омега-3-жирных кислот. Таким образом, казалось бы невкусный рыбий жир — просто лакомство для наших клеток!
Из липидов — в дирижеры клеточных реакций
Исследования редокс-липидомики, проведенные при помощи масс-спектрометрии в сочетании с обращенно-фазовой хроматографией, выявили удивительный факт: липиды контролируют активность иммунной системы [4]! При попадании в организм чужеродных агентов, желающих нанести вред и повредить ткани, развивается воспаление, цель которого — устранить патоген. Иммунные клетки, встав на защиту организма, в зоне повреждения вырабатывают «провоспалительные» производные ПНЖК (лейкотриены, липоксины, гипоксины и т.д.), которые усиливают воспаление и таким образом избавляют организм от патогена (рис. 2).
Рисунок 2. Провоспалительные производные арахидоновой кислоты: простагландины, тромбоксаны и лейкотриены
рисунок авторов статьи
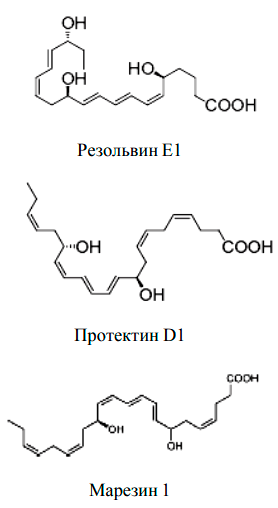
Рисунок 3. Противовоспалительные медиаторы: резолвины, протектины, марезины
Но воспаление — патологический процесс, и при удалении повреждающего фактора важно вовремя остановиться и прекратить воспалительный ответ. Здесь на помощь приходят противовоспалительные липидные медиаторы — резолвины, протектины, марезины (рис.3). Они останавливают образование «провоспалительных» медиаторов и обеспечивают защиту клеток от повреждающих факторов.
Кроме того, собственные поврежденные клетки, не способные восстановиться, для перехода воспаления в завершающую фазу и сохранения постоянства внутренней среды должны подвергнуться уничтожению, чему также способствуют липидные медиаторы. Как это возможно? Оказалось, что липидные молекулы фосфатидилсерина (фосфолипида клеточной мембраны) выставляются на мембрану поврежденных клеток и «помечают» их. Фосфатидилсерин на поверхности клеток является сигналом для их поглощения макрофагами и клетками микроглии [5]. В исследованиях также была продемонстрирована значимость этого медиатора: наличие даже одной молекулы фосфатидилсерина уже достаточно для активации фагоцитоза!
Две стороны одной медали
Оказалось, что роль липидов велика не только в уничтожении старых или поврежденных клеток, но и их компонентов, или органелл. Например, для удаления митохондрий, безвозвратно утративших свои функции, на поверхности ее внешней мембраны появляется кардиолипин — фосфолипид, который в норме присутствует только на внутренней мембране органелл. Именно он и служит сигналом митофагии, или уничтожения митохондрий [5]. Удаление исключительно ненужных организму структур без повреждения нормальных клеток требует точной передачи сигналов и имеет решающее значение для поддержания постоянства внутренней среды.
Однако данный процесс может стать опасным для организма. Чрезмерная митофагия описана при многих острых и хронических заболеваниях центральной нервной системы. Так, при болезни Паркинсона она может привести к гибели нейронов [6]. Контроль качества митохондрий с целью избежания излишнего уничтожения имеет центральное значение для функционирования и благополучия нейронов. Это открывает новые возможности для исследований в области лечения нейродегенеративных заболеваний!
Как липиды «помогают» клетке погибнуть?
Что же делать со старыми клетками, честно отслужившими свой срок? Безусловно, оставлять их на своем месте нельзя, иначе новым здоровым клеткам будет некуда деться. Остается один вариант — аккуратно разобрать и удалить из организма те из них, которые не способны более функционировать. Данный процесс носит названия апоптоза. Валериан Каган и его соавторы доказали, что для осуществления этого процесса необходимо окислить ПНЖК кардиолипина [7]. При необратимых изменениях в клетке знакомый нам кардиолипин образует комплекс с белком дыхательной цепи — цитохромом c — и превращает его в фермент пероксидазу. Пероксидаза тотчас окисляет ПНЖК кардиолипина, и он перемещается на внешнюю мембрану митохондрий, увеличивая ее проницаемость (рис.4). Это приводит к высвобождению других проапоптотических факторов клетки, действие которых приводит к клеточной гибели.
Рисунок 4. Окисление кардиолипина как фактор апоптоза. На рисунке представлена клеточная мембрана, состоящая из бислоя липидов, один из которых — кардиолипин (показан желтым цветом). При взаимодействии с белком цитохромом c (cyt c) кардиолипин превращает его в пероксидазу, которая, в свою очередь, окисляет ПНЖК кардиолипина (на рисунке — cardiolipin hydroperoxide, CL-OOH). Гидроперекись кардиолипина выходит на внешнюю мембрану митохондрии, изменяя ее проницаемость, что приводит к апоптозу.
Новый взгляд на клеточную смерть
Одним из важнейших достижений редокс-липидомики является открытие уникального варианта неапоптотической программируемой гибели клетки — ферроптоза [8]. По сравнению с другими формами этот путь клеточной гибели неповторим. В чем же его особенность? Оказалось, что, в отличие от апоптоза, при котором происходит аккуратная разборка клетки, ферроптоз приводит к клеточному коллапсу, в котором железо и АФК принимают активное участие. Давайте разберемся, как это происходит!
Ферроптоз назван так неспроста. Железо (Fe от лат. ferrum) — основной элемент, необходимый для осуществления ключевого звена данного пути гибели клетки: перекисного окисления липидов (рис. 5) [9], [10]. Перекисное окисление может происходить под действием свободного двухвалентного железа (через реакцию Фентона), а также посредством фермента липоксигеназы, содержащей железо.
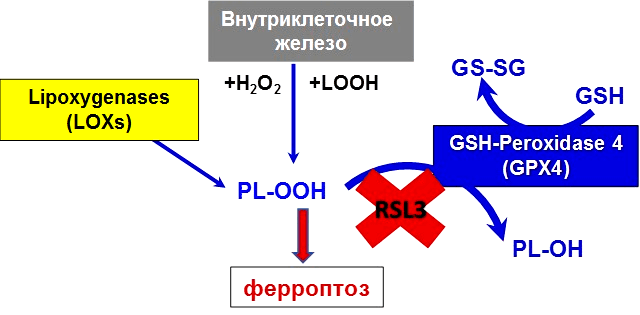
Рисунок 5. Ионы железа в организме находятся под строгим метаболическим контролем. Нарушение баланса ионов железа в клетке и возникновение окислительного стресса приводит к цепной реакции окисления липидов и формированию избытка гидроперекисей. Накопление гидроперекисей липидов приводит к развитию ферроптоза. Гидроперекиси фосфолипидов (PL-OOH) образуются внутри клетки с участием различных форм низкомолекулярного внутриклеточного железа и железосодержащих ферментов. Активная GPX4 восстанавливает гидроперекиси липидов до спиртов. В случае ингибирования фермента, например, специфическим ингибитором RSL3, PL-OOH накапливаются в клетках, усиливая развитие окислительного стресса.
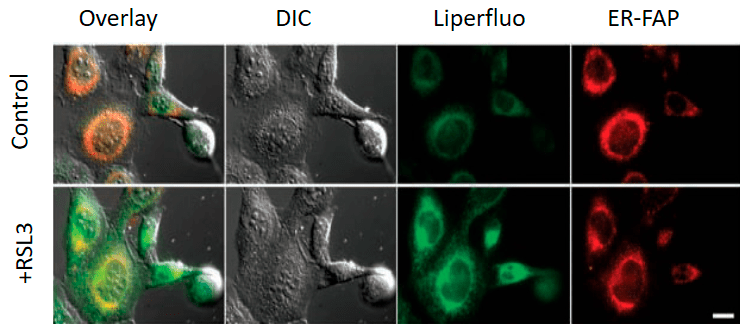
Конкретные механизмы редокс-модификации липидов, задействованные в выполнении программы ферроптоза, на сегодняшний день остаются тайной. Но, окрасив клетку различными флуоресцентными красителями, можно увидеть, насколько удивительные очертания они приобретают при ферроптозе (рис. 6) [11]!
Рисунок 6. Снимок конфокальной микроскопии эмбриональных фибробластов мыши, обработанных индуктором ферроптоза RSL3 (100 nM, 6h). Control — необработанные клетки. Liperfluo — флуоресцентный зонд, который после взаимодействия с гидроперекисями липидов способен флуоресцировать, если он встроен в плазматическую мембрану клеток. ER-FAP (ER-targeted fluorogen-activating protein) — флуоресцентный белок, чья флуоресценция активируется при связывании метки с эндоплазматическим ретикулумом.
В клетках организма существуют механизмы, препятствующие неконтролируемому перекисному окислению. Одним из ключевых ферментов здесь является глутатионпероксидаза 4 (GPX4), которая восстанавливает гидроперекиси липидов до спиртов за счет окисления глутатиона (GSH). Далее окисленная молекула глутатиона (GS-SG) восстанавливается с помощью фермента глутатион-редуктазы. В случае инактивации клеточного глутатиона и GSH-зависимой антиоксидантной защиты происходит накопление токсичных липидных АФК и запуск ферроптоза [12].
Две крайности одной и той же сущности. Как ферроптоз реализуется в целом организме и можно ли обернуть его в свою пользу?
Проведенные исследования показывают, что ферроптоз осуществляется во многих типах тканей человека. Так, при отравлении парацетамолом в организме накапливается N-ацетил-p-бензохинонимин, при этом наблюдается истощение глутатиона, в результате чего происходит массивная гибель клетки по механизму ферроптоза [13].
Имеющиеся данные указывают на то, что ферроптоз может выступать одним из ключевых механизмов развития некоторых нейродегенеративных заболеваний, а также является одной из возможных причин гибели клеток в условиях глутаматной эксайтотоксичности [14].
Ионы железа могут играть ключевую роль в гибели эпителиальных клеток почечных канальцев в условиях острой почечной недостаточности [13]. Данный механизм обусловлен нарушением гломерулярной фильтрации и накоплением ионов железа как внутриклеточно, так и в полости канальца, что приводит к реализации клеточной смерти.
Ферроптоз, как механизм регулируемой клеточной смерти, имеет и терапевтическую ценность. Существует ряд потенциальных молекул, ингибирующих Xc – — транспортную систему (эрастин, RSL3), которые, воздействуя на культуру опухолевых клеток, вызывают их гибель по механизму ферроптоза [12], [13]. Как доказать, что это происходит благодаря ферроптозу, а не случайному совпадению? При добавлении к клеткам веществ, связывающих железо, оно становится «неподвижным» и не может участвовать в химических процессах. В этом случае процессы ферроптоза значительно замедляются. Однако не все так просто и радужно! Эти молекулы не обладают высокой специфичностью, и при более высоких дозах клеточная гибель может происходить по механизму апоптоза!
Вывод
Благодаря редокс-липидомике стало известно, что кислородсодержащие липиды играют огромную роль в сохранении постоянства внутренней среды, запуская апоптоз, ферроптоз и контролируя воспаление. Однако стоит принять во внимание, что, несмотря на очевидное значение в регуляции множества биологических функций, содержание окисленных липидов в организме крайне мало (0,03–3,0 моль% от всего липидома организма) [4]. Кроме того, трудности анализа окисленных липидов заключаются в их химической нестабильности, термолабильности и неоднородности окисленных продуктов. Не зря их сравнивают с иголкой в стоге сена!
Антиоксиданты
АНТИОКСИДАНТЫ ПРОТИВ СВОБОДНЫХ РАДИКАЛОВ
доступным языком о сложном.
Свободные радикалы (оксиданты, окислители) — это частицы (атомы, молекулы или ионы), как правило, неустойчивые, содержащие один или несколько неспаренных электронов на внешней электронной оболочке, поэтому их молекулы обладают невероятной химической активностью. Поскольку у них есть свободное место для электрона, они всегда стремятся отнять его у других молекул, тем самым окисляя любые соединения, с которыми соприкасаются.
Антиоксиданты или противоокислители — вещества, которые ингибируют процессы окисления.
Рис. 1. Свободные радикалы повреждают оболочку клетки, вызывая преждевременную потерю ею влаги и других жизненно важных элементов.
Содержание страницы:

Радикал, отнявший чужой электрон, становится неактивным и, казалось бы, выходит из игры, однако лишенная электрона (окисленная) другая молекула взамен ему сразу становится новым свободным радикалом и затем, уже она, перенимая эстафету, следом встает на путь очередного «разбоя». Даже молекулы, которые раньше всегда были инертными и ни с кем не реагировали, после такого «разбоя» запросто сами начинают вступать в новые причудливые химические реакции.
В настоящее время развитие многих болезней связывают с разрушительным действием оксидантов — свободных радикалов.
К этим болезням относятся рак, сахарный диабет, астма, артриты, атеросклероз, болезни сердца, болезнь Альцгеймера, тромбофлебиты, рассеянный склероз и другие.
Обозначение и виды свободных радикалов
Алкоксильные радикалы (RO * ). Образуются при взаимодействии с липидами и являются промежуточной формой между ROO * и O H * радикалами. Например, липидный радикал (алкоксил) LO * индуцирует ПОЛ (перекисное окисление липидов), обладает цитотоксическим и канцерогенным действием.
Таблица 1. Названия некоторых радикалов и молекул согласно рекомендациям Комиссии по Номенклатуре Неорганической Химии (1990)
Первичные, вторичные и третичные свободные радикалы.
Таблица 2. Первичные радикалы, образующиеся в нашем организме
Вторичные радикалы, в отличие от первичных, не выполняют физиологически полезных функций. Напротив, они оказывают разрушительное действие на клеточные структуры, стремясь отнять электроны у «полноценных» молекул, вследствие чего «пострадавшая» молекула сама становится свободным радикалом (третичным), но чаще всего слабым, не способным к разрушающему действию.
Таблица 3. Вторичные радикалы
ИСТОЧНИКИ СВОБОДНЫХ РАДИКАЛОВ
Источники из окружающей среды:
Это: радиация, курение, напитки с высокой окислительной способностью, хлорированная вода, загрязнение окружающей среды, окисление почвы и кислотные дожди, непомерное количество консервантов и полуфабрикатов, антибиотики и ксенобиотики, компьютеры, телевизоры, мобильники. сигаретный дым, ионизированный воздух; Высокообработанная, просроченная, испорченная еда и лекарства. Кроме всего этого свободные радикалы могут также образовываться в нормальных процессах метаболизма, под влиянием солнечных лучей (фотолиз), радиоактивного облучения (радиолиз) и даже ультразвуков.
Источники внутри организма:
В процессах образования энергии в митохондриях, например из углеродов; В процессе распада вредных жиров в организме при сжигании многонасыщенных жирных кислот; В воспалительных процессах, при нарушениях метаболизма – диабет; В продуктах обмена веществ в толстом кишечнике.
Стресс (психо-эмоциональный) также способствуют окислительному стрессу. Состояние стресса заставляет организм вырабатывать адреналин и кортизол. В больших количествах эти гормоны нарушают нормальное протекание обменных процессов и способствуют появлению свободных радикалов во всем организме.
Возникнув в них, радикалы повреждают оболочки митохондрий, а также другие внутренние структуры клетки, и это усиливает их утечку. Со временем активных форм кислорода становится там все больше и больше, в результате чего они полностью разрушают клетку и распространяются по всему организму. Как «молекулярные террористы» они хаотично «рыщут» по всем живым клеткам и, внедряясь туда, повергают вокруг себя всё в хаос. Свободные радикалы также могут еще образовываться во многих продуктах нашего питания, например, таких, как: кондитерские изделия длительных сроков хранения, мясные продукты и продукты растительного происхождения. Особенно это касается жиров, содержащих ненасыщенные жирные кислоты, которые очень легко окисляются.
Митохондрия — двумембранный сферический или эллипсоидный органоид диаметром обычно около 1 микрометра. Характерна для большинства эукариотических клеток. Энергетическая станция клетки; основная функция — окисление органических соединений и использование освобождающейся при их распаде энергии для генерации электрического потенциала, синтез а АТФ и термогенеза. Эти три процесса осуществляются за счёт движения электронов по электронно-транспортной цепи белков внутренней мембраны.
Многие из вышеперечисленных факторов нам неподвластны, что-то мы и не хотим менять, но многое мы все же в силах изменить. Во всяком случае знать своих «врагов» в лицо мы просто обязаны. Реакции с участием свободных радикалов могут являться причиной или осложнять течение многих опасных заболеваний, таких как астма, артрит, рак, диабет, атеросклероз, болезни сердца, флебиты, болезнь Паркинсона, болезнь Альцгеймера, эпилепсия, рассеянный склероз, депрессии и другие.
ВОЗДЕЙСТВИЕ СВОБОДНЫХ РАДИКАЛОВ НА ОРГАНИЗМ
Отрицательные результатов действия свободных радикалов:
Таблица 4. Некоторые заболевания, связанные с действием активных форм кислорода (Surai & Sparks, 2001)
Свободные радикалы атакуют наш организм 24 часа в сутки, но их атаки могут происходить чаще или реже. Это зависит от многих факторов. Курение, алкоголь, стрессы, неправильное питание и долгое пребывание на солнце увеличивают количество свободных радикалов, а правильный образ жизни, полноценный отдых и рациональное питание, наоборот, снижают их активность. Объектами атак свободных радикалов в организме человека преимущественно являются соединения, которые имеют двойные связи в частицах, например: белок, ненасыщенные жирные кислоты, входящие в состав клеточной оболочки, полисахариды, липиды и даже ДНК.
1. ЭНЕРГЕТИЧЕСКАЯ ДИСФУНКЦИЯ МИТОХОНДРИЙ КЛЕТКИ
Свободные радикалы вызывают повреждение наружной клеточной мембраны (разрушение рецепторного аппарата клетки и снижение чувствительности клетки к гормонам и медиаторам), ДНК (нарушают генетический код), митохондрий (нарушение энергетического обеспечения клетки).
2. ПЕРЕКИСНОЕ ОКИСЛЕНИЕ ЛИПИДОВ
Наиболее серьезным следствием появления свободных радикалов в клетке является перекисное окисление. Перекисным его называют потому, что его продуктами являются перекиси. Чаще всего по перекисному механизму окисляются ненасыщенные жирные кислоты, из которых состоят мембраны живых клеток.
Процесс перекисного окисления липидов (ПОЛ) является важной причиной накопления клеточных дефектов. Основным субстратом ПОЛ являются полиненасыщенные цепи жирных кислот (ПНЖК), входящих в состав клеточных мембран, а также липопротеинов. Их атака кислородными радикалами приводит к образованию гидрофобных радикалов, взаимодействующих друг с другом.
Вначале происходит атака сопряженных двойных связей ненасыщенных жирных кислот со стороны св. радикалов (гидроксила и гидродиоксида), что приводит к появлению липидных радикалов.
Липидный радикал может реагировать с О2 с образованием пероксильного радикала, который, в свою очередь, взаимодействует с новыми молекулами ненасыщенных жирных кислот и приводит к появлению липидных пероксидов. Скорость этих реакций зависит от активности антиоксидантной системы клетки.
При взаимодействии с комплексами железа гидроперекиси липидов превращаются в активные радикалы, продолжающие цепь окисления липидов.
Образующиеся липидные радикалы, могут атаковать молекулы белков и ДНК. Альдегидные группы этих соединений образуют межмолекулярные сшивки, что сопровождается нарушением структуры макромолекул и дезорганизует их функционирование. Окисление липидов свободными радикалами вызывает глаукому, катаракту, цирроз, ишемию и т.д.
Каждая клетка организма состоит из множества элементов, каждый из которых, да и вся она, окружены оболочками — мембранами. Ядро клетки также защищено мембраной. Таким образом до 80% массы клетки в ней могут составлять различные мембраны, а они состоят из легко окисляющихся жиров, очень слабо удерживающих электроны. Поэтому свободные радикалы наиболее легко вырывают электроны, именно, из мембран. Такое окисление называются перекисным окислением липидов.



Точно так же перекисное окисление может идти в маслах, которые содержат ненасыщенные жирные кислоты, и тогда масло прогоркает (перекиси липидов имеют горький вкус). Опасность перекисного окисления в том, что оно протекает по цепному механизму, т. е. продуктами такого окисления являются не только свободные радикалы, но и липидные перекиси, которые очень легко превращаются в новые радикалы. Таким образом, количество свободных радикалов, а значит, и скорость окисления лавинообразно нарастают.
3. ПОВРЕЖДЕНИЕ БЕЛКА
Таблица 5. Уровень окисленных белков в разных тканях и организмах