Что такое печеночная двуустка
Печёночная двуустка (Fasciola hepatica)
 |
| Взрослые особи (мариты) Fasciola hepatica* |
Печёночная двуустка, или овечий печёночный сосальщик, или обыкновенная фасциола (лат. Fasciola hepatica, англ. liver fluke или sheep liver fluke) — вид плоских червей, трематод, возбудитель фасциолёза человека, а также паразит парнокопытных. Имеет листовидную форму. Длина — до 30 мм, ширина — до 12 мм. Яйца размером 0,15-0,19 на 0,075-0,09 мм.
Fasciola hepatica в систематике эукариот
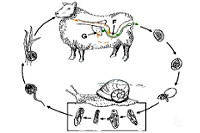
Жизненный цикл Fasciola hepatica
Окончательные хозяева Fasciola hepatica — копытные, чаще всего овцы, козы и коровы. Человек также может быть окончательным хозяином. Взрослые, половозрелые печёночные двуустки, мариты, являются гермафродитами, каждая из них обладает семенниками, яичниками, маткой. Оплодотворение, в большинстве своём, перекрёстное. Размер яиц — до 100 на 180 мкм.
Промежуточными хозяевами двуусток Fasciola hepatica являются дышащие воздухом пресноводные улитки из семейства прудовиков (лат. Lymnaeidae). Печёночная двуустка развивается только у одного или двух основных видов на каждом континенте. В Европе, частично в Азии, Африке и Южной Америке промежуточным хозяином двуустки являются малые прудовики (лат. Galba truncatula). В Центральной и частично в Южной Америке — Lymnaea viator, Galba neotropica, Galba cubensis и Pseudosuccinea columella.
Яйца двуусток Fasciola hepatica выделяются во внешнюю среду с фекалиями млекопитающих. При попадании их в воду или во влажную почву через 4-6 недель развиваются личинки — мерацидии. В воде мерацидии покидают яйца и внедряются в промежуточных хозяев — прудовиков, где превращаются в церкариев. Церкарии в воде инцистируются и превращаются в адолескариев. Заражение животных происходит при заглатывании адолескариев с водой или поедании растущих в водоемах со стоячей и медленно текущей водой трав.
Жизненный цикл Fasciola hepatica
Фасциолёз, вызванный Fasciola hepatica
Человек заражается фасциолами при употреблении в пищу водных растений или питье воды загрязнённой личинками (адолескариями) двуустки Fasciola hepatica пищу зараженных растений: огородной зелени, кресс-салата, дикого лука и других, а также сырой воды из непроточных водоемов. Также заражение возможно при мытье салатных трав и овощей прудовыми водами. Фасциолы из кишечника проникают в брюшную полость, затем в печень и желчные протоки, где через 3-4 месяца из них вырастают половозрелые особи (мариты), которые начинают выделять яйца. Взрослые двуустки паразитируют в более крупных желчных протоках и в желчном пузыре, где они вызывают воспаление, фиброз, непроходимость, колики и желтуху. Часто также развиваются фиброз печени и анемия.
 |
| Яйцо Fasciola hepatica |
Инкубационный период длится примерно 2-4 недели.
Фасциолёз наиболее широко распространён в странах Азии, Африки и Южной Америки. На территории бывшего СССР — на Кавказе и в Средней Азии.
У фасциолёза выделяют две стадии: острую и хроническую. Главные патологические изменения в организме больного происходят во время острой стадии, при миграции двуусток через паренхиму печени: боли в животе, лихорадка, потливость, крапивница, кашель, значительная эозинофилия, лейкоцитоз. Повышенная температура тела возникает с самого начала заболевания и может наблюдаться несколько месяцев. Длительность острой стадии обычно от четырёх до шести недель.
Попав в желчные потоки, двуустки там остаются. достигают половозрелой стадии и начинают выделять яйца. У больного во время хронической стадии фасциолёза развивается пролиферативный холангит с аденоматозными изменениями эпителия и перидуктальным фиброзом и фиброзом стенок желчного пузыря. Иногда также развивается обструкция желчных потоков. Клинические проявлеия присутствуют не всегда, обычно они соотвествуют аналогичным при острой стадии, но в более мягкой форме.
На сайте GastroScan.ru в разделе «Литература» имеется подраздел «Паразитарные и инфекционные заболевания ЖКТ», содержащий статьи, затрагивающие, в том числе, вопросы лечения фасциолёзов.
Триклабендазол
Основным препаратом при лечение фасциолёзов считается триклабендазол (англ. triclabendazole). Его принимают однократно исходя из дозы 10 мг на кг массы пациента или двукратно, два дня подряд, с перерывом 24 часа, каждая доза также рассчитывается исходя из 10 кг мг на кг массы пациента (Бронштейн А.М., Малышев Н.А.).
Аналогичных рекомендаций придерживается ВОЗ, добавляя, что при ведении отдельных случаев необходимо проводить описанное выше лечение во всех подтверждённых случаях фасциолёзов, а в эндемичных районах проводить диагностику во всех предполагаемых случаях. Превентивную терапию триклабендазолом проводят в отдельных местностях, селениях или сообществах, где имеются кластеры случаев заболевания фасциолезом: выполняется лечение всех детей школьного возраста (5-14 лет) или всех жителей каждые 12 месяцев однократно исходя из дозы 10 мг триклабендазола на кг массы пациента.
Триклабендазол не имеет допуска к применению в лечебной практике в России***. В США триклабендазол впервые разрешён FDA к применению 13.2.2019 года под торговой маркой Egaten. При этом он уже много лет допущен к применению во многих странах Европы, Азии и других.
Триклабендазол по фармакологическому указателю относится к группе «антигельминтные средства». По АТХ триклабендазол входит в группу «P02 Антигельминтные препараты», подгруппу «P02B Препараты для лечения трематодоза» и имеет код P02BX04. Кроме того, в группе «Q Ветеринарные препараты» он имеет код QP52AC01.
У триклабендазола имеются противопоказания, побочные действия и особенности применения, необходима консультация со специалистом.
Fasciola hepatica и фасциолёз в Номенклатуре медицинских услуг
 |
| Наиболее частый в Европе промежуточный хозяин Fasciola hepatica — малый прудовик (Galba truncatula) |
Фасциолёз в МКБ-10
Фасциолёз
Фасциолез – это паразитарная инвазия, вызываемая печеночной или гигантской двуусткой и характеризующаяся преимущественным поражением гепатобилиарной системы. Течение фасциолеза сопровождается недомоганием, лихорадкой, крапивницей, тошнотой, болями в правом подреберье, увеличением размеров печени, желтухой. В диагностике фасциолеза информативны серологические методы (ИФА, РИФ, РИГА), исследование дуоденального содержимого и фекалий на яйца гельминтов, УЗИ печени и желчевыводящих путей. В комплексную терапию фасциолеза включают диету, прием антигельминтных средств (триклабендазол, празиквантел), желчегонных, антигистаминных препаратов.
МКБ-10
Общие сведения
Причины фасциолеза
Характеристика возбудителя
Возбудителями фасциолеза выступают два вида трематод (сосальщиков): двуустка печеночная (Fasciola hepatica) и двуустка гигантская (Fasciola gigantea). Печеночная фасциола имеет тело плоской листовидной формы, на головном конце которого расположено 2 присоски. Длина взрослого паразита 20-30 мм, ширина 8-12 мм. Гигантская фасциола имеет более крупные размеры: длину 33-76 мм, ширину 5-12 мм.
Механизм передачи
Окончательными хозяевами сосальщиков служат травоядные сельскохозяйственные животные, реже – человек. Паразитируя в желчевыводящей системе, гельминты откладывают яйца, которые с испражнениями попадают в окружающую среду и свое дальнейшее развитие проходят в пресной воде. Там вышедшие из яиц личиночные стадии (мирацидии) внедряются в тело брюхоногих моллюсков, являющихся промежуточными хозяевами возбудителя фасциолеза.
Во внутренних органах моллюсков мирацидии превращаются сначала в спороцисты, а затем в хвостатые церкарии. Через 1-2 месяца церкарии снова выходят в воду, инцистируются, превращаясь в адолескарий, и прикрепляются к поверхности водных растений или водной пленке. В этой стадии личинки становятся инвазионными, т. е способными вызывать фасциолез у животных и человека.
Заражение животных фасциолезом происходит при поедании травы на выпасе, загрязненной личинками двуустки; инфицирование человека возможно при употреблении в пищу дикорастущих или огородных растений, полив которых осуществлялся водой из пресных водоемов; питье некипяченой воды; во время купания и т. д. В желудочно-кишечном тракте личинки фасциолы высвобождаются из оболочек, через стенку кишечника выходят в брюшную полость, где через капсулу внедряются в паренхиму печени и таким образом попадают в желчные протоки. Возможен гематогенный путь миграции – через кишечные и воротную вены в печеночные протоки.
Через 3-4 месяца паразитирования в организме окончательного хозяина фасциолы достигают половозрелой стадии и начинают откладывать яйца. В гепатобилиарной системе человека возбудители фасциолеза способны паразитировать 5-10 и более лет.
Патогенез
Развивающиеся в миграционную фазу инвазии токсико-аллергические реакции связаны с сенсибилизацией организма антигенами личинок, а также механическим травмированием тканей на пути их продвижения. В хронической стадии фасциолеза патологические эффекты обусловлены паразитированием гельминтов в желчных протоках. Половозрелые гельминты вызывают повреждение печеночной паренхимы с развитием микроабсцессов и фиброзных изменений печени.
Скапливаясь в желчных ходах, фасциолы могут способствовать их обструкции и нарушению оттока желчи, развитию пролиферативного (а в случае присоединения вторичной инфекции – гнойного) холангита. Общетоксическое воздействие на организм при фасциолезе обусловлено поступлением в кровь продуктов жизнедеятельности гельминтов и распада печеночной ткани. В исходе длительного течения фасциолеза может развиваться цирроз печени и портальная гипертензия.
Симптомы фасциолеза
В развитии фасциолеза выделяют инкубационный период, острую (миграционную) и хроническую (связанную с паразитированием взрослых гельминтов) стадии. В зависимости от инвазирующей дозы, инкубационный период может длиться от 1 до 8 недель.
В миграционную фазу главным образом выражены общетоксические и аллергические симптомы. Больные фасциолезом жалуются на подъемы температуры, слабость, недомогание, головную боль. Лихорадка может быть субфебрильной или высокой (до 39-40°С), носить ремитирующий или волнообразный характер. На этом фоне появляется крапивница и кожный зуд, отек Квинке, высокая (до 80-85%) эозинофилия в крови. Развиваются диспепсические расстройства: тошнота, рвота, боли в эпигастрии и правом подреберье; происходит увеличение размеров печени, сопровождающееся желтухой. В раннем периоде часто развивается аллергический миокардит, характеризующийся загрудинными болями, артериальной гипертензией, тахикардией. Через несколько недель клинические проявления острого фасциолеза значительно или полностью стихают.
Спустя 3-6 месяцев заболевание вступает в хроническую стадию, симптомы которой обусловлены непосредственным поражением печени и желчных путей. Течение хронического фасциолеза сопровождается гепатомегалией, приступообразными болями в правом боку; в периоды обострения – желтухой. Длительная инвазия приводит к развитию диспепсического синдрома, анемии, гепатита, цирроза печени.
Вторичное инфицирование чревато возникновением гнойного холецистита и холангита, абсцессов печени, стриктуры желчных путей. В литературе описаны казуистические случаи фасциолеза с нетипичной локализацией сосальщиков в головном мозге, легких, молочных железах, евстахиевых трубах, гортани, подкожных абсцессах.
Диагностика
Чаще всего фасциолез диагностируется уже в хронической стадии, когда с беспокоящими жалобами больные обращаются к терапевту или гастроэнтерологу. Предположительный диагноз основывается на совокупности эпидемиологических данных и клинических данных. В пользу фасциолеза свидетельствует наличие ранее зафиксированных случаев инвазии на данной территории, групповая заболеваемость, употребление в пищу салатных растений, питье воды из открытых источников или использование ее для мытья посуды, фруктов, овощей и пр.
Фасциолез необходимо отличать от описторхоза, клонорхоза, вирусных гепатитов, панкреатита, холангита, холецистита другой этиологии.
Лечение фасциолеза
Лечение фасциолеза проводится стационарно. В острую фазу назначается щадящая диета, десенсибилизирующие препараты; при развитии миокардита и гепатита показаны глюкокортикостероиды. К противопаразитарной терапии переходят только после стихания острых явлений. В качестве этиотропных препаратов при фасциолезе используются триклабендазол, гексахлорпараксилол, празиквантел. С целью изгнания погибших фасциол из желчных протоков назначаются желчегонные средства.
Контрольное паразитологическое обследование (анализ кала на яйца гельминтов, дуоденальное зондирование с исследованием порций желчи) проводится спустя 3 и 6 месяцев. В случае развития гнойных осложнений требуется назначение антибиотиков и проведение хирургического вмешательства (дренирования абсцесса печени, дренирования желчных протоков и др.).
Прогноз и профилактика
Ранняя диагностика фасциолеза позволяет провести своевременную терапию и добиться выздоровления. При высокоинтенсивной инвазии или вторичной бактериальной инфекции прогноз может быть серьезным, вплоть до летального исхода. Индивидуальная профилактика фасциолеза заключается в недопущении употребления сырой воды из водоемов, плохо промытой огородной зелени. Меры общественного контроля включают очистку водоемов, их защиту от фекального загрязнения, ликвидацию промежуточных хозяев фасциолеза – моллюсков, ветеринарное обследование и дегельминтизацию скота, санитарно-просветительскую работу.
Что такое печеночная двуустка
Фасциолез – глистная инвазия, вызываемая Fasciola hepatica (двуустка печеночная) – паразитом из класса печеночных сосальщиков. Заболевание характеризуется поражением печени, желчевыводящих протоков и желчного пузыря. Ранняя стадия инвазии характеризуется аллергическими реакциями, воспалением желчевыводящих протоков и застоем желчи. При хроническом течении возможны деструктивные изменения печеночной ткани, существует опасность развития фиброза печени и кровотечений. Концентрация специфических IgG достигает максимума к 2-3 месяцам от начала заражения и держится на таком уровне довольно долго. Исследование проводят в целях выявления в крови антител IgG к антигенам Fasciola hepatica.
Фасциолез, печеночная двуустка.
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Возбудитель фасциолеза, печеночная двуустка Fasciola hepatica, распространена повсеместно и паразитирует в печени и желчных путях крупного рогатого скота. Взрослые мужские и женские особи гельминта имеют листовидную форму и достигают в размерах 2 см. Они могут сохранять жизнеспособность в желчных протоках более десяти лет, откладывая яйца, которые попадают в кал и загрязняют водоемы. Промежуточными хозяевами фасциол являются улитки, в которых из яиц паразита развиваются церкарии. Заражение овец, крупного рогатого скота, а также человека происходит при поедании растений с берегов загрязненных водоемов. Попав в кишечник, метацеркарии выходят через его стенку в брюшную полость, откуда проникают в паренхиму печени через ее капсулу и после созревания, которое длится 1-3 мес., выходят в желчные пути, завершая жизненный цикл. Фасциолез овец и крупного рогатого скота наносит серьезный материальный ущерб сельскому хозяйству в районах, где скот пасется на берегу водоемов. В анамнезе больных фасциолезом часто имеется указание на употребление в пищу водных растений, в частности водяного кресса, или неочищенной воды. Фасциолез чаще встречается в развивающихся странах с влажным климатом и особенно распространен среди сельского населения; в странах Европы и Северной Америки фасциолезом болеют реже.
Острый фасциолез проявляется повышением температуры тела, длящимся до 3 мес., неприятными ощущениями в правой верхней части живота, увеличением печени. Зрелые особи гельминта, перемещаясь в паренхиме печени, оставляют за собой след в виде коагуляционного некроза с эозинофилами. Фасциолы могут мигрировать, опережая развитие воспалительной реакции, которая могла бы послужить эффективной защитой от паразита. На компьютерных томограммах следы миграции фасциол имеют вид извилистых линейных ходов размером 1-3 см., напоминающих абсцессы.
Атипичные клинические проявления при остром фасциолезе могут быть связаны с гемобилией, возникающей при попадании паразитов в желчные протоки, или с формированием абсцесса. Незрелые фасциолы, не проникнувшие в печень, могут стать причиной образования инфильтратов и абсцессов различной локализации. Наиболее часто они образуются под кожей в виде узелков, представляющих собой эозинофильные инфильтраты вокруг дегенерирующей ткани паразитов. Острый фасциолез может сопровождаться эозинофильным плевритом или перикардитом без инвазии фасциол в плевру или перикард.
Повышение температуры тела и боль в правой верхней части живота при остром фасциолезе и симптомы поражения желчных путей при хроническом фасциолезе в сочетании с данными об употреблении в пищу водяных растений или неочищенной воды позволяют заподозрить фасциолез. Эозинофилия и наличие паразитов в печени подтверждают диагноз. При серологическом исследовании на антитела к паразиту методом ИФА в качестве антигена используют очищенный препарат катепсина L1 (специфическая протеаза фасциол). Антитела класса IgG образуются спустя несколько недель после инфицирования, достигая пика в острый период заболевания. Титр антител в крови после успешного лечения постепенно уменьшается.
Когда назначается исследование?
Что означают результаты?
Референсные значения: не обнаружено.
Коэффициент позитивности (КП):
1.1 – положительный результат.
КП – концентрация специфических антител в единице объема. Чем выше КП пробы, тем выше концентрация антител.
Отрицательный результат (не обнаружено):
Положительный результат (обнаружено):
В случае получения сомнительного результата рекомендуется повторить исследование через 14 дней. При повторном результате «Сомнительно» результат следует рассматривать как отрицательный.
41 Скрининг функции печени и поджелудочной железы
55 Анализ кала на яйца и личинки гельминтов, простейшие и их цисты (Parasep)
31 Скрининговое обследование на гельминтозы (Opisthorchis IgG, Toxocara IgG, Trichinella IgG, Echinococcus IgG)
35 Клинический анализ крови с микроскопией лейкоцитарной формулы
Кто назначает исследование?
Инфекционист, гастроэнтеролог, ревматолог, терапевт.
Описторхоз в клинической практике врача-инфекциониста
Рассмотрены распространение, патогенез, клиническая картина описторхоза, формы заболевания, методы лабораторной диагностики и подходы к лечению пациентов, а также применяемые препараты и меры по контролю эффективности терапии.
Propagation, pathogenesis, clinical picture of opistorchosis, are examined, as well as forms of disease, methods of laboratory diagnostics and approaches to the treatment of patients, and also applied preparations and the measures to control the therapy efficiency.
Описторхоз — внекишечный природно-очаговый биогельминтоз, вызываемый трематодами из семейства Opisthorchidae, характеризующийся полиморфизмом клинических проявлений, обусловленных паразитированием этих гельминтов в желчных протоках печени и протоках поджелудочной железы и длительным течением.
История изучения и распространение описторхоза
Возбудитель описторхоза был открыт и описан S. Rivolta в 1884 г. у кошек и назван Opisthorchis (Distomum) felineus. В 1891 г. профессор Томского университета К. Н. Виноградов при вскрытии трупа человека обнаружил подобного же гельминта, подробно описал его и назвал Distomum sibiricum (сибирская двуустка) [4]. В 1894 г. M. Braun доказал идентичность Distomum felineum Rivolta (1884 г.) и Distomum sibiricum Winogradov (1891 г.) [1, 2].
Описторхоз занимает доминирующее место в краевой инфекционной патологии Западной Сибири, где существует самый напряженный в мире очаг этой инвазии. В низовьях Иртыша и среднего течения Оби пораженность местного населения достигает 70–80% и даже 90% [1].
Очаги описторхоза расположены также в бассейнах рек Днестра, Немана, Волги, Днепра. Имеются данные о наличии очагов с низким уровнем экстенсивности в притоках Енисея, в бассейне Урала, Северной Двины и Бирюсы. За рубежом очаги описторхоза зарегистрированы в Италии, Германии, Франции, Болгарии и других странах [1].
Жизненный цикл паразита
Описторхисы относятся к классу трематод, семейству Opisthorchidae. O. felineus — плоский гельминт ланцетовидной формы, длиной 4–20 мм и шириной 1–4 мм. Яйца описторхисов с уже сформированными личинками выделяются с фекалиями во внешнюю среду, и дальнейшее развитие происходит в пресноводных водоемах, где обитает промежуточный хозяин описторхисов — пресноводные моллюски Codiella inflata и Codiella troscheli. Моллюск с пищей заглатывает яйцо, из которого выходят мирацидии, превращающиеся в спороцисту, редию и хвостатую личинку — церкария. Церкарий покидает тело моллюска, выходит в водоем и в силу хемо- и фототаксиса прикрепляется к телу своего дополнительного хозяина — рыбы семейства карповых. К семейству карповых относится 23 вида рыб (язь, лещ, карп, чебак, елец, линь, красноперка, сазан, пескарь и др.). Проникшие в мышечную и соединительную ткань рыбы церкарии инцистируются и превращаются в метацеркарий. Метацеркарии достигают инвазионной стадии через 6 недель. В организм окончательного хозяина — человека и животных — метацеркарии попадают при употреблении в пищу инвазированной необезвреженной рыбы. Круг дефинитивных хозяев паразита насчитывает 34 вида рыбоядных млекопитающих (кошка, собака, свинья, лисица, волк, корсак, песец, бурый медведь, росомаха, хорь, бобр и др.). В желудке окончательного хозяина происходит переваривание наружной капсулы, а под действием дуоденального сока метацеркарии освобождаются от своей внутренней оболочки и через ампулу дуоденального сосочка мигрируют в общий желчный проток и внутрипеченочные желчные протоки. У 20–40% зараженных лиц описторхисы также обнаруживаются и в протоках поджелудочной железы, куда они проникают по вирсунгову протоку [3]. Проникшие в гепатобилиарную систему и поджелудочную железу метацеркарии через 3–4 нед достигают половой зрелости и начинают продуцировать яйца. Число паразитов у одного человека может быть от единиц до десятков тысяч. Весь цикл развития описторхиса от яйца до половозрелой стадии длится 4–4,5 мес.
Патогенез
В патогенезе описторхоза, как и многих других гельминтозов, прослеживается 2 фазы: ранняя и поздняя. Ранняя фаза, или острый описторхоз, длится от нескольких дней до 4–8 и более недель и связана с проникновением эксцистированных метацеркариев паразита в гепатобилиарную систему и поджелудочную железу. Поздняя фаза или хронический описторхоз продолжается многие годы.
Молодые описторхисы повреждают стенки желчных протоков своими шипиками, а половозрелые — присосками, отрывая эпителий желчных протоков, которым они питаются, чем определяется развитие множественных кровоточащих эрозий и бурной регенеративно-гиперпластической реакции эпителия. Это эволюционно сформировавшееся качество описторхисов, направленное на создание оптимальных условий для их жизнедеятельности и поддержание вида. В условиях этого процесса чрезвычайно велика возможность мутации, что в сочетании с иммуносупрессорным влиянием описторхисов значительно повышает риск канцерогенеза [4]. Скопление в желчных и панкреатических протоках гельминтов, их яиц, слизи, слущенного эпителия создает препятствие для оттока желчи и секрета, что способствует развитию пролиферативного холангита и каналикулита поджелудочной железы, сопровождающихся различной степенью фиброза этих органов.
Механическое раздражение стенок желчных протоков печени и панкреатических протоков приводит к развитию патологических висцеро-висцеральных рефлексов, ведущих к нарушению моторной и секреторной функции органов желудочно-кишечного тракта.
Альтеративные изменения в органах локализации и других органах обусловлены и влиянием продуктов метаболизма описторхисов, которые преодолевают эпителиальный барьер и поступают в кровеносное русло, оказывая токсическое воздействие на организм человека.
Пролиферативные процессы в желчных протоках, а также сами гельминты, слизь, слущенный эпителий, создают условия для развития желчной гипертензии, способствуют формированию дискинезии желчевыводящих путей, стазу желчи, созданию благоприятных условий для развития вторичной инфекции (кишечная палочка, стафилококки, дрожжеподобные грибки и различные микробные ассоциации).
Клиническая картина заболевания
Клиническая картина описторхоза полиморфна и варьирует от бессимптомных форм до тяжелых проявлений, обусловленных развитием гнойного холангита, абсцесса печени и др.
Общепризнанной классификации описторхоза не существует. Выделяют раннюю фазу (острый описторхоз) и позднюю (хронический описторхоз). Острый описторхоз длится от нескольких дней до 4–8 и более недель и связан с проникновением личинок паразита в гепатобилиарную систему и поджелудочную железу. В ранней фазе описторхоза ведущим звеном в патогенезе является развитие аллергических реакций и органных поражений в ответ на воздействие продуктов метаболизма паразита. В патогенезе хронической стадии описторхоза большую роль играют повторные заражения с обострением воспалительного процесса, фиброзом билиарных путей, поджелудочной железы, дистрофией паренхимы печени, дискинезией желчевыводящих путей, холестазом. Хронический описторхоз продолжается многие годы.
Инкубационный период равняется в среднем 2–3 нед.
Клинические варианты острого описторхоза разнообразны — от латентных до генерализованных аллергических реакций с множественными поражениями.
В эндемичных по описторхозу очагах у коренных жителей и у длительно проживающих в течение нескольких поколений местных жителей чаще не выявляется клинически выраженная острая фаза болезни, в то время как у вновь прибывших из благополучных по описторхозу местностей острая фаза описторхоза наблюдается почти всегда. Причина этого явления заключается в том, что у аборигенов (иммунное население) формируется иммунологическая толерантность супрессорного типа. Иммунологическая толерантность к описторхозному антигену формируется в связи с поступлением описторхозного антигена в организм на ранних стадиях эмбриогенеза. После рождения уже зрелый организм воспринимает этот антиген как «свое» [5, 6].
Инаппарантная (субклиническая) форма описторхоза выявляется случайно, когда при исследовании периферической крови отмечается большая эозинофилия.
При клинически выраженном остром описторхозе у больных наблюдается лихорадка — от субфебрильной до фебрильной длительностью от 3–4 дней до нескольких недель, интоксикационный синдром, умеренные артралгии и миалгии, экзантема различного характера, гепатобилиарный синдром: боли в правом подреберье (тупые, ноющие, давящие, жгучие), желтуха — от субиктеричности до интенсивной, кожный зуд, гепатомегалия, у части больных выявляются положительные пузырные симптомы. Характерны симптомы диспепсического характера (тошнота, рвота, изжога). Более чем у 80% больных выявляется цитолитический синдром с повышением активности аминотрансфераз (аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ)) в 2–7 раз по сравнению с нормой, часто холестаз (повышение уровня гамма-глутамилтранспептидазы (ГГТП) и щелочной фосфатазы (ЩФ)), развивается мезенхимально-воспалительный печеночный синдром [7]. Одним из проявлений острого описторхоза может быть бронхолегочный синдром: катаральные проявления со стороны верхних дыхательных путей (гиперемия зева, зернистость задней стенки глотки, насморк), астматоидный бронхит, эозинофильные инфильтраты в легких и экссудативные плевриты [8]. Реже наблюдается гастроэнтероколитический синдром, характеризующийся субфебрильной лихорадкой, умеренно выраженный интоксикацией и преобладанием симптомов поражения желудочно-кишечного тракта (боли в эпигастрии, изжога, тошнота, рвота, частый жидкий стул, иногда с примесью слизи).
Описанные синдромы острой фазы описторхоза не исчерпывают всего разнообразия клиники этого гельминтоза, и при любом варианте общие и локальные симптомы тесно переплетаются, что обусловливает полиморфизм клинических проявлений и индивидуальную неповторимость этих сочетаний у каждого больного.
У больных в острую фазу описторхоза могут развиваться и очень тяжелые токсико-аллергическиие проявления, такие как острый эпидермальный некролиз (синдром Лайелла), синдром Стивена–Джонсона, острый миокардит, отек Квинке, крапивница.
Большое значение для диагностики острого описторхоза имеет исследование периферической крови. У всех больных наблюдается лейкоцитоз до 20–60 × 10 9 л, умеренно повышенная скорость оседания эритроцитов (СОЭ) и эозинофилия — 20–40%, иногда до 90%.
С переходом заболевания в хроническую фазу симптоматика существенно изменяется и характеризуется, прежде всего, устранением лихорадки и нормализацией гематологических показателей.
Латентное течение описторхоза чаще наблюдается у коренного и местного населения в очагах этой инвазии, а также нередко у лиц молодого возраста, инвазированных описторхисами.
Проявления клинически выраженного хронического описторхоза неспецифичны, полиморфны и не укладываются в какой-либо один синдром. Холангит при описторхозе является абсолютно обязательным звеном патогенеза. Некоторые исследователи [7, 9] не относят желчный пузырь к числу органов постоянного пребывания описторхисов и считают, что паразиты в желчный пузырь попадают случайно с током желчи. Учитывая функционально-морфологические связи внутрипеченочных желчных протоков и желчного пузыря, сочетанное поражение этих органов у больных описторхозом наблюдается очень часто, и синдромы холангита и холецистита относится к наиболее распространенным (80–87% случаев) [7, 9]. Проявления этих синдромов зависят от длительности и интенсивности инвазии. Так, в первые 3 года после заражения у 86% больных наблюдается гиперкинетический тип дискинезии желчевыводящих путей, у 11% — нормокинетический и у 3% — гипокинетический. Спустя 5–7 лет в 87% случаев выявляется гипокинетический тип дискинезии, в 6% — нормокинетический, в 7% — гиперкинетический [9]. У 50–85% больных отмечается гепатомегалия, у 30–40% — положительные пузырные симптомы [7].
У 13–17% больных хроническим описторхозом наблюдается гепатит, основными проявлениями которого являются боли в правом подреберье, тошнота, рвота, отрыжка, артралгии, нередко — кожный зуд, гепатомегалия, при обострении развивается желтуха различной интенсивности [7–9].
У части больных развивается панкреатит, отличающийся волнообразным течением с частой сменой периодов обострений и ремиссий, и редко наблюдается прогрессирующее течение [10]. Чаще всего панкреатит протекает в виде болевой формы. Редкими формами панкреатита являются хронический псевдоопухолевый панкреатит и описторхозные кисты поджелудочной железы.
У больных описторхозом отмечаются и поражения органов, не являющихся местом постоянной локализации возбудителя. Так, у 45–50% больных описторхозом отмечаются различные формы гастродуоденальной патологии (гастриты, дуодениты, язвенная болезнь желудка и двенадцатиперстной кишки) [10–11]. Поражение кишечника у больных хроническим описторхозом отмечается довольно часто, и основным его проявлением является кишечная диспепсия. При изучении состава микрофлоры фекалий у них выявляется дисбактериоз, который характеризуется отсутствием или резким снижением количества бифидобактерий, уменьшением количества эшерихий, нередко в сочетании с угнетением их ферментативных свойств, и повышенным содержанием факультативной условно-патогенной микрофлоры (S. epidermidis, S. aureus и др.) [7].
Изменения со стороны сердечно-сосудистой системы проявляются сердцебиениями, болями в области сердца, наклонностью к гипотонии, диффузными дистрофическими изменениями миокарда по данным электрокардиографии (ЭКГ).
Описторхозная инвазия может приводить к нарушению деятельности центральной и вегетативной нервной системы, о чем свидетельствуют частые жалобы больных на повышенную утомляемость, раздражительность, бессонницу, головную боль, головокружение [3, 9]. Наблюдаются признаки лабильности вегетативной нервной системы: потливость (часто локальная — потные руки), слюнотечение, выраженный дермографизм, тремор век, языка, пальцев рук, проявления вазомоторных сосудистых реакций, субфебрильная температура. В ряде случаев неврологическая симптоматика выступает на первый план, и больным ставят диагноз нейроциркуляторной дистонии, вегетативного невроза и т. д.
Аллергический синдром при хроническом описторхозе может проявляться кожным зудом, крапивницей, рецидивирующим отеком Квинке, артралгией, пищевой аллергией, умеренной эозинофилией.
Лабораторная диагностика
Лечение
При назначении лечения больным описторхозом необходимо учитывать фазу болезни, вариант ее течения с учетом всех клинических синдромов, степень тяжести и особенности организма (возраст, сопутствующие заболевания и т. д.), возможность супер- и реинвазии.
Лечение описторхоза включает 3 этапа.
1-й этап — подготовительная патогенетическая терапия, направленная на обеспечение должного оттока из желчевыводящих путей и протоков поджелудочной железы; восстановление моторно-кинетической функции желчевыделительной системы; купирование аллергического, интоксикационного синдромов, воспалительных процессов в желчевыводящих путях и желудочно-кишечном тракте.
В качестве противоаллергических средств рекомендуется применение блокаторов Н1-гистаминовых рецепторов, которые назначаются во время курса подготовительной патогенетической терапии, при проведении этиотропной терапии и по показаниям — в период реабилитации.
При наличии воспалительных процессов в желчевыводящих путях показаны коротким курсом (чаще всего 5-дневным) антибиотики широкого спектра действия.
Желчегонная и спазмолитическая терапия должна осуществляться дифференцированно, с учетом типа дискинезии желчевыводящих путей в течение 1–3 месяцев.
Классификация желчегонных препаратов
I. Препараты, стимулирующие желчеобразовательную функцию печени — истинные желчегонные (холеретики):
II. Препараты, стимулирующие желчевыведение:
Из спазмолитических средств можно использовать традиционные препараты (Но-шпа, дротаверин, Бускопан), но предпочтительнее применение селективных препаратов (мебеверина гидрохлорид (Дюспаталин)), ввиду их преимуществ селективности в отношении желудочно-кишечного тракта, отсутствия побочных эффектов; двойного механизма действия (снижение тонуса и уменьшение сократительной активности гладкой мускулатуры), высокой тропности к сфинктеру Одди.
При явлениях холестаза назначаются препараты урсодезоксихолевой кислоты (Урсофальк, Урсосан), Гептрал.
По показаниям применяются прокинетики (метоклопрамид, домперидон — Мотилиум, Мотилак), ферментные препараты (Мезим форте, Креон, Панкреофлат, Пензитал и др.), пре- и пробиотики, средства эрадикационной терапии
Показано физиотерапевтическое лечение (микроволновая терапия, магнитотерапия, электрофорез с 10% раствором сернокислой магнезии), оказывающее спазмолитическое, десенсибилизирующее, микроциркуляторное действия.
2-й этап лечения описторхоза предусматривает проведение специфической химиотерапии. В настоящее время эффективным средством специфической терапии описторхоза является празиквантел. Фармакокинетика празиквантела и его аналогов связана с повышением проницаемости клеточных мембран паразитов для ионов кальция, сокращением мускулатуры паразитов, переходящим в спастический паралич. Препараты празиквантела назначаются из расчета 50–60 мг на 1 кг массы тела больного в 3 приема с интервалом между приемами 4–6 часов. А. И. Пальцев [6] предлагает щадящую методику применения празиквантела, когда указанная суточная доза делится на двое суток. При щадящей методике применения празиквантеля курсовую дозу делят на 6 приемов в течение 2 сут: 3 приема в первые сутки с интервалом 4 ч и 3 — на вторые сутки. По данным автора, антигельминтная эффективность при этом остается такой же.
Противопоказаниями к приему препаратов празиквантела являются повышенная чувствительность к препарату, цистицеркоз глаз и печени, первый триместр беременности, лактация, детский возраст до 4 лет, печеночная недостаточность.
Необходимо отметить, что наличие описторхоза не является абсолютным показанием к дегельминтизации. Например, ее нужно назначать с осторожностью лицам пожилого и старческого возраста. Назначение антигельминтиков больным с тяжелой сопутствующей патологией (декомпенсированные пороки сердца, тяжелые поражения почек и печени и др.) также должно проводиться с известной осторожностью. Лечение препаратами празиквантела рекомендуется начинать не ранее 3-й недели от начала болезни и при уровне эозинофилии не более 20%.
После приема препарата могут возникать побочные явления: головная боль, головокружение, слабость, нарушение координации, тошнота, усиление или возобновление болей в правом подреберье. В большинстве случаев побочные реакции кратковременны и исчезают в течение суток. В части случаев в первые 2–3 недели после лечения больные отмечают общую слабость, усиление болей в животе и диспептических проявлений, возможно появление эозинофилии, ухудшение показателей функциональных проб печени, высыпания на коже типа крапивницы. Эти симптомы обусловлены в основном дополнительным антигенным воздействием в результате гибели гельминтов.
На 2-й день после приема празиквантела назначают дуоденальное зондирование или слепое зондирование с минеральной водой, сорбитом, ксилитом для эвакуации продуктов жизнедеятельности и распада описторхисов. Для увеличения пассажа желчи можно рекомендовать электростимуляцию правого диафрагмального нерва, импульсное магнитное поле.
3-й этап лечения — реабилитационная патогенетическая терапия, направленная на максимальное выведение продуктов жизнедеятельности и распада паразитов: желчегонная терапия, адекватная типу дискинезии желчевыводящих путей, беззондовое дуоденальное зондирование (тюбажи с ксилитом, сорбитом, сернокислым магнием, минеральной водой) 2–3 раза в течение 1-й недели, далее 1–2 раза в неделю (до 3 мес), сорбенты (Лактофильтрум, Энтеросгель, Полифепан и др.), пре- и пробиотики — для восстановления биоценоза кишечника.
При усилении аллергических реакций, интоксикационного синдрома, связанных с дополнительным антигенным воздействием при гибели гельминтов, требуется назначение десенсибилизирующей (антигистаминные препараты, при необходимости — глюкокортикоиды) и дезинтоксикационной (инфузии растворов, сорбенты) терапии.
Комплекс реабилитационных мероприятий включает также прием гепатопротекторов, отваров желчегонных трав в течение 3–4 месяцев (табл.), по показаниям применяют спазмолитики, антихолестатические препараты и другие патогенетические средства.
Контроль эффективности дегельминтизации проводится через 1, 3 и 6 месяцев после лечения: выполняются гельминтоовоскопические исследования фекалий не менее 3 раз в каждый из указанных сроков и исследование дуоденального содержимого. Необходимо подчеркнуть, что паразитологическое выздоровление далеко не всегда сопровождается клиническим выздоровлением: у лиц, страдавших описторхозом более 5 лет, жалобы и объективные изменения, имевшие место в период хронической фазы, сохраняются [4, 6]. Объясняется это наличием глубоких морфологических изменений в органах, сформировавшихся в хроническую фазу болезни. Вопрос же о тактике лечения резидуальных форм описторхоза остается до сих пор нерешенным.
Литература
ГБОУ ВПО НГМУ МЗ РФ, Новосибирск


_575.gif)