Что такое эпителий без атипии
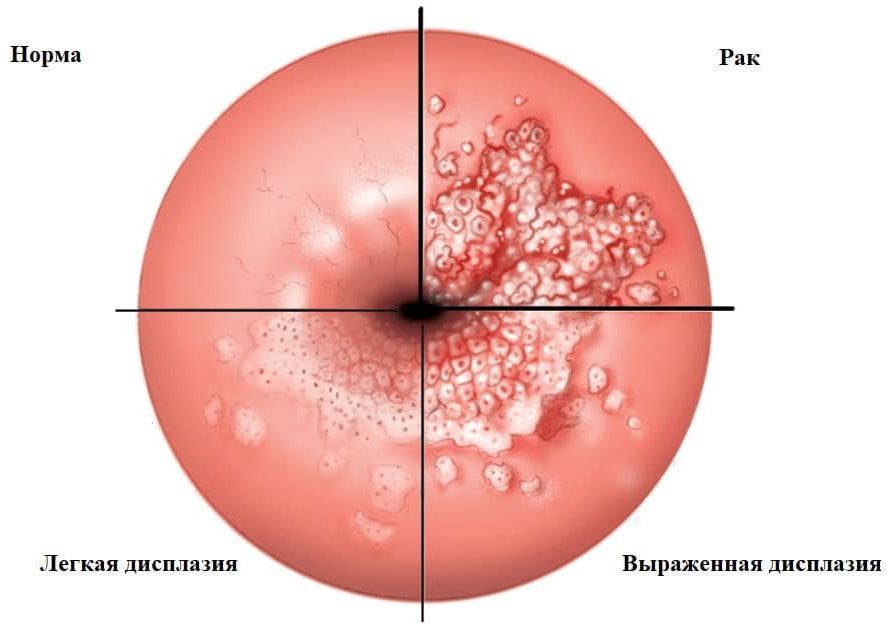
Типичные признаки дисплазии шейки матки
Дисплазия шейки матки — болезнь, которая имеет несколько стадий и почти всегда приводит к раку шейки матки. Только первая стадия у молодых женщин, которая обозначается латинскими буквами LSIL, может пройти сама по себе, во всех остальных случаях пациентке требуется наблюдение, а иногда и оперативное лечение.
Дисплазия — состояние, при котором клетки шейки матки изменили свое строение. Поэтому основной и иногда единственный симптом — плохие результаты анализа на онкоцитологию.
Лечение прижиганием или замораживанием актуально только на ранних стадиях, потом нужно удалять часть органа, чтобы не пропустить и не «запечатать» атипию.
Симптомы дисплазии шейки матки
К сожалению, большинство женщин вообще не испытывают никаких симптомов при дисплазии шейки матки, особенно на ранних стадиях. Могут возникать следующие признаки, характерные в целом для гинекологических патологий:
Но все эти симптомы неспецифичны, только анализ дает возможность поставить диагноз. Признак дисплазии — атипичные изменения в строении клеток шейки матки.
Признаки дисплазии шейки матки
Основа для постановки диагноза — лабораторное исследование мазка. Вот что могут увидеть специалисты, изучая материал:
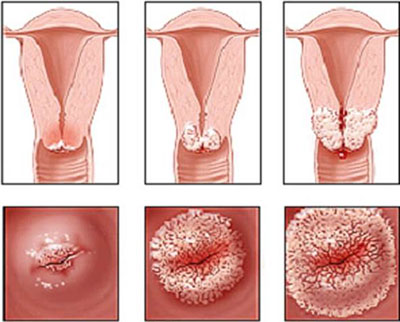
Во время кольпоскопического обследования врач может заметить следующие изменения на шейке матки:
Иногда требуется биопсия, чтобы точно определить, нет ли у женщины дисплазии. Например, анализ на цитологию хороший, но врач видит какие-то изменения на шейке. Так как любой анализ имеет погрешности, женщине могут предложить биопсию сомнительного участка. Чтобы точно знать, что вашему здоровью ничего не угрожает и что с шейкой матки у вас все в порядке, обратитесь в клинику Dr. AkNer.
Онкологические аспекты гиперпластических процессов эндометрия
Гиперплазия — это увеличение количества клеток без увеличения их размеров. Гиперпластические процессы могут предшествовать развитию онкологического заболевания. Гиперплазия эндометрия — одна из форм патологических пролиферативных изменений эндометрия, с преимущественной пролиферацией железистого компонента по сравнению со стромальным компонентом [1].
Существует гистологическая классификация гиперпластических процессов эндометрия, предложенная ВОЗ (2014) [2]:
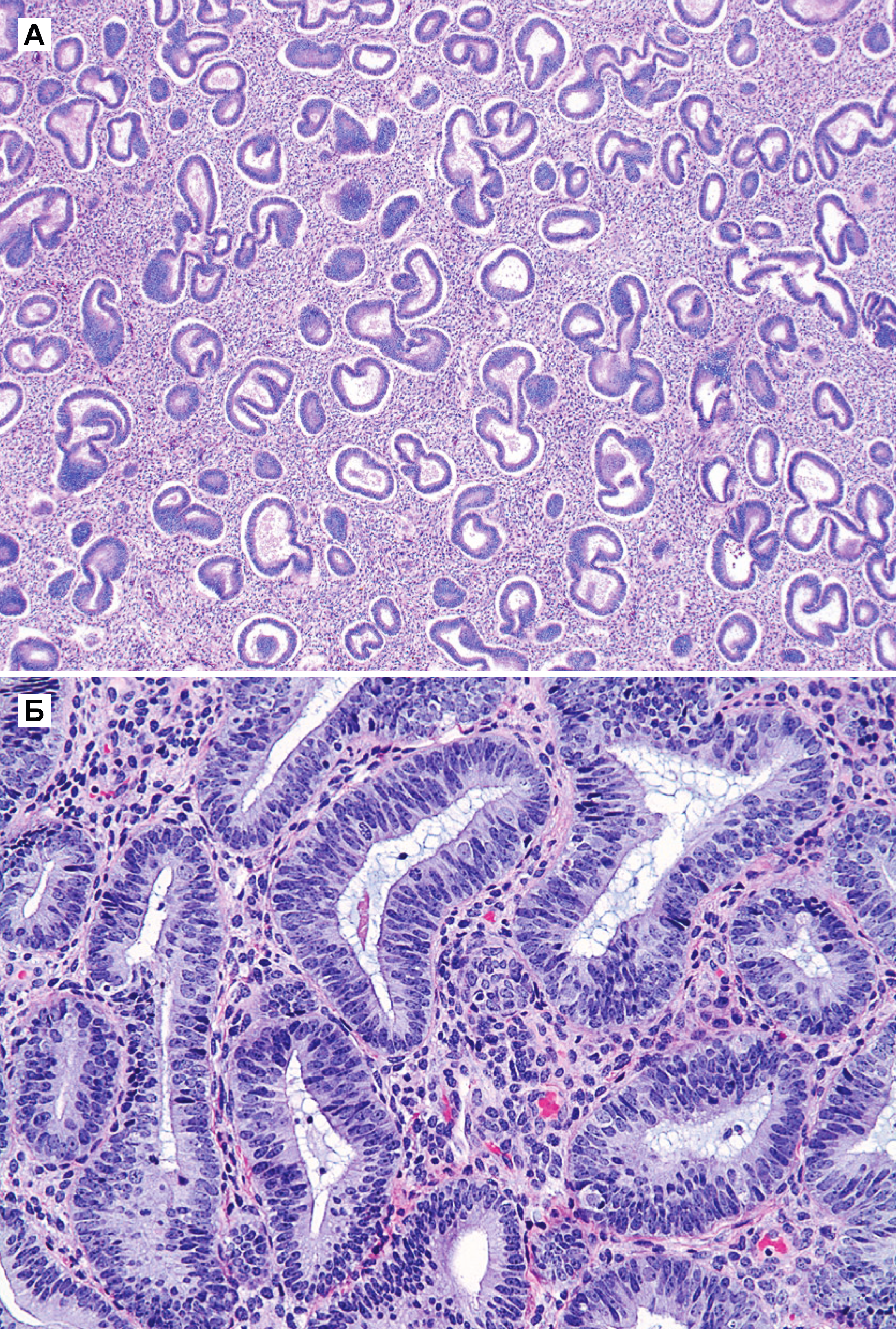
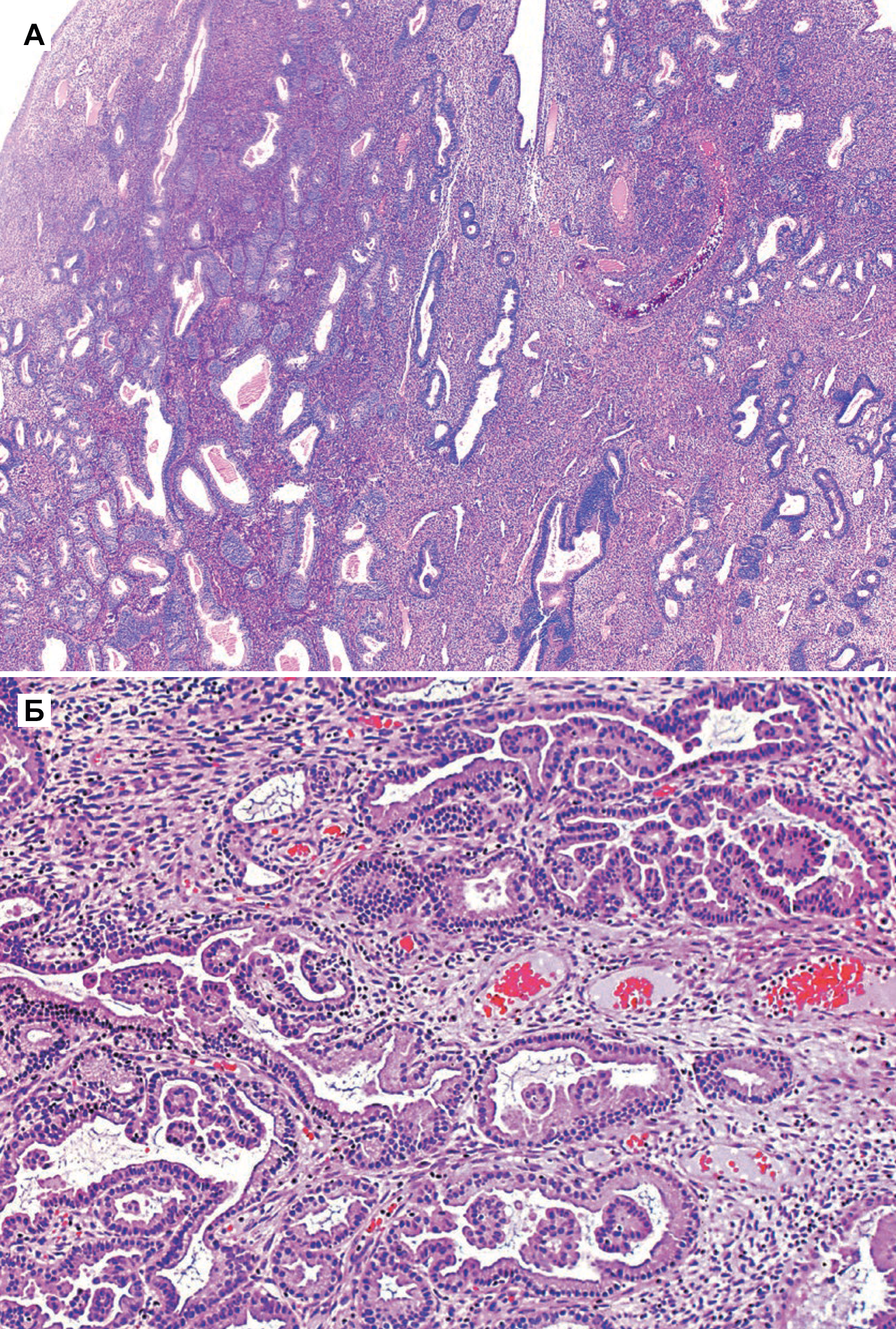
Гиперплазия эндометрия без атипии — это пролиферация с изменением строения желез и клеток, но без клеточной атипии. Изменения в строении обычно видны при малом увеличении, но важной особенностью, которая определяет прогноз и возможность малигнизации — это клеточная атипия. Все типы гиперплазии характеризуются увеличением отношения железы к строме, неравномерностью формы железы и изменением размера железы (рис. 1 а и б). При гиперплазии без атипии железистый эпителий напоминает пролиферирующий эндометрий (рис. 1 б). Клетки столбчатые с амфофильной цитоплазмой и имеют псевдостратифицированные ядра, ориентированы к базальной мембране и имеют овальную форму с гладкими контурами, равномерно распределенный хроматин и небольшие незаметные ядрышки. Митотическая активность может быть переменной и может быть меньше, чем в пролиферирующем эндометрии. Частота митоза не влияет на диагноз [5].
Как правило, гиперплазия диффузная, но может быть очаговой из-за локальных различий в содержании рецепторов эстрогена и прогестерона в эндометрии. При простой гиперплазии присутствует строма в значительном объеме. Строение стромы напоминает нормальное, характерное для пролиферативной фазы, строма состоит из маленьких овальных клеток со скудной цитоплазмой. Как и в железах, в строме отмечена митотическая активность. Когда гиперплазия является полипоидной, строма может содержать артерии с толстой стенкой, подобные тем, которые наблюдаются в полипах. По мере прогрессирования гиперплазии железы располагаются более тесно. Обычно железы плотно прилегают друг к другу, хотя всегда присутствует небольшое количество стромы между ними [5].
К предраковым заболеваниям эндометрия относятся [2]:
Эндометрий — мишень половых гормонов, так как эта ткань имеет специфические рецепторы. Клетки эндометрия обновляются ежемесячно под влиянием гормональной регуляции. Нарушение гормонального статуса женщины может изменять рост и дифференцировку клеток. Поэтому могут возникнуть гиперпластические процессы [2].
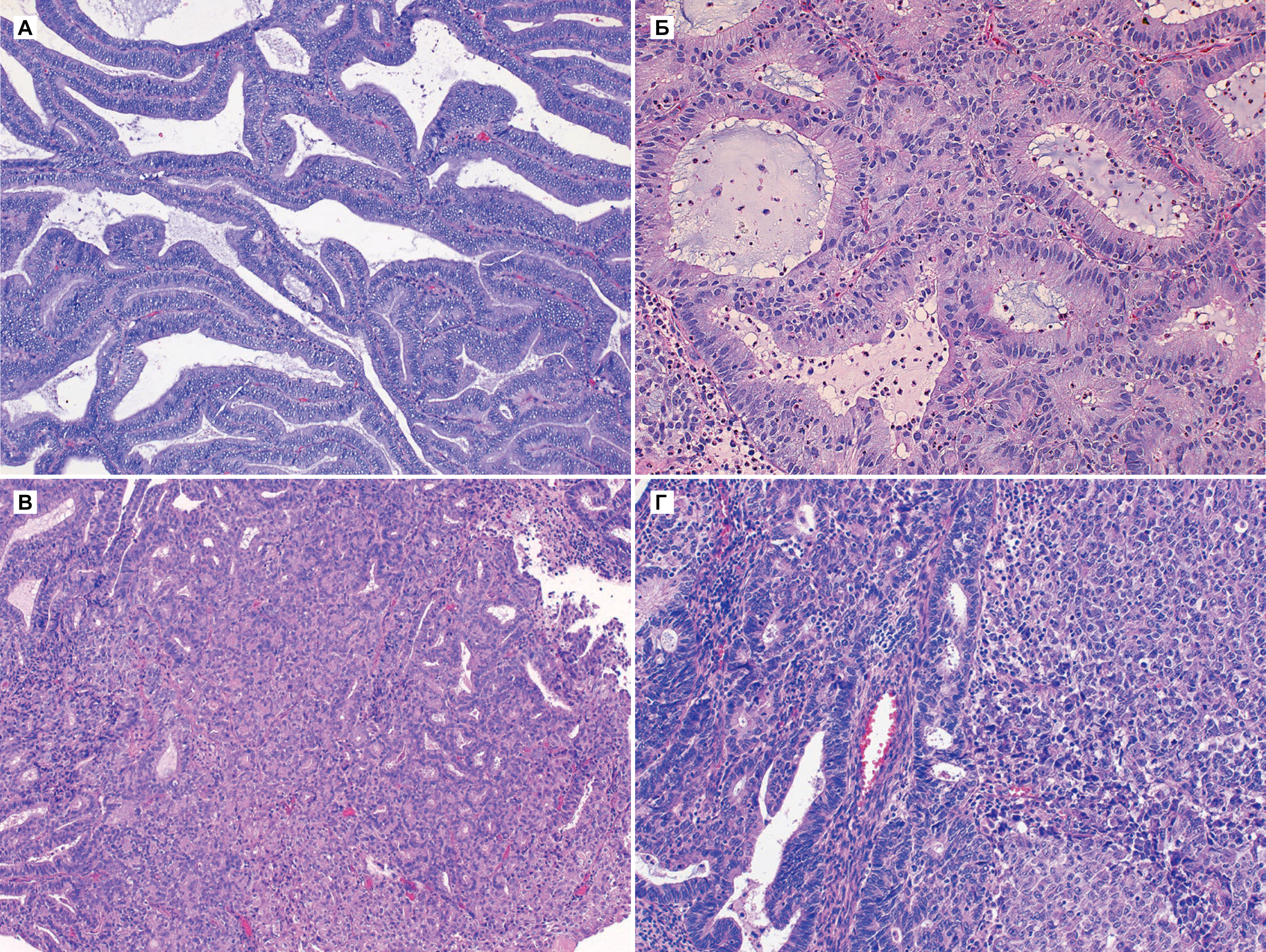
Атипичная гиперплазия отличается наличием ядерной атипии и сложным строением с тесно расположенными железами. Железы обычно неправильной формы и размера. Каждая железа имеет базальную мембрану, окруженную тонким слоем стромы, отделяющей его от соседних желез. Однако в некоторых случаях железы расположены далеко друг от друга. Встречаются как железы без клеточной атипии, так и атипичные [5].
Специфические особенности при атипичной гиперплазии включают: стратификацию, увеличение размера ядер с измененным хроматином и ядрышками. В ядрах отмечена истинная стратификация (2–4 слоя), и потеря ориентирования к базальной мембране [5].
На фоне гиперпластических процессов в эндометрии, возникающих при длительной пролиферации желез эндометрия без перехода их в секреторную фазу, может развиваться рак тела матки (РТМ) — это злокачественная опухоль, происходящая из слизистой оболочки тела матки (эндометрия). Чаще всего РТМ носит спорадический характер, и в 5 % случаев РТМ ассоциирован с наследственными синдромами, например, с синдромом Линча. Среди факторов риска: гиперэстрогения, ранние менархе, отсутствие родов в анамнезе, поздняя менопауза, возраст старше 55 лет, применение тамоксифена [3].
Эпидемиология РТМ
РТМ — самая частая злокачественная опухоль женских половых органов в развитых странах и вторая по частоте после рака шейки матки злокачественная опухоль женских половых органов в мире. В США в 2015 г. зарегистрировано более 54800 новых случаев заболевания РТМ, и более 10150 смертей от этого заболевания. В России ежегодно регистрируется более 21 тысячи больных РТМ. В структуре заболеваемости женского населения в России в 2016 г. РТМ занимал 3-е ранговое место (7,7 %). Средний возраст заболевших РТМ в России составляет 62,6 года [3,4].
Патогенез
Развитие РТМ обусловлено гиперэстрогенией, основной причиной которой является нарушение овуляции. Клиническое изучение метаболических нарушений у больных раком тела матки и морфологические особенности рака эндометрия позволили обосновать концепцию о двух основных патогенетических вариантах заболевания [2].
I тип (более частый). Опухоль развивается в более молодом возрасте, в отличие от пациенток II патогенетического варианта, на фоне длительной гиперэстрогении и гиперплазии эндометрия. У больных РТМ I патогенетического типа часто наблюдаются ожирение, сахарный диабет и гипертоническая болезнь, возможны эстрогенсекретирующие опухоли яичников или синдром склерокистозных яичников. Опухоли I патогенетического варианта, как правило, высокодифференцированные, имеют более благоприятный прогноз [2].
II тип. Опухоли эндометрия обычно низкодифференцированные, имеют менее благоприятный прогноз. Опухоли II патогенетического типа возникают в более старшем возрасте, в отсутствие гиперэстрогении, на фоне атрофии эндометрия. Примерно у 80% больных РТМ диагностируют эндометриоидную аденокарциному [2].
Выделяют три степени дифференцировки аденокарциномы эндометрия [2]:
G1 — высоко дифференцированная;
G2 — умеренно дифференцированная;
G3 — низко дифференцированная или недифференцированная.
Клиника
Ранний симптом прогрессирования рака эндометрия — появление жидких водянистых белей, нередко с примесью крови, и зуда наружных половых органов. Кровянистые выделения из половых путей бывают в виде мажущих серозно-кровянистых выделений, которые становятся порой обильными. Кровотечение, как правило, контактное или появляется после физической нагрузки [2].
Возможны боли внизу живота, которые на ранних стадиях рака носят схваткообразный характер. Это связано с сокращениями эндометрия и опорожнением матки от скопившейся в ней крови или гноевидной жидкости (гематометра, пиометра), отток которой в результате обтурации внутреннего зева затруднен. После таких схваткообразных болей появляются обильные выделения из матки — гной и кровь. При поздних стадиях боли постоянные, особенно интенсивные по ночам, связаны со сдавлением раковым инфильтратом нервных сплетений в малом тазу. При переходе процесса на мочевой пузырь и прямую кишку появляются симптомы нарушения функционирования этих органов [2].
Хирургическое вмешательство рекомендуется как наиболее эффективный метод лечения РТМ независимо от стадии как самостоятельно, так и в комбинации с другими методами [6].
Список литературы:
Что такое атипичные клетки шейки матки
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/02/atipichnye-kletki.png?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/02/atipichnye-kletki.png?fit=829%2C550&ssl=1″ />
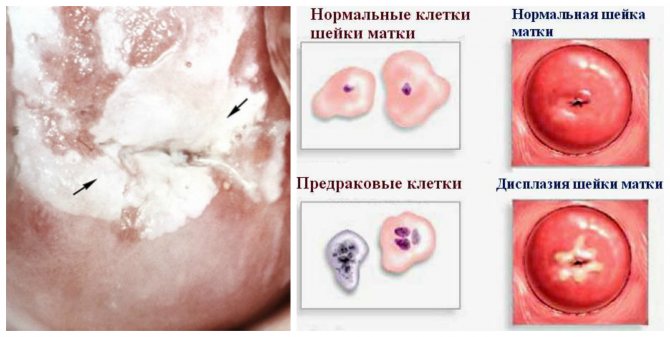
Нарушение строения эпителиальных клеток — это термин для обозначения клеток необычного размера или формы, обнаруженных на шейке матки. Этот результат теста, чаще всего полученный после мазка Папаниколау, не обязательно указывает на злокачественный рост опухоли, но уже говорит о том, что могут быть предраковые клетки или начальные раковые клетки.
Особенности анализа на атипичные клетки
Типы аномалий
Атипичные эпителиальные клетки делятся на две широкие категории: плоскоклеточные и железистые.
Наиболее распространенными типами являются атипичные плоскоклеточные клетки (ASC), плоскоклеточные интраэпителиальные образования (SIL) или плоскоклеточный рак. Проблемы, возникающие обнаружением железистых клеток обычно классифицируются как атипичные железистые клетки (AGC) или аденокарцинома.
Из обнаруженных плоскоклеточных и железисто-клеточных аномалий только имеющие признаки плоскоклеточного рака и аденокарциномы почти наверняка указывают на развитие рака.
ASC-клетки
ASC-клетки явно не нормальны, но не совсем понятно, почему. Клетки в этой категории могут быть либо атипичными плоскоклеточными неопределенного значения (ASCUS), либо атипичными плоскоклеточными клетками с возможными изменениями высокого уровня риска рака (ASC-H).
Кольпоскопия — диагностический тест, при котором гинеколог визуально исследует внутреннюю часть влагалища на наличие патологий или повреждений.
SIL-клетки
SIL — это клетки, образующие наросты на поверхности шейки матки, которые могут привести к раку. Они относятся к категории среднего или высокого риска в зависимости от вероятности возникновения рака.
После обнаружения SIL-клеток специалист обычно рекомендует кольпоскопию или биопсию, чтобы подтвердить уровень риска, связанного с обнаружением данной клетки.
Плоскоклеточный рак
Плоскоклеточный рак — наиболее распространенный тип рака шейки матки и может быть смертельным, если его не лечить.
Если на него указывает мазок Папаниколау, гинекологи срочно проводят кольпоскопию или биопсию, чтобы определить, на какой стадии находится рак, начиная с «in situ», что означает, что раковые клетки существуют, но еще не распространились в ткани, до стадии 4, на которой рак распространился за пределы шейки матки.
Как только это будет определено, женщина может начать лечение.
AGC-клетки
Их обнаружение может указывать на то, что у железистых клеток в шейке матки или слизистой оболочке матки, также называемой эндометрием, могут возникнуть проблемы. Около половины случаев обнаружения AGC-клеток не вызывают беспокойства, как ASCUS. Однако они могут быть предраковыми, поэтому также нужно пройти биопсию для уверенности.
Аденокарцинома
Это довольно редкий тип рака, который похож на плоскоклеточный рак, но поражает железистые клетки.
Как и в случае обнаружения плоскоклеточного рака, необходимо срочное дополнительное тестирование для определения стадии рака, а затем начинают лечение.
Причины
Одна из причин появления аномальных эпителиальных клеток — дисплазия шейки матки. В этом случае шеечные клетки растут ненормально, и они либо имеют странную форму, либо разрастаются в огромных количествах.
Рост клеток не является однозначно злокачественным симптомом, но со временем аномальная клетка может переродиться в рак в течение примерно 10 лет или немного дольше. Дисплазия шейки матки чаще встречается у женщин от 25 до 35 лет и обычно не имеет симптомов.
Иногда сообщается о необычных клетках, возникающих из-за инфекций, таких как герпес и вирус папилломы человека. ВПЧ — один из ведущих факторов риска развития рака шейки матки.
Наличие паразитов или грибковых инфекций также может дать положительный результат. Клеточная ткань может оказаться ненормальной из-за травмы. Если есть подозрение на инфекцию или травму, то, как правило, не возникает проблем с диагностикой рака в результате обнаружения такой аномалии эпителиальных клеток.
Лечение
Лечение аномалий эпителиальных клеток зависит от конкретной проблемы.
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
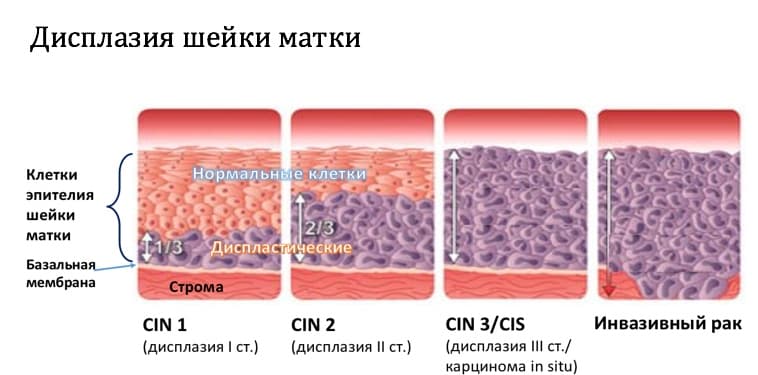
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Что ПАП-мазок может показать, классификация заключений, расшифровка ПАП-мазка
Проведение ежегодной диспансеризации позволяет выявить отклонения, хорошо поддающиеся коррекции. Лечение малых проблем и назначение соответствующей профилактики позволяют укрепить здоровье, обеспечить долгую и полнокровную жизнь. И.И.Гузов, к.м.н., главный врач ЦИР
Результаты ПАП-мазка могут указывать на доброкачественные изменения клеток, в том числе, инфекции, реактивные (воспалительные) изменения, атрофические изменения и злокачественные поражения.
В первую очередь оценивается качество мазка: исследуют только мазки достаточного качества.
К другим составляющим образцов относятся лейкоциты, эритроциты и другие клетки крови, слизь, флора и другие, более редкие, компоненты.
Число и тип клеток в мазке зависит от возраста и гормонального статуса женщины. Мазок должен содержать достаточное количество видимых клеток плоского эпителия, чтобы быть признанным мазком удовлетворительного качества.
В конце практически всегда указывается заключение. В разных странах используются разные цитологические классификации. Наиболее распространена классификация Bethesda (Бетезда) разных лет утверждения (The Bethesda System, TBS).
Заключение «NILM» — Negative for intraepithelial lesion or malignancy — говорит об отсутствии внутриклеточного поражения или злокачественности, то есть клетки не изменены, онкологической настороженности нет. По другой классификации это заключение звучит как «цитограмма без особенностей».
Возможные особенности цитограммы в пределах нормы — атрофический типа мазка, например, после родов или в связи с возрастными изменениями. Некоторые изменения эпителия также могут быть при беременности, при приеме гормональных контрацептивов.
Измениния, относящиеся к дисплазии, обычно появляются за несколько лет до развития инвазивного рака.
Общая классификация изменений плоского эпителия
Степени дисплазии по глубине поражения эпителия
Плоскоклеточный инвазивный рак: стадия уточняется при гистологическом исследовании после биопсии, подтверждается после операции.
Требуется дообследование и лечение, повторение анализа через несколько месяцев.
Необходимо дообследование, динамическое наблюдение, лечение.
В зависимости от степени поражения может быть рекомендовано: повторение ПАП-мазка, анализ на HPV, кольпоскопия, а по результатам и биопсия шейки матки.
Необходимо дообследование и лечение.
Изменения в железистом эпителии
Система классов — это устаревшая система классификации ПАП-мазков по Папаниколау
Также существуют классификации ВОЗ, обучающей программы европейской комиссии