Оланзапин что за препарат
Оланзапин что за препарат
Проблема оптимальной профилактики тошноты и рвоты остается одной из наиболее актуальных и злободневных для всех практикующих врачей-онкологов. Развитие тяжелой тошноты, а тем более рвоты на фоне проведения даже успешной противоопухолевой терапии может оказать поистине опустошающее влияние на повседневную жизнь пациента и его близких. До появления современных режимов противорвотной терапии её развитие отмечалась более чем у 90% пациентов, получавших высокоэметогенную химиотерапию [1]. За последнее десятилетие арсенал лекарственных препаратов, доступных онкологам и пациентам, значительно расширился, однако проблема остается до конца нерешенной – до 50% пациентов по-прежнему испытывают тошноту на фоне лечения [2].
Одним из последних «прорывов» в лечении тошноты и рвоты у онкологических пациентов стал оланзапин – препарат, который изначально был разработан как лекарственное средство для лечения различных заболеваний психической сферы. Оланзапин обладает ингибирующей активностью в отношении 5-HT2a, 5-HT2c, 5-HT3, 5-HT6 рецепторов, различных подтипов дофаминовых рецепторов (D1-4), H1-гистаминовых рецепторов, а также холинергического и адренергического путей передачи сигнала в центральной нервной системе – то есть спектр его фармакологической активности включает многие «мишени», участвующие в развитии тошноты и рвоты на фоне проведения противоопухолевой терапии. Результаты многих клинических исследований продемонстрировали высокую эффективность оланзапина в профилактике тошноты и рвоты у онкологических пациентов 3.
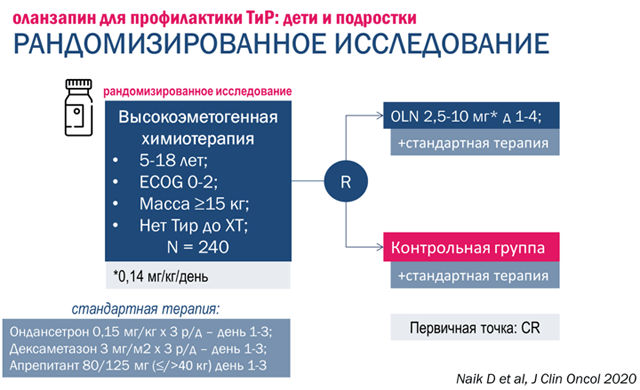
В сентябре 2020 года в Journal of Clinical Oncology были представлены результаты рандомизированного исследования, посвященного изучению эффективности оланзапина в комбинации со «стандартной» противорвотной терапией апрепитантном, ондансетроном и дексаметазоном. В исследование включались пациенты в возрасте от 5 до 18 лет, которым была назначена высокоэметогенной химиотерапия. Пациенты рандомизировались в соотношении 1:1 в группу оланзапина или контрольную группу, дизайн исследования схематично изображен на рисунке 1. Оценка эффективности лечения проводилась при помощи специальных опросников после первого курса химиотерапии. Первичной конечной точкой исследования была частота полного контроля тошноты и рвоты (отсутствие рвоты и потребности в использовании дополнительных противорвотных препаратов в течение 120 часов после проведения курса химиотерапии) [7].
По результатам исследования частота полного контроля тошноты и рвоты в общем периоде (0-120 часов) составила 64% в группе оланзапина по сравнению с 38% в контрольной группе (p
Оланзапин что за препарат
Университетская клиника головной боли, Москва
Всовременных условиях для практикующих врачей различных специальностей возникает возможность использовать широчайшее информационное поле для междисциплинарного взаимопроникновения в терапию различных заболеваний. Успешное и правильное использование специфических лекарственных средств, к которым относятся нейролептики, невозможно без знания не только их формальных показаний, противопоказаний и побочных эффектов, но и правильного понимания их механизма действия, оправданности их назначения. За последние годы оланзапин нашел широкое применение не только в психиатрических стационарах в качестве одного из основных антипсихотиков, но и в амбулаторных условиях как часто используемый препарат для постпсихотического поддерживающего и профилактического лечения [2], а также при терапии пограничных неврозо- и психопатоподобных состояний, например деперсонализационных, тревожных, обсессивно-компульсивных расстройств, а также негативных личностных расстройств с социальным снижением, ослаблением мотиваций, когнитивными нарушениями. Следовательно, кардиологам, невропатологам, эндокринологам и другим специалистам приходится все чаще сталкиваться с пациентами, принимающими оланзапин или, возможно, нуждающимися в его приеме.
Оланзапин является современным атипичным нейролептиком. Данная группа препаратов характеризуется в первую очередь отсутствием или наличием только дозозависимых экстрапирамидных побочных эффектов, таких как паркинсонизм, дистония, тремор, атетоз, акатизия, тики, миоклонии, стереотипии. Благодаря лучшей переносимости атипичных нейролептиков, и оланзапина в частности, была решена серьезнейшая проблема низкой приверженности пациентов к лечению и профилактике периодических психозов и эндогенных заболеваний с непрерывным течением. Тем же вызваны успехи в профилактике возникновения поздних злокачественных дискинезий, связанных с применением традиционных нейролептиков (галоперидола, трифтазина, клопиксола и т.д.), которые требовали отдельного подхода и тяжело поддавались лечению [12].
Другой очень важной особенностью атипичных нейролептиков, в т.ч. и оланзапина, служит способность значительно снижать выраженность негативной симптоматики (эмоциональной уплощенности, нарушений мышления, снижения социальной активности, обеднения речи). По своему химическому строению оланзапин является производным тиенобензодиазепина. В структурном отношении оланзапин представляет собой 2-метил-4-(4-ме-тил-1-пиперазинил)-10Н-тиено[2.3-Ь] [1,5]бензодиазепин. Препарат был зарегистрирован в России в 1997 г. (регистрационное удостоверение П-8-242 № 009601) и начал активно применяться с 2000-х гг. Впервые врачи и пациенты узнали оланзапин под коммерческим названием «Зипрекса» (Eli Lilli). Препарат имеет различные формы выпуска: таблетированную в виде таблеток и жидкую в виде раствора для инъекций. На сегодняшний момент помимо оригинального препарата на российском рынке существует немалое количество генериков оланзапина, таких как зипрекса-зидис, выпускаемый также Eli Lilli, заласта и заласта-Ку-таб (KRKA), оланзапин (Тева, Израиль; KERN Pharma), эголанза (EGIS), парнасан (Gedeon Richter).
Особенности фармакокинетики и фармакодинамики оланзапина
Было установлено, что препарат связывается с дофаминовыми рецепторами типа D1, D2, D3, D4 и D5, с серотониновыми рецепторами типа 5НТ2А, 5НТ2С, 5НТ3 и 5НТ6, гистаминовыми рецепторами – Н1- и α1-адренергическими рецепторами, а также мускариновыми рецепторами — М1. Тропизм оланзапина к серотониновым рецепторам превышает сродство к дофаминергическим рецепторам типа D2, что является отличительной особенностью всех атипичных нейролептиков. В общем виде сравнительное антагонистическое влияние оланзапина на нейрорецепторы можно представить в следующем виде: 5НТ2А > Н1 > 5НТ2С > M1 > D2 > D4 > α1.
В соответствии с этим в клинических условиях оланзапин уменьшает проявления негативной симптоматики (за счет блокады серотониновых рецепторов типа 5НТ2А), вызывает умеренный седативный эффект и усиление аппетита (за счет блокады гистаминовых рецепторов). Относительно слабая блокада дофаминовых рецепторов по отношению к холинергическим мускариновым рецепторам предполагает отсутствие побочных неврологических эффектов. Слабая блокада а-адренергических рецепторов свидетельствует об отсутствии явлений заторможенности, чрезмерной седации и влияния на сосудистый тонус (ортостатическая гипотензия и рефлекторная тахикардия). Таким образом, профиль психофармакологической активности оланзапина характеризуется значительной поливалентностью, что отличает препарат как от классических, так и от некоторых новых атипичных антипсихотиков. При изучении и анализе фармакокинетики было установлено, что максимальная концентрация препарата в плазме крови после однократного перорального приема достигается через 5–8 часов. Оланзапин быстро всасывается из желудочно-кишечного тракта независимо от приема пищи. Концентрация препарата в плазме нарастает пропорционально вводимой дозе. Время его полужизни составляет в среднем 33 часа, что позволяет принимать его 1 раз в сутки. У лиц старше 65 лет период полувыведения оланзапина может существенно удлиняться, поэтому среднесуточные дозы препарата должны быть ниже обычных. Устойчивая концентрация препарата в плазме достигается через 5–7 дней приема. Около 60 % оланзапина в виде метаболитов выводится с мочой, но у лиц с нарушением функции почек период полувыведения и клиренс оланзапина не меняются[10, 11].
Было обнаружено, что карбамазепин и фенитоин вызывают индукцию фермента CYP ЗА, что может часть больных приводить к снижению концентрации оланзапина в плазме крови. Напротив, флуоксетин, флувоксамин и циметидин тормозят активность ферментов CYP 1А2, что может вызывать повышение концентрации препарата в плазме [22, 23].
На фоне устойчивой концентрации оланзапина фармакокинетика этанола не изменяется. Однако прием этанола вместе с оланзапином может сопровождаться усилением фармакологических эффектов оланзапина, например седативного действия. Совместное применение оланзапина с этанолом или диазепамом повышает риск развития ортостатической гипотензии.
В условиях in vitro оланзапин обнаруживает антагонизм в отношении дофамина и, как и другие нейролептики, теоретически может подавлять действие леводопы и агонистов дофамина.
Из всего вышесказанного можно сделать вывод о достаточно широком спектре применения препарата оланзапин.
Как гласит официальная информация о показаниях к применению препарата, к ним относятся:
Наряду с информацией, полученной из исследований по общей эффективности данного препарата, поводились и сравнительные исследования с традиционными нейролептиками в лечении острых психозов. В ходе данных исследований была выявлена высокая эффективность оланзапина, не уступающая традиционным нейролептикам. [5, 7, 14, 20, 24].
Типичная динамика антипсихотического действия оланзапина состоит в следующем: как правило, в первые дни применения отмечается определенный седативный эффект без выраженной заторможенности, что проявляется в виде легкой сонливости, редукции тревоги и психомоторного возбуждения. По мере адаптации к действию препарата выраженность седации уменьшается, больные становятся более активными [1].
У больных с обострениями параноидной шизофрении уже с первых дней можно отметить влияние препарата на выраженность бредовых расстройств, негативизма, агрессивности и других нарушений поведения, которые редуцируются практически одновременно с аффективными расстройствами (страхом, тревогой, явлениями растерянности). В течение первых двух недель терапии больные становятся более доступными и открытыми в плане своих переживаний, которыми охотно начинают делиться с лечащим врачом. Существенно, что довольно быстро (в течение 2–3-й недели) у многих больных восстанавливается критика и возникает частичное осознание болезни еще при наличии сохранных бредовых и галлюцинаторных расстройств [3, 6, 13].
Вышесказанное особенно важно для формирования приверженности больного к терапии. Как правило, больной достаточно позитивно оценивает терапевтический успех и связывает этот эффект с лечением. Наиболее заметна подобная реакция больных с повторными приступами болезни, когда они отмечают отсутствие заторможенности, «лекарственной загруженности», побочных нейролептических проявлений, что, как правило, неизбежно ассоциируется с терапией классическими нейролептиками. Подобный позитивный настрой позволяет продолжить терапию и воздействовать на негативную симптоматику в виде аутизма, эмоционального уплощения, трудностей контакта с окружающими. Больные все больше становятся обращенными к окружающему миру, начинают интересоваться состоянием дел в семье, с теплотой заботиться о родных и близких. При этом во внешнем облике больных появляются живость, активность, эмоциональность, естественность, открытость, которые отсутствовали в остром периоде болезни. Нормализуется речевое общение с персоналом и другими больными. В последнюю очередь (через 6–8 недель) улучшается мыслительная способность больных (когнитивная сфера).
Опыт терапии оланзапином больных параноидной шизофренией с преобладанием негативных расстройств показывает, что устойчивая редукция негативных признаков по шкале позитивных и негативных синдромов PANSS (Positive and Negative Syndrome Scale) [4, 17] отмечается в течение 6 месяцев и лишь после этого она замедляется и у некоторых больных выходит на уровень плато. В целом коррекция дефицитарных проявлений (негативных и когнитивных нарушений) происходит крайне постепенно и требует длительной (от 3 до 9 месяцев) терапии оланзапином в сочетании с адекватной психотерапией, дифференцированной психологической коррекцией и социально-трудовой реабилитацией [16].
Динамика психотической симптоматики в процессе лечения оланзапином шизоаффективного расстройства и других острых психозов отличается гармоничным характером. При этом на 2–3-й неделе терапии происходит равномерная редукция как аффективных, так и бредовых и галлюцинаторных расстройств с быстрым восстановлением критики к психозу. Все это сопровождается нарастанием психической активности больных. В ряде случаев наступает резкий обрыв приступа с полной редукцией всех продуктивных расстройств и критикой к заболеванию, что напоминает действие шоковых методов. Особенно часто это происходит при острейших состояниях, сопровождающихся напряженными аффектами (страх, тревога, экстаз, гнев, растерянность), изменчивостью симптоматики, нарушениями сознания, онейроидно-кататоническими расстройствами.
Эффективность препарата в отношении больных шизоаффективным расстройством в целом выше, чем больных шизофренией, что характерно вообще для всех нейролептиков. Характер редукции аффективной симптоматики при терапии оланзапином показывает, что несколько лучших результатов терапии можно добиться при наличии депрессивного аффекта в картине острого психоза, в т.ч. при депрессивно-параноидном варианте. Маниакально-бредовые и особенно маниакальные состояния на терапию препаратом реагируют несколько хуже. Для более быстрого контроля над возбуждением нередко требуется присоединение седативных нейролептиков. Тем не менее препарат можно применять как для купирования острых маниакально-бредовых состояний, так и для лечения психозов более сложной структуры с отчетливыми маниакальными включениями [21].
Особо следует остановиться на характере соматотропных эффектов оланзапина. Для препарата очень характерен т.н. трофотропный эффект, что находит свое выражение не только в увеличении массы тела [9], но и в нормализации пищевого поведения вообще, а также в улучшении цвета кожных покровов и слизистых оболочек. Это актуально для депрессивно-бредовых состояний с резким снижением аппетита на высоте депрессивного состояния (F31.5).
Профиль психотропной активности оланзапина позволяет использовать препарат при лечении практически всех клинических форм шизофрении с различной выраженностью продуктивной и негативной симптоматики и на разных стадиях патологического процесса, т.е. при лечении как острых и подострых, так и хронических состояний, в т.ч. с грубыми дефицитарными расстройствами. Вполне обоснованно применение оланзапина и в качестве поддерживающей терапии больных шизофренией с длительным течением. В этих случаях можно использовать препарат в виде монотерапии и рассчитывать на развитие стойкого профилактического (противорецидивного) эффекта с улучшением нейрокогнитивных процессов у больных. Это в свою очередь приводит к повышению уровня их социальной адаптации и качества жизни.
В силу доказанной эффективности при лечении негативных расстройств оланзапин получил широкое применение в амбулаторной терапии в рамках таких расстройств, как неврозоподобные (обсессивно-компульсивные, деперсонализационные), психопатоподобные и поведенческие расстройства в рамках малопрогредиентной шизофрении и шизотипического расстройства (F21). Пациенты данной группы отмечают улучшение работоспособности, когнитивных возможностей, возрастание мотивации, а также значительное ослабление деперсонализационных расстройств (отчужденности, дезавтоматизацияи психических процессов), редукцию обсессивных расстройств, улучшение коммуникации.
Способ применения оланзапина и особенности дозирования
Дозы препарата подбираются эмпирическим путем в зависимости от клинической картины психоза. Препарат можно принимать однократно за сутки независимо от приема пищи. Стандартная начальная доза оланзапина составляет 5–10 мг/сут. При необходимости дозу постепенно повышают, однако увеличение суточной дозы выше 15 мг рекомендуется осуществлять не ранее чем через 4 дня после начала приема препарата.
Следует иметь в виду, что улучшение состояния может быть достигнуто на малых и средних дозах. Максимальная суточная доза составляет 20 мг. Хотя повышение дозировки не сопровождается увеличением числа побочных эффектов, заметного усиления клинического эффекта также не происходит. Поэтому превышать дозу в 20 мг/сут не рекомендуется. При лечении лиц пожилого и старческого возраста, а также лиц с тяжелой соматической патологией препарат следует использовать в дозах, меньших в 1,5–2,0 раза.
При лечении шизофрении и сходных психотических расстройств пациентам с малой прогредиентностью процесса можно рекомендовать более низкие дозы оланзапина (порядка 5–10 мг/сут), а при более прогредиентных формах (параноидная непрерывная, юношеская злокачественная и параноидная приступообразная форма) – средние и высокие дозы препарата (15–20 мг/сут). При формах с большим удельным весом аффективной и чувственно-бредовой симптоматики, т.е. при явных приступообразных формах и шизоаффективном расстройстве, эффективную дозу следует подбирать эмпирическим путем, но обычно она редко превышает 15 мг/сут. При т.н. хронических бредовых психозах (параноидных расстройствах) доза должна быть максимальной, т.е. 20 мг/сут [1]. Начинать лечение больных, склонных к развитию седации, можно с дозы 5 мг/сут.
Период стабилизации психического состояния продолжается не менее 2–3 месяцев. При полном контроле состояния доза оланзапина постепенно снижается и обычно составляет 10–15 мг/сут. Развитие побочных эффектов — сигнал к снижению дозы либо отмене препарата.
Поддерживающая (противорецидивная) терапия обычно проводится в дозах, отработанных на предшествующем этапе. Рекомендовано сохранение уровня доз на протяжении нескольких месяцев, после чего можно предпринимать попытку снижения дозы. При хорошем состоянии (без психотической симптоматики и при минимальной выраженности дефекта) вопрос о прекращении приема препарата можно рассматривать не ранее чем через 1,5–2,0 года его непрерывного применения. У впервые выявленных больных шизофренией, т.е. перенесших первый психотический эпизод, длительность непрерывной поддерживающей терапии оланзапином должна также составлять не менее 2 лет [2]. Длительность непрерывного приема препарата больными, имеющими в анамнезе большее число эпизодов, возрастает еще на 2–3 года.
Перевод с классических нейролептиков на оланзапин возможен на любом этапе лечения больного, особенно при выраженных экстрапирамидных побочных эффектах или резистентности к проводимой терапии [8]. Как правило, осуществляется перекрестное применение препаратов с последующим постепенным уменьшением доз предыдущей терапии. Начальная доза и темп наращивания дозы оланзапина зависят от клинического состояния больного. Несмотря на то что оланзапин крайне редко вызывает побочные экстрапирамидные расстройства и даже, согласно некоторым исследованиям, способен положительно влиять на их динамику, при наличии выраженных нейролептических проявлений вследствие предыдущей терапии следует на некоторое время сохранять прием антихолинергических корректоров.
Побочные эффекты, меры предосторожности и осложнения
Побочные эффекты при терапии оланзапином носят особый характер и значительно отличаются от таковых у классических нейролептиков. Одним из наиболее часто встречающихся побочных эффектов (наблюдается не менее чем у 30–50 % больных) является прирост массы тела. Это связывают с высокой антигистаминной активностью препарата, что стимулирует аппетит и, соответственно, приводит к повышению массы тела.
В среднем увеличение массы тела составляет около 2 кг за 6 недель терапии. Примерно у трети больных, принимающих оланзапин, прирост массы тела составляет более 7 % от первоначальной массы [9]. С целью коррекции этого побочного эффекта больному в первую очередь рекомендуется диета с уменьшенным содержанием калорий, при неэффективности возможно снижение суточной дозы препарата. Установлено, что у большинства больных повышение массы тела по мере продолжения лечения оланзапином на 2–3-м месяце достигает плато и больше не прогрессирует.
Вторым по частоте побочным эффектом, развивающимся почти у трети больных, является сонливость, которая также связана с антигистаминными свойствами препарата. Сонливость обычно больше выражена в первые дни приема оланзапина, проходит по мере продолжения лечения и адаптации к действию препарата.
Еще одним значительно распространенным побочным эффектом у больных, получающих оланзапин (примерно треть), служит незначительное повышение концентрации пролактина в плазме крови. Клинические проявления гиперпролактинемии, связанные с приемом оланзапина (гинекомастия, галакторея и увеличение молочных желез), отмечаются редко. У большинства больных нормализация уровня пролактина наблюдается без отмены препарата. Тем не менее при длительном приеме оланзапина рекомендуется периодически проводить обследование на гиперпролактинемию [10]. Побочные эффекты, связанные с холинолитическим действием (головокружение, акатизия, тремор, диспептические расстройства, периферические отеки, ортостатическая гипотензия, сухость во рту, запоры, задержка мочеиспускания) хотя и развиваются достаточно редко, однако о них следует помнить лицам с клинически значимой гипертрофией простаты, закрытоугольной глаукомой, паралитической непроходимостью кишечника и сходными состояниями.
По сравнению с классическими нейролептиками оланзапин практически не вызывает таких экстрапирамидных побочных эффектов, как лекарственный паркинсонизм, острые и поздние дискинезии [24]. Тем не менее следует помнить, что по мере повышения суточной дозы препарата и длительности применения вероятность их возникновения возрастает и у некоторых больных может возникать лекарственная акатизия при терапии оланзапином (около 5 %). В этих случаях целесообразно назначать антипаркинсонические корректоры, транквилизаторы бензодиазепинового ряда или β-адреноблокаторы.
При лабораторных исследованиях изредка наблюдается транзиторное, асимптоматическое увеличение печеночных трансаминаз, повышение уровня глюкозы в плазме крови более 200 мг/дл (подозрение на диабет), а также от 160 до 200 мг/дл (подозре-ние на гипергликемию) у больных с исходным уровнем глюкозы менее 140 мг/дл. Поэтому больным с повышенным риском целесообразно проведение консультации эндокринолога и многократных анализов крови на уровень сахара. В случае развития кетоацидоза и при подтверждении диагноза сахарного диабета терапию оланзапином следует немедленно прекращать.
После продолжительного лечения может развиваться синдром отмены (т.н. холинергические симптомы отдачи). Его риск при отмене данного препарата (так же как и клозапина) значительно выше, чем при отмене традиционных нейролептиков. Причины его возникновения предположительно связаны с развитием при приеме нейролептика гиперчувствительности холинергических и дофаминергических рецепторов, а также с тем, что оказываются задействованными серотонинергическая, норадренергическая, ГАМКергическая и серотонинергическая системы. Резкая отмена оланзапина допустима лишь при наличии серьезных клинических показаний, и без консультации с врачом, без постепенного снижения дозы отменять препарат нежелательно.
При применении препарата пациентами с деменцией альцгеймеровского типа может отмечаться нарушение походки.
Синдром отмены оланзапина может включать различную симптоматику, начиная от физического дискомфорта вплоть до тяжелого психоза. При отмене оланзапина могут развиваться бессонница, беспокойство, возбуждение, раздражительность. Несмотря на низкий риск возникновения экстрапирамидных расстройств на приеме оланзапина, данные расстройства могут обостряться при резкой отмене данного препарата.
Таким образом, с учетом всех особенностей данного препарата, правильного назначения, внимательного контроля нежелательных явлений и коррекцией соматических эффектов создается возможность его успешного использования как в психиатрическом стационаре, так и в амбулаторных условиях.
Оланзапин
В настоящее время многие исследователи считают оланзапин (Zyprexa) наиболее эффективным и одновременно безопасным препаратом для лечения шизофрении. Это медикамент появился на фармацевтическом рынке в 1996 г.
Химическая группа: тиенобензодиазепин.
Форма выпуска: таблетки 2,5, 5, 7,5, 10, 15, и 20 мг; выпускается в растворимой форме (зидис) в таблетках 5, 10, 15 и 20 мг, растворах для инъекций — 10 мг.
Фармакокинетика: период полувыведения — 31 час, пик концентрации — 6 часов, стабилизация концентрации достигается в течение 7 дней, биодоступность — 60%.
Режим дозирования: диапазон доз для взрослых колеблется от 5 до 20 мг, однако на практике, к сожалению, максимально допустимые дозы препарата нередко превышают рекомендуемый уровень. Детям оланзапин назначается из расчета 0,12 — 0,2 мг на кг веса обычно раза в день, для лиц пожилого возраста рекомендуемый диапазон доз — в день.
Показания: Оланзапин приводит к выраженной редукции психопатологических симптомов шизофрении и дольше других принимается больными без отказа при необходимости длительного назначения (Lieberman J. et al., 2005).
Согласно данным некоторых исследователей, отчетливо выраженное антипсихотическое действие оланзапина наблюдается (через 2 — 3 недели) прежде всего у больных приступообразно-прогредиентной шизофренией с острой параноидной симптоматикой (Ешимбетова С.З., 2005). Терапевтический эффект острого эпизода шизофрении при лечении оланзапином составляет (Морозова М.А. с соавт., 2000), причем общая редукция психоза опережает уменьшение выраженности бреда и галлюцинаций (Морозова М.А., Жаркова Н.Б., Бениашвили А.Г., 2000).
При переходе с типичных нейролептиков на внутримышечные инъекции оланзапина, при параноидной шизофрении, в литературе встречаются указания на возможное обострение состояния. Вследствие вышесказанного в данном случае желателен постепенный переход с одного препарата на другой. Возможно кратковременное назначение транквилизаторов бензодиазепинового ряда. После инъекций оланзапина больные становятся более доступными для общения с медицинским персонала.
По данным некоторых авторов (Козырев В.Н. с соавт., 2005), галлюцинаторно-бредовая симптоматика на фоне внутримышечного введения оланзапина редуцируется значительно медленнее, чем возбуждение, злобно-напряженный аффект, тревога и страх.
Лечение оланзапином шизофрении позволяет в течение двух недель снизить выраженность общей психопатологической симптоматики при этом заболевании на 52,46%, продуктивной симптоматики на 47,73%, негативной — на 13,33%. Заметно улучшаются параметры нейропсихологических нарушений: вербальной памяти на 13%, зрительной памяти на 10%, рабочей памяти и внимания — на 5%, исполнительской функции — на 1%. При дальнейшей терапии в течение недель значительно редуцируется негативная (на 46,67%) и в меньшей степени позитивная симптоматика (25,05%), продолжают улучшаться показатели вербальной памяти (на 10%) и рабочей памяти (на 8%), значительно повышаются показатели зрительной памяти и исполнительских функций (на 2%). (Панина А.Н., Говорин Н.В., 2005).
Исследования показали, что когнитивные нарушения у больных шизофренией связаны с психопатологическими расстройствами позитивного и негативного спектра, причем их редукция в процессе лечения оланзапином происходит неравномерно.
При терапии резистентной шизофрении отмечен более позитивный эффект оланзапина неделя лечения), чем клозапина (Оленева Е.В., Цукарзи Э.Э., Мосолов С.Н., 2005).
Препарат по сравнению с клозапином и рисперидоном обладает большей способностью устранять проявления депрессии при шизофрении, тем самым снижая риск суицида (Meltzer H., 1999).
Механизм действия: оланзапин обладает выраженным антагонизмом по отношению к рецепторам 5НТ2A, 5HT2C (увеличение веса?), 5HT3, 5НТ6 и менее выраженным антагонизмом в отношении D2-рецепторов (3: 1) (D2/D3 > D1/D3/D4). Кроме того, данный препарат обладает заметной чувствительностью к М1 и М5 (антихолинергические побочные эффекты), средним тропизмом к Н1 (сомноленция) рецепторам и слабо влияет на альфа1-адренорецепторы.
По спектру своего фармакологического эффекта оланзапин из всех антипсихотиков нового поколения наиболее близок к клозапину, но в отличие от последнего слабее действует на серотонинергические, на альфа2-адренорецепторы и холинорецепторы. Оланзапин, так же как и клозапин, имеет более высокое сродство к НТ2А-рецепторам, чем к дофаминовым рецепторам типа D2.
Показания к терапии шизофрении оланзапином
Оланзапин (зипрекса) назначают в дозе однократно внутрь на ночь. На второй день терапии дозу можно увеличить до 15 мг При отсутствии в течение двух-трех недель эффекта дозу повышают до 20 мг в сутки. Средние дозы оланзапина при лечении шизофрении составляют средняя поддерживающая доза — 12,5 мг
Длительность лечения оланзапином при его внутримышечном введении составляет от 1 до 7 дней (в среднем 3 дня). Первая инъекция препарата назначается в дозе 10 мг, вторая через 2 часа, третья при необходимости — через 4 часа (максимальная суточная доза 30 мг). При патологии печени и почек, при сочетании факторов, снижающих период полувыведения препарата (пожилые женщины, некурящие), число инъекции ограничивается — (Козырев В.Н. с соавт., 2005).
Перевод с внутримышечных инъекций на пероральный прием рекомендуется при дозе последнего, равной в сутки.
Помимо приема препарата в форме таблеток, используется внутримышечная форма оланзапина, обладающая седативным свойством и предложенная для купирования психомоторного возбуждения при шизофрении.
Парентеральное введение препаратов в процессе лечения шизофрении показано для быстрого купирования психомоторного возбуждения, неудовлетворительного сотрудничества больного с врачом, при наличии гастроэнтерологических заболеваниях.
Побочные эффекты: к побочным эффектам оланзапина относят сонливость, головокружение и прибавку в весе. В литературе встречаются работы, свидетельствующие о способности препарата вызывать агранулоцитоз, отмечены редкие случаи рабдомиолиза.
Побочные эффекты оланзапина
Увеличение веса при приеме оланзапина более выражено, чем при приеме других атипичных антипсихотиков. Это осложнение терапии тяжело переносится пациентами, особенно женщинами, и может повлечь за собой не только соматические, но и невротические расстройства. Профилактикой данного осложнения является низкокалорийная диета и продуманные программы физических упражнений.
Диета представляет собой уменьшенные порции приема пищи, предпочтение овощей и фруктов, сокращение калорийных продуктов до минимума и прием не менее 8 стаканов воды ежедневно.
В разное время для лечения этого осложнения предлагались такие препараты, как низатидин, амантадин, топирамат, сибутрамин и др. Однако эффект приема этих препаратов и механизм их действия в отношение снижения веса больных в большинстве исследований оказался слабовыраженным.
В настоящее время предпринимаются попытки ограничить прибавку веса, вызванную приемом оланзапина, бупропионом антидепрессанта, обладающим норадренергическим и дофаминергическим эффектом. Бупропион является относительно слабым ингибитором обратного захвата норэпинефрина и практически не оказывает влияние на центральные серотонинергические нейроны (Gadde K. et al., 2006).
Бупропион можно принимать совместно с оланзапином без негативного взаимодействия этих препаратов. Однако требуется некоторая осторожность приема бупропиона в плане возникновения маниакального синдрома, у лиц, имевших в анамнезе его проявления. Кроме того, прием бупропиона способствует более быстрой редукции негативной симптоматики шизофрении.
Замечено, что курс терапии этим антидепрессантом в среднем снижает вес за этот период почти на 3 кг, также фиксируется снижение уровня холестерина в крови, при этом уровень холестерола, липопротеидов, триглицеридов и глюкозы в крови практически остается неизменным.
Первоначальная потеря веса сохраняется после прекращения приема бупропиона не протяжение почти трех месяцев.
Сканирование тела с использованием рентгеновского метода абсорптиометрии (DXL) показало, что снижение веса в процессе лечения бупропионом, происходит за счет потери жировой ткани туловища. При этом снижение веса не сопровождается изменением плотности и минерального состава костей. Отметим, что при наличии булимии или анорексии прием бупропиона противопоказан.
Более редкими побочными эффектами оланзапина считаются тошнота, ортостатическая гипотония, брадикардия, отеки, антихолинергические эффекты и экстрапирамидная симптоматика.
При приеме оланзапина возможно повышение уровня трансаминаз печени (АСТ и АЛТ), однако практически оно не имеет клинического значения. Крайне редко наблюдаются обратимое снижение нейтрофилов и судороги. Согласно нашему наблюдению, последнее осложнение встречается в 0,5% случаев и чаще у детей и подростков.
Прием оланзапина может вызвать гиперлипедемию, увеличение концентрации в крови гликолизированного гемоглобина, гиперинсулинемию и устойчивость к инсулину (Melkersson K. et al., 2000). Рекомендуется в процессе лечения данным препаратом следить за уровнем глюкозы и липидов в крови, а также контролировать изменение плотности костных минералов организма.
Пролактинемия при приеме оланзапина отмечается редко.
Противопоказания к приему оланзапина: лейкопения, глаукома, гиперплазия простаты. Требуется соблюдать осторожность при лечении пациентов с заболеваниями печени и купировании интоксикационных психозов.
Взаимодействие с медикаментами: при совместном назначении с бензодиазепинами возможно возникновение ортостатической гипотензии и синкопальных состояний. Карбамазепин снижает уровень концентрации оланзапина в плазме крови; флувоксамин, циметидин и курение, напротив, снижают его.