какая валентность у фосфора
Таблица валентности.
В таблице валентности приведены значения валентности элементов периодической таблицы Менделеева. Что такое валентность?
Точками здесь обозначаются неподеленные пары электронов, однако в структурных формулах их отмечают не каждый раз.
В химии принято, что валентность химических элементов можно узнать по группе (колонке) в таблице Менделеева. В действительности не всегда валентность элемента соответствует номеру группы, но в большинстве случаев определенная валентность по такому методу даст правильный результат часто элементы, в зависимости от разных факторов, имеют не одну валентность. Чтобы проще было понимать и не путаться, ниже приведена таблица валентностей всех элементов периодической таблицы.
Цифра положительной валентности элемента соответствует количеству отданных атомом электронов, а отрицательной валентности – количеству электронов, которые атом должен забрать себе для завершения внешнего энергетического уровня.
Значение, приведенное в скобках таблицы валентности, перечисляет менее распространенные валентности. Если у элемента указана только одна цифра, значит он может иметь только одну валентность.
Таблица валентности химических элементов.
Порядковый номер химического элемента, он же: атомный номер, он же: зарядовое число атомного ядра, он же: атомное число
Русское / Английское наименование
Валентность фосфора
Валентность фосфора.
Валентность фосфора:
Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
| Валентность фосфора в соединениях | |
| III | P2O3, Ca3P2, PH3 |
| V | P2O5, H3PO4, PCl5х |
Валентность фосфора
Общие сведения о валентности фосфора
Фосфор образует несколько аллотропических изменений: белый, красный и черный фосфор.
Валентность фосфора в соединениях
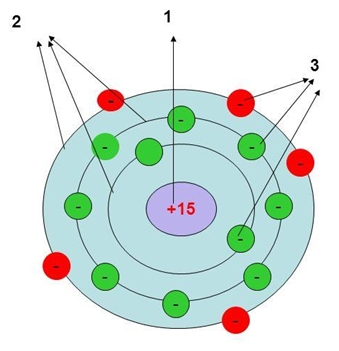
Фосфор — пятнадцатый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в третьем периоде в VA группе. В ядре атома фосфора содержится 15 протонов и 16 нейтронов (массовое число равно 31). В атоме фосфора есть три энергетических уровня, на которых находятся 15 электронов (рис. 1).
Рис. 1. Строения атома фосфора.
Электронная формула атома фосфора в основном состоянии имеет следующий вид:
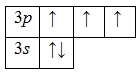
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие трех неспаренных электронов свидетельствует о том, что фосфор способен проявлять валентность III (P III 2O3, Ca3P III 2, P III H3и т.д.).
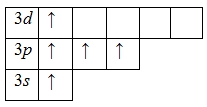
Поскольку на третьем энергетическом слое помимо 3s- и 3p-подуровней есть еще и 3d-подуровень, для атома фосфора характерно наличие возбужденного состояния: пара электронов 3s-подуровня распаривается и один из них занимает вакантную орбиталь 3d-подуровня.
Наличие пяти неспаренных электронов свидетельствует о том, что для фосфора также характерна валентность V (P V 2O5, H3P V O4, P V Cl5и др.).
Примеры решения задач
| Задание | Вычислите массу фосфора, который надо сжечь в кислороде для получения оксида фосфора (V) массой 3,5 г. |
| Решение | Запишем уравнение реакции сжигания фосфора в кислороде с образованием оксида фосфора (V): |
Рассчитаем количество вещества оксида фосфора (V) (молярная масса – 284 г/моль):
n (P) = 2 × n (P2O5) = 2 × 0,01 = 0,02моль.
Найдем массу фосфора (молярная масса – 31 г/моль):
m (P) = 0,02 × 31 = 0,62 г.
| Задание | Каков тип химической связи в соединениях: а) PH3; б) PCl5; в)Li3P. В полярных веществах укажите направления смещения общих электронных пар. |
| Ответ | В соединениях состава PH3 и PCl5 реализуется ковалентная полярная связь, поскольку эти вещества образованы атомами неметаллов, отличающихся по своей электроотрицательности. Поскольку значения электроотрицательности фосфора в фосфине и хлора в пентахлориде фосфора выше, чем у водорода и фосфора, соответственно, то общие электронные пары будут смещены в их сторону. |
В соединении Li3P реализуется ионный тип связи.
Фосфор. Химия фосфора и его соединений.
Фосфор
Положение в периодической системе химических элементов
Фосфор расположен в главной подгруппе V группы (или в 15 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение фосфора
Электронная конфигурация фосфора в основном состоянии:
Атом фосфора содержит на внешнем энергетическом уровне 3 неспаренных электрона и одну неподеленную электронную пару в основном энергетическом состоянии. Следовательно, атом фосфора может образовывать 3 связи по обменному механизму. Однако, в отличие от азота, за счет вакантной 3d орбитали атом фосфора может переходить в возбужденное энергетическое состояние.
Электронная конфигурация фосфора в возбужденном состоянии:
При этом один электрон из неподеленной электронной пары на 3s-орбитали переходит на переходит на 3d-орбиталь. Для атома фосфора в возбужденном энергетическом состоянии характерна валентность V.
Таким образом, максимальная валентность фосфора в соединениях равна V (в отличие от азота). Также характерная валентность фосфора в соединениях — III.
Физические свойства и нахождение в природе
Фосфор образует различные простые вещества (аллотропные модификации).
Черный фосфор – то наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Чёрный фосфор — это чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, полностью нерастворимое в воде или органических растворителях.
Известны также такие модификации, как желтый фосфор и металлический фосфор. Желтый фосфор – это неочищенный белый фосфор. При очень высоком давлении фосфор переходит в новую модификацию – металлический фосфор, который очень хорошо проводит электрический ток.
Соединения фосфора
Типичные соединения фосфора:
Способы получения фосфора
2. Вместо фосфатов можно использовать другие неорганические соединения фосфора, например, метафосфорную кислоту.
3. Красный и черный фосфор получают из белого фосфора.
Химические свойства фосфора
При нормальных условиях фосфор довольно химически активен.
1.1. При взаимодействии с кислородом воздуха образуются оксиды – ангидриды соответствующих кислот:
1.3. При взаимодействии фосфора с серой образуются сульфиды:
1.4. При взаимодействии с металлами фосфор проявляет свойства окислителя, продукты реакции называют фосфидами.
Например, кальций и магний реагируют с фосфором с образованием фосфидов кальция и магния:
Еще пример: натрий взаимодействует с фосфором с образованием фосфида натрия:
1.5. С водородом фосфор непосредственно не взаимодействует.
2. Со сложными веществами фосфор реагирует, проявляя окислительные и восстановительные свойства. Фосфор диспропорционирует при взаимодействии с некоторыми веществами.
2.1. При взаимодействии с окислителями фосфор окисляется до оксида фосфора (V) или до фосфорной кислоты.
Например, азотная кислота окисляет фосфор до фосфорной кислоты:
Серная кислота также окисляет фосфор:
Соединения хлора, например, бертолетова соль, также окисляют фосфор:
Некоторые металлы-сильные окислители также окисляют фосфор. Например, оксид серебра (I):
2.2. При растворении в щелочах фосфор диспропорционирует до гипофосфита и фосфина.
Например, фосфор реагирует с гидроксидом калия:
Или с гидроксидом кальция: