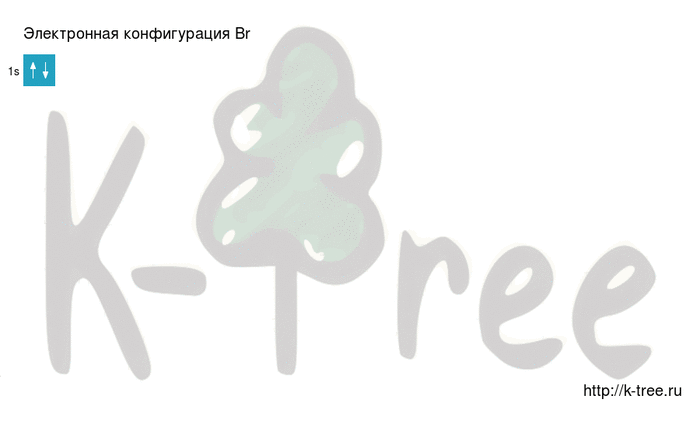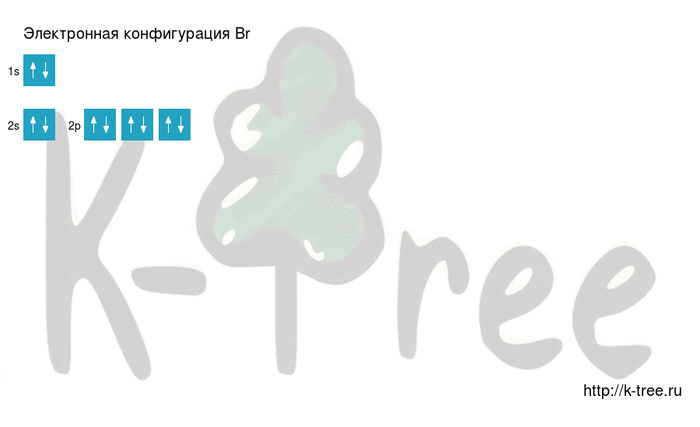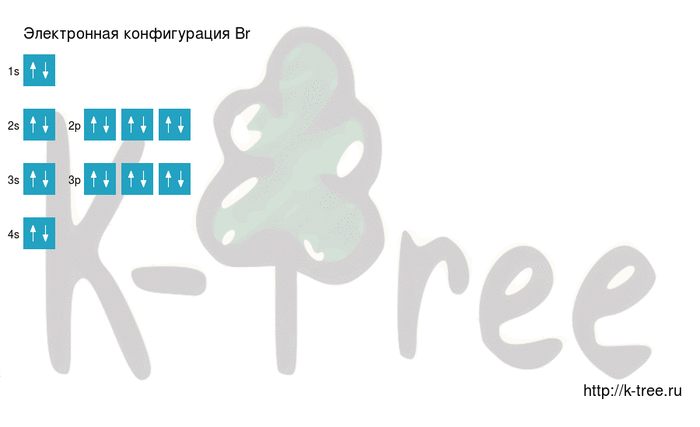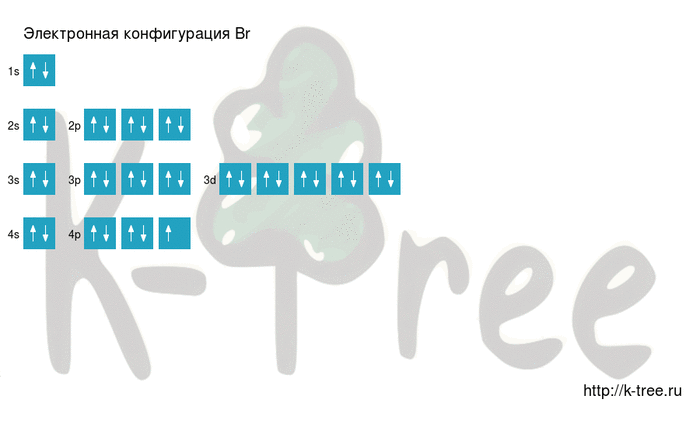какая валентность у брома
Валентность брома
Общие сведения о валентности брома
В виде простого вещества бром представляет собой жидкость красно-бурого цвета, обладающую резким неприятным запахом. Ядовит. Плотность 3,19 г/см 3 (при t 0 = 0 o C). При кипении (t 0 = 58,6 o C) бром из жидкого состояния переходит в газообразное – образует буро-коричневый пар.
Молекула брома двухатомна Br2.
Валентность брома в соединениях
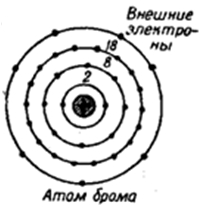
Бром – тридцать пятый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в четвертом периоде в VIIA группе. В ядре атома брома содержится 35 протонов и 45 нейтронов (массовое число равно 80). В атоме брома есть четыре энергетических уровня, на которых находятся 35 электронов (рис. 1).
Рис. 1. Строение атома брома.
Электронная формула атома брома в основном состоянии имеет следующий вид:
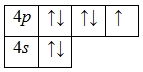
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие одного неспаренного электрона свидетельствует о том, что бром способен проявлять валентность I (низшая валентность) в своих соединениях (HBr, HBrO).
Наличие трех, пяти и семи неспаренных электронов в возбужденном состоянии свидетельствует о том, что бром проявляет в своих соединениях валентности III (AuBr3, HBrO2), V (HBrO3) и VII (HBrO4) (высшая валентность).
Примеры решения задач
| Задание | Относительная плотность паров брома по воздуху равна 5,37. Какова молекулярная (истинная) формула брома? |
| Решение | Молярная масса брома будет рассчитываться по формуле: |
M = 5,37 × 29 = 155,73 г/моль.
Относительная атомная масса брома равна 79,904 а.е.м. Значит, в молекуле брома имеется:
x=M/Ar = 155,73/79,904 = 2 атома брома.
Молекулярная (истинная) формула брома имеет вид Br2.
| Задание | Алкен массой 4,2 г может максимально присоединить 16,0 г брома. Установите формулу алкена. |
| Решение | Общая формула алкенов имеет вид CnH2n. Молярная масса равна 14n.Составим уравнение реакции присоединения брома алкеном: |
Согласно уравнению реакции n(Br2) :n (CnH2n) = 1:1, т.е. n(Br2) = n (CnH2n). Найдем число моль брома (молярная масса – 160 г/моль):
n (Br2) = 16 / 160 = 0,1 моль.
Тогда, n (CnH2n) =0,1 моль. Определим молярную массу алкена:
Таблица валентности.
В таблице валентности приведены значения валентности элементов периодической таблицы Менделеева. Что такое валентность?
Точками здесь обозначаются неподеленные пары электронов, однако в структурных формулах их отмечают не каждый раз.
В химии принято, что валентность химических элементов можно узнать по группе (колонке) в таблице Менделеева. В действительности не всегда валентность элемента соответствует номеру группы, но в большинстве случаев определенная валентность по такому методу даст правильный результат часто элементы, в зависимости от разных факторов, имеют не одну валентность. Чтобы проще было понимать и не путаться, ниже приведена таблица валентностей всех элементов периодической таблицы.
Цифра положительной валентности элемента соответствует количеству отданных атомом электронов, а отрицательной валентности – количеству электронов, которые атом должен забрать себе для завершения внешнего энергетического уровня.
Значение, приведенное в скобках таблицы валентности, перечисляет менее распространенные валентности. Если у элемента указана только одна цифра, значит он может иметь только одну валентность.
Таблица валентности химических элементов.
Порядковый номер химического элемента, он же: атомный номер, он же: зарядовое число атомного ядра, он же: атомное число
Русское / Английское наименование
Валентность брома
Валентность брома.
Валентность брома:
Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
| Валентность брома в соединениях | |
| I | Br2O, HBr, HBrO |
| III | AuBr3, HBrO2 |
| V | BrF5, HBrO3 |
| VII | NaBrO4, HBrO4 |
Бром Br
Бром в таблице менделеева занимает 35 место, в 4 периоде.
| Символ | Br |
| Номер | 35 |
| Атомный вес | 79.9010000 |
| Латинское название | Bromum |
| Русское название | Бром |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема брома
Br: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5
Короткая запись:
Br: [Ar]4s 2 3d 10 4p 5
Порядок заполнения оболочек атома брома (Br) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Бром имеет 35 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
5 электронов на 4p-подуровне
Степень окисления брома
Ионы брома
Валентность Br
Атомы брома в соединениях проявляют валентность VII, V, IV, III, I.
Валентность брома характеризует способность атома Br к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Br
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Таблица валентности химических элементов
Таблица валентности химических элементов.
Таблица валентности химических элементов:
Ниже приводится таблица валентности химических элементов с примерами соединений.
Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Таблица валентности химических элементов:
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.