какая артерия питает печень
Какая артерия питает печень
Печень обладает двойным кровоснабжением: приблизительно 70% крови поступает из воротной вены, остальная часть — из печеночной артерии. По ветвям печеночной вены кровь отводится в нижнюю полую вену. На сложном взаимодействии этих сосудов основано функционирование печени.
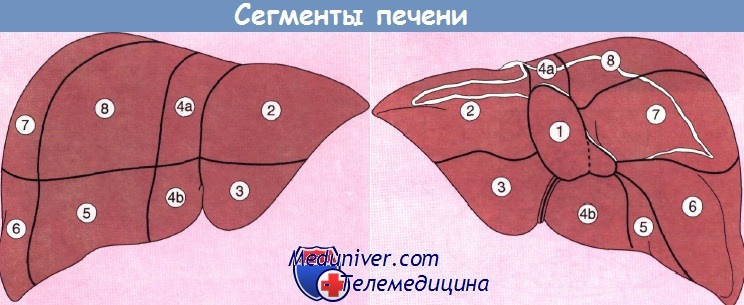
В зависимости от хода сосудов печень делится на восемь сегментов, что с хирургической точки зрения имеет большое значение, поскольку при выборе типа оперативного вмешательства предпочтение зачастую отдают сегментэктомии, а не лобэктомии.
Сегмент 1 (каудальная доля) автономен, поскольку снабжается кровью как от левой и правой ветвей воротной вены, так и от печеночной артерии, в то время как венозный отток от данного сегмента осуществляется непосредственно в нижнюю полую вену. При синдроме Бадда—Киари тромбоз главной печеночной вены приводит к тому, что отток крови от печени происходит полностью через хвостатую долю, которая при этом значительно гипертрофируется.
Печень хорошо видна на обзорной рентгенограмме брюшной полости. Часто обнаруживают придаток правой доли, направленный к области правой подвздошной ямки — так называемую долю Риделя.

Задний сегмент правой доли редко просматривают на этом уровне, поскольку основной объём данного сегмента лежит ниже переднего сегмента правой доли:
1 — медиальный сегмент левой доли печени; 2 — левая печеночная вена; 3 — латеральный сегмент левой доли печени;
4 — срединная печеночная вена; 5 — передний сегмент правой доли печени; 6 — задний сегмент правой доли печени;
7 — правая печеночная вена; 8 — аорта; 9 — пищевод;
10 — желудок; 11 — селезенка. 
Сцинтиграфия с использованием технеция. 
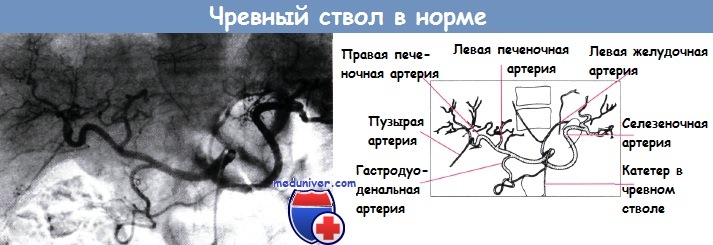
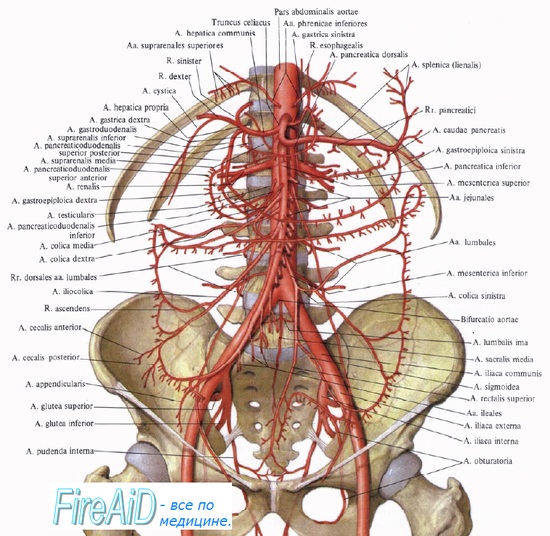
Печеночная артерия, воротная вена и общий печеночный проток в воротах печени располагаются рядом. Печеночная артерия в норме представляет собой ветвь чревного ствола, тогда как желчный пузырь снабжается кровью от пузырной артерии; нередко встречают анатомические особенности строения этих сосудов.
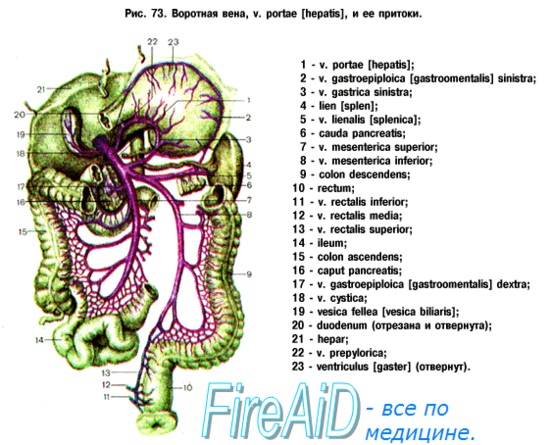
Существует несколько способов контрастирования воротной вены, формирующейся при слиянии селезеночной и верхней брыжеечной вен позади головки поджелудочной железы.
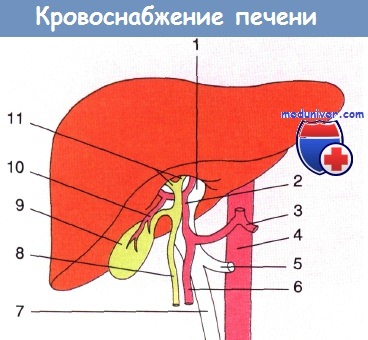
1 — воротная вена; 2 — печеночная артерия; 3 — чревный ствол;
4 — аорта; 5 — селезеночная вена; 6 — гастродуоденальная артерия;
7 — верхняя брыжеечная вена; 8 — общий желчный проток; 9 — желчный пузырь;
10 — пузырная артерия; 11 —печеночные протоки
Метод прямой чрескожной инъекции в селезеночную пульпу (спленовенография) раньше был широко распространен, но в настоящее время его используют редко даже при увеличении селезенки и признаках портальной гипертензии. У младенцев при открытой пупочной вене возможна прямая катетеризация с контрастированием системы левой воротной вены. В настоящее время чаще используют селективную ангиографию, когда воротную систему визуализируют при катетеризации селезеночной артерии и последующем наблюдении фазы венозного возврата после прохождения контраста через селезенку.
У пациентов с портальной гипертензией качество изображения может быть плохим вследствие гемодилюции и снижения концентрации контрастного вещества, что можно скорректировать методом цифровой субтракционной ангиографии. Сразу после прохождения катетера через правое предсердие и желудочек его можно ввести в печеночные вены. При этом легко оценить рентгеновское изображение и измерить венозное давление, для чего сначала фиксируют величину свободного печеночного венозного давления в просвете сосуда, затем катетер аккуратно погружают в печеночную паренхиму.
Наконечник баллона расширяется, и измеряемая величина (фиксированное печеночное венозное давление) практически соответствует давлению в воротной вене, что позволяет рассчитать градиент указанного параметра. Наиболее легко провести катетер через правую внутреннюю яремную вену, поскольку в этом случае обеспечивается практически прямолинейный доступ. Аналогичную технику доступа применяют при трансвенозной биопсии печени.
С помощью УЗИ нормальной печени оценивают ее размер и консистенцию, дефекты наполнения, анатомию системы желчных протоков и воротной вены. Печеночную паренхиму и окружающие ткани также можно исследовать с помощью компьютерной томографии.
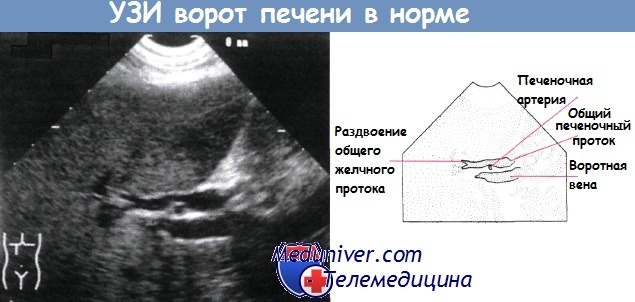
Печеночная артерия расположена между расширенным общим печеночным протоком и воротной веной.
При магнитно-резонансной холангиопанкреатографии применяют Т1 и Т2 время релаксации среды. Сигнал от жидкостной среды имеет очень низкую плотность (обеспечивает темный цвет) на Т,-изображениях и высокую плотность (с получением светлого оттенка) на Т2-изображениях. При данном методе исследования Т2-изображения используют для получения холангиограмм и панкреатограмм. Чувствительность и специфичность методики различаются в зависимости от техники и показаний.
Если подозрение на патологию небольшое, лучше провести магнитно-резонансную холангио- и панкреатографию, а при высокой вероятности оперативного вмешательства предпочесть эндоскопическую ретроградную холангиографию. Кроме того, периампуллярные образования зачастую остаются незамеченными из-за артефактов, обусловленных скоплением воздуха в двенадцатиперстной кишке. К сожалению, магнитно-резонансный метод исследования недостаточно чувствителен при ранней диагностике патологии желчных протоков, например в случае с едва различимыми повреждениями, часто встречающимися при первичном склерозирующем холангите. Метод сканирования TESLA для визуализации желчных протоков применяют редко.
Компьютерная или МРТ — лучшие методы для исследования патологии печени. Благодаря контрастированию и получению изображений в артериальной и венозной фазе возможна диагностика как доброкачественных, так и злокачественных образований. 3D-компьютерная и МРТ позволяют получать изображение сосудов. При дополнительном использовании MRC либо TESLA-изображений можно диагностировать рак желчных путей.
Компьютерную либо МРТ можно использовать в качестве единственных методов исследования для обнаружения опухолей, описания анатомии сосудов и определения степени поражения желчных путей.

Исследование можно проводить совместно со стимуляцией холецистокинином для оценки дисфункции желчного пузыря или сфинктера Одди.
1 — поверхностные маркеры грудной клетки; 2 — печень; 3 — селезенка
Радиоизотопный метод исследования печени в настоящее время используют значительно реже. Данным способом исследования определяют концентрацию технеция в ретикулоэндотелиоцитах (клетки Купфера), введенного внутривенно.
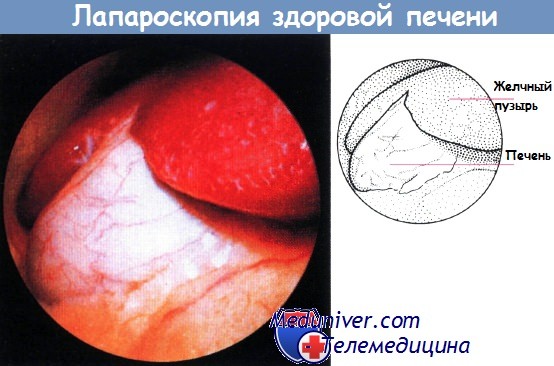
Лапароскопический метод достаточно редко применяют для непосредственного визуального исследования печени, однако он позволяет проводить биопсию под визуальным контролем, поскольку в этом случае достаточно четко просматривается нижняя поверхность органа.
Видео анатомия, кровоснабжение и иннервация печени
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Состояние артериального кровообращения печени при сердечной недостаточности и портальной гипертензии
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
Ангиоархитектоника печени уникальна в организме человека, она объединяет портальную и кавальную венозные, артериальную, лимфатическую и билиарную системы в единое целое. Печеночная гемодинамика чрезвычайно чувствительна к любому воздействию на организм, а ее первичные нарушения могут влиять на функцию сердца, являясь причиной легочной гипертензии. Врачи, подчас, не задумываются о влиянии этих патологических процессов в печени на состояние сердечно-сосудистой системы, тем более, что масса лекарств, будучи вазоактивной, изменяет гемодинамику печени. Поэтому назрела необходимость разработки простого комплекса допплерэхографической оценки разнообразных нарушений кровообращения печени и гемодинамики сердца. Одной из составляющих кровотоков, исследуемых в комплексе при оценке печеночной гемодинамики, является артериальный печеночный кровоток, изучение которого требует определенных подходов.
Материалы и методы
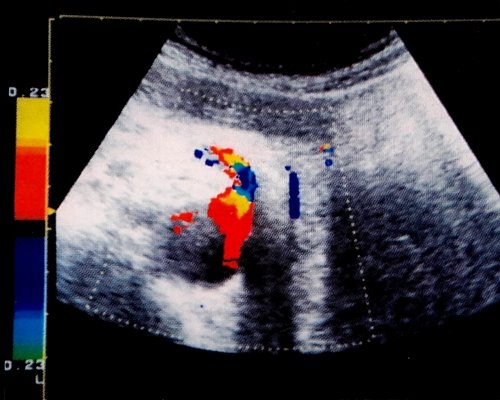
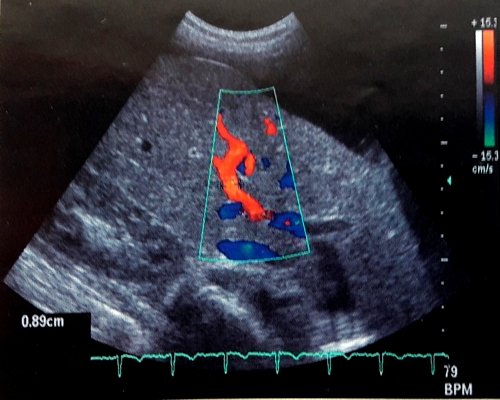
Всем обследованным лицам проводилось допплерографическое исследование в импульсно-волновом режиме, цветного допплеровского картирования и энергетической цветной допплерографии, на ультразвуковых томографах датчиками 3,5 и 3,75 Мгц (30°-90°). Допплерэхография общей печеночной артерии проводилась из субкостального доступа в месте ее отхождения от чревного ствола, где угол между УЗ-лучом и ходом сосуда не превышает 45°, а также собственно печеночной артерии во внутрипеченочном участке, где она расположена между воротной веной и желчным протоком. Для дифференциации сосудов обязательным является подключение режимов цветного допплеровского картирования и энергетического допплера (рис. 1, 2).
Рис. 1. Общая печеночная артерия в режиме цветного допплеровского картирования.
Рис. 2. Печеночная артерия в режиме энергетического допплера.
Анализировались допплерограммы с максимальным спектром кровотока. Оценивались диаметр общей печеночной артерии (ДоПА) и площадь сечения (ПСоПА) во внепеченочном отделе, конечные систолическая и диастолическая (Vмакс, Vмин), средняя скорости, RI, PI. Рассчитывались следующие параметры объемного кровотока:
Расчет допплерэхографических индексов печеночной гемодинамики проводился в рамках стандартного блока математических функций и статистики программы EXCEL пакета программ MS-Office для WINDOWS-95.
Результаты исследования
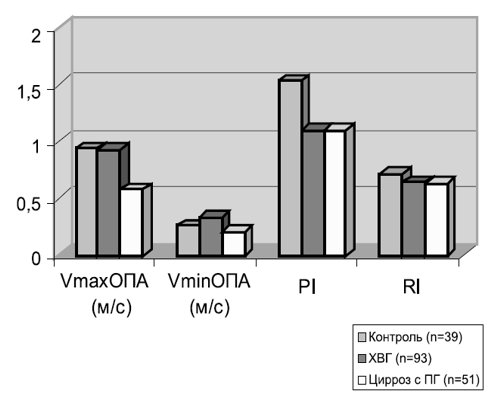
Анализ линейных скоростных параметров кровотока в общей печеночной артерии выявил значительное снижение максимальной и минимальной скоростей у больных 2-й группы по сравнению с другими группами. Средние интегральные скорости кровотока в общей печеночной артерии у больных 2-й группы были лишь немного меньше, чем в 4-й группе (табл. 1).
Колебания пульсативного индекса Гослинга (PI) во всех группах больных были недостоверными. В контрольной группе PI был максимальным, составляя 1,53. Нами не выявлено информативности индекса Гослинга в дифференциальной диагностике нарушения кровообращения печени. Индекс резистивности Пурсело (RI) оказался минимальным у больных 4-й и 3-й групп, составив 0,628 и 0,643 соответственно, тогда как во 2-й, 1-й и контрольной группах он составил 0,70, 0,71 и 0,72, достоверно не отличаясь один от другого, но выше, чем у больных с диффузными поражениями печени (рис. 3).
Рис. 3. Соотношение линейных скоростей и индексов в общей печеночной артерии.
Какая артерия питает печень
В печени кровь протекает по печеночной артерии (25—30 %) и воротной вене (70—75 %). По прохождении капиллярной сети кровь дренируется в систему печеночных вен, которые впадают в нижнюю полую вену. Важной особенностью сосудистого русла печени является наличие большого количества анастомозов между сосудами систем воротной вены, печеночной артерии и печеночных вен.
Давление в печеночной артерии соответствует давлению в других магистральных сосудах—100—120 мм рт. ст. В воротной вене оно в 10 раз меньше и составляет около 10 мм рт. ст., в синусоидах — 3—5 мм рт. ст., в печеночных венах — 2—3 мм рт. ст. Такая небольшая разница между портальным давлением и давлением в печеночных венах оказывается достаточной для портального кровотока вследствие низкого сопротивления портальных сосудов.
Величина кровотока через печень человека составляет около 100 мл/ 100 г/мин, т. е. 20—30 % от величины сердечного выброса. На долю портального кровотока приходится 70—80 % этого объема, а на долю кровотока в печеночной артерии 20—30 %. При максимальной вазодилатации кровоток в печени может возрастать до 5000 мл/мин.
Печень является одним из органов, выполняющих функцию депо крови в организме (в норме в печени содержится свыше 500 мл крови). За счет этого может поддерживаться определенный объем циркулирующей крови (например, при кровопотере) и обеспечиваться необходимая каждой конкретной гемодинамической ситуации величина венозного возврата крови к сердцу. Но эта функция печени не исключает необходимость применения шины для остановки кровотечения. Под шиной понимается не указанная автомобильная шина, а специальная медицинская шина в виде жгута.
Миогенная регуляция обеспечивает высокую степень ауторегуляции кровотока в печени. Даже небольшое увеличение объемной скорости портального кровотока приводит к сокращению гладких мышц воротной вены, что ведет к уменьшению ее диаметра, а также включает миогенную артериальную констрикцию в печеночной артерии. Оба этих механизма направлены на обеспечение постоянства кровотока и давления в синусоидах.
Гуморальная регуляция. Адреналин вызывает сужение воротной вены, активируя расположенные в ней а-адренорецепторы. Действие адреналина на артерии печени сводится, преимущественно, к вазодилатации вследствие стимуляции преобладающих в печеночной артерии B-адренорецепторов. Норадреналин при действии как на артериальную, так и на венозную систему печени приводит к сужению сосудов и повышению сосудистого сопротивления в обоих руслах, что ведет к уменьшению кровотока в печени. Ангиотензин суживает как портальные, так и артериальные сосуды печени, значительно уменьшая при этом кровоток в них. Ацетилхолин расширяет артериальные сосуды, увеличивая приток артериальной крови к печени, но сокращает печеночные венулы, ограничивая отток венозной крови из органа, что приводит к увеличению портального давления и увеличению объема крови в печени.
Метаболиты и тканевые гормоны (двуокись углерода, аденозин, гистамин, брадикинин, простагландины) вызывают сужение портальных венул, уменьшая портальный кровоток, но расширяют печеночные артериолы, усиливая приток артериальной крови к печени (артериализация печеночного кровотока). Другие гормоны (глюкортикостероиды, инсулин, глюка-гон, тироксин) вызывают увеличение кровотока через печень вследствие усиления метаболических процессов в печеночных клетках.
Нервная регуляция выражена сравнительно слабо. Вегетативные нервы печени идут от левого блуждающего нерва (парасимпатические) и от чревного сплетения (симпатические). Электрическая стимуляция блуждающего нерва существенно не влияет ни на скорость печеночного кровотока, ни на его распределение в органе. Стимуляция печеночных симпатических нервов повышает сосудистое сопротивление в печеночной артерии и в воротной вене.
Сосудистые заболевания печени
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Сосудистые-заболевания-печени.jpeg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Сосудистые-заболевания-печени.jpeg?fit=825%2C550&ssl=1″ />
Заболевания сосудов печени – относительно редкие болезни, при них может нарушаться кровоток в печени, что приводит к ряду серьезных осложнений. В этой статье рассматриваются основные вопросы, связанные с патогенезом, клинической картиной и лечением.
Обструкция печеночной артерии
Определение
Это осложнение множества различных патологических состояний, приводящих к частичному или полному нарушению кровотока по этому сосуду.
Эпидемиология
Обструкция печеночной артерии встречается относительно редко и точных эпидемиологических данных по этому поводу нет. Тромбоз печеночной артерии, приводящий к обструкции, может быть осложнением (примерно 2% трансплантатов печени).
Патогенез
Обструкция печеночной артерии может быть вызвана атеросклерозом, тромбозом, эмболией, инфильтрацией печени или травмой. Это происходит в ходе истинной полицитемии, узелкового артериита, эндокардита и, как упоминалось выше, у небольшого процента пациентов после трансплантации печени.
Непроходимость может возникнуть в результате:
Клиническая картина
У многих пациентов обструкция печеночной артерии протекает бессимптомно и выявляется только при вскрытии. Из-за двойной васкуляризации печени, окклюзия просвета печеночной артерии, не является синонимом инфаркта печени (эмболизация печеночной вены, является, признанным методом лечения рака печени).
Тем не менее, одновременная и полная непроходимость печеночной артерии и воротной вен, почти всегда заканчивается летальным исходом. Клинически инфаркт печени проявляется болью в правой верхней части живота, тахикардией и падением артериального давления. В редких случаях может развиться острая печеночная недостаточность.
Диагностика
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%94%D0%B8%D0%B0%D0%B3%D0%BD%D0%BE%D1%81%D1%82%D0%B8%D0%BA%D0%B0-1.jpg?resize=450%2C300&ssl=1″ alt=»Диагностика» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Диагностика
Лабораторные исследования показывают повышение активности трансаминаз и увеличение протромбинового времени. Визуализирующие тесты играют важную роль в диагностике:
Допплерография
В случае тромбоза печеночной артерии, после трансплантации печени, клинические симптомы обычно появляются в течение нескольких дней после сеанса, а тесты показывают быстрое повышение активности трансаминаз и усиление холестаза. Это связано с быстро прогрессирующей ишемией желчевыводящих путей.
Пациентам с трансплантацией печени проводится тромбэктомия или повторная трансплантация. При окклюзиях другой этиологии может применяться тромболитическая терапия (стрептокиназа или рекомбинантный активатор плазминогена), или антикоагулянтная терапия (гепарин).
Тромбоз воротной вены
Кровоток в воротной вене может быть нарушен в результате тромбоза или инфильтрации опухоли. Клинически тромбоз воротной вены подразделяется: на острый и хронический. Этиология обоих состояний схожа, хроническая форма,- это чаще все продолжение острой формы. Однако методы лечения у них разные.
Факторы риска
Факторы риска тромбоза воротной вены обычно подразделяются на местные и общие. Наиболее частые местными факторы риска: рак брюшной полости и цирроз печени.
Тогда как наиболее распространенные общие факторы риска – это миелопролиферативные нарушения, а также врожденная и приобретенная недостаточность факторов, модулирующих каскад коагуляции. Следует помнить, что диагностика местной причины тромбоза воротной вены не исключает одновременного наличия одной или нескольких общих причин.
Тромбоз воротной вены при миелопролиферативном синдроме
Тромбоз воротной вены – это клинический симптом миелопролиферативного заболевания. Поскольку портальная гипертензия приводит к отклонениям в анализе крови, (таким как анемия и тромбоцитопения), у большинства пациентов нет изменений в периферической крови, характерных для миелопроферативного синдрома, поэтому, диагноз расширяется до определения мутации гена JAK2 (киназа Януса 2 типа) и в таких ситуациях биопсия костного мозга находит полное оправдание.
Дифференциация
В соответствии с рекомендациями Американской ассоциации по изучению заболеваний печени, при диагностике тромбоза воротной вены на основании визуализационных исследований (УЗИ, КТ, в первую очередь следует исключить следующее:
Клинические формы
Острый тромбоз воротной вены – это внезапное образование сгустка частично или полностью закупоривающего воротную вену.
Клиническая картина
Выраженность клинических симптомов зависит от степени окклюзии воротной вены. Острый тромбоз проявляется:
Диагностика
Лабораторные тесты
Лабораторные исследования показывают увеличение показателей острой фазы. Чаще всего сохраняется функция печени, что объясняется компенсаторным кровотоком из печеночной артерии и коллатеральным кровообращением по мелким венозным сосудам в воротах печени. Однако, у некоторых пациентов наблюдается умеренное повышение уровня трансаминаз.
Визуальные исследования
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%92%D0%B8%D0%B7%D1%83%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B5-%D0%B8%D1%81%D1%81%D0%BB%D0%B5%D0%B4%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F.jpg?resize=450%2C300&ssl=1″ alt=»Визуальные исследования» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Визуальные исследования
Визуальная диагностика имеет решающее значение для постановки диагноза:
Фармакотерапия
Антикоагулянтное лечение. Методом выбора является быстрое введение низкомолекулярного гепарина, предотвращающего инфаркт кишечника и значительно улучшает прогноз. Терапия пероральными антикоагулянтами (варфарин или не так часто, применяемый аценокумарол) возможна, если клиническое состояние пациента стабильно и хирургическое вмешательство не планируется.
Консервативное лечение дает шанс полной реканализации сосуда примерно у 40% пациентов. Оно должно длиться не менее 3 месяцев, хотя следует отметить, что полное восстановление тромбоза наблюдалось даже после 6 месяцев терапии. В случаях тромбофилии, для которой не существует радикальной терапии, антикоагулянтное лечение, скорее всего, следует использовать до конца жизни.
Антимикробное лечение. При появлении признаков инфекции требуется антибактериальная терапия.
Инвазивное лечение. Инвазивные процедуры, такие как: тромболизис стрептокиназой или тканевым активатором плазминогена, вводимыми непосредственно в воротную вену или в верхнюю брыжеечную артерию, не показывают более высокой эффективности, чем антикоагулянты, и имеют гораздо более высокий риск серьезных осложнений.
Конечно, в случае инфаркта кишечника, методом выбора будет хирургическая резекция некротических фрагментов кишечника. Это лечение можно сочетать с удалением сгустка из просвета сосуда.
Хронический тромбоз воротной вены
Это клиническое состояние, при нем в результате тромбоза воротной вены развивается коллатеральное кровообращение, соединяющее вены до и после сгустка, образуя сеть сосудов, известную как кавернозная трансформация.
Клиническая картина
Чаще всего хронический тромбо, диагностируется при поиске причины симптомов портальной гипертензии, проявляющейся кровотечением из варикозно расширенных вен пищевода или увеличением селезенки. Пациенты с хроническим тромбозом воротной вены переносят кровотечение из варикозно расширенных вен пищевода лучше, чем пациенты с циррозом, что в основном связано с хорошо сохраненной функцией печени.
Иногда сеть сосудов кавернозной трансформации может сужать желчные протоки, что приводит к портальной билиопатии, приводящей к симптомам холестаза и холангита. Иногда трудно отличимым от первичного склерозирующего холангита.
Физикальное обследование показывает характерное расширение поверхностных сосудов брюшной полости. Минимальная энцефалопатия наблюдается примерно у половины пациентов с хроническим тромбозом, что, однако, может ухудшить точность или способность управлять автомобилем.
Диагностика
Биохимия печени обычно в норме. Визуализирующие исследования, такие как УЗИ, КТ или МРТ, показывающие многочисленные коллатеральные сосуды в области воротной вены и невидимый (неконтрастный) фрагмент воротной вены, играют решающую роль в диагностике, (как при остром тромбозе). Иногда при допплеровском исследовании коллатеральные сосуды имитируют воротную вену, увеличение поджелудочной железы или опухоль желчевыводящих путей.
Нет хорошо задокументированных исследований эффективности бета-адреноблокаторов для первичной профилактики или бандажирования, при вторичной профилактике кровотечения из варикозно расширенных вен пищевода у пациентов с тромбозом воротной вены.
Аналогичная проблема существует при лечении этих пациентов антикоагулянтами. Кажется логичным, сначала лечить варикозное расширение вен пищевода с помощью бандажа пациентам, у которых был эпизод кровотечения, а затем начать антикоагулянтную терапию. Имеются сообщения о том, что хроническая антикоагулянтная терапия снижает риск рецидива тромбоза, без увеличения риска кровотечения из варикозного расширения вен. Пациентам с развивающимся симптомом портальной билиопатии, осложненной холангитом, оправдан эндоскопический стеноз.
Прогноз
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?fit=480%2C320&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9F%D1%80%D0%BE%D0%B3%D0%BD%D0%BE%D0%B7.jpg?resize=450%2C300&ssl=1″ alt=»Прогноз» width=»450″ height=»300″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?w=480&ssl=1 480w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Прогноз
Типичные осложнения хронического тромбоза воротной вены, связанные с симптомами портальной гипертензии – это редкая причиной смерти у пациентов, умирающих от последствий портальной билиопатии или прогрессирования миелопролиферативного заболевания до острого лейкоза или миелофиброза.
Тромбоз воротной вены у пациентов с циррозом печени
Тромбоз воротной вены у пациентов с циррозом печени коррелирует со степенью декомпенсации органа.Тромбоз может развиться у 1/4 пациентов, требующих трансплантации печени. Рак печени может быть причиной тромбоза у пациентов с циррозом.
Клиническая картина
Наиболее частые клинические симптомы тромбоза:
В этой группе чаще выявляются мутации фактора V Лейдена, гена протромбина или метилентетрагидрофолатредуктазы (MTHFR), чем у пациентов с циррозом печени без тромбоза.
К сожалению, никаких рекомендаций по лечению антикоагулянтами у этих пациентов не разработано. Рекомендуется принимать индивидуальные решения. Однако, у подавляющего большинства пациентов, ожидающих трансплантации печени, после начала антикоагулянтной терапии воротная вена восстанавливается.
Тромбоз воротной вены после трансплантации печени
Это осложнение может возникнуть у 2-3% пациентов и часто связано с разницей в диаметре воротной вены донора и реципиента, а также со спленэктомией, выполняемой во время операции по трансплантации.
Синдром обструкции синуса печени
Определение
Это процесс, нарушающий кровообращение в печени в результате токсического повреждения эндотелиальных клеток, выстилающих пазухи печени. У некоторых пациентов в этот процесс также вовлекаются центральные вены.
Эпидемиология
В развитых странах синдром синусоидальной обструкции (SOS), ранее называвшийся (VOD) веноокклюзионная болезнь, является наиболее частым осложнением абляции костного мозга, при его подготовке к трансплантации, (в этом контексте, следует использовать термин – трансплантация гемопоэтических стволовых клеток). Острая обструкция синуса печени – это третья по значимости причина смерти пациентов, перенесших трансплантацию костного мозга.
Другие причины SOS включают:
Клиническая картина
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9A%D0%BB%D0%B8%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F-%D0%BA%D0%B0%D1%80%D1%82%D0%B8%D0%BD%D0%B0.jpg?resize=450%2C300&ssl=1″ alt=»Клиническая картина» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Клиническая картина
Клинические симптомы могут имитировать синдром Бадда-Киари и включают наиболее распространенные:
Выделяют три степени тяжести симптомов: легкую, среднюю и тяжелую.
Если заболевание стало результатом применения циклофосфамида, первые признаки появляются через 10-20 дней после начала лечения. При других схемах миелоабляции симптомы могут развиться позже. На практике синдром обструкции синусовых сосудов печени диагностируется у пациентов:
Диагностика
Балтиморские критерии
Балтиморские критерии полезны при постановке диагноза. Синдром обструкции печеночного синуса подтверждается при соблюдении следующих условий:
Дифференциация
Дифференциальный диагноз должен включать:
Дополнительные исследования
В сомнительных случаях диагноз подтверждается если:
При допплеровском исследовании печеночных сосудов можно наблюдать изменение направления кровотока в воротной вене.
Профилактика
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9F%D1%80%D0%BE%D1%84%D0%B8%D0%BB%D0%B0%D0%BA%D1%82%D0%B8%D0%BA%D0%B0.jpg?resize=450%2C300&ssl=1″ alt=»Профилактика» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Профилактика
Для профилактики закупорки сосудов синуса печени используются менее агрессивные, чем стандартные схемы миелоаблативной терапии, с применением флударабина, более низкие дозы бусульфана или дозы облучения.
Наибольший риск закупорки сосудов синуса печени связан с назначением циклофосфамида и облучением в дозе> 12 гр. Смертность у пациентов с синдромом обструкции синуса печени, получавших такое лечение может составлять 15-20%.
Кроме того, в профилактике используются:
Руководящие принципы Американской ассоциации по изучению заболеваний печени (AASLD) не рекомендуют какие-либо из этих методов лечения, поскольку рандомизированные испытания не подтвердили их эффективность. Антикоагулянтная терапия, также может привести к опасным для жизни кровотечениям.
Симптоматическое лечение перегрузки жидкостью включает:
Из-за отсутствия достаточных данных не рекомендуется использовать дефибротид, тканевый активатор плазминогена или TIPS (трансъюгулярный внутрипеченочный портосистемный шунт).
Трансплантация печени может быть терапевтическим вариантом у пациентов с незлокачественными заболеваниями, например, аутоиммунными заболеваниями.
Прогноз
Плохой прогноз определяется:
Тромбоз печеночной вены (синдром Бадда-Киари)
Тромбоз печеночной вены (синдром Бадда-Киари)
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%A2%D1%80%D0%BE%D0%BC%D0%B1%D0%BE%D0%B7-%D0%BF%D0%B5%D1%87%D0%B5%D0%BD%D0%BE%D1%87%D0%BD%D0%BE%D0%B9-%D0%B2%D0%B5%D0%BD%D1%8B-%D1%81%D0%B8%D0%BD%D0%B4%D1%80%D0%BE%D0%BC-%D0%91%D0%B0%D0%B4%D0%B4%D0%B0-%D0%9A%D0%B8%D0%B0%D1%80%D0%B8.jpg?resize=450%2C300&ssl=1″ alt=»Тромбоз печеночной вены (синдром Бадда-Киари)» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Тромбоз печеночной вены (синдром Бадда-Киари)
Определение
Нарушение кровотока, возникающее на любой стадии оттока крови из печени, от мелких печеночных вен, до места соединения главной вены с правым предсердием.
Разделение
Синдром Бадда-Киари делится на:
Причины
Клинически заболевание может иметь вид:
Существуют значительные расхождения между клинической картиной и длительностью тромбоза. Например, у пациентов с симптомами острого тромбоза очень часто встречаются признаки длительного заболевания, такие, как выраженный фиброз и цирроз.
Общие клинические симптомы включают:
Заболевание протекает бессимптомно примерно у 20% пациентов с развивающимся коллатеральным кровообращением.
Диагностика
Биохимические исследования
Биохимические тесты выявляют нарушения разной степени тяжести, в зависимости от клинического состояния. Асцитная жидкость имеет характеристики транссудата.
Изображение венозных сосудов
При допплеровском исследовании печеночные вены демонстрируют расширение в сочетании с отсутствием или изменением направления кровотока. Кроме того, могут быть расширенные коллатеральные сосуды, соединяющие печеночную вену с меж реберной и диафрагмальной венами. Магнитно-резонансная томография с контрастным веществом позволяет точно визуализировать обструкцию в просвете сосудов или источник внешнего давления на печеночные вены или нижнюю полую вену.
Гипертрофия хвостатой доли
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%93%D0%B8%D0%BF%D0%B5%D1%80%D1%82%D1%80%D0%BE%D1%84%D0%B8%D1%8F-%D1%85%D0%B2%D0%BE%D1%81%D1%82%D0%B0%D1%82%D0%BE%D0%B9-%D0%B4%D0%BE%D0%BB%D0%B8.jpg?resize=450%2C300&ssl=1″ alt=»Гипертрофия хвостатой доли» width=»450″ height=»300″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=825%2C550&ssl=1 825w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=768%2C512&ssl=1 768w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Гипертрофия хвостатой доли
У большинства пациентов с синдромом Бадда-Киари наблюдается увеличение хвостатой доли. Это связано с тем, что хвостатая доля имеет венозное соединение с нижней полой веной, независимо от печеночных вен. Таким образом, в случае обструкции печеночных вен, по хвостатому отростку протекает гораздо больше крови, что приводит к его компенсаторной гипертрофии.
Регенеративные узелки
У пациентов с синдромом Бадда-Киари все визуальные исследования могут показать макро регенеративные узелки, демонстрирующие усиление артериальной фазы, и могут морфологически напоминать гепатоцеллюлярную карциному.
Эти узелки имеют иную этиологию, чем регенеративные, при циррозе печени. Их дифференциация от гепатоцеллюлярной карциномы может быть трудной. Многочисленные небольшие узелки указывают на довольно доброкачественные поражения, в то время, как единичные, увеличивающиеся поражения, могут указывать на рак.
Патоморфологическое обследование
При типичных симптомах синдрома Бадда-Киари в биопсии печени нет необходимости, более того, зачастую она невозможна по техническим причинам (нарушения свертываемости, асцит). Гистопатологическое исследование показывает расширение пазух с признаками застоя и фиброза в центральной части долек. Иногда в крошечных венах можно увидеть сгустки крови.
Мероприятия по порядку:
Антикоагулянтное лечение
Согласно рекомендациям AASLD, во время диагностики синдрома Бадда-Киари следует начать антикоагулянтную терапию (низкомолекулярные гепарины), а затем перейти на пероральные антикоагулянты, поддерживая нормализованный индекс активности протромбина (INR) в диапазоне 2- 3. Только противопоказания или серьезные осложнения, дают право прекратить лечение антикоагулянтами.
Чрескожная ангиопластика
Ангиопластика и протезирование печеночной вены следует рассматривать у всех пациентов с симптомами, чьи результаты визуализационных исследований показывают, что такое вмешательство возможно, например, в случае сегментарного стеноза или тромбоза.
Если антикоагуляция не улучшается, рассматривается возможность портальной системной трансъюгулярной внутрипеченочной фистулы (TIPS), очевидно, с предварительным подтверждением проходимости воротной вены.
TIPS у пациентов с синдромом Бадда-Киари – технически, очень сложная процедура, иногда она требует введения проводника непосредственно из просвета нижней полой вены, поэтому выполняется только в нескольких медицинских центрах в мире.
Пересадка печени
Показанием к трансплантации печени может быть мгновенная недостаточность органов. Трансплантация также должна рассматриваться, когда хирургия портальной системной трансцервикальной внутрипеченочной фистулы невозможна или неэффективна.
Прогноз
Независимые прогностические факторы при синдроме Бадда-Киари – это компоненты шкалы Чайлда-Тюркотта-Пью. Прогноз для этого синдрома значительно улучшился за последнее десятилетие и часто больше зависит от прогрессирования основного заболевания, (например, миелодиспластического синдрома), чем от симптомов печеночной недостаточности. Около 80% пациентов выживают через пять лет после трансплантации печени.
Резюме
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%A0%D0%B5%D0%B7%D1%8E%D0%BC%D0%B5.jpg?resize=450%2C300&ssl=1″ alt=»Резюме» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Резюме
Причиной обструкции печеночной артерии могут быть: атеросклероз, тромбоз, эмболия, инфильтрация печени, травмы, заболевания сосудов. Обструкция также может быть осложнением трансплантации печени.
Из-за двойной васкуляризации печени окклюзия печеночной артерии не является синонимом инфаркта органа. Визуализирующие исследования играют важную роль в диагностике: допплерография, компьютерная томография с контрастным веществом и магнитно-резонансная томография.
Тромбоз воротной вены подразделяется на острый и хронический. Оба состояния имеют схожую этиологию и чаще всего второе будет продолжением первого. Однако, методы лечения различаются. Наиболее частые факторы риска тромбоза воротной вены – это миелопролиферативные нарушения, а также врожденная и приобретенная недостаточность факторов, модулирующих каскад коагуляции.
Общие осложнения хронического тромбоза воротной вены, связанные с симптомами портальной гипертензии, являются редкой причиной смерти пациентов, умирающих от последствий портальной билиопатии или прогрессирования миелопролиферативного заболевания до острого лейкоза или миелофиброза.
Синдром заложенности носовых пазух печени приводит к нарушениям кровообращения в ней, в результате токсического повреждения эндотелиальных клеток, выстилающих пазухи.
Это наиболее частое осложнение миелоаблативного лечения при подготовке пациентов к трансплантации костного мозга.
Балтиморские критерии полезны в диагностике. Профилактика основана на менее агрессивных режимах миелоаблативной терапии, чем при стандартной терапии.
Тромбоз печеночных вен (синдром Бадда-Киари) может проявляться, как фульминантная, острая или хроническая печеночная недостаточность. В курс лечения входят: антикоагулянтная терапия, чрескожная ангиопластика, TIPS и трансплантация печени. Благодаря такому режиму лечения до 90% пациентов живут больше 5 лет.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter