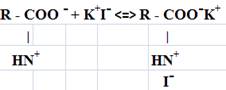Научная электронная библиотека
1.2. Коллаген
Коллагены составляют основу структуры кожи, костей, хрящей, сухожилий, кровеносных сосудов и играют важную роль в сохранении нормальной структуры и функции соединительной ткани всех животных (Слуцкий, 1969, 1985; Риггз, Мелтон, 2000; Руденская, 2003).
Коллаген (К) – нерастворимый фибриллярный белок, первичная структура которого складывается из повторяющихся последовательностей триплетов аминокислот глицин-X-Y, где X и Y позиции чаще заняты, соответственно, пролином и гидроксипролином. Эти повторяющиеся последовательности позволяют трем коллагеновым полипептидам (называемым α-цепями) формировать полужесткие, очень стабильные трехспиральные молекулы (рис. 3). Они могут быть гомополимерными (три идентичные α-цепи) и гетерополимерными (две или три разные α-цепи). Под влиянием регулярно располагающихся остатков пролина и оксипролина цепь принимает форму ломаной спирали; это обусловливается жесткостью боковых групп пролина, а также тем обстоятельством, что пептидные связи, в образовании которых участвуют пролин и оксипролин, не могут образовать водородных связей. Остатки глицина образуют межцепочечные водородные связи, способствующие сохранению прочности структуры коллагена.


Рис. 3. Структура коллагена: а – электронная микрофотография коллагена соединительной ткани. Расстояние между повторяющимися структурными единицами равно 700 Å; б – конформация полипептидных цепей в трёхцепочечной молекуле тропоколлагена; в – ступенчатое расположение молекул тропоколлагена обусловливает появление в гидратированных волокнах коллагена повторяющихся структурных единиц, расстояние между которыми равно 700 Å (по Мусил и др., 1984)
Аминокислотные цепи коллагена обернуты друг вокруг друга и образуют «трехволоконный канат», где отдельные волокна связаны между собой водородными связями. Такая пространственная структура возможна, только если аминокислотная последовательность строго соблюдается.
В результате образуется трехволоконная фибриллярная молекула – тропоколлаген, обладающая большой прочностью на растяжение. Это название происходит от слова тропос – обращенный внутрь – из-за того, что коллагеновые волокна всех соединительных тканей, выстланы тропоколлагеновыми молекулами, соединенными «конец в конец» и «бок о бок» – в шахматном порядке. Гидроксильные группы некоторых остатков лизина и оксилизина участвуют в образовании связи между соседними молекулами тропоколлагена. Таким образом, формируется жесткое нерастяжимое волокно. Фибробласты синтезируют молекулы тропоколлагена и выбрасывают их в матрикс, и только здесь происходит сборка коллагеновых волокон (рис. 4).
Коллагены кожи содержат в больших концентрациях пролин и оксипролин (около 20 % от всех остальных аминокислот), глицин и аланин (свыше 50 % от содержания других аминокислотных остатков), ароматические и серосодержащие аминокислоты практически отсутствуют или содержатся в весьма малых количествах. Кроме того, коллаген является одним из немногих белков, содержащих оксипролин и оксилизин. Оксипролин и оксилизин образуются в молекуле проколлагена не в результате биосинтеза, а при гидроксилировании пролина и лизина, которое начинается в период трансляции коллагеновой мРНК на рибосомах (Неклюдов, 2003).
Рис. 4. Строение фибробласта и основные этапы синтеза коллагена. Г – аппарат Гольджи; Я – ядро; ШЭР – шероховатый эндоплазматический ретикулум; СП –секреторный пузырек; ТК – тропоколлаген; КВ – коллагеновое волокно
В настоящее время идентифицировано более 25 различных α-цепей, из которых формируется до 14 разных типов коллагеновых молекул, некоторые из них являются тканеспецифичными (Ленинджер, 1974; Риггз, Мелтон, 2000).
Таким образом, коллагены – это белки, которые:
б) могут состоять из трех цепей с повторяющимися последовательностями, обладающими способностью к сворачиванию в характерную тройную спираль. По меньшей мере, 19 белков определены в настоящее время как принадлежащие к коллагенам. 10 родственных им белков содержат коллагеноподобные домены.
Коллагеновые белки составляют около половины массы сухого вещества суставного хряща; вблизи суставной поверхности их концентрация приближается к 90 %. В других видах хрящевой ткани коллагены количественно преобладают над другими белками, обеспечивая прочность на растяжение и разрыв. (Слуцкий, 1985). Количественно преобладающим белком протеогликанового комплекса хрящевой ткани является коллаген второго типа (КII). Он в незначительных количествах обнаружен в других специализированных тканях, например, в стекловидном теле глаз некоторых видов животных. Хрящевой ткани присущ необычный полиморфизм коллагеновых компонентов, проявляющийся присутствием большого числа минорных коллагенов. Молекулярная формула КII хрящевой ткани имеет следующий вид: [α1(ΙΙ)]3, что означает наличие трех идентичных α1(II)-цепей, которые отличаются от α1(I)-цепей более высоким содержанием оксилизина. Столь высокая концентрация оксилизина способствует увеличению количества связанных с ним углеводов. По-видимому, такая структура обеспечивает большую сольватную оболочку коллагена типа II по сравнению с типами I или III. В процессе биосинтеза коллагена С-пропептиды соединяются между собой бисульфидными мостиками и после отщепления от молекулы образуют белок, который называется хондрокальцин, с м.м. около 100 000 Да (Слуцкий, 1985).
Коллаген одиннадцатого типа (КXI) составляет приблизительно 3 % хрящевого коллагена и образован двумя разными типами цепей (формула молекулы α1(XI)2 α2(XI)). Со старением организма его количество в хряще уменьшается в пользу коллагена пятого типа (КV) (Канунго, 1982; Риггз и Мелтон, 2000).
Для хрящевой ткани характерно наличие наибольшего количества минорных коллагеновых компонентов. Такой полиморфизм коллагенов позволяет считать минорные компоненты регуляторами адаптационной пластичности хряща, метаболизма хондроцитов и морфогенетических процессов (Слуцкий, 1985).
Содержание коллагена в различных тканях и органах сельскохозяйственных животных (КРС, свиньи) характеризуют следующие данные (% от массы сухого вещества): дерма – 80–90; ахиллово сухожилие – 86; костная ткань – 17,5–25; хрящи – 46–67; роговица и склера глаз – 70; мышцы – 10. При этом коллаген составляет от 25 до 33 % от общего количества белка (Титов, Апраксина, 1995). У костистых рыб коллагеновые белки преобладают в коже, сухожилиях, плавательном пузыре; у кольчатых червей и иглокожих в кожно-мускульном мешке; у моллюсков в кожных покровах и опорных хрящевых элементах.
Наиболее изучены свойства коллагенов в коже и мышечной ткани рыб. Коллаген кожи костистых рыб характеризуется частой встречаемостью молекул, состоящих из трех генетически различающихся α-цепочек, гетеротримера α1 α2 α3; среди изученных позвоночных животных цепочка α3 отмечена лишь у костистых рыб. В целом коллагены мышечной ткани костистых рыб, полученные методом электрофореза, идентичны соответствующим коллагенам типа I из кожи и имеют сходный аминокислотный состав. Однако коллагены мышечной ткани рыб более устойчивы к тепловой денатурации (более 100 °С), чем коллагены кожи, что объясняется более высокой степенью гидроксилирования пролина в мышечном коллагене. Термальная устойчивость мышечного коллагена определяется видом рыбы и по мере ее возрастания рыб можно расположить в следующем порядке: карп, угорь, скумбрия, сайра, кета.
В табл. 1 приведены данные о содержании коллагена и гексозаминов в соединительных тканях различных видов животных.
Составы субъячеек коллагена I типа из мышечной ткани и кожи являются идентичными у угря, скумбрии, сайры и карпа и отличаются у кеты. У последней коллаген кожи состоит из α1 α2 α3 гетеротримеров, а основная часть мышечного коллагена – из (α1)2α2 гетеротримеров (Богданов, Сафронова, 1993).
Содержание гексозаминов и коллагена в соединительной ткани животных
Краткий обзор некоторых кофакторов, участвующих в синтезе коллагена
Качественные коллагеновые волокна — одна из
основных составляющих здоровой кожи. Поэтому
большое количество косметологических методов
направлено на восстановление ее коллагенового каркаса.
Как витамины и микроэлементы могут влиять на синтез
коллагена? И почему для достижения стойкого эффекта
необходимо учитывать их количественный состав
в организме?
Ежегодно создаются новые методики и препараты для улучшения синтеза коллагена с целью профилактики инволюционных процессов в организме и уменьшения выраженности возрастных изменений.
Но за стремлением повлиять на коллагеногенез извне порой забывают о тех веществах, без достаточного количества которых в самом
организме синтез коллагена крайне затруднен. Никто не будет отрицать, что продукция этого жизненно важного белка зависит от гормонов, гормоны, в свою очередь, от присутствия металлов, усвоение металлов — от витаминов; и эту цепочку можно продолжать долго, тем более что она замкнутая. Осветить все нюансы в одной статье не представляется возможным, но сделать шаг навстречу пониманию некоторых процессов — в наших силах.
Синтез и процессинг (созревание) коллагена включает в себя несколько этапов:
Всем известно об участии магния и кальция в синтезе соединительной ткани и коллагена, но о железе, цинке, меди, витаминах С и D часто забывают. Именно эти кофакторы рассмотрим в статье.
Железо
Железодефицитная анемия в той или иной степени присутствует у 40–60 % женщин детородного возраста по всему миру [2, 26]. И это при том, что железо — один из важнейших микроэлементов, необходимых для нормального функционирования биологических систем организма. Оно требуется для осуществления функции дыхания, кроветворения, участвует в иммунобиологических и окислительно-восстановительных реакциях.
Причины дефицита железа:
Учитывая высокую распространенность дефицита железа в популяции, сложно говорить о нормальном синтезе коллагена при таких состояниях.
Цинк — единственный металл, представленный в небелковой части ферментов каждого класса, и никаким другим металлом цинк не может быть заменен. Несмотря на малую концентрацию цинка в крови, стабильные связи с макромолекулами делают его доступным для всех тканей организма, что в дальнейшем позволяет удовлетворять потребности в нем белков и ферментов, выполняющих различные биологические функции [28].
Распространенность дефицита цинка в мире не менее значительная, чем железа и витамина С, и составляет до 60% [29].
Для транспорта эритроцитами кислорода и углекислого газа абсолютно необходим цинк, и большая часть цинка крови содержится именно в эритроцитах в составе цинковых металлоферментов — карбоангидраз. Карбоангидразы катализируют превращения углекислого газа в угольную кислоту (угольная кислота участвует в поддержании pH крови в физиологическом диапазоне (7,25–7,35). В капиллярах легких эти процессы идут в обратном направлении: угольная кислота распадается на углекислый газ и воду, и углекислый газ удаляется наружу [18].
Без нормального дыхания ни одна клетка не способна осуществлять свои функции.
В мире распространенность дефицита меди в организме, приводящего, наряду с железом, к анемии, составляет до 30%. А ведь этот микроэлемент крайне необходим для нормальной физиологии организма.
Если говорить о коже, то медь играет ключевую роль в ангиогенезе, синтезе и стабилизации белков внеклеточного матрикса [3].
В физиологически значимых концентрациях (2 мг — средняя суточная потребность) медь ускоряет заживление ран [16].
Ионы меди, которые являются кофакторами лизилоксидазы, принимают участие в последнем этапе синтеза коллагена. Медь имеет важное значение для формирования внутри- и межмолекулярных поперечных связей в коллагене, а соответственно, и прочности коллагеновых и эластиновых фибрилл [8, 13,
15]. Недостаток меди ухудшает формирование сшивок коллагена и приводит к тяжелой патологии костей, легких и сердечно-сосудистой системы [12].
Компенсация дефицита этого микроэлемента, бесспорно, улучшает синтез коллагена, в том числе в коже (рис. 4) [7, 10].
Аскорбиновая кислота (витамин С)
Аскорбиновая кислота играет в организме фундаментальную роль — нет фактически ни одного физиологического процесса, в котором бы она не принимала участия.
Роль витамина С в организме
Аскорбиновая кислота в организме человека оказывает влияние на множество важнейших биологических процессов:
Распространенность дефицита витамина С в мире по разным данным составляет 20–40% [14, 15].
В последнее время много исследований посвящено аскорбиновой кислоте и ее биодоступности для кожи [9]. При недостатке витамина С в организме его нанесение на кожу не будет иметь ожидаемого эффекта, так как не сможет восполнить нутритивный дефицит. В ходе проведенных исследований выяснилось, что витамин С ускоряет заживление ран, участвует в активизации синтеза коллагена I типа (рис. 5) и снижении параметров
окислительного стресса. Никаких значимых побочных эффектов при добавлении витамина С в питание в ходе проведенных исследований выявлено не было [5, 6].
Синтез коллагена зависит от гормонов, гормоны, в свою очередь, от присутствия металлов, усвоение металлов — от витаминов, и эту цепочку можно продолжать долго, тем более что она замкнутая.
Витамин D
Распространенность дефицита витамина D в российской популяции составляет более 90% (в мире 50–60%) [19]. Этот витамин стимулирует увеличение синтеза секретируемых белков TGF-β (регулируют деление
и дифференцировку различных типов клеток, включая фибробласты и кератиноциты) и их связывание с рецепторами на мембране клеток. Поэтому при его дефиците происходит нарушение активности сигнальных каскадов TGF-β, что ухудшает заживление кожи после любой травмы (включая косметологические манипуляции). Например, во время термолифтинга часть коллагеновых волокон дермы сжимается и уменьшается в объеме. Это приводит к повышению зернистости базального слоя и при достаточном количестве витамина D создает благоприятные условия для воздействия его активных форм на экспрессию TGF-β1, который и способствует обновлению соединительной ткани [11].
Выводы
Мы кратко обсудили лишь некоторые кофакторы, участвующие в синтезе коллагена. Но даже этот незначительный пласт информации позволяет судить о зависимости синтеза коллагена от нутритивного статуса организма, чем не следует пренебрегать, решая многие эстетические задачи. Изменение синтеза
коллагена происходит постепенно и усугубляется нутритивным дефицитом [19].
Три вида коллагена для косметологии
Коллагену уделяют большое внимание в косметологии, в первую очередь потому, что именно он отвечает за молодость нашей кожи. Он представляет собой белковые закрученные (спиральные) цепи пептидов, которые поддерживают соединительные ткани тела в нужном состоянии.
В состав коллагена входят следующие аминокислоты:
глицин 33,5%, пролин 11,82%, аланин 10,93%, гидроксипролин 9,21%, глутаминовая кислота 7,19%, аргинин 4,45%, серин 3,87%, лейцин 2,66%, лизин 2,6%, валин 2,0%, треонин 1,87%, изолейцин 1,36%, фенилаланин 1,31%,гидроксилизин 0,76%, метионин 0,61%, тирозин 0,52%, гистидин 0,42%.
Главными функциями коллагена являются:
— поддержать прочность тканей;
— защитить все структуры организма от повреждений;
— обеспечить процесс регенерации (восстановления);
— повысить эластичных свойств ткани (вместе с эластином);
— ускорить формирования клеточных оболочек;
— предотвратить развитие злокачественных опухолевых процессов в тканях.
Синтез коллагена в организме
Сложный восьмиэтапный биологический процесс. Первые пять этапов проходят в пределах клеток (фибробластов), а последние три осуществляются на внеклеточном уровне. Сначала на рибосомах клеток осуществляется синтез предшественника коллагена (препроколлагена). Затем образуется проколлаген на эндоплазматической сети фибробластов после отделения участка пептидной цепи. Аминокислотные остатки окисляются под воздействием особых ферментов. Глюкоза и галактоза переносятся на проколлаген посредством специальных ферментов и образуется тройная спираль растворимого коллагена – тропоколлагена, который выделяется в межклеточную среду, и происходит отщепление части молекулярных звеньев. Затем формируются прочные спирали нерастворимого коллагена из соединенных частей молекул. Процесс биосинтеза коллагена протекает при участии витамина С, глюкокортикоидов и половых гормонов.
Процесс распада волокон коллагена непрерывен и происходит под влиянием коллагеназы и некоторых других ферментов, что приводит к образованию аминокислот, которые, в свою очередь, участвуют в синтезе нового коллагена и в формировании клеток.
На данный момент описаны двадцать восемь типов коллагена, кодируемых при помощи более чем сорока генов. Данные типы имеют отличия по степени их модификации (интенсивности гликозилирования или гидроксилирования), а также по последовательности аминокислот. Для всех видов коллагенов общим является наличие одного или больше доменов белка, которые содержат тройную спираль, а также их присутствие во внеклеточных структурах ткани. Более девяноста процентов всех коллагенов высших организмов составляют коллагены IV, III, II и I типов.
Существуют следующие разновидности коллагена и их типы:
Основными и важными для поддержания здоровья и красоты являются 1, 2 и 3 тип.
Коллаген третьего типа III – уникальная составляющая внеклеточного матрикса и метаболизма. Он служит базой соединительной ткани человеческих органов. Отвечает за обмен веществ и эластичность кожи, волос и ногтей. Также, он влияет на сердечную область и кровеносную систему.
В целом все три типа коллагена отвечают за омоложение, тонус и общее состояние организма.
Из продуктов ежедневного рациона, каким бы богатым и разнообразным он ни был мы не можем получить коллаген в достаточном количестве, поэтому сегодня разработаны десятки технологий получения коллагена в промышленных масштабах из всевозможных источников.
Технологический коллаген бывает трех типов, в зависимости от сырья, из которого его производят.
Современная косметология на сегодняшний день имеет два направления:
— использование технологического коллагена;
— активизация синтеза собственного коллагена в организме человека.
Применяют косметический коллаген следующим образом:
— Как ингредиент множества косметических средств (масок, гелей, кремов). Такой белок на какое-то время заполняет неровности на коже и образует тонкую гигроскопичную пленку, благодаря чему происходит активное увлажнение и питание тканей.
— В качестве филеров в контурной инъекционной пластике и как один из компонентов коктейлей для мезотерапии.
— В составе биологических добавок, в виде капсул, порошков и таблеток.
Стимуляция самостоятельного синтеза коллагена в организме может осуществляться следующими способами:
Коллаген имеет высокую важность в вопросе поддержания молодости нашей кожи. Он повышает тонус кожи, делает ее эластичной и прочной, благоприятствует увлажнению. В норме в молодом человеческом организме полный цикл распада и синтеза коллагеновых волокон длится около месяца, и обмен коллагена доходит до 6 кг в год. Однако с возрастом показатели меняются. После 30 лет процессы распада начинают преобладать над синтезом, и количество коллагена в кожных покровах постепенно снижается. Качество волокон ухудшается, они становятся хрупкими, накапливается фрагментированный коллаген. Поэтому кожа со временем теряет эластичность, становится обвисшей, дряблой и тонкой, ухудшается ее цвет. Также белок перестает удерживать достаточный объем воды. Из-за этого кожа пересыхает, и на ней появляются морщины. Формируется птоз (обвисание тканей кожи), который ведет к разрушению фибробластов, необходимых для синтеза коллагена. То есть возникает замкнутый круг, и процессы увядания кожи ускоряются. Поэтому своевременное обращение к специалисту – косметологу поможет подобрать эффективные средства и методики для замедления процесса старения кожи и улучшения ее состояния.
Откройте для своей кожи 8 пищевых продуктов, богатых коллагеном
Влияние коллагена, что важно?
Коллаген является основным компонентом, который составляет основу соединительной ткани организма: мышц, сухожилий, связок, кожи, хрящей, суставов и т.д. Это один из главных компонентов, отвечающий за ь прочность и эластичности всей соединительной ткани, в том числе и стенок кровеносных сосудов и сердца.
С возрастом выработка коллагена постепенно снижается. Примерно после 35-40 лет выработка коллагена в организме сокращается, что может вызывать проблемы (дряблость и провисание кожи, появление морщин). Кроме того, снижение выработки коллагена может привести к таким заболеваниям как: остеоартрит, боли в суставах и мышцах.
Преимущества коллагена для кожи
К основным преимуществам коллагена для кожи относятся:
Продукты, которые улучшают выработку коллагена в коже
Не секрет, что для того, чтобы организм получал все необходимые витамины и питательные вещества, питание должно быть разнообразным и сбалансированным. Употребление достаточного количества жидкости также влияет на выработку коллагена и гидратации кожи. Это самый простой и доступный способ поддерживать выработку коллагена.
Не существует никаких чудодейственных препаратов и средств для кожи, но есть те, которые способствуют повышению упругости кожи и позволяют ей выглядеть здоровой.
Мы составили список продуктов, которые способствуют выработке коллагена:
1. Животный белок: мясо и рыба
В белке животного происхождения (мясо, субпродукты, желатин животного происхождения) содержится большое количество коллагена.
Важно избегать полуфабрикатов.
Эксперты рекомендуют употреблять мясо красного цвета умеренно (не более одного раза в неделю).
Рыба, особенно лосось, тунец или форель с высоким содержанием омега-3 жирных кислот естественно повышает концентрацию коллагена (также являясь полезными для костей и суставов).
2. Фрукты и овощи
А фрукты богатые витамином С необходимы для производства коллагена: апельсин, киви, грейпфрут, манго, ананас и некоторых других. Например, лимон не стимулирует производство коллагена, но и действует, как антиоксидант.
3. Яйца
Яйца являются лучшей пищей для нашей кожи, ведь в них большая концентрация ценных белков и витаминов группы В, Е, аминокислот и серы).
4. Сухофрукты и орехи
Арахис, грецкие орехи, фисташки, миндаль также стимулирует выработку коллагена.
5. Молочные продукты
Молочные продукты (молоко, сыр, йогурт и т.д.) благотворно влияют на производство коллагена благодаря высокому содержанию белка.
6. Серные продукты
Нужно употреблять в пищу продукты, которые содержат серу в своём составе (чеснок, лук, сельдерей, огурцы, оливки, виноград) они тоже обеспечивают хороший уровень коллагена в организме.
7. Чай
Чай (зеленый, белый, черный или красный) является натуральным антиоксидантом, который предотвращает снижение коллагена в нашем организме.
8. Желе
Желатин в организме превращается в коллаген и это тоже ценный источник животного белка.
Масло Bio-Oil способствует улучшению эластичности вашей кожи
Употребляйте в пищу полезные продукты и не забывайте про ритуал красоты с использованием масла Bio-Oil утром и вечером для сохранения красоты и молодости вашей кожи.
Какая аминокислота отсутствует в коллагене
На долю соединительной ткани приходится более 50 % массы тела животного. Существенной особенностью, отличающей ее от других и присущей в большей или меньшей степени всем ее разновидностям, является количественное преобладание межклеточного вещества над клеточными элементами. Межклеточный матрикс состоит из волокнистых компонентов, а пространство между ними заполнено основным веществом, содержащим гликопротеины. Волокнистые компоненты состоят из коллагеновых и эластиновых волокон.
Для соединительнотканных белков характерно присутствие внутри- и межмолекулярных поперечных сшивок: альдольная, гистидин-альдольная, лейцин-норлейциновая, основание шиффа. В результате появляется возможность ковалентного связывания четырех боковых цепей друг с другом, причем они могут принадлежать разным молекулам белка.
В эластине значительно меньше содержание лизина это обусловлено тем, что боковые цепи четырех остатков аминокислоты ферментативным путем превращаются в десмозин, в результате формируется поперечная сшивка между соседними полипептидными цепями в молекуле эластина. Именно присутствие десмозина отличает эластин от всех других белков, включая и коллаген.
Благодаря своей уникальной структуре белки соединительной ткани в нативном состоянии не подвергаются действию протеолитических ферментов. Ткани, содержащие коллаген и эластин, отличаются особой прочностью, способностью выдерживать значительные нагрузки.
При всем сходстве данных белков, каждый из них является индивидуальным белком, со свойствами присущими только ему одному.
Молекула коллагена имеет относительную молекулярную массу 300000, длину 280 нм и толщину 1,4 нм. Каждая a-цепь содержит в среднем около 1000 аминокислотных остатков. Еще одной особенностью коллагена является его гетерогенность. В настоящее время описано 28 типов коллагена, которые кодируются более чем 40 генами. Они отличаются друг от друга по аминокислотной последовательности, а также по степени модификации – интенсивности гидроксилирования или гликозилирования. Общим для всех коллагенов является существование одного или более доменов, содержащих тройную спираль и присутствие их во внеклеточном матриксе [5].
Практическое применение имеет в основном коллагенсодержащее сырье, это связано со способностью коллагена образовывать гели при взаимодействии с водой. Коллаген находит широкое применение в медицине для пластики сосудов, дефектов кожи, кости, мозговой оболочки, тазового дна, трахеи, печени и селезенки. Применяется в виде гемостатических средств и тампонов, мембран для диализа, шовного материала, а также для доставки лекарственных средств в организм человека, в пищевой промышленности – в качестве гелеобразователя.
Цель работы исследование возможности использования соединительнотканных белков в качестве носителей биологически активных веществ.
Материалы и методы исследований
Объектами исследования были сухожилия и выйная связка крупного рогатого скота, желатин, растворы гидролизатов коллагена и эластина, соли йода и железа, а также растительные настои, содержащие фенольные соединения, в частности антоцианы.
Основные этапы получения гидролизата коллагена: измельчение сухожилий, последовательная солевая и кислотная экстракция, тепловая обработка и охлаждение. Раствор гидролизата коллагена имел светло-матовый цвет, без видимых границ раздела фаз.
Эластин выделяли из выйной связки при последовательной экстракции: солевой, щелочной, водной. Растворимую форму белка получали методом биотрансформации.
Гидролизат представляет собой сложную смесь пептидов, жидкость светло-желтого цвета, без вкуса и запаха. Содержание белка в 1 мл гидролизата коллагена и эластина составило 30 мг и 40 мг соответственно.
При проведении экспериментов использовали аналитические методы качественного и количественного анализа.
Результаты исследований и их обсуждение
В результате проведенных исследований получены растворимые формы соединительнотканных белков – гидролизаты коллагена и эластина, которые исследовали в качестве матрицы микроэлементов, в частности железа и йода.
Источниками микроэлементов служили сульфат железа (II) и йодид калия. Одним из основных условий при проведении реакции являлся показатель рН среды. Выбор рН среды связан со свойствами микроэлементов и фермента. Так, в кислой среде йод восстанавливается до молекулярного состояния и улетучивается, в щелочной среде рН > 8,0 образуется гипойодид. Фермент при рН выше 6,0 инактивируется. Учитывая данные факторы, в растворах устанавливали рН 7,0 – 7,2. Расчет вводимого количества йодида калия производили по содержанию йода (76,5%).
При взаимодействии железа и гидролизатов коллагена и эластина были исследованы значения рН (9,0; 5,5; 3,5)±0,2. При рН 9,0±0,2 наблюдалось изменение окраски от светло-желтого (гидролизат эластина) и светло-матового (гидролизат коллагена) до темно-коричневого цвета с выпадением осадка в виде хлопьев, что снижало органолептические свойства и указывало на окисление железа.
При рН среды 3,5 и 5,5 наблюдалось одинаковое связывание железа без визуальных изменений растворов. Однако, учитывая значения рН максимальной устойчивости комплексов и большинства пищевых систем, выбрано значение 5,5±0,2.
Оптимальная температура процессов связывания йода и железа соединительнотканными белками выбрана 0-4 °С, так как при положительных температурах возможно микробное обсеменение исследуемых растворов.
Известно, что химические процессы протекают во времени. Для установления максимальной степени связывания в растворы гидролизатов эластина и коллагена вносили разные концентрации солей железа и йода и контролировали содержание микроэлементов через каждые 2 часа. Концентрации микроэлементов были подобраны исходя из суточной потребности организма человека в них [3]. Экспериментально установлено, что максимальное взаимодействие железа с гидролизатами наблюдалось по истечении 24 часов, в случае йода – 20 часов.
Для выяснения взаимодействия катиона железа с пептидами эластина и коллагена проведены исследования с использованием методов ИК и ЯМР-спектроскопии.
Для более полной информации о взаимодействии между соедительнотканными белками и железом исследовали ядерно-магнитно-резонансные (ЯМР) спектры опытных образцов.
Анализ спектров показал, что в гидролизатах содержится большее количество СОО- групп (области 160-180 м.д., наличие большего количества пиков), в отличие от той же области в гидролизатах с железом. В области 50-65 м.д., которая отвечает за >СН-N