к какому семейству относится цинк
Урок №56. Цинк
ЦИНК И ЕГО СОЕДИНЕНИЯ
СТРОЕНИЕ АТОМА
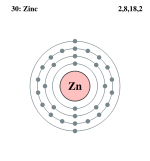
Цинк – элемент IIБ подгруппы четвертого периода. Цинк относится к семейству d-элементов, поскольку электронное строение цинка отражается конфигурацией.
Нахождение в природе
Цинковую обманку считают первичным минералом, из которого образовались другие минералы цинка:
§ каламин 2ZnO · SiO 2 · Н 2 O
В организме взрослого человека содержится в среднем около 2 г цинка, в виде его соединений, который концентрируется преимущественно в простате, мышцах, печени и поджелудочной железе.
Недостаток цинка в организме приводит к ряду расстройств — раздражительность, утомляемость, потеря памяти, депрессивные состояния, снижение остроты зрения, уменьшение массы тела, снижение уровня инсулина, аллергические заболевания, анемия и др.
ЦИНК
СФАЛЕРИТ
Способы получения
Цинк получают из сульфидной руды. Сульфид цинка обжигают в печи кипящего слоя:
Чистый цинк из оксида получают двумя способами.
При пирометаллургическом способе оксид цинка восстанавливают углём или коксом при 1200—1300 °C:
Получаемый раствор сульфата цинка очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу. При электролизе чистый цинк осаждается на алюминиевых катодах, с которых его удаляют и подвергают плавлению в индукционных печах. Таким образом можно получить цинк с высокой чистотой (до 99,95 %).
Качественные реакции
При дальнейшем добавлении избытка щелочи амфотерный гидроксид цинка растворяется с образованием комплексной соли тетрагидроксоцинката :
Химические свойства
2. Цинк взаимодействует со сложными веществами:
§ с парами воды при температуре красного каления с образованием оксида цинка и водорода:
§ с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой и др.).
§ Аналогично: при нагревании с азотной кислотой образуются различные продукты в зависимости о концентрации кислоты – N 2 O, N 2 и др. :
Цинк реагирует с расплавом щелочи с образованием цинката и водорода :
С газообразным аммиаком при 550–600°С образует нитрид цинка:
растворяется в водном растворе аммиака, образуя гидроксид тетраамминцинка:
Оксид цинка
Способы получения
1. Окислением цинка кислородом:
2. Разложением гидроксида цинка при нагревании:
3. Оксид цинка можно получить разложением нитрата цинка:
Химические свойства
Оксид цинка растворяется в избытке раствора щелочи с образованием тетрагидроксоцинката :
3. Оксид цинка не взаимодействует с водой.
7. Оксид цинка — твердый, нелетучий. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Гидроксид цинка
Способы получения
Химические свойства
3. Гидроксид цинка взаимодействует с растворимыми основаниями (щелочами).
В расплаве образуются соли — цинкаты:
Гидроксид цинка растворяется в избытке щелочи с образованием тетрагидроксоцинката :
4. Гидроксид цинка разлагается при нагревании:
Соли цинка
Нитрат и сульфат цинка
Комплексные соли цинка
§ с кислотными оксидами
§ Под действием избытка сильной кислоты осадок не выпадает, т.к. амфотерный гидроксид цинка реагирует с сильными кислотами.
§ Под действием небольшого количества ( недостатка ) сильной кислоты осадок все-таки выпадет, для растворения гидроксида цинка кислоты не будет хватать:
§ Аналогично с недостатком азотной кислоты выпадает гидроксид цинка:
§ Если выпарить воду из раствора комплексной соли и нагреть образующееся вещество, то останется обычная соль-цинкат:
Цинкаты
Соли, в которых цинк образует кислотный остаток (цинкаты) — образуются из оксида цинка при сплавлении с щелочами и основными оксидами:
§ цинкаты реагируют с кислотами с образованием солей цинка :
§ под действием избытка воды цинкаты переходят в комплексные соли:
Сульфид цинка
Сульфид цинка — так называемый «белый сульфид». В воде сульфид цинка нерастворим, зато минеральные кислоты вытесняют из сульфида цинка сероводород (например, соляная кислота):
Под действием азотной кислоты сульфид цинка окисляется до сульфата:
(в продуктах также можно записать нитрат цинка и серную кислоту).
Концентрированная серная кислота также окисляет сульфид цинка:
При окислении сульфида цинка сильными окислителями в щелочной среде образуется комплексная соль:
Цинк (химич. элемент)
Цинк / Zinc (Zn) | |
|---|---|
| Атомный номер | 30 |
| Внешний вид простого вещества | вязкий металл голубовато-серого цвета |
| Свойства атома | |
| Атомная масса (молярная масса) | 65,39 а. е. м. (г/моль) |
| Радиус атома | 138 пм |
| Энергия ионизации (первый электрон) | 905,8(9,39) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 3d 10 4s 2 |
| Химические свойства | |
| Ковалентный радиус | 125 пм |
| Радиус иона | (+2e) 74 пм |
| Электроотрицательность (по Полингу) | 1,65 |
| Электродный потенциал | -0,763 |
| Степени окисления | 2 |
| Термодинамические свойства простого вещества | |
| Плотность | 7,133 г/см³ |
| Удельная теплоёмкость | 25,470 Дж/(K·моль) |
| Теплопроводность | 116 Вт/(м·K) |
| Температура плавления | 692,73 K |
| Теплота плавления | 7,28 кДж/моль |
| Температура кипения | 1180 K |
| Теплота испарения | 114,8 кДж/моль |
| Молярный объём | 9,2 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Период решётки | 2,660 Å |
| Отношение c/a | n/a |
| Температура Дебая | 234,00 K |
Запрос Цинк перенаправляется сюда, если вы имели в виду венгерскую теннисистку см. статью Цинк, Мелинда
СодержаниеИсторияСплав цинка с медью — латунь — был известен еще в Древней Греции, Древнем Египте, Индии (VII в.), Китае (XI в.). Долгое время не удавалось выделить чистый цинк. В 1746 А. С. Маргграф разработал способ получения чистого цинка путём прокаливания смеси его окиси с углём без доступа воздуха в глиняных огнеупорных ретортах с последующей конденсацией паров цинка в холодильниках. В промышленном масштабе выплавка цинка началась в XVII в. Происхождение названияЛатинское zincum переводится как «белый налет». Происхождение этого слова точно не установлено. Предположительно, оно идет от персидского «ченг», хотя это название относится не к цинку, а вообще к камням. Слово «цинк» встречается в трудах Парацельса и других исследователей 16—17 вв. и восходит, возможно, к древнегерманскому «цинко» — налет, бельмо на глазу. Общеупотребительным название «цинк» стало только в 1920-х гг. Нахождение в природеНаиболее распространенный минерал цинка — сфалерит, или цинковая обманка ZnS. Разнообразные примеси придают этому веществу всевозможные цвета. Видимо, за это минерал и называют обманкой. Цинковую обманку считают первичным минералом, из которого образовались другие минералы элемента № 30: смитсонит ZnCO3, цинкит ZnO, каламин 2ZnO · SiO2 · Н2O. На Алтае нередко можно встретить полосатую «бурундучную» руду — смесь цинковой обманки и бурого шпата. Кусок такой руды издали действительно похож на затаившегося полосатого зверька. ПолучениеЦинк в природе как самородный метал не проявляется. 3. Физические свойстваВ чистом виде — довольно пластичный серебристо-белый металл. Обладает гексагональной решеткой с параметрами а = 0,26649 нм, с = 0,49468 нм. При комнатной температуре хрупок, при сгибании пластинки слышен треск от трения кристаллитов (обычно сильнее, чем «крик олова»). При 100—150°C цинк пластичен. Примеси, даже незначительные, резко увеличивают хрупкость цинка. Химические свойстваТипичный амфотерный металл. Стандартный электродный потенциал −0,76 В, в ряду стандартных потенциалов расположен до железа. На воздухе цинк покрывается тонкой пленкой оксида ZnO. При сильном нагревании сгорает с образованием амфотерного белого оксида ZnO: Оксид цинка реагирует как с растворами кислот: Цинк обычной чистоты активно реагирует с растворами кислот: и растворами щелочей: образуя гидроксоцинкаты. С растворами кислот и щелочей очень чистый цинк не реагирует. Взаимодействие начинается при добавлении нескольких капель раствора сульфата меди CuSO4. При нагревании цинк реагирует с галогенами с образованием галогенидов ZnHal2. С фосфором цинк образует фосфиды Zn3P2 и ZnP2. С серой и ее аналогами — селеном и теллуром — различные халькогениды, ZnS, ZnSe, ZnSe2 и ZnTe. С водородом, азотом, углеродом, кремнием и бором цинк непосредственно не реагирует. Нитрид Zn3N2 получают реакцией цинка с аммиаком при 550—600°C. ПрименениеЧистый металлический цинк используется для восстановления благородных металлов добываемых подземным выщелачиванием (золото, серебро). Кроме того, цинк используется для извлечения серебра, золота и др. Из чернового свинца в виде так называемой «серебристой пены» интерметаллидов цинка с серебром и золотом, и обрабатываемых обычными методами аффинажа. Применяется для защиты стали от коррозии (оцинковка, которая хорошо известна всем, кто видел оцинкованное ведро, или металлизация — для мостов, емкостей, металлоконтрукций). Также используется в качестве материала для отрицательного электрода в химических источниках тока, то есть в батарейках и аккумуляторах, например: Марганцево-цинковый элемент, серебряно-цинковый аккумулятор (ЭДС 1,85 В, 150 Вт·ч/кг, 650 Вт·ч/дм³, малое сопротивление и колоссальные разрядные токи, ртутно-цинковый элемент (ЭДС 1,35 В, 135 Вт·ч/кг, 550—650 Вт·ч/дм³), диоксисульфатно-ртутный элемент, йодатно-цинковый элемент, медно-окисный гальванический элемент (ЭДС 0,7—1,6 Вольт, 84—127 Вт·ч/кг, 410—570 Вт·ч/дм³), хром-цинковый элемент, цинк-хлоросеребряный элемент, никель-цинковый аккумулятор (ЭДС 1,82 Вольт, 95—118 Вт·ч/кг, 230—295 Вт·ч/дм³), свинцово-цинковый элемент, цинк-хлорный аккумулятор, цинк-бромный аккумулятор и др). Очень важна роль цинка в цинк-воздушных аккумуляторах, в последние годы интенсивно разрабатываются на основе системы цинк-воздух — аккумуляторы для компьютеров (ноутбуки) и в этой области достигнут значительный успех (большая, чем у литиевых батарей энергия, ресурс и они дешевле в 3 раза), так же эта система очень перспективна для пуска двигателей (свинцовый аккумулятор — 55 Вт·ч/кг, цинк-воздух — 220—300 Вт·ч/кг) и для электромобилей (пробег до 900 км). Входит в состав многих твёрдых припоев для снижения их температуры плавления. Цинк — важный компонент латуни. Окись цинка широко используется в медицине как антисептическое и противовоспалительное средство. Также окись цинка используется для производства краски — цинковых белил. Хлорид цинка — важный флюс для пайки металлов и компонент при производстве фибры. Теллурид, селенид, фосфид, сульфид цинка — широко применяемые полупроводники. Селенид цинка используется для изготовления оптических стёкол с очень низким коэффициентом поглощения в среднем инфракрасном диапазоне, например, в углекислотных лазерах. Список стран по производству цинка в 2006 году (на основе «Геологического обзора Соединенных Штатов») [1] :
Биологическая рольСреди продуктов, употребляемых в пищу человеком, наибольшее содержание цинка — в устрицах. Однако в тыквенных семечках содержится всего на 26 % меньше цинка, чем в устрицах. Например, съев 45 грамм устриц, человек получит столько же цинка, сколько содержится в 60 граммах тыквенных семечек. Цинк, свойства атома, химические и физические свойстваЦинк, свойства атома, химические и физические свойства.65,38(2) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 Цинк — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 30. Расположен в 12-й группе (по старой классификации — побочной подгруппе второй группы), четвертом периоде периодической системы. Физические свойства цинка Атом и молекула цинка. Формула цинка. Строение атома цинка:Цинк (лат. Zincum, от нем. Zinke – «зубец») – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением Zn и атомным номером 30. Расположен в 12-й группе (по старой классификации – побочной подгруппе второй группы), четвертом периоде периодической системы. Цинк – амфотерный металл. Относится к группе переходных металлов. Относится к цветным металлам. Цинк обозначается символом Zn. Как простое вещество цинк при нормальных условиях представляет собой хрупкий металл голубовато-белого цвета (тускнеет на воздухе, покрываясь тонким слоем оксида цинка). Молекула цинка одноатомна. Химическая формула цинка Zn. Строение атома цинка. Атом цинка состоит из положительно заряженного ядра (+30), вокруг которого по четырем оболочкам движутся 30 электронов. При этом 28 электронов находятся на внутреннем уровне, а 2 электрона – на внешнем. Поскольку цинк расположен в четвертом периоде, оболочек всего четыре. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлена s- и р-орбиталями. Третья – внутренняя оболочка представлена s-, р- и d-орбиталями. Четвертая – внешняя оболочка представлена s-орбиталью. На внешнем энергетическом уровне атома цинка – на s-орбитали находится два спаренных электрона. В свою очередь ядро атома цинка состоит из 30 протонов и 35 нейтронов. Радиус атома цинка (вычисленный) составляет 142 пм. Атомная масса атома цинка составляет 65,38(2) а. е. м. Цинк с давних пор широко используется человеком. Изотопы и модификации цинка:Свойства цинка (таблица): температура, плотность, давление и пр.: | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 204 | Радиус атома (вычисленный) | 142 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 205 | Эмпирический радиус атома* | 135 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 206 | Ковалентный радиус* | 122 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 207 | Радиус иона (кристаллический) | Zn 2+ 6,57 г/см 3 (при температуре плавления 419,53 °C и иных стандартных условиях , состояние вещества – жидкость), 6,4 г/см 3 (при 800 °C и иных стандартных условиях , состояние вещества – жидкость) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 402 | Температура плавления* | 419,53 °C (692,68 K, 787,15 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 403 | Температура кипения* | 907 °C (1180 K, 1665 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 404 | Температура сублимации | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 405 | Температура разложения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 406 | Температура самовоспламенения смеси газа с воздухом | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 7,32 кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 115 кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 409 | Удельная теплоемкость при постоянном давлении | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 410 | Молярная теплоёмкость* | 25,47Дж/(K·моль) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 411 | Молярный объём | 9,2 см³/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 412 | Теплопроводность | 116 Вт/(м·К) (при стандартных условиях ), 116 Вт/(м·К) (при 300 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 500 | Кристаллическая решётка | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 511 | Кристаллическая решётка #1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 512 | Структура решётки | Гексагональная плотноупакованная | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 513 | Параметры решётки | a = 2,6648 Å, c = 4,9468 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 514 | Отношение c/a | 1,856 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 515 | Температура Дебая | 234 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 516 | Название пространственной группы симметрии | P63/mmc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 517 | Номер пространственной группы симметрии | 194 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 900 | Дополнительные сведения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 901 | Номер CAS | 7440-66-6 |
205* Эмпирический радиус атома цинка согласно [1] и [3] составляет 134 пм и 138 пм соответственно.
206* Ковалентный радиус цинка согласно [1] и [3] составляет 122±4 пм и 125 пм соответственно.
402* Температура плавления цинка согласно [3] и [4] составляет 419,6 °С (692,75 K, 787,28 °F) и 419,5 °С (692,65 K, 787,1 °F).
403* Температура кипения цинка согласно [3] и [4] составляет 906,2 °С (1179,35 K, 1663,16 °F) и 906 °C (1179,15 К, 1662,8 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) цинка согласно [3] и [4] составляет 7,28 кДж/моль и 7,24 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) цинка согласно [3] и [4] составляет 114,8 кДж/моль и 115,3 кДж/моль соответственно.
410* Молярная теплоёмкость цинка согласно [3] составляет 25,4 Дж/(K·моль).
 Планета
Планета Китай
Китай Австралия
Австралия Перу
Перу США
США Канада
Канада Мексика
Мексика Ирландия
Ирландия Индия
Индия Казахстан
Казахстан Швеция
Швеция Россия
Россия Бразилия
Бразилия Боливия
Боливия Польша
Польша Иран
Иран Марокко
Марокко Намибия
Намибия Северная Корея
Северная Корея Турция
Турция Вьетнам
Вьетнам Таиланд
Таиланд Гондурас
Гондурас Финляндия
Финляндия ЮАР
ЮАР Чили
Чили Аргентина
Аргентина Болгария
Болгария Румыния
Румыния Япония
Япония Алжир
Алжир Саудовская Аравия
Саудовская Аравия Грузия
Грузия Босния и Герцеговина
Босния и Герцеговина Мьянма
Мьянма










