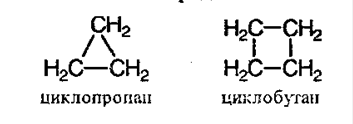к какому классу углеводородов относятся циклопропан циклопентан
Циклоалканы
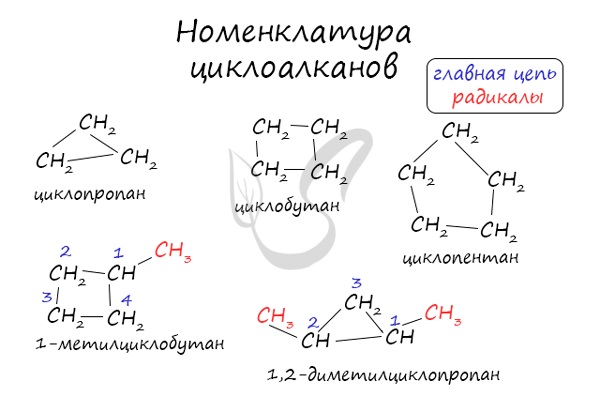
Номенклатура и изомерия циклоалканов
Названия циклоалканов формируются путем добавления приставки «цикло-» к названию алкана с соответствующим числом: циклопропан, циклобутан и т.д.
Как и у алканов, атомы углерода циклоалканов находятся в sp 3 гибридизации.
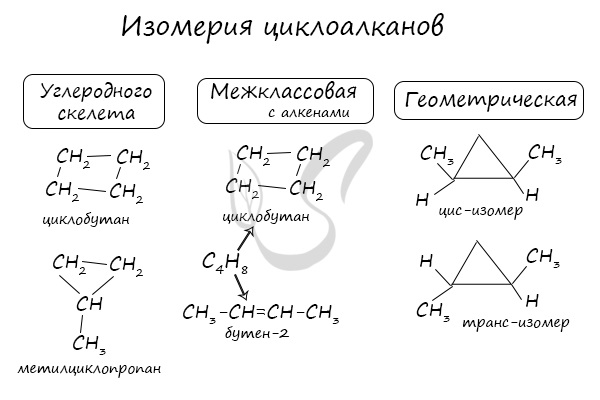
Помимо изомерии углеродного скелета, для циклоалканов характерна межклассовая изомерия с алкенами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
Получение циклоалканов
Циклоалканы можно получить гидрированием (присоединением водорода) бензола и его гомологов.
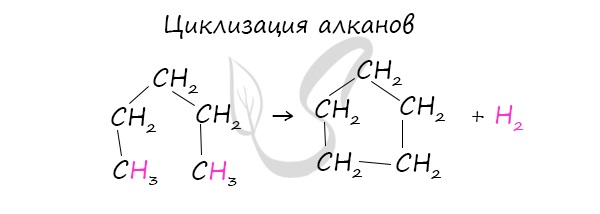
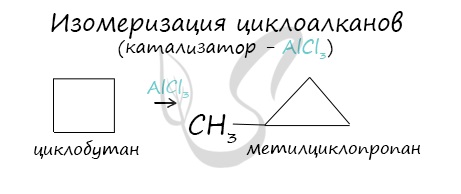
При наличии катализатора и повышенной температуры алканы способны образовывать цикл, отщепляя при этом водород.
Химические свойства циклоалканов
Важно заметить, что циклопропан и циклобутан вступают в реакции присоединения, проявляя свойства ненасыщенных соединений. Для циклопентана и циклогексана реакции присоединения не характерны, они преимущественно вступают в реакции замещения.
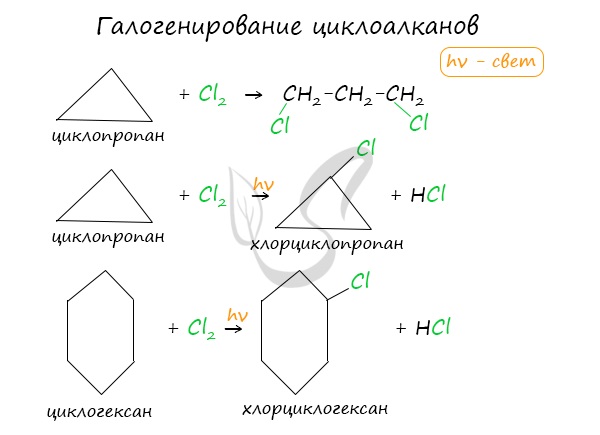
Без освещения реакция циклопропана и циклобутана с хлором идет по типу присоединения. При освещении хлор образует свободные радикалы, реакция идет, как и у алканов, по механизму замещения.
У циклопентана и циклогексана реакция идет только путем замещения.
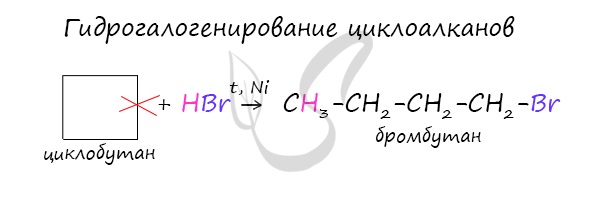
В реакции гидрогалогенирования, протекающие по типу присоединения, вступают циклопропан и циклобутан.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
К какому классу углеводородов относятся циклопропан циклопентан
Циклоалканы, также нафтены, циклоны или циклопарафины – ациклические насыщенные углеводороды, по химическим свойствам близки к п редельным углеводородам. Входят в состав нефти. Циклоалканы открыты В.В. Марковниковым в 1883 году. ( Циклопарафины главным образом находятся в составе некоторых нефтей. Отсюда и другое название циклопарафинов — нафтены )

Прочность связей в циклических соединениях зависит от числа атомов, участвующих в образовании цикла. Она определяется степенью его напряженности, обусловленной изменением валентных углов атомов цикла и отклонением этих атомов от нормального направления.
Для циклопропана межъядерные углы составляют 60º, как в равностороннем треугольнике, для циклобутана – 90º, как в квадрате, а в циклопентане – 108º, как в правильном пятиугольнике. Нормальный валентный угол для атома углерода – 109,5º. Поэтому при расположении в названных соединениях всех атомов углерода в одной плоскости уменьшение валентных углов составляет в циклопропане – 49,5º, в циклобутане – 19,5º, в циклопентане – 1,5º.
Чем больше отклонение валентного угла от нормального, тем более напряжены и, следовательно, непрочны циклы. Однако в отличие от циклопропана циклобутан и циклопентан имеют неплоские циклы. Один из атомов углерода непрерывно выходит из плоскости. Циклобутан существует в виде неплоских «сложенных» конформаций. Циклопентан характеризуется конформацией «конверт».
Для циклогексана, как правильного шестиугольника, межъядерные углы составляют 120º. Если бы молекула циклогексана имела плоское строение, то отклонение от нормального валентного угла атома углерода составляло:109,5º–120º = 10,5º.
Однако циклогексан и большие циклы имеют неплоское строение. В рассматриваемой молекуле циклогексана сохраняются обычные валентные углы при условии его существования в двух конформациях «кресла» и «ванны». Конформация «кресла» менее напряжена, поэтому циклогексан существует преимущественно в виде конформеров I и III, причем цикл претерпевает непрерывную инверсию с промежуточным образованием конформера II:
ось симметрии II III
I
К какому классу углеводородов относятся циклопропан циклопентан
Циклоалканами называют алициклические углеводороды, в которых углеродные атомы, образующие цикл, находятся в sp3-гибридизации.
Циклоалканы классифицируют по величине цикла, числу циклов и способу соединения циклов в молекуле. По величине цикла различают:
В зависимости от числа циклов в молекуле выделяют:
Бициклические циклоалканы по способу соединения циклов подразделяют на 3 группы:
спираны (два кольца имеют один общий атом углерода);
конденсированные (два кольца имеют два общих соседних атома углерода);
мостиковые (два кольца имеют три и более общих атомов углерода).
Названия моноциклических циклоалканов образуют в соответствии с правилами ИЮПАК путем добавления к названию алкана с соответствующим количеством атомов углерода префикса цикло-.
Бициклические циклоалканы называют в зависимости от числа углеродных атомов циклической системы и способа соединения циклов.
Спираны называют путем прибавления префикса спиро- к названию алкана с соответствующим числом атомов углерода. Между префиксом и корнем (названием алкана) в квадратных скобках указывают в порядке возрастания число атомов углерода в каждом из циклов, исключая общий. Нумерацию атомов углерода спирановой системы начинают с меньшего цикла, с углеродного атома, расположенного рядом с общим.
Конденсированные и мостиковые бициклические циклоалканы называют путем прибавления префикса бицикло- к названию алкана с соответствующим числом углеродных атомов. В квадратных скобках между префиксом и названием алкана в порядке убывания указывают число углеродных атомов в каждой из трех цепей, соединенных общими узловыми (третичными) атомами углерода. Нумерацию атомов углерода следует начинать с одного из узловых атомов. В первую очередь нумеруют самую длинную углеродную цепь, затем – более короткую. В мостиковых системах в заключение нумеруют самую короткую углеродную цепь – мостик:
Наряду с систематическими названиями многие бициклические системы имеют тривиальные названия.
Поли циклические соединения содержат более двух циклов, соединенных мостиками. Названия каркасных полициклических углеводородов происходят от эмпирических названий соответствующих геометрических фигур, напоминающих их строение.
Для циклоалканов характерны все виды изомерии. Структурная изомерия циклоалканов обусловлена величиной цикла, природой и взаимным расположением заместителей:
а) изомерия размера цикла;
б) изомерия положения заместителей;
в) изомерия боковых цепей.
Геометрическая изомерия циклоалканов обусловлена различным расположением заместителей относительно плоскости цикла.
Следует учитывать, что циклоалканы, как правило, имеют не плоское (кроме циклопропана), а пространственное строение в виде определенных конформаций.
При рассмотрении геометрических изомеров условно считают строение циклоалканов плоским.
Оптическая изомерия характерна для циклоалканов, молекулы которых не имеют плоскости симметрии.
Циклопропан, циклогексан и их гомологи могут быть выделены в чистом виде из некоторых видов нефти.
Синтетические способы получения циклоалканов
2. Пиролиз кальциевых, бариевых или ториевых солей дикарбоновых кислот. При пиролизе (сухой перегонке) солей дикарбоновых кислот образуются циклические кетоны, которые затем восстанавливают до соответствующих циклоалканов.
Позволяет получить пяти- и шестичленные циклоалканы.
3. Циклоприсоединение. Это процесс соединения двух или более ненасыщенных молекул с образованием продукта циклического строения. В зависимости от числа атомов, принимающих участие в образовании цикла, различают [2+1], [2+2] и [4+2] циклоприсоединение. Например, димеризация алкенов ([2+2] циклоприсоединение) позволяет получить циклобутан и его гомологи.
Реакцию Дильса – Альдера (диеновый синтез) относят к реакциям [4+2] циклоприсоединения.
Реакция широко используется для получения циклогексана и его производных.
Данный способ позволяет получить ненасыщенные алициклические соединения, которые могут быть восстановлены до циклоалканов.
В обычных условиях циклопропан и циклобутан – газы; циклоалканы, содержащие от 5 до 11 атомов углерода в цикле, – жидкости; последующие представители – твердые вещества.
Температуры кипения и плавления циклоалканов выше по сравнению с константами соответствующих алканов. Практически не растворимы в воде.
Циклоалканы представляют собой в определенной степени жесткие структуры.
Для циклоалканов характерны следующие виды напряжений:
1) торсионное (Питцеровское) напряжение – связано со взаимодействием химических связей в заслоненной или частично заслоненной конформациях;
2) напряжение Ван-дер-Ваальса – обусловлено взаимным отталкиванием заместителей при сближении на расстояние, близкое сумме их ван-дер-ваальсовых радиусов;
3) угловое (Байеровское) напряжение – присуще отдельным циклоалканам и связано с отклонением валентных углов между углерод-углеродными связями в цикле от нормального (тетраэдрического) значения.
Теория напряжения циклов была предложена немецким химиком-органиком А. Байером в 1885 г. Согласно этой теории циклоалканы представляют собой плоские многоугольники. Единственным фактором, определяющим прочность цикла, считалось напряжение, вызванное отклонением внутренних валентных углов цикла по сравнению с тетраэдрически м углом.
Если рассматривать форму циклоалканов в виде простых геометрических фигур, имеющих плоское строение, то можно отметить, что при переходе от одного цикла к другому происходит изменение валентного угла.
Чем значительнее отклонение, тем выше угловое напряжение и менее устойчив цикл.
В соответствии с вышеприведенным, трехчленный цикл менее устойчив, чем четырехчленный, а последний – менее устойчив, чем пятичленный. Эти представления подтверждались накопленным к тому времени экспериментальным материалом. Однако для шестичленного цикла экспериментальные данные вступали в противоречия с теорией. Шестичленные циклы (внутренний угол 120°), имеющие значительное отклонение валентных углов от тетраэдрического, оказались устойчивее пятичленных, в которых внутренние углы наиболее близки к тетраэдрическим.
Причиной несоответствия теории Байера с экспериментальным материалом явилось ошибочное представление о плоском строении циклов. В действительности же циклоалканы (исключая циклопропан) не имеют плоского строения.
Пространственное строение циклоалканов определяется разной конформационной подвижностью углеродных атомов, зависящей от числа звеньев в цикле. Молекула любого циклоалкана стремится принять в пространстве такую форму (конформацию), в которой сумма углового, торсионного и ван-дер-ваальсового напряжений была бы минимальной.
Наиболее жесткую структуру имеет циклопропан. В соответствии с правилами геометрии три точки всегда лежат в одной плоскости. Именно поэтому молекула циклопропана имеет плоское строение. Атомы водорода в данной молекуле находятся в заслоненной конформации, что и обуславливает сильное торсионное напряжение. Свободное вращение относительно углерод-углеродных связей невозможно. Внутренние валентные углы в молекуле циклопропана сильно отклонены от тетраэдрического значения, в результате чего и возникает большое угловое напряжение. Искажение валентных углов при sp3-гибридизации орбиталей углеродных атомов должно составлять α =(109°28`-60°):2 = 24 º 44′.
Вследствие взаимного отталкивания электронных облаков углерод-углеродных связей максимальная электронная плотность перекрывающихся орбиталей атомов углерода в молекуле циклопропана расположена не по прямой, соединяющей центры связываемых атомов, а за пределами треугольника молекулы.
Четырехчленный цикл, в отличие от трехчленного, все же обладает незначительной гибкостью. Валентные углы искажены меньше, чем в трехчленном цикле, несколько ниже и угловое напряжение. Один из углеродных атомов циклобутана выходит из плоскости трех атомов на угол 25–30°, что приводит к уменьшению торсионного напряжения цикла.
В пятичленном цикле практически отсутствует угловое напряжение (отклонение внутренних валентных углов от тетраэдрического составляет менее 1º ). Однако в плоском пятичленном цикле связи С–Н находятся в заслонен ной конформации, что обуславливает значительное торсионное напряжение. Каждый из пяти углеродных атомов циклопентана, стремясь уменьшить торсионное напряжение в цикле, поочередно выходит из плоскости, в которой расположены четыре оставшихся атома углерода. Кольцо находится в непрерывном волнообразном движении – псевдовращении. Эта неплоская осциллирующая структура называется конформацией «конверта». В конформации «конверта» угловое напряжение увеличивается, однако это в полной мере компенсируется снижением торсионного напряжения молекулы.
Если представить шестичленный цикл плоским, то его внутренние валентные углы должны быть равными 120°. Это обусловило бы значительное угловое напряжение. Следует отметить, что в плоской
структуре появляются взаимодействия, связанные с заслонением С–Н-связей, то есть торсионное напряжение.
Однако же циклогексан не является плоской структурой и существует без углового напряжения, так как все валентные углы в нем тетраэдрические (109°28′).
Более устойчивой является конформация «кресла», так как лишена торсионного напряжения (все атомы углерода и водорода находятся в заторможенной конформации). В конформации «ванны» происходит заслонение связей, расположенных вдоль двух параллельных боковых сторон молекулы, что обуславливает торсионное напряжение.
В настоящее время с помощью физико-химических методов исследования установлено, что циклогексан может существовать в различных конформациях: «кресло», твист-форма (искаженная ванна), «полукресло», «ванна». Второй по устойчивости является твист-форма.
Она образуется в результате «скручивания» конформации «ванны» в продольном направлении, что уменьшает напряжение в цикле.
В обычных условиях преобладающая часть молекул циклогексана (99,9 %) существует в конформации «кресла». В результате вращения вокруг углерод-углеродных связей одна конформация «кресла» переходит в другую, энергетически равноценную, форму кресла. Такой процесс называют инверсией цикла.
Две конформации «кресла» могут взаимно превращаться как с промежуточным образованием конформации «ванны», твист-конформации, так и без прохождения через конформацию «ванны».
Изучая пространственное строение циклогексана, было установлено, что шесть С–Н связей расположены вдоль оси симметрии молекулы, а другие шесть – под углом 109°28′. Связи, параллельные оси симметрии, называют аксиальными (обозначают символом «а»), а расположенные радиально – называют экваториальными (обозначают символом «е»). Каждый атом углерода имеет одну аксиальную, а другую экваториальную связь С–Н. При инверсии цикла (
100000 раз в секунду при 25 °С) все экваториально связанные атомы водорода становятся аксиальными, а все аксиально связанные – экваториальными. Взаимопревращения в циклогексане протекают настолько быстро, что все атомы водорода циклогексана становятся эквивалентными.
Две конформации «кресла» монозамещенного циклогексана энергетически не равноценны. Более стабильной является конформация с экваториальным положением заместителя. Аксиальное положение заместителя для циклогексана менее выгодно, так как возникает стерическое отталкивание, обусловленное взаимодействием заместителя с аксиально расположенными атомами водорода в положении 3 и 5.
Химические свойства циклоалканов
Для циклоалканов характерны реакции свободнорадикального замещения (SR).
Циклоалканы с малыми циклами проявляют своеобразные химические свойства, связанные с особенностями их строения. Из-за значительного углового и торсионного напряжения трехчленный и, в меньшей степени, четырехчленный циклы являются неустойчивыми. Именно поэтому для циклопропана и циклобутана наряду с реакциями замещения характерны реакции присоединения, сопровождающиеся раскрытием цикла.
Следует отметить, что с бромом циклобутан вступает в реакцию замещения SR.
Представляет интерес реакция присоединения галогеноводородов к алкилзамещенным циклопропана, протекающая в соответствии с правилом Марковникова:
Однако циклобутан не реагирует с галогеноводородами.
Для циклоалканов и их производных характерны реакции сужения и расширения циклов. Данные реакции являются каталитическими и протекают в присутствии кислот Льюиса:
В связи с низкой реакционной способностью и отсутствием функциональных групп идентификация алканов с помощью каких-либо аналитических реакций невозможна. Прежде всего используют физико-химические константы (температуры кипения, плавления; коэффициент преломления, удельное вращение – для оптически активных жидких циклоалканов и др.); определяют процентное содержание углерода и водорода путем сжигания, молекулярную массу и др.; данные физических (инструментальных) методов исследования (ИК-, ПМР-спектроскопии и масс-спектрометрии).
Циклоалканы. Свойства циклоалканов.
Циклоалканы – предельные циклические углеводороды. Простейшие представители:
Строение циклоалканов.
Атомы углерода находятся в sp 3 – гибридизации. Угол зависит от размера цикла.
Изомерия циклоалканов.
Для циклоалканов характерна изомерия углеродного скелета и пространственная изомерия:
Физические свойства циклоалканов.
При обычных условиях:
С17 и выше – твердые вещества.
Температуры плавления и кипения выше, чем у алканов.
Получение циклоалканов.
1. Отщепление 2х атомов галогена от дигалогенов:
2. Гидрирование ароматических углеводородов:
Химические свойства циклоалканов.
Малые и обычные циклы имеют различные свойства. Например, для циклобутана и циклопропана свойственна реакция присоединения:
Б) водорода (в присутствие никелевого катализатора):
В) галогенводорода (по правилу Марковникова):
Реакция замещения свойственна для обычных циклов, т.к. они более устойчивы:
Под воздействием окислителей образуется кислота:
Применение циклоалканов.
Циклоалканы используют для получения циклогексанола, циклогексанона, адипиновой кислоты, капролактама, а также в качестве растворителя. Циклопропан выступает в качестве ингаляционного средства.