ДНЕВНОЙ СТАЦИОНАР ЛЕКАРСТВЕННОГО ЛЕЧЕНИЯ ОПУХОЛЕЙ МНИОИ ИМЕНИ П.А. ГЕРЦЕНА
Комфортно и оперативно
Пациенты из любого региона России, ближнего и дальнего зарубежья
Дневной стационар является структурным подразделением Отдела лекарственного лечения опухолей МНИОИ имени П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России и размещается в здании поликлиники по адресу: Москва, улица Погодинская, д.6 стр. 1
Феденко Александр Александрович
д.м.н., онколог, заведующий отделом лекарственного лечения опухолей
Записаться к врачу
Оставьте заявку и ожидайте консультацию нашего специалиста
Коломейцева Алина Андреевна
к.м.н., онколог, заведующая дневным стационаром лекарственного лечения опухолей
Записаться к врачу
Оставьте заявку и ожидайте консультацию нашего специалиста
ОСНОВНЫЕ НАПРАВЛЕНИЯ ДЕЯТЕЛЬНОСТИ ОТДЕЛЕНИЯ
ЛЕКАРСТВЕННОЕ ЛЕЧЕНИЕ
Мощность дневного стационара составляет 32 койки, что позволяет проводить лекарственную терапию 50-60 пациентам ежедневно. В дневном стационаре ежемесячно лекарственное лечение получают 450-500 пациентов. Отделение оснащено современным высокотехнологичным оборудованием для проведения как краткосрочных введений, так и длительных инфузий противоопухолевых препаратов. Тактика ведения пациентов основывается на современных международных стандартах диагностики и лечения злокачественных новообразований. Принятие решения о выборе тактики лечения в каждом конкретном случае осуществляется мультидисциплинарной командой специалистов на совместных консилиумах.
На базе дневного стационара проводится лекарственная терапия цитостатическими препаратами, гормональная терапия, таргетная терапия, направленная прицельно на блокирование в опухоли определенной молекулярной мишени, индуцирующей опухолевый рост, иммунотерапия ингибиторами иммунных контрольных точек, реактивирующих противоопухолевый иммунный ответ. В зависимости от конкретной клинической ситуации лекарственная терапия используется как самостоятельный метод лечения, так и в составе комплексного и комбинированного лечения.
ПРОГРАММЫ ЛЕЧЕНИЯ
Что значит bdr в дневном стационаре в онкологии
Доктор Питер
Кому и когда нужна амбулаторная онкология
Можно ли без отрыва от дома лечиться в онкологическом стационаре? Борис Каспаров, к.м.н., заведующий Клинико-диагностическим отделением НМИЦ онкологии им. Н.Н. Петрова, рассказал «Доктору Питеру» о том, как стационар-замещающие технологии могут облегчить жизнь пациентам.
— Борис Сергеевич, под словосочетанием «амбулаторная онкология» мы подразумеваем помощь пациентам с установленным диагнозом в районной поликлинике. Как и зачем амбулаторная помощь оказывается в стационаре?
И лечиться можно в условиях, когда пациент живет дома, но регулярно посещает клинику. Большинство исследований и даже процедур, назначенных врачом, можно сделать амбулаторно.
Есть еще одна важная часть амбулаторной помощи — паллиативная: когда человека уже нельзя вылечить, ему необходимо создать условия, в которых он без страданий проживет оставшуюся часть жизни.
— Но ведь такие пациенты чаще всего лежат в клинике?
— Что нужно, чтобы лечение, которое раньше проводилось только в стационаре, теперь могло быть доступно амбулаторно?
— Есть такое понятие «стационар-замещающие технологии». Они позволяют делать то, что раньше делалось в стационаре, амбулаторно. Например, у нас есть целое отделение малой хирургии, где мы проводим процедуры, которые не требуют круглосуточного наблюдения медперсонала: малые гинекологические вмешательства, иссечения в онкодерматологии. Кроме хирургических вмешательств, есть много других процедур: фотодинамическая терапия новообразований кожи (вводится фотосенсибилизирующий химиопрепарат, в разы усиливающий воздействие света, который «убивает» раковые клетки), криодеструкция (охлаждение тканей до предельно низких температур). Есть новообразования, которые невозможно прооперировать, но можно уменьшить их криодеструкцией и таким образом снять боль.
У нас есть пациенты, которые даже не говорят родственникам, что болеют и проходят химиотерапию, — ничего не заметно благодаря использованию параллельно с химиотерапией холодовых шлемов для профилактики аллопеции (выпадения волос).
В амбулаторных условиях можно выполнять и химиотерапию — так называемую краткосрочную.
— Считается, что в Петербурге есть где лечиться, но нет клиник, где можно реабилитироваться после лечения. Точнее, есть, но их всего две…
— Третья — у нас, в НМИЦ онкологии. У нас есть целое амбулаторное отделение, где мы занимаемся реабилитацией пациентов после хирургических операций, после лучевой терапии, корректируем лимфедему (лимфатический отек руки) после хирургического лечения рака молочной железы, недержание — после вмешательств на органах малого таза, и так далее.
— Все же получается, что амбулаторная онкология нужна прежде всего тем, кто уже прошел полноценный курс лечения. Тем временем к вам приезжают люди, которым даже окончательный диагноз еще не установили.
— С одной стороны, НМИЦ онкологии им. Петрова — учреждение четвёртого уровня, то есть должен оказывать высокотехнологичную помощь. В идеале это означает, что мы должны заниматься только теми, кому не могут помочь на первых трех уровнях. Первый уровень — терапевт, он что-то заподозрил и послал человека к районному онкологу. Тот делает то, что нужно на своем уровне: назначает специальные исследования. Дальше, если диагноз поставлен или нужно его уточнить, человек направляется в онкодиспансер, там его диагностируют, определяют тактику лечения и, собственно, лечат — хирургия, химиотерапия или лучевая терапия (или все сразу). А вот если пациенту требуется что-то более сложное, чего в онкодиспансере нет, — тогда его направляют к нам. В этом случае пациент уже обследован, диагноз поставлен, определены вопросы и запросы — понятно, что хотят от нас получить.
Но это идеальная ситуация — так должно быть. В жизни в 99% случаях из регионов пациенты приезжают к нам частично или вообще не обследованные. Со снимком МРТ сомнительного качества, на котором «что-то нашли». Иногда приезжают те, кого ни диагностика, ни лечение, которые доступны в регионе, никак не устраивают ни по срокам, ни по качеству. В регионах МРТ или ПЭТ-КТ можно ждать месяцами, а человек с подозрением на онкологическое заболевание не может ждать так долго. Так и получается, что к нам идут делать «сразу всё»: и диагностироваться, и лечиться.
— Нам обещают, что когда заработает национальная программа «онкология», специализированная эффективная помощь будет доступна в любом уголке страны. Если МРТ и ПЭТ-КТ можно купить, то где взять специалистов?
— Национальный медицинский исследовательский центр должен не только лечить, но и учить. Регулярно ездим с циклами лекций по Северо-Западу (были уже в Вологде, Архангельске), готовимся к выездам в Южный и Северо-Кавказский федеральные округа. Наш цикл будет постоянно обновляться. Мы будем стараться сделать всё, чтобы и в регионах качественная и своевременная помощь стала доступной.
Уже сейчас готовимся к научно-практической конференции по амбулаторной онкологии, которая состоится в следующем ноябре в Петербурге. Будет небольшой лекционный цикл, от лидеров мнений, которые специализируются на амбулаторной химиотерапии, на стационар-замещающих технологиях, на лечении сопутствующих заболеваний. Будут циклы по реабилитации.
Лекарственная терапия
С помощью лекарств сегодня лечат большинство опухолей. Это самый универсальный и самый распространенный метод лечения рака в силу его особенностей:
Виды лекарственной терапии
С развитием нанотехнологий, молекулярной медицины и генной инженерии в портфеле онкологов появились множество новых противоопухолевых препаратов, лекарства стали более избирательными к злокачественным клеткам и менее токсичными для здоровых тканей и организма в целом. Появились прицельные лекарства, так называемые таргетированные, молекулы которых воздействуют более избирательно на клетки рака.
Все лекарства против рака по механизму действия делят на цитостатические и цитотоксические. Первые, цитостатические, тормозят размножение злокачественных клеток и вызывают их апоптоз, или программу самоуничтожения, клеточный распад. Вторые, цитотоксические, препараты вызывают гибель клеток вследствие их интоксикации, разрушения оболочки и ядра клетки, других структур, и в конечном итоге некроз опухоли.
Учитывая разные механизмы действия, в большинстве случаев онкологи подбирают комбинацию из двух-трех препаратов разных фармакологических групп.
К лекарственному лечению онкологических заболеваний относят:
Лекарственное лечение обычно проводится курсами. Курс включает время введения препарата (от 1 до 5 дней для внутривенных препаратов, может быть дольше для таблетированных препаратов) и время перерыва для восстановления организма и снижения риска побочных эффектов лечения. Перед началом каждого нового курса обычно производится контроль анализов крови и консультация врача онколога для решения вопроса о необходимости корректировки доз препаратов и/или увеличения интервала до следующего введения препарата.
Для длительного лекарственного лечения есть понятие «линий» лечения. «Линия» лечения – последовательное назначение одинаковых курсов химио- (или других видов) терапии. «Линия» лечения проводится до достижения необходимого эффекта или до момента потери чувствительности со стороны болезни. Если опухоль продолжила расти на фоне одной схемы химиотерапии – производится смена лекарств. Продолжение лечения с использованием новой схемы химиотерапии называется «Второй (третьей, четвёртой и т.д.) линией» лечения.
Химиотерапия
Химиотерапия – наиболее распространённый вид лекарственной терапии. Химиотерапия бывает:
1. Лечебной – когда химиотерапия является основным методом лечения заболевания. Например, для многих пациентов с лейкозами, лимфомами, герминогенными опухолями яичка химиотерапия может быть основным методом лечения, который часто приводит к выздоровлению. Для большинства пациентов с распространёнными формами рака, с метастазами в различные органы, химиотерапия является основным методом лечения, дающим максимальную возможность длительно сдерживать болезнь.
2. Неоадъювантной – когда химиотерапия предшествует основному методу лечения. Чаще всего такая химиотерапия назначается перед некоторыми видами операций, с целью уменьшения опухоли и снижения активности её клеток.
3. Адъювантной – её ещё называют «профилактической». Она назначается после основного метода лечения, чаще всего после операции, с целью снижения риска возврата болезни.
К наиболее распространённым противоопухолевым препаратам относят следующие группы:
1. Алкилирующие антинеопластические препараты.
2. Алкилирующие триазины.
Неклассические алкилирующие агенты, пролекарства, которые для проявления своей противоопухолевой активности должны пройти ряд метаболических превращений в организме, в результате которых образуются метилирующие агенты. Последние, внедряясь в ДНК и РНК раковой клетки, не позволяют ей дальше делиться.
3. Антиметаболиты.
Конкурентно вмешиваются в процесс деления клетки, вызывая ее апоптоз.
4. Антрациклиновые антибиотики.
Механизм их действия основан на цитотоксическом действии. Они ингибируют синтез ДНК, нарушают проницаемость клеточных мембран и другие механизмы жизнедеятельности клеток.
5. Ингибиторы топоизомеразы I и топоизомеразы II, ингибиторы образования микротубул и ингибиторы веретена деления.
Цитостатические препараты, избирательно нарушающие структуру ДНК и деление раковых клеток на разных этапах.
Химиопрепараты в большинстве случаев вводятся внутривенно или перорально, тогда они оказывают системное воздействие на весь организм. Но могут быть использованы и местно, например, во время хирургической операции для обработки операционного поля, или регионарно, например, в желудочки головного мозга.
Гормональная терапия
Показана только для гормоночувствительных видов рака. Будет ли опухоль реагировать на лечение гормонами или нет, определят с помощью специальных анализов и лабораторных исследований клеточного материала, взятого из опухоли.
Опухоли, реагирующие на гормоны, часто обнаруживают в репродуктивной системе и железах внутренней секреции, например, это:
На поздних неоперабельных стадиях опухолей, чувствительных к данному лечению, гормональная терапия может использоваться в качестве основного лечения. Как паллиативное лечение некоторых видов рака она достаточно эффективна и может продлить жизнь пациента на 3-5 лет.
Иммунотерапия
Иммунитет играет важную роль в профилактике и борьбе с раком. В норме иммунные тельца распознают атипичную клетку и убивают ее, защищая организм от развития опухоли. Но когда иммунитет нарушается в силу разных причин, и раковых клеток становится много, тогда опухоль начинает расти.
Иммунотерапия при раке помогает организму справится с заболеванием за счет активизации защитных ресурсов и не допустить развития повторных опухолей и метастазов. В онкологии используют интерфероны, вакцины от рака, интерлейкины, колониестимулирующие факторы и другие иммунные препараты.
Лечение подбирает иммунолог на основе лабораторных данных о состоянии иммунной системы онкопациента совместно с лечащим врачом-онкологом и другими специалистами, участвующими в лечении конкретного пациента.
Основные механизмы иммунотерапии:
Таргетная терапия
Таргетные лекарства очень специфичны и разрабатываются под конкретный мутировавший ген раковой клетки данного вида опухоли. Поэтому до таргетного лечения обязательно проводят генетическое исследование материала, взятого на биопсию.
Например, разработаны эффективные таргетные препараты для лечения различных генетических форм рака молочной железы, множественной миеломы, лимфомы, рака предстательной железы, меланомы.
В силу своей специфики и целевого попадания на раковую клетку-мишень таргетные препараты более эффективны для лечения опухолей, чем например, классические противоопухолевые. И менее вредны для нормальных клеток, не обладающими характеристиками опухолевых. Многие таргетные методы относят к иммунотерапии, так как по сути они формируют нужный иммунный ответ.
Фотодинамическая терапия
Осуществляется препаратами, воздействуя световым потоком определённой длины волны на раковые клетки и разрушая их.
Побочные эффекты лекарственного лечения рака
Выраженные осложнения наблюдаются далеко не у всех пациентов, но риск их возрастает с увеличением продолжительности лечения.
Часто встречаются следующие побочные эффекты после проведения лекарственной терапии:
Большинство осложнений поддаётся корректировке, при правильном проведении лечения многие из них можно предотвратить или остановить при первом проявлении. Тяжёлые осложнения могут быть причиной увеличения интервалов между курсами химиотерапии.
Эффективность
Чем раньше обнаружен рак и точнее диагностирован тип опухолевых клеток, тем успешнее лечение рака и благоприятнее прогноз выздоровления. Поэтому следует постоянно следить за состоянием своего здоровья, проходить диагностические исследования согласно возрасту, не закрывать глаза на недомогание или периодический дискомфорт в теле. Также лучше не тратить время на попытки вылечиться самостоятельно или при помощи нетрадиционной медицины, не имеющей никаких убедительных данных об эффективности, игнорируя современные методы медицинского лечения. Так можно только запустить онкологический процесс, усугубить стадию заболевания и затруднить последующее лечение. Не теряйте драгоценное время, обследуйтесь в специализированных центрах на современном оборудовании у высококвалифицированных врачей.
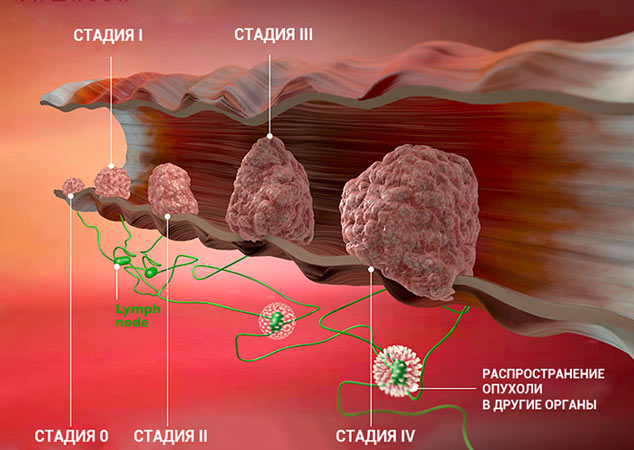
Стадии рака
Все опухоли (или, на языке врачей — новообразования) делят на две большие группы: доброкачественные и злокачественные. Первые обычно не опасны для жизни, а вторые, если человек не получает лечения, приводят к гибели. В 2015 году от рака во всем мире умерло почти 9 миллионов человек.
Фатальность злокачественных опухолей связана с двумя их главными свойствами, которые, собственно, и отличают их от доброкачественных новообразований:
Для врача важно понимать, насколько сильно рак успел распространиться в организме пациента. Ведь от этого зависит лечение и прогноз. Для того чтобы упростить эту задачу и внести четкость, в течении каждого онкологического заболевания принято выделять определенные стадии.
Классификация TNM
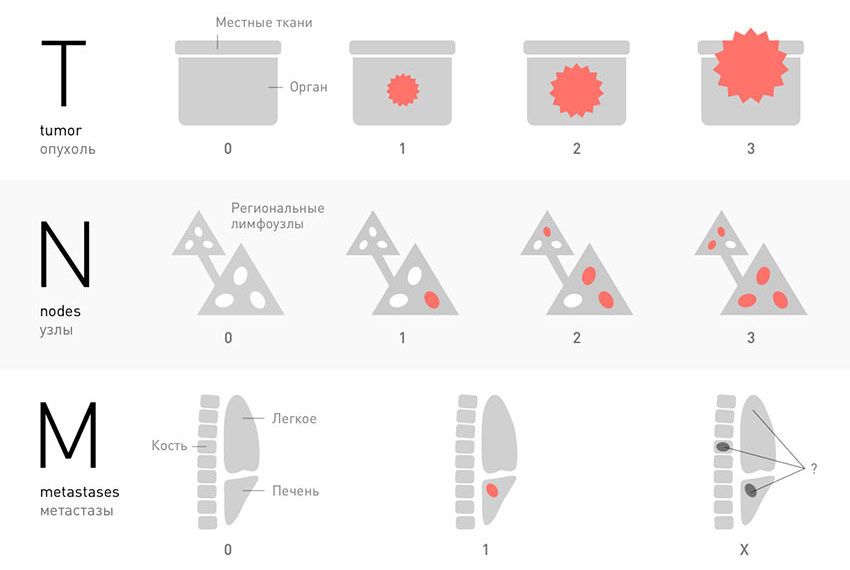
В большинстве случаев, для того чтобы установить стадию рака, ориентируются на три характеристики злокачественной опухоли, которые соответствуют трем буквам аббревиатуры TNM. К каждой букве приписывают индекс в виде цифры или специального обозначения.
T — tumor. Эта буква обозначает первичную опухоль, ее размеры, прорастание в стенку органа, соседние ткани:
N — nodus. Когда раковые клетки отрываются от первичной опухоли и мигрируют с током лимфы, в первую очередь они попадают в близлежащие (регионарные) лимфатические узлы. Можно сказать, что это первые баррикады на пути распространения рака в организме. В зависимости от того, обнаружены ли опухолевые клетки в регионарных лимфатических узлах, N может принимать значения:
M — metastasis. Эта буква показывает, обнаружены ли в теле больного отдаленные метастазы — вторичные очаги в различных органах:
Классификация TNM применима для большинства видов рака. Она позволяет очень подробно описывать злокачественные опухоли. В пределах основных групп выделяют подгруппы, их обозначают с помощью букв, например: T1a, T1b, T1c.
Однако, зачастую система TNM оказывается слишком громоздкой и не совсем удобной. Существует ее упрощенный вариант, когда возможные сочетания значений T, N и M сводят к пяти стадиям.
Стадии злокачественной опухоли
Часто онкологи обозначают стадию рака римской цифрой от I до IV. Эта классификация основана на TNM, но она проще и зачастую удобнее:
Это очень приблизительное описание стадий. Деление зависит от типа рака, от того, в каком органе он находится. Для того чтобы обозначить подстадию, к букве приписывают цифру. Например, стадия I может делиться на подстадии IA и IB.
Сторожевой лимфатический узел
Когда хирург оперирует онкологического пациента, зачастую ему приходится решать сложную задачу: стоит ли удалять регионарные лимфатические узлы? Если в них есть раковые клетки, и они будут оставлены в организме больного, произойдет рецидив. Если же удалить «чистые» лимфоузлы, это чревато осложнением в виде лимфедемы — отека на руке или ноге из-за нарушения оттока лимфы.
Раньше врачи нередко предпочитали меньшее из зол и удаляли лимфатические узлы «на всякий случай». Современные хирурги уже не действуют вслепую и могут более точно определить показания к лимфодиссекции. Это стало возможно благодаря появлению сентинель-биопсии или биопсии сторожевого лимфатического узла.
Сторожевым называется лимфатический узел (или группа лимфатических узлов), который первым принимает лимфу, оттекающую от злокачественной опухоли. Его можно обнаружить во время операции: для этого нужно ввести в опухоль флуоресцентный краситель или препарат с радиоактивной меткой. Препарат проникает в лимфатические сосуды, затем в сигнальный лимфоузел и «прокрашивает» его. Лимфатический узел удаляют и проверяют, нет ли в нем раковых клеток.
Для обозначения состояния сигнального лимфоузла используют специальную классификацию:
Если в сигнальном лимфоузле обнаружена опухолевая ткань — это показание к удалению регионарных лимфоузлов.
Степень злокачественности
Злокачественность и степень дифференцировки — два показателя, которые тесно взаимосвязаны. Они описывают внешний вид раковых клеток под микроскопом. Степень дифференцировки показывает, насколько раковая клетка отличается от здоровой. Если она высокая — опухолевая ткань похожа на здоровую. Низкодифференцированные раковые клетки полностью теряют сходство с нормальными.
Чем ниже степень дифференцировки и выше злокачественность, тем агрессивнее ведет себя рак и быстрее распространяется в организме. Для оценки используют гистологическую классификацию:
Шкала Глисона при раке простаты
Для того чтобы оценить степень злокачественности и агрессивности рака предстательной железы, используют шкалу Глисона, разработанную в 1960-х годах. В зависимости от того, как опухолевая ткань выглядит под микроскопом, ей присваивают оценку от 1 до 5. Чем ниже оценка, тем более высокодифференцированными и менее злокачественными являются клетки. Патологоанатом должен выявить два преобладающих типа ткани и выставить две оценки. Итоговая сумма баллов может колебаться от 2 до 10. Чем она больше, тем агрессивнее ведет себя опухоль, и выше риски.
Классификации рака печени
Классификация TNM не очень хорошо отражает течение злокачественных опухолей печени, поэтому в разных странах были созданы специальные классификации печеночно-клеточного рака. Например, многие врачи используют Барселонскую клиническую классификацию. В ее рамках выделяют следующие стадии рака печени:
В некоторых странах практикуется классификация итальянской программы по изучению рака печени (CLIP). В ней учитывается четыре фактора: состояние функции печени, распространение опухолевых очагов (больше или меньше половины печени), уровень альфа-фетопротеина (опухолевый маркер) и наличие тромбоза портальной вены. По каждому показателю врач выставляет оценку 0, 1 или 2 балла. Выживаемость пациентов зависит от суммы баллов:
В соответствии с системой CLIP, всех больных печеночно-клеточным раком можно поделить на две группы: 0–2 балла — значительно более благоприятный прогноз; более 2 баллов — значительно менее благоприятный прогноз.
В 1985 году была предложена классификация Okuda, в которой учитываются: степень поражения печени, наличие асцита (скопления жидкости в брюшной полости), изменение уровня альбумина и билирубина в крови. В соответствии с классификацией Okuda, выделяют три стадии рака печени:
Почему важно установить стадию злокачественной опухоли?
Знание стадии рака по TNM и другим системам помогает онкологу решать важные задачи:
Единые классификации помогают врачам из разных клиник и стран «разговаривать на одном языке». Видя стадию опухоли, диагностированную в другой клинике, онколог четко понимает, что это значит, и как дальше работать с пациентом.
Наблюдение после лечения
Пациенты, пережившие рак, подлежат тщательному наблюдению у специалиста-онколога как минимум первые 5 лет. Динамическое отслеживание состояния здоровья преследует две цели:
График визитов к врачу и набор диагностических исследований будет зависеть в первую очередь от стадии, на которой был обнаружен рак, а также его патоморфологии и локализации.
Чем выше стадия, тем чаще и более тщательно нужно проходить обследование. Так при I и II стадиях онкозаболевания обычно достаточно динамического наблюдения у онколога с примерным графиком визитов каждые 6 мес яцев в первые 5 лет и затем раз в год. При III и IV стадиях визиты к врачу в первые 2-3 года происходят раз в 3-4 месяца, а при назначении так называемой адъювантной терапии, которая предполагает курсы профилактической химиотерапии или других видов лечения, они становятся регулярными.
Минимальный набор для регулярного обследования пролеченного онкопациента, как правило, включает:
После получения результатов обследования, врач принимает следующие тактики ведения пациента:
Будьте бдительны к общим симптомам болезни: потере в весе, снижению аппетита, общей слабости, головной боли, необоснованному повышению температуры. А если заметили боль в области живота или в костях скелета, кашель, одышку, увеличение лимфатических желез и наличие крови в моче не откладывайте визит к врачу. Любое отклонение в вашем здоровье имеет значение. Лучше опровергнуть подозрение, чем пропустить болезнь.