Транскраниальное УЗИ черной субстанции при болезни Паркинсона.
Обращаем Ваше внимание на то, что в соответствии с п. 10.ст.16 Федерального Закона «Об обязательном медицинском страховании» №326-ФЗ от 29.11.2010 года, при каждом обращении за медицинской помощью в ОКДЦ, вы должны предъявить свой полис ОМС в регистратуре центра.
Как узнать результаты исследований?
Уважаемые пациенты!
В приемном отделении ОКДЦ с 8.00 до 15.00 работает процедурный кабинет, где по назначению врача, на платной основе выполняются инъекции, включая:
-внутривенно-капельную инфузию,
-внутривенно-струйную инъекцию,
-внутримышечную инъекцию,
— подкожную инъекцию,
-премедикацию (обезболивание) перед проведением исследований МРТ. СКТ, коронарографии, ФГДС, ФКС и бронхоскопии.
Если Вы хотите получить эту медицинскую услугу, Вам необходимо обратиться в регистратуру ОКДЦ, имея при себе заключение Вашего лечащего врача и его рекомендации.
Уважаемые пациенты!
Запись на повторный прием проводится только через телефон Вашего лечащего врача ОКДЦ, информация об этом имеется в маршрутном листе.
На первичный прием Вы можете записаться самостоятельно через сайт или единый телефон Call-центра 8(863) 227-00-00
Уважаемые пациенты!
С целью предупреждения распространения вирусных инфекций, таких как грипп, ОРВИ, новый коронавирус 2019-nCoV, а так же ввиду отсутствия в ГАУ РО «ОКДЦ» врача-инфекциониста, пациентам с температурой, насморком, чиханием, кашлем, головной болью, болью в горле, рекомендовано обращаться к врачу-инфекционисту либо врачу-терапевту в медицинскую организацию по месту жительства.
Ультразвуковая диагностика- черной субстанции головного мозга
Сложность дифференциальной диагностики БП (особенно в дебюте болезни), а также необходимость диагностики доклинических стадий требуют поиска информативных инструментальных методов исследования. В последние годы в этой связи все больше внимания уделяется ультразвуковому исследованию (УЗ) структур головного мозга — транскраниальной сонографии (ТКС).
Сонографические характеристики черной субстанции подтверждают клинико-патогенетическую гетерогенность болезни Паркинсона.
Поздняя форма заболевания характеризуется особенно высокой частотой феномена гиперэхогенности черной субстанции (98%) и независимостью этого маркера по отношению к клиническим характеристикам. При раннем паркинсонизме феномен гиперэхогенности черной субстанции встречается реже (80%), а площадь гиперэхогенной зоны коррелирует с параметрами прогрессирования заболевания.
Гиперэхогенность черной субстанции может рассматриваться как важный маркер болезни Паркинсона, помогающий совместно с некоторыми другими лабораторно-инструментальными признаками выделять группу риска развития заболевания.
Дифференциально-диагностические возможности ТКС основываются на сопоставлении таких сонографических феноменов, как площадь гиперэхогенного сигнала в области черной субстанции (в норме В диагностический алгоритм болезни Паркинсона следует включать применение транскраниальной сонографии в качестве информативного, доступного и неинвазивного инструментального метода исследования.
Транскраниальная сонография черной субстанции (уникальная методика)
Черной субстанцией называется область среднего мозга, отвечающая за регуляцию движений. Наш центр одним из первых в РФ внедрил методику оценки изменения эхогенности ультразвукового сигнала от чёрной субстанции у пациентов с экстрапирамидными заболеваниями и, в частности, при болезни Паркинсона. Выявляемый феномен «гиперэхогенности» ножек среднего мозга является общепризнанным в мире биомаркером, характерным для болезни Паркинсона, который помогает неврологу поставить диагноз. Необходимо понимать, что данный признак не является 100% для болезни Паркинсона, поэтому окончательное заключение делает врач на основании всей информации о пациенте. Накопленный многолетний опыт (около 20 лет) изложен в уникальной монографии «Транскраниальная сонография при экстрапирамидных заболеваниях» и учебном пособии «Ультразвуковое исследование структур головного мозга при экстрапирамидной патологии».
*Показания к проведению исследования определяются неврологом!
Что исследуется?
Оценивается эхогенность сигнала от черной субстанции, размеры третьего и боковых желудочков головного мозга.
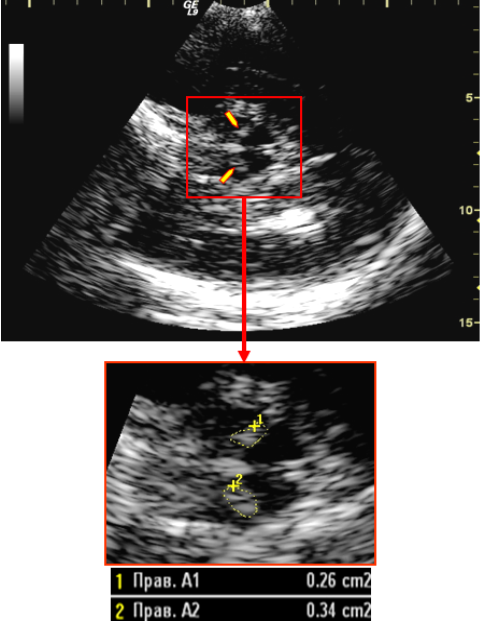
Подготовка
Специальной подготовки не требуется.
Обращаем внимание, что у 10-20% людей, особенно у лиц пожилого возраста, исследование провести невозможно из-за отсутствия ультразвуковых окон, поэтому сначала проводится исследование, а затем осуществляется оплата.
Что такое ботулинотерапия?
Ботулинотерапия – это современный метод лечение различных заболеваний и синдромов с помощью местных инъекций препаратов ботулинического токсина.
Ботулинический токсин – “загадочная молекула 20 века”, препарат 21 века, доказавший свою высокую клиническую эффективность и успешно использующийся практически во всех областях медицины, а не только косметологии, как это принято считать.
Особенно широкие показания к лечению ботулотоксином в неврологии. К ним относятся:
Механизм действия
Механизм действия ботулотоксина обусловлен временным блокированием нервно-мышечной передачи, в результате чего мышца, в которую введен препарат, расслабляется. В первые 30 минут после введения препарата в мышцу токсин связывается, но эффект начинает ощущаться, в зависимости от заболевания, к концу первой недели. Локальное действие токсина обратимое, что одновременно является и преимуществом, и недостатком метода. Полностью способность мышцы сокращаться возобновляется в среднем через 3-4 месяца, после чего инъекцию можно повторить. Также к преимуществам метода относится его безопасность, хорошая переносимость, минимальное количество побочных эффектов и противопоказаний (гемофилия, миастения, синдром Ламберта-Итона, беременность, лактация, воспалительный процесс в месте предполагаемой инъекции, острое заболевание или обострение хронического заболевания)
Выбор области инъекций, дозировка препарата и периодичность введения зависит от того, какие мышцы выбраны мишенями, выраженности проявлений заболевания, а также индивидуальных особенностей анатомии человека. В какие именно мышцы вводить препарат специалист решает только после осмотра пациента. Перед проведением инъекций совместно с пациентом необходимо четко определить реалистичную, достижимую, индивидуальную цель лечения.
Инъекции ботулотоксина проводит врач-невролог, владеющий методом ботулинотерапии, в кабинетах, оснащенных необходимым оборудованием для проведения инъекций.
Перед проведением инъекции пациент подписывает информированное согласие – добровольное подтверждение пациентом его согласия на лечение, после того, как был ознакомлен со всеми аспектами терапии.
Точность инъекции, особенно в мелкие мышцы, имеет решающее значение. Для этого используются различные методы контроля: электромиография, электростимуляция, УЗИ или другие методы визуализации (МРТ, КТ). Эти методы позволяют точнее идентифицировать мышцы-мишени, четко локализовать даже мелкие и труднодоступные мышцы, что позволяет достичь наилучшего клинического эффекта. Чаще всего инъекции проводятся под контролем электромиографии. Для этого инъекция проводится специальной иглой, являющейся одновременно электродом и инъекционной иглой, подключающейся к электромиографу. Поэтому при необходимости повторных инъекций ботулотоксина мы настоятельно рекомендуем приобретать индивидуальную многоразовую иглу. Альтернативой является УЗИ-контроль, преимуществом которого заключается в том, что это неинвазивный метод, который позволяет в режиме реального времени визуализировать саму мышцу, окружающие сосуды и нервы, а также контролировать непосредственное введение препарата.
В период действия препарата противопоказан прием антибиотиков группы аминогликозидов, эритромицина, тетрациклина, полимиксинов, курареподобных миорелаксанов. Рекомендуется также избегать приема алкоголя и воздействия высоких температур на область инъекции в течение первых двух недель из-за возможного ослабления эффекта.
Что такое танцевальная терапия?
Пациенты с болезнью Паркинсона часто страдают от проблем с началом движений, «застываний» и постепенного ухудшения состояния. Тремо представляет собой еще одну причину возможной изоляции пациента, депрессии и нежелания выходить на улицу, что приводит к значительному ухудшению качества жизни. Танцы для больных Паркинсоном – это один из тех методов, который может использоваться с целью реабилитации, восстановления и поддержки общего состояния здоровья. Танцы помогают чувствовать себя лучше пациентам с болезнью Паркинсона.
Стоит также отметить, что именно танцы для больных Паркинсоном могут отвлечь их и от самой болезни. Известный факт, когда пациент думает о своей болезни часто и преимущественно в негативном контексте, его состояние ухудшается гораздо стремительнее, чем тех пациентов, которые относятся к жизни с любовью и позитивом. Всплеск положительных эмоций, которые испытываются в процессе танцевальных занятий, отражается и на внутреннем состоянии пациентов с болезнью Паркинсона.
Танец – это движение, а Движение – ЖИЗНЬ!
Занятия должны проводить инструкторы с медицинским образованием. Перед началом занятий необходима консультация специалиста.
Что такое комплекс Блетона?
Цервикальная дистония – это локальная форма мышечной дистонии, которая характеризуется непроизвольными движениями мышц шеи с формированием патологических поз головы и шеи.
Огромным дополнением к лечению цервикальной дистонии инъекциями ботулинического токсина является специальный кинезиотерапевтический комплекс для цервикальной дистонии, который был предложен французским физиотерапевтом Ж. П. Блетоном.
Основные цели этого метода: путем активации здоровых мышц и растягивания дистонических, поддержать гибкость позвоночника в области шеи, уменьшить интенсивность спазмов, достигнуть самоконтроля положения шеи, уменьшить болевой синдром.
Классически реабилитационная программа включает следующие шаги: уменьшение патологических движений с помощью специальных методов релаксации; усиление корригирующих мышц приведением головы в противоположную от кривошеи сторону; точная и продуманная активация корригирующих мышц; замена спазма произвольными и компенсаторными движениями головы.
Упражнения индивидуальны и преподаются во время одной или двух сессий физиотерапии в неделю. После обучения пациентам рекомендуется продолжать интенсивные занятия самостоятельно, так же рекомендуется исправлять патологическую позу постоянно, организуя повседневную и рабочую деятельность таким образом, чтобы держать голову на стороне противоположной патологической позе.
Результатом лечебной физкультуры по методу Ж.П. Блетона является в первую очередь улучшение качества жизни пациента, улучшение постурального контроля, снижение флюктуации симптомов в период между инъекциями, удлиннение межинъекционного периода.
Транскраниальное ультразвуковое сканирование мозга при болезни Паркинсона
Опубликовано в журнале:
Визуализация в клинике »» N17, Декабрь 2000 TRANSCRANIAL ULTRASOUND SCANNING OF THE BRAIN IN PARKINSON’S DISEASE
А.О. Чечеткин
Chechetkin A.О.
Научно-исследовательский институт неврологии РАМН, Москва
Research Institute of Neurology, Russian Academy of Medical Sciences, Moscow
В обзоре дана оценка возможностей транскраниального ультразвукового сканирования (ТКУС) в выявлении структурных изменений головного мозга при болезни Паркинсона (БП). Показано, что у большинства больных БП выявляют повышение эхогенности ткани мозга в области черной субстанции (ЧС), а также расширение третьего желудочка. Однако наличие гиперэхогенного ультразвукового сигнала от области ЧС и размер его площади не являются специфическими признаками заболевания, так как схожие изменения выявлены и у лиц без клинических признаков БП. Роль ТКУС в диагностике БП остается неясной. Проведение дальнейших исследований с верификацией полученных ультразвуковых данных с помощью позитронно-эмиссионной томографии, возможно, поможет решить эту задачу.
The potentialities of transcranial ultrasound scanning (TCUS) in identification of structural changes of the brain in patients presenting with Parkinson’s disease (PD) are reviewed. It is demonstrated that the majority of PD patients show an increase of brain tissue echogenicity in the area of substantia nigra (SN) and an enlargement of the third ventricle. However, the presence of the hyperechogenic ultrasound signal from the SN region and the size of its area are not specific signs of the disease because the similar changes were also revealed in persons without the clinical evidence of PD. The role of TCUS in the diagnosis of PD remains unclear. Further studies including verification of the ultrasound data by positron emission tomography are likely to be of help in solving this problem. («Визуализация в клинике». 2000, 17. 45-48)
Ключевые слова: болезнь Паркинсона, транскраниальное ультразвуковое сканирование, черная субстанция.
Key words: Parkinson’s disease, transcranial ultrasound scanning, substantia nigra.
Диагностика болезни Паркинсона (БП) может представлять определенные трудности, особенно в дебюте заболевания. Для ее распознавания из визуализирующих методов исследования используют магнитно-резонансную томографию (МРТ) и позитронно-эмиссионную томографию (ПЭТ). МРТ головного мозга позволяет выявлять только неспецифические и едва уловимые изменения [4, 11, 18, 24]. Более точные сведения о нигростриарной системе позволяет получать ПЭТ, которая способствует ранней диагностике БП даже в доклинической стадии [9, 13, 15, 17, 19, 21]. Однако понятно, что такой дорогостоящий вид исследования не может быть использован как рутинный диагностический метод.
В последние годы возросла роль транскраниального ультразвукового дуплексного сканирования в диагностике церебральных заболеваний, которое позволяет визуализировать сосудистую систему и вещество головного мозга. Данные об использовании транскраниального ультразвукового сканирования (ТКУС) вещества мозга у больных БП немногочисленны и неоднозначны.
В 1995 г. Becker G. et аl. [5] впервые выполнили ТКУС мозга у больных БП. Поскольку этот метод позволяет визуализировать ткани головного мозга в зависимости от их эхогенности, авторы поставили перед собой задачу выяснить, можно ли с его помощью выявлять структурные изменения мозга при БП. Для этого они оценивали состояние области предполагаемого анатомического расположения черной субстанции (ЧС) на уровне ножек среднего мозга, проводя исследование через височное ультразвуковое окно. Авторы считали, что в норме ультразвуковой сигнал от ЧС идентичен эхогенности прилежащей ткани мозга.
При исследовании 30 больных БП и 30 лиц без клинических проявлений этого заболевания они получили следующие данные: у 17 больных и у 2 лиц контрольной группы было выявлено гомогенное повышение эхогенности ткани мозга в области ЧС. Следует отметить, что у 5 больных и двух лиц контрольной группы эти изменения определялись с трудом. Анализ полученных данных показал, что у больных с четкой гиперэхогенной зоной в области ЧС (12 пациентов, т.е. 40% от числа всех больных) клиническая симптоматика была более выражена, а доза антипаркинсонических препаратов оказалась выше, чем у больных с изоэхогенной ЧС (18 больных). Авторы предположили, что повышение эхогенности в области ЧС, по-видимому, обусловлено относительным увеличением глиальных клеток в сочетании с микроструктурными изменениями клеточной архитектоники, о чем сообщали Bogerts В. et аl. [8].
Сопоставление длительности заболевания с наличием выявленной зоны повышенной эхогенности в области ЧС дало противоречивые результаты. Becker G. et аl. [5] обнаружили гиперэхогенную зону в области ЧС примерно у половины больных БП и только при длительном течении заболевания (в среднем 14,6+/-4,5 лет), когда клинический диагноз уже не вызывал сомнения; в то же время у больных с изоэхогенной ЧС продолжительность заболевания составляла в среднем 6,5+/-4,2 года. В. Лелюк с соавт. [1, 16] наблюдали такие изменения абсолютно у всех больных независимо от длительности заболевания с момента появления первых симптомов.
Результаты измерения третьего желудочка свидетельствуют о его расширении у больных БП по сравнению с соответствующими данными в контрольных группах. Так, в работе Becker G. et аl. [5] и В. Лелюка с соавт. [1] размеры третьего желудочка у больных БП составляли в среднем 8,6+/-2,3 мм и 6,3+/-1,2 мм против 7,4+/-2,2 мм и 2,6+/-1,2 мм в контрольных группах соответственно. Авторы объясняют это атрофическими изменениями головного мозга у больных БП, описанными Schneider Е. et аl. [20].
Как указывалось выше, Becker G. et аl. [5] обнаружили гиперэхогенный сигнал у 2 лиц контрольной группы. Эти находки навели Berg D. et аl. [6] на мысль о проведении скринингового исследования эхогенности в области предполагаемого анатомического расположения ЧС у лиц без клинических проявлений БП. Они исследовали 301 человека (146 мужчин и 155 женщин) в возрасте до 79 лет (средний возраст около 30 лет). В число исследованных вошли здоровые добровольцы (студенты и сотрудники госпиталя), а также пациенты, страдающие грыжами межпозвоночного диска и невоспалительной миопатией. Поскольку сигнал эхогенности (яркости) в В-режиме не является количественным параметром, котур видимых гиперэхогенных изменений в области ЧС обводили, а затем определяли полученную площадь. Исследования выполнялись двумя независимыми специалистами. Полученные ими данные о зоне повышенной эхогенности в области ЧС суммировали, определяли средние значения и использовали их для дальнейшего анализа. В среднем площадь гиперэхогенного сигнала с одной или с обеих сторон у исследованных лиц составляла 0,11 см2 при этом наблюдалась четкая закономерность повышения полученных значений с возрастом. Была выделена группа из 26 человек (16 мужчин и 10 женщин) с более широкой зоной гиперэхогенного сигнала, площадь которой с одной или с обеих сторон превышала 0,25 см2. Численность этой группы составила 8,6% от числа включенных в исследование лиц. Площадь гиперэхогеиного сигнала справа и слева была равна у них в среднем 0,32 см2. Для более детального исследования отобрали по 10 человек, сопоставимых по полу и возрасту, из обследованных с площадью гиперэхогенного сигнала менее 0,2 см2 (первая группа) и из пациентов с площадью, превышающей 0,25 см2 (вторая группа). У них было проведено исследование двигательных функций (использование доски со штифтами и серия тестов с применением печатной машинки), когнитивных функций (стандартизированный психометрический тест) и МРТ. ПЭТ выполнили только у лиц второй группы, и для сравнения полученных данных отобрали 10 человек из числа ранее обследованных в клинике больных без БП, которым вводили [18F]-dopa. Были получены следующие результаты: 1) тесты по оценке двигательных функций не показали статистически значимых различий между двумя группами; 2) при оценке когнитивных функций выявлены значительные различия только в плавности речи, которая была хуже во второй группе; 3) относительные интенсивности сигналов от ЧС при МРТ были повышены у лиц второй группы; 4) обнаруженные при ПЭТ соотношения активности внутривенно введенной [18F]-dopa в базальных ганглиях во второй группе были значительно ниже, чем в группе лиц, взятых для сравнения. Несмотря на полученную корреляцию данных ультразвукового исследования, МРТ и ПЭТ, природа гиперэхогенного сигнала от области ЧС осталась для авторов неясной. Ими высказано предположение, что у лиц второй группы нигростриарная система более уязвима по отношению к различным патогенетическим факторам (экзо- и эндотоксинам), под воздействием которых может произойти нейрональная дегенерация ЧС, о чем сообщали другие авторы [14, 23]. На наш взгляд, это высказывание является гипотетическим, так как подтвердить происходящие изменения в области ЧС могут только патоморфологические, гистохимические и электронно-микроскопические исследования.
Любопытные результаты получены при сопоставлении площади гиперэхогенной зоны в области ЧС у больных БП и у лиц без клинических симптомов этого заболевания. Так, в работе В. Лелюка с соавт. [1] у больных БП она была практически равна площади гиперэхогенной зоны той же области у лиц без клинических признаков БП, найденной Berg D. et аl. [6], и составляла примерно 0,32 см2. Эти находки позволяют считать, что получение сигнала повышенной эхогенности и размер его площади не являются специфическими признаками БП.
В работе Berg D. et аl. [6] показано, что гиперэхогенный сигнал площадью более 0,25 см2 в области ЧС встречался у 8,6% от общего числа исследованных. Однако эти результаты существенно превышают данные о частоте встречаемости БП в популяции, которая, по данным Golbe L. [12], составляет 0,1%, а по данным других авторов [2], колеблется от 60 до 140 случаев на 100000 населения, что составляет соответственно 0,06 и 0,14%.
Исходя из изложенного выше, можно отметить, что у больных БП методом ТКУС в большинстве случаев выявляются повышение эхогенности ткани мозга в области предполагаемого анатомического расположения ЧС и расширение третьего желудочка по сравнению с контрольной группой. Однако данные о частоте обнаруженных изменений в области ЧС у больных БП, а также о связи между длительностью заболевания и их наличием противоречивы. Кроме того, в работах, где больным БП было проведено ТКУС, для верификации полученных данных не была произведена ПЭТ, которая, в отличие от МРТ, в настоящий момент является наиболее информативной методикой в диагностике этого заболевания.
Наличие зоны повышенной эхогенности в области ЧС при ТКУС не является специфическим признаком для БП, поскольку она обнаруживается не у всех больных БП и такие же изменения находят и у лиц без клинических проявлений этого заболевания. Размер площади гиперэхогенного ультразвукового сигнала также не может служить диагностическим критерием, так как у больных БП, как показано выше, он был практически идентичен размеру исследуемой зоны у лиц без БП.
Следует отметить, что визуализация структур головного мозга при ультразвуковом исследовании в В-режиме в значительной степени зависит от ультразвукового окна, а оценка видимых изменений весьма субъективна (особенно в отношении измеряемой площади), так как сигнал эхогенности (яркости) не является количественным параметром.
Таким образом, роль ТКУС в диагностике БП остается неясной. Проведение дальнейших исследований с верификацией полученных ультразвуковых данных с помощью ПЭТ, возможно, поможет решить эту задачу.