что такое твердые растворы
ТВЕРДЫЕ РАСТВОРЫ
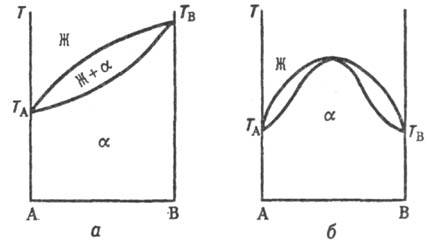
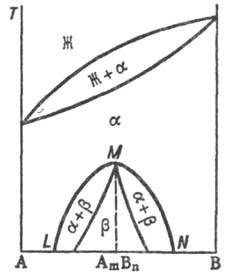
Типы диаграмм состояния. На диаграмме состояния двойных систем в координатах т-ра-состав образованию непрерывных твердых растворов отвечают три типа линий ликвидуса и солидуса (рис. 1, а, б и в), отграничивающих области существования жидкой фазы (расплава) и твердого раствора (Ж и a соотв.) и область сосуществования обеих фаз (Ж + a ). Тип б встречается крайне редко, гл. обр. в случае оптич. изомеров орг. в-в. В системах с непрерывными твердыми растворами, согласно принципу соответствия (см. Физико-химический анализ), должна быть только одна кривая ликвидуса и одна кривая солидуса. Поэтому в точке минимума или максимума происходит плавный переход одной части кривой в другую.
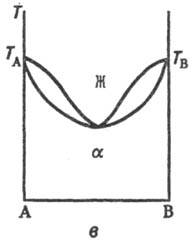
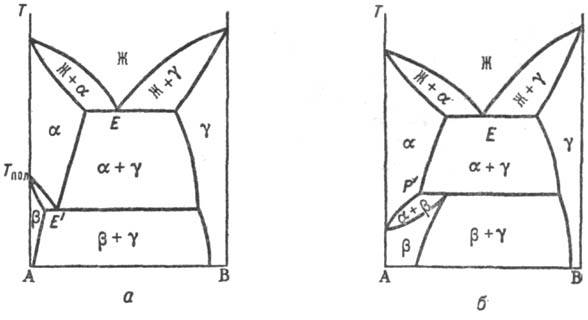
Рис. 2. Диаграммы состояния двойных систем с ограниченными по составу твердыми р-рами a и b : а-система с эвтектич. точкой Е; б-система с пери-тектич. точкой Р. Остальные обозначения те же, что и на рис.’1.
Распад твердых растворов. Предельная концентрация твердого раствора зависит от т-ры и давления. При понижении т-ры взаимная р-римость компонентов, как правило, понижается. Влияние давления неоднозначно, для большинства систем повышение давления приводит к уменьшению взаимной р-римости.
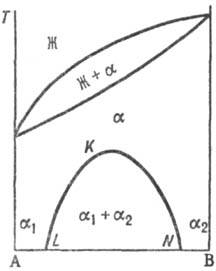
При охлаждении однородного р-ра ниже критич. т-ры р-римости (смешения) (точка К) образуется двухфазная система, состоящая из несмешивающихся твердых растворов a 1 и a 2 (рис. 3), составы к-рых изменяются с т-рой по линиям KL и KN соответственно. Др. тип распада твердого раствора a наблюдается, если компоненты А и В могут образовать хим. соед. А m В n (рис. 4), характеризующееся упорядоченным расположением частиц (атомов или ионов) в кристаллической решетке, в отличие от статистического беспорядка в расположении частиц, характерного для твердых растворов. На основе А m В n образуется твердый раствор b с компонентами А и В. Превращение в упорядоченную фазу (сегрегация) может происходить как фазовый переход II рода. При этом выше температуры перехода вероятности заполнения к.-л. кристаллографич. позиции разл. атомами (ионами) равны, а ниже точки перехода различаются.
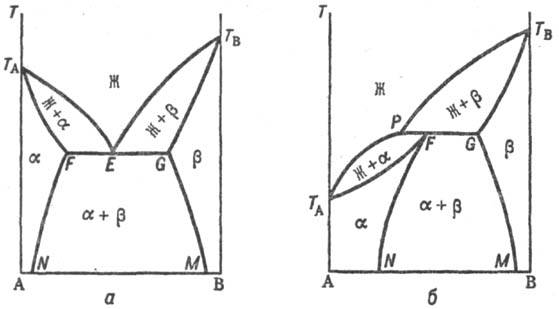
Рис. 5. Диаграммы состояния двойных систем с полиморфным превращением твердого р-ра по эвтектоидному типу (а) и по перитеггоидному типу (б).
Типы твердых растворов. В твердых растворах замещения растворенное в-во замещает исходное-атом на атом, ион на ион или молекула на молекулу. При этом число частиц (атомов, молекул) в элементарной кристаллич. ячейке остается постоянным. Один из важнейших факторов, определяющих возможность образования твердых растворов замещения,-это размеры замещающих друг друга атомов (ионов, молекул). Согласно правилу Гольдшмидта, для образования широких по составу областей гомогенности твердых растворов при т-рах, далеких от т-р плавления компонентов, разница D r в ионных радиусах замещающих друг друга ионов не должна превышать 15%, т.е. отношение D r/r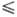
Т вердые растворы как внедрения, так и замещения м.б. неупорядоченными-со статистич. распределением атомов в решетке либо частично или полностью упорядоченными, с определенным расположением атомов разного сорта относительно друг друга. Упорядоченные твердые растворы иногда наз. сверхструктурами. В нек-рых случаях в твердых растворах атомы одного сорта могут образовывать скопления, к-рые, в свою очередь, могут определенным образом упорядочиваться или ориентироваться в данном направлении. Т. обр., твердые растворы, будучи истинно гомогенным в макроскопич. масштабе, т.е. система, находящаяся в термодинамич. равновесии, м.б. неоднородной при рассмотрении на микроуровне. Эксперим. данные об упорядочении твердых растворов получают в осн. при использовании рентгеновского структурного анализа. Упорядоченность твердых растворов и ее изменения в процессах старения важны для материаловедения (см. Сплавы).
числа атомов в элементарной кристаллич. ячейке оптим. размер иона-заместителя не совпадает с размером замещаемого иона. А.Е.Ферсман (1933) полагал, что наиболее благоприятна для образования твердых растворов ситуация, когда ион-заместитель, несущий больший электрический заряд, имеет и больший радиус. Однако часто, напр. при образовании твердых растворов сульфатов двухвалентных металлов в сульфатах Na или К, наблюдается обратная зависимость. Вообще размерный фактор иногда очень сильно, а иногда относительно слабо влияет на ширину областей гомогенности таких твердых растворов, в зависимости от природы соединения-основы.
Нек-рые гетеровалентные твердые растворы (напр., КС1О 4 в BaSO 4 или KBF 4 в SrSO 4 ) относятся к числу т. наз. аномальных твердых растворов, в к-рых наблюдается ниж. температурный предел смешения или при понижении концентрации коэф. сокрис-таллизации стремится к 0 (см. Соосаждение). Это объясняется замещением отдельных блоков элементарных ячеек, так что образуется не истинный, а микродисперсный («коллоидный») твердый раствор.
Выяснение механизма образования твердых растворов требует применения физ. методов исследования, в частности рентгеновского структурного анализа. К числу наиб. часто применяемых методов исследования твердых растворов относится рентгенография порошков. Параметры кристаллич. решетки твердого раствора линейно зависят от состава (Л. Вегард, 1921); реально наблюдаются отклонения от этого правила. Широко используют также измерения плотности; согласно правилу Ретгерса (1889), плотность, а также молярный объем аддитивно зависят от концентрации. Измерение т-р фазовых переходов (см. Термография) позволяет строить диаграммы р-римости с их последующим физико-химическим анализом.
Для твердых растворов, как и для жидких растворов, применяют термодинамические модели и рассматривают идеальные твердые растворы, в к-рых энтальпия смешения равна нулю, регулярные, субрегулярные твердые растворы (см. Растворы неэлектролитов).
Природные кристаллич. в-ва (минералы) и синтетич. кристаллы представляют собой многокомпонентные твердые растворы; даже в-ва высокой чистоты с очень малым содержанием примесей являются твердыми растворами. Как было показано Н. С. Курна-ковым и С.Ф.Жемчужным (1906), св-ва твердых растворов отличаются (иногда очень сильно) от св-в чистых компонентов. В частности, при образовании твердых растворов на основе металла возрастает твердость и уменьшается электропроводность в-ва. Изменение состава твердых растворов позволяет изменять в широких пределах св-ва сплавов, полупроводниковых материалов, ионных проводников, ферритов, лазерных материалов и т. п. и получать материалы с нужными св-вами (см. Легирование). Св-ва
Т вердые растворы могут изменяться в результате термич. обработки, к-рая позволяет получать твердые растворы либо в неравновесном состоянии (закалка), либо в состоянии, в той или иной степени приближенном к равновесному (отжиг, отпуск). Термин «твердые растворы» предложен Я. Вант-Гоффом в 1890.
Лит.: Макаров Е. С., Изоморфизм атомов в кристаллах, М., 1973; Хачатурян А. Г., Теория фазовых превращений и структура твердых растворов, М., 1974; Урусов В. С., Теория изоморфной смесимости, М., 1977; его же, Теоретическая кристаллохимия, М., 1987; Федоров П. П., Соболев Б. П., Федоров П. И., «Кристаллография», 1981, т. 26, № 3, с. 512-20; Китайгородский А. И., Смешанные кристаллы, М., 1983. П.И. Федоров,
Твердые растворы



Твердыми растворами называют однородные кристаллические фазы переменного состава.
Рис. 10. Типы твердых растворов: а — замещения; б — внедрения; в — вычитания
Твердые растворы не являются каким-то исключительным явлением. Наоборот, это весьма характерное состояние реальных веществ, поскольку не существует веществ абсолютно нерастворимых друг в друге в твердом состоянии. Точно так же практически не существует соединений с координационными решетками, состав которых всегда точно соответствовал бы стехиометрическому составу.
Твердые растворы замещения. Если атомы или ионы одного вещества, внедряясь в решетку другого вещества, замещают его собственные атомы или ионы в узлах решетки, возникают твердые растворы замещения.
Твердыми растворами замещения называются такие растворы, которые образуются в результате статистического замещения атомов или ионов в структуре какого-либо кристаллического вещества (растворители или матрицы) атомами или ионами другого (растворенного) вещества, занимающими в результате этого регулярные узлы кристаллической решетки.
Твердые растворы замещения (рис. 10, а)часто называют также смешанными кристаллами и изоморфными смесями, а процесс образования твердых растворов замещения называют изоморфным замещением.
При образовании твердых растворов замещения в принципе замещать друг друга могут как катионы, так и анионы.
Некоторые вещества могут образовывать твердые растворы весьма легко, например при их совместной кристаллизации из растворов. Однако чаще всего, например в силикатных системах, для образования твердых растворов требуется значительная энергия активации, поэтому их возникновение связано с различными термическими процессами (нагреванием до высокой температуры, плавлением с последующей кристаллизацией, гидротермальными процессами).
Способность атомов или ионов входить в структуру другого вещества определяется, с одной стороны, индивидуальными свойствами атомов или ионов (размер, заряд, электронное строение) и, с другой стороны, особенностями кристаллической структуры веществ, образующих твердые растворы.
Твердые растворы внедрения.Атомы или ионы одного вещества могут не замещать атомы или ионы другого, а располагаться в промежутках между ними (рис. 10, б). В этом случае возникают твердые растворы внедрения.
Следует отметить, что твердые растворы внедрения в отличие от твердых растворов замещения могут быть только ограниченными, поскольку обычно при определенной концентрации растворяющегося компонента напряжения в решетке за счет внедряющихся атомов становятся столь значительными, что существование устойчивого твердого раствора мало вероятно.
Дефекты нестехиометрии.В настоящее время установлено, что практически все химические соединения в твердом состоянии с координационными (атомными, ионными или металлическими) решетками имеют переменный состав, т. е. обнаруживают в той или иной степени отклонения от стехиометрического состава, выражаемого формулой этого соединения. Область составов, лежащих внутри граничных значений нарушения стехиометрического состава, называется областью гомогенности или областью нестехиометрии. Постоянный и неизменный химический состав, соответствующий стехиометрической формуле, могут иметь только соединения с молекулярными решетками.
Отклонения от стехиометрии являются следствием дефектов решетки (дефектов нестехиометрии), которые могут проявляться в виде избытка (по сравнению со стехиометрическим) катионов вследствие анионных вакансий (КС1, ТhO2, СеO2, РbО, ТiO и т. д.) или в результате присутствия катионов в междоузлиях решетки (ZnО, СdO и т. д.), избытка анионов из-за наличия в решетке катионных вакансий (FеО, NiO, FеS, ТiO и т. д.) или присутствия анионов в междоузлиях (UO2 и т. д.). Возможны и комбинации указанных видов дефектов в одном и том же соединении.
Поскольку нестехиометрические соединения в пределах области гомогенности представляют собой одну фазу переменного состава, их можно квалифицировать как твердые растворы. Если нарушения стехиометрии вызваны наличием в решетке катионных или анионных вакансий, т. е. при недостатке атомов в соответствующей катионной или анионной подрешетке, то такие твердые растворы иногда называют твердыми растворами вычитания (рис. 10, е), если же эти нарушения вызваны избытком катионов или анионов в междоузлиях, то такие твердые растворы можно рассматривать как твердые растворы внедрения собственных катионов или анионов данного соединения в его кристаллическую решетку.
Твёрдый раствор
Твёрдые растворы — фазы переменного состава, в которых атомы различных элементов расположены в общей кристаллической решётке.
Могут быть неупорядоченными (с хаотическим расположением атомов), частично или полностью упорядоченными. Экспериментально упорядоченность определяют, главным образом, рентгеновским структурным анализом.
Способность образовывать твёрдые растворы свойственна всем кристаллическим твёрдым телам. В большинстве случаев она ограничена узкими пределами концентраций, но известны системы с непрерывным рядом твёрдых растворов (например, Cu—Au, Ti—Zr, GaAs—GaP). По существу, все кристаллические вещества, считающиеся чистыми, представляют собой твёрдые растворы с очень малым содержанием примесей.
Различают три вида твёрдых растворов:
Согласно полуэмпирическим правилам Юм-Розери, непрерывный ряд твёрдых растворов замещения в металлических системах образуются лишь теми элементами, которые, во-первых, имеют близкие по размерам атомные радиусы (отличающиеся не более чем на 15 %) и, во-вторых, находятся не слишком далеко друг от друга в электрохимическом ряду напряжений. При этом элементы должны иметь один и тот же тип кристаллической решётки. В твёрдых растворах на основе полупроводников и диэлектриков, благодаря более «рыхлым» кристаллическим решёткам образование твёрдых растворов замещения возможно и при большем различии атомных радиусов.
Если атомы компонентов существенно различаются по размерам или электронной структуре, возможно внедрение атомов одного элемента в междоузлия решётки, образованной другим элементом. Подобные твёрдые растворы часто образуются при растворении неметаллов (B, H2, O2, N2, C) в металлах.
Твёрдые растворы вычитания, возникающие за счёт появления в кристаллической решётке вакантных узлов, образуются при растворении одного из компонентов в химическом соединении и характерны для нестехиометрических соединений.
Природные минералы часто представляют собой твёрдые растворы (см. Изоморфизм в кристаллах). Образование твёрдых растворов при легировании элементов и соединений имеет большое значение в производстве сплавов, полупроводников, керамики, ферритов.
Твёрдые растворы — основа всех важнейших конструкционных и нержавеющих сталей, бронз, латуней, алюминиевых и магниевых сплавов высокой прочности. Свойства твёрдых растворов регулируют их составом, термической или термомеханической обработкой. Легированные полупроводники и многие сегнетоэлектрики, являющиеся основой современной твердотельной электроники, также являются твёрдыми растворами.
При распаде твёрдых растворов сплавы приобретают новые свойства. Наиболее ценными качествами обладают сплавы с очень тонкой неоднородностью — так называемые дисперсионно-твердеющие, или стареющие твёрдые растворы. Дисперсионное твердение может наблюдаться и при распаде твёрдых растворов на основе соединений, например, нестехиометрических шпинелей.
Различные типы твердых растворов
При охлаждении и кристаллизации образуются твердые растворы и промежуточные фазы.
Твердый раствор — это такая фаза, в которой атомы одного компонента размещаются в кристаллической решетке другого компонента. Твердый раствор сохраняет кристаллическую решетку основного компонента (или растворителя). В зависимости от того, в каких местах кристаллической решетки находятся атомы растворенного компонента, различают твердые растворы замещения и внедрения. На рис. 2.10. показаны различные типы твердых растворов.

В связи с большим количеством ограничений для полной растворимости компонентов чаще встречаются твердые растворы замещения с ограниченной растворимостью. Твердые растворы замещения, также, как любые фазы переменного состава, обозначаются греческими буквами: ос, р, у, 6 и т. д.
Упорядоченные твердые растворы, для которых расположение атомов растворенного элемента в кристаллической решетке основного элемента имеет определенную закономерность, иногда обозначают химической формулой, например, Cu3Au или CuAu. Перестройка структуры твердого раствора при переходе от одного упорядоченного состояния в другое влияет на физические и механические свойства сплавов. При этом структурных изменений под микроскопом чаще всего не наблюдается. Упорядоченность может быть уменьшена или полностью устранена при пластической деформации.
Твердые растворы внедрения чаще всего образуются металлами переходных групп и неметаллами с малым атомным радиусом (г
твёрдые растворы
Полезное
Смотреть что такое «твёрдые растворы» в других словарях:
ТВЁРДЫЕ РАСТВОРЫ — твердотельные двух или многокомпонентные однородные системы переменного состава (напр., типа А xB1 x), в к рых атомы или ионы компонентов, смешиваясь в разл. соотношениях (0 Физическая энциклопедия
Твёрдые растворы — однородные кристаллические веществ (фазы), состоящие из двух или большего числа компонентов и сохраняющие однородность при изменении соотношений между компонентами в определен интервале концентраций. В твёрдых растворах замещения, образованных… … Энциклопедический словарь по металлургии
ТВЁРДЫЕ РАСТВОРЫ — однородные кристаллические вещества (фазы), состоящие из двух или большего числа компонентов и сохраняющие однородность при изменении соотношений между компонентами в определенном интервале концентраций. В твёрдом растворе замещения,… … Металлургический словарь
Твёрдые растворы — твёрдые фазы (См. Фаза)переменного состава, в которых атомы раз личных элементов смешаны в известных пределах или неограниченно в общей кристаллической решётке (См. Кристаллическая решётка). Растворимость в твёрдом состоянии свойственна… … Большая советская энциклопедия
ТВЁРДЫЕ РАСТВОРЫ — однородные твёрдые в ва, состоящие из неск. компонентов, концентрации к рых могут быть изменены в нек рых пределах при данных темп ре, давлении и т. п. без нарушения однородности. Многие металлич. сплавы (напр., сталь, бронза), минералы (полевые… … Естествознание. Энциклопедический словарь
ТВЁРДЫЕ РАСТВОРЫ — однородные кристаллич. в ва, состоящие из двух или большего числа компонентов и сохраняющие однородность при изменении соотношений между компонентами в определ. интервале концентраций. ВТ. р. замещения, образованных двумя металлами (напр., медью… … Большой энциклопедический политехнический словарь
РАСТВОРЫ — системы, состоящие из молекул, атомов и(или) ионов неск. разл. типов, при этом числа разл. частиц не находятся в к. л. определённых стехиометрич. соотношениях друг с другом (что отделяет Р. от хим. соединений). К Р. обычно относят такие… … Физическая энциклопедия
Растворы (химич.) — Растворы, макроскопически однородные смеси двух или большего числа веществ (компонентов), образующие термодинамически равновесные системы. В Р. все компоненты находятся в молекулярно дисперсном состоянии; они равномерно распределены в виде… … Большая советская энциклопедия
Растворы — I Растворы макроскопически однородные смеси двух или большего числа веществ (компонентов), образующие термодинамически равновесные системы. В Р. все компоненты находятся в молекулярно дисперсном состоянии; они равномерно распределены в… … Большая советская энциклопедия