Болезнь Тея-Сакса

Частота заболеваемости составляет около 1 случая на 250 000 населения.
Классификация болезни Тея-Сакса
Причины болезни Тея-Сакса
Болезнь развивается из-за генетического дефекта, который приводит к нарушению синтеза гексозаминидазы А, химического посредника (фермента), находящегося в лизосомах клеток и необходимого для преобразования, хранения, использования веществ, а также утилизации продуктов обмена некоторых веществ (липидов, или ганглиозидов) в ЦНС. При отсутствии фермента, данные вещества накапливаются в нейронахмозга, нарушая их работу и затем разрушая их.
Болезнь Тея-Сакса предается детям через патологический ген, находящийся в 15 хромосоме, от родителей. Если оба носителя гена имеют ребенка, то риск рождения больного ребенка при каждой беременности составляет 25%. Ребенок может унаследовать только один ген в 50% случаев и станет носителем, но в 25% случаев он вообще не унаследует данного гена, не будет ни больным, ни носителем.
Таким образом, наследование болезни Тея-Саксачаще происходит скрыто (аутосомно-рецессивным путем) из поколения в поколение.
Симптомы болезни Тея-Сакса
Ранний признак болезни Тея-Сакса – это повышенная чувствительность младенца на громкие звуки, а также необычная реакция на них. Первыми симптомами также являются задержка роста и развития. Больной теряет интерес к окружающему, к членам семьи, приобретенные навыки, например, ребенок перестает ползать. Спустя некоторое время ребенок слепнет, задерживается в умственном развитии; снижаются мышечные функции вплоть до их потери, включая способность передвигаться, есть и пить, производить звуки. На поздних стадиях могут появиться припадки.
В финальных стадиях заболевания может потребоваться зондовое кормление. В этом состоянии ребенку практически ничем нельзя помочь, за исключением поддержки и ухода, лечения сопутствующих инфекций, ослабляющих ребенка. Причиной смерти часто является воспаление легких (пневмония) или другая инфекция.
Если есть подозрения болезнь Тея-Сакса, необходимо обратить внимание на симптомы:
В 3-6-месячный период:
В 6-10-месячный период:
После 10 месяцев:
Диагностика болезни Тея-Сакса в Израиле
Лечение болезни Тея-Сакса в Израиле
Лечение в клиниках “АССУТА” и “ХАДАССА”
Вас интересует лечение в Израиле?
Крупнейшие профессиональные больницы Израиля – «Ассута» в Тель-Авиве и «Хадасса» в Иерусалиме предлагают реальную возможность получить качественное и специально для вас подобранное лечение у замечательных специалистов по адекватным ценам.
Мы помогаем найти решение ваших проблем со здоровьем, а также предоставляем полную информацию о лучших израильских врачах.
Болезнь Тея-Сакса (ранняя детская амавротическая идиотия): Обзор заболевания
Что может вызывать эту болезнь?
Они входят в состав клеток организма и содержат генетическую информацию или дезоксирибонуклеиновую кислоту (ДНК), которая отвечает за физические характеристики человека. Гены (по отдельности или в совокупности) определяют какие генетические черты ребёнок унаследует от родителей, на пример, группу крови, цвет волос, глаз, а также вероятность развития того или иного заболевания. Определённое количество генов составляют хромосому. Поражения как гена, так и хромосомы, вызывают изменения в процессах и функциях организма. Эти дефекты могут практически не проявляться, однако иногда они становятся причиной развития таких серьёзных заболеваний как гемофилия или синдром Дауна. Такие проблемы со здоровьем как болезнь Стилла (форма ревматоидного артрита у детей) или депрессия также могут быть следствием отклонений на генетическом уровне. Мутировавший ген переходит от родителей к детям. Болезни, передающиеся по наследству, обычно имеют генетический характер. Человек может родиться с генетическим фоном, который будет влиять на повышенную восприимчивость или риск проявления определённого заболевания.
Когда малыш унаследует искажённый ген от обоих родителей, он заболевает.
Это человек, который может передать своим детям наследственную (генетическую) болезнь, хотя сам и не является поражённым недугом. Кроме этого, существует также риск передачи статуса носителя заболевания. Некоторые недуги вызваны именно отклонениями на генном и хромосомном уровнях. Каждый человек унаследует 23 хромосомы от каждого из родителей. Таким образом, у него получается 23 пары хромосом в организме. Если одна или обе хромосомы из пары поражены, возникает генетическое заболевание. В большинстве случаев, у человека с вышеуказанным дефектом обе хромосомы в паре являются повреждёнными. Такое расстройство называется болезнью с аутосомно-рецессивным типом наследования. Определённые генетические заболевания возникают из-за поражения X и Y хромосом, которые отвечают за определение пола. Если хотя бы одна хромосома из пары с отклонением, человек может быть носителем заболевания.
Мутировавший ген препятствует выработке в организме такого фермента как гексозаминидаза А, который отвечает за расщепление ганглиозидов (сложных природных липидов) в клетках. В случае их накопления происходит блокирование работы мозга и повреждение нервных клеток, что и вызывает болезнь Тея-Сакса.
Ферменты Это белок, который вырабатывается для ускорения протекания определённой химической реакции. В нашем организме существует много ферментов для обеспечения различных процессов жизнедеятельности, таких как пищеварение и свёртывание крови. Некоторые генетические заболевания напрямую связаны с выработкой определённых ферментов. Чтобы установить диагноз (на пример, проблемы с почками) врач измеряет количество необходимого фермента в крови пациента.
При болезни Тея-Сакса с поздним началом в организме производится пониженное количество вышеуказанного фермента. Люди с таким заболеванием унаследуют ген гексозаминидаза А с поздним развитием от обоих родителей или же по одному гену с поздним развитием и неспособностью к активности. Риск появления мутировавшего гена возрастает у людей с корнями, которые уходят к евреям-ашкенази, так как 1 из 30 представителей этой национальности является носителем данного заболевания. Кроме того, к развитию болезни Тея-Сакса также предрасположены люди французско-канадского происхождения, проживающие в восточной части долины реки Святого Лоренса провинции Квебек и каджуны (франкоязычные жители штата Луизиана).
Болезнь Тея-Сакса – симптомы
После рождения ребёнок с таким пороком выглядит абсолютно здоровым. Однако вы можете заметить следующее:
В ходе развития у малыша болезни Тея-Сакса с поздним началом такие симптомы как неуклюжесть и перепады настроения могут не восприниматься серьёзно. К более поздним признакам заболевания относятся судорожное подёргивание и слабость мышц, невнятная речь и проблемы с мыслительными процессами. Характер осложнений зависит от того, какое количество гексозаминидазы А вырабатывается в организме.
Болезнь Тея-Сакса – система распознавания заболевания
Если у лечащего врача есть подозрение, что ребёнок поражён болезнью Тея-Сакса, он прежде всего проведёт обследование пациента и возьмёт анализ крови, чтобы проверить уровень гексозаминидазы А в организме. Генетический тест необходим для подтверждения диагноза.
В чём заключается лечение?
Основным лечением болезни Тея-Сакса является контроль симптомов и обеспечение ребёнку комфорта в повседневной жизни, так как панацеи от этого недуга на сегодняшний день не существует. В данном случае полезным будет пройти генетическое консультирование и посетить сеансы терапии, где можно найти поддержку и пообщаться с людьми, у которых есть аналогичная проблема. Если у вас развивается болезнь Тея-Сакса с поздним началом, лечение также основывается на мониторинге симптомов. В зависимости от симптомов вы можете получать определённые препараты, на пример, от депрессии. Несомненно, известие о том, что у вашего ребёнка обнаружили болезнь Тея-Сакса, может повергнуть вас в шок. В такой ситуации кроме заботы о ребёнке, следует помнить и о своём здоровье. Необходимо разговаривать с лечащим врачом на такие темы:
По мере развития заболевания ребёнку может понадобиться более тщательный уход. Подбадривайте его и внушайте, что нужно бороться, подарите свою любовь и ласку. Возможно, у вас возникнет необходимость в дополнительной помощи по уходу за малышом. Проконсультируйтесь с лечащим врачом о том, куда можно обратиться по этому вопросу.
Носители данного порока могут передать детям заболевание даже если они сами не больны. Если вы и партнёр являетесь носителями болезни Тея-Сакса, риск развития аналогичного дефекта у ваших детей повышается до 1 из 4 случаев (25%). Когда вы планируете заводить ребёнка, Американская корпорация акушёров и гинекологов рекомендует сделать следующее:
Если хотя бы один из партнёров соответствует вышеуказанным категориям, он также должен пройти процедуру тестирования. Один положительный результата на носителя заболевания предполагает также обследование другого партнёра.
Из семейного анамнеза врач может узнать, есть ли у пациента кровные родственники с аналогичным заболеванием. Это поможет специалисту установить степень риска передачи порока по наследству.
К кровным родственникам относятся как живые, так и умершие члены семьи. Это могут быть:
В некоторых случаях семейный анамнез бывает довольно сложным. Это зависит от нескольких факторов:
Генетическое консультирование – это пояснения медицинского работника (консультанта по генетическим вопросам или генетика), специализация которого, помогать людям разобраться в опасности передачи генетических заболеваний, а также объяснять возможность унаследования ребёнком такого вида болезни (серповидно-клеточная болезнь, кистозный фиброз, гемофилия).
Генетическое консультирование включает:
Что такое тея сакса болезнь
Этиология и встречаемость болезни Тея-Сакса. Болезнь Тея-Сакса (MIM №272800), раннедетский ганглиозидоз GM2, — панэтническое аутосомно-рецессивное заболевание распада ганглиозидов, вызванное недостаточностью гексозаминидазы А (см. главу 12). Кроме раннедетской тяжелой формы, недостаточность гексозаминидазы А вызывает легкую форму болезни с началом в юношеском или взрослом возрасте.
Встречаемость недостаточности гексозаминидазы А широко варьирует в различных популяциях; встречаемость болезни Тея-Сакса в Северной Америке колеблется от 1 на 3600 новорожденных у евреев ашкенази до 1 на 360 000 среди не ашкенази евреев. Сравнимую с евреями-ашкенази встречаемость болезни Тея-Сакса имеют французские канадцы, каджуны в Луизиане и амиши в Пенсильвании. Повышенная частота носительства в этих четырех популяциях — следствие генетического дрейфа, хотя не исключено преимущество гетерозигот.
Патогенез болезни Тея-Сакса
Ганглиозиды — церамидовые олигосахариды, присутствующие в поверхностных мембранах всех клеток, но больше всего их в клетках мозга. Ганглиозиды концентрируются в поверхностных мембранах нейронов, особенно в аксонах и дендритах. Они функционируют как рецепторы различных гликопротеиновых гормонов и бактериальных токсинов и задействованы в дифференцировке клеток и межклеточном взаимодействии.
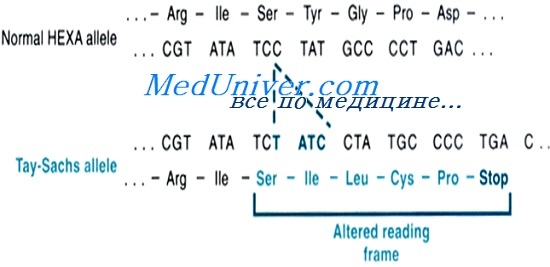
Гексозаминидаза А — лизосомный фермент, состоящий из двух субъединиц. а-Субъединица кодируется геном НЕХА в хромосоме 15, а бета-субъединица — геном НЕХВ в хромосоме 5. В присутствии белка-активатора гексозаминидаза А удаляет концевой N-ацетилгалактозамин из ганглиозида GM2.
Мутации генов а-субъединицы или белка-активизатора вызывают накопление GM2 в лизосомах и, этим самым, раннедетский, позднедетский или взрослый тип болезни Тея-Сакса. [Мутация а-субъединицы вызывает болезнь Сандхоффа (MIM № 268800)].
Пациенты с раннедетской формой ганглиозидоза GM2 имеют два патологических аллеля, приводящих к полному отсутствию активности гексозаминидазы. Пациенты с формами ганглиозидоза GM2 с началом в юношеском или взрослом возрасте — обычно сложные гетерозиготы по аллелю с полным отсутствием функции и аллелю с небольшой остаточной активностью гексозаминидазы А.
Фенотип и развитие болезни Тея-Сакса
Раннедетский тип ганглиозидоза GM2 характеризуется неврологическим ухудшением, начинающимся в возрасте 3-6 мес и приводящим к смерти к 2-4 года. Обычно моторное развитие останавливается или начинает регрессировать к 8-10 мес жизни, и в течение второго года жизни развивается неспособность к самостоятельному передвижению. Потеря зрения начинается на первом году жизни и быстро прогрессирует; почти всегда это связано с «вишнево-красным» пятном («косточкой») при обследовании глазного дна.
Судороги обычно начинаются в конце первого года жизни и непрерывно становятся все тяжелее. Дальнейшее ухудшение на втором году жизни заканчивается децеребрационной ригидностью, затруднениями глотания, тяжелыми судорогами и, наконец, вегетативным состоянием.
Ганглиозидоз GM2 с позднедетским началом выявляют на 2-4 годах жизни, он характеризуется неврологической симптоматикой, начинающейся с атаксии и дискоординации. К концу первого десятилетия большинство пациентов имеют спастичность и судороги; к 10-15 годам у большинства развивается децеребрационная ригидность и вегетативное состояние со смертью обычно во втором десятилетии жизни. Снижение зрения отмечают, но может не быть «вишневой косточки» на глазном дне; атрофия зрительного нерва и пигментный ретинит часто появляются в конце течения болезни.
Взрослый тип ганглиозидоза GM2 имеет выраженную клиническую изменчивость (прогрессирующая дистония, спиноцеребеллярная дегенерация, патология моторных нейронов или психиатрические нарушения). До 40% больных имеют прогрессирующие психиатрические проявления без психоза. Зрение затрагивается редко, и данные офтальмологического обследования обычно в норме.
Особенности фенотипических проявлений болезни Тея-Сакса:
• Возраст начала: от раннего детства до взрослого возраста
• Нейродегенерация
• «Вишневая косточка»
• Психоз
Лечение болезни Тея-Сакса
Диагноз ганглиозидоза GM2 ставят на основании выявления как отсутствующей или почти отсутствующей активности гексозаминидазы А в сыворотке крови или в лейкоцитах, так и нормальной или повышенной активности гексозаминидазы В. Для диагностики также можно использовать анализ мутаций в гене НЕХА, но обычно его выполняют только для уточнения транспортного носительства и пренатальной диагностики.
Болезнь Тея-Сакса в настоящее время — инкурабельное заболевание; следовательно, лечение направлено на устранение симптомов и паллиативный уход. Почти все больные требуют фармакологического лечения судорог. Психиатрические проявления пациентов с взрослым типом ганглиозидоза GM2 обычно не поддаются стандартным антипсихотическим или противодепрессивным средствам; наиболее эффективны препараты лития и электросудорожная терапия.
Риски наследования болезни Тея-Сакса
Для потенциальных родителей без GM2-ганглиозидоза в семейном анамнезе эмпирический риск родить ребенка, больного СМ2-ганглиозидозом, зависит от частоты заболевания в их этнических группах. Для большинства жителей северной Америки эмпирический риск носительства составляет приблизительно 1 на 250-300, но для евреев-ашкенази эмпирический риск носительства — приблизительно 1 на 30. Для пары, в которой оба родителя носители, риск родить ребенка с ганглиозидозом GM2 равен 1/4.
Пренатальная диагностика основана на идентификации мутаций в гене НЕХА или на определении недостаточности гексозаминидазы А в тканях плода, например, ворсинах хориона или амниоцитах. Для эффективной идентификации пораженного плода с помощью анализа мутации в гене НЕХА обычно необходимо, чтобы мутации, вызывающие ганглиозидоз GM2 в семье, уже были известны.
Скрининг популяций высокого риска на носительство и последующие превентивные мероприятия уменьшили встречаемость болезни Тея-Сакса среди евреев-ашкенази почти на 90%. По традиции такой скрининг выполняют по определению активности гексозаминидазы А сыворотки крови с искусственным субстратом.
Этот чувствительный метод, тем не менее, не способен различить патологические мутации и псевдонедостаточность (снижение распада искусственного субстрата, но нормальный распад естественного субстрата); следовательно, носительство обычно подтверждают молекулярным анализом НЕХА. В гене НЕХА обнаружено два аллеля псевдонедостаточности и более 70 патологических мутаций.
Среди евреев-ашкенази, положительных по результатам ферментного скрининга, 2% — гетерозиготны по аллелю псевдонедостаточности, и 95-98% гетерозиготны по одной из трех патологических мутаций, две вызывают раннедетскую форму, одна — взрослую форму GM2-ганглиозидоза. В отличие от этого, среди остальных североамериканцев, положительных по результатам ферментативного скрининга, 35% — гетерозиготны по аллелям псевдонедостаточности.
Пример болезни Тея-Сакса. Семейная пара, оба евреи ашекенази, направлена в клинику генетики для оценки риска родить ребенка с болезнью Тея-Сакса. Сестра жены умерла от болезни Тея-Сакса в детстве. Дядя мужа по отцу находится в психиатрической лечебнице, но его диагноз неизвестен. Как муж, так и жена отказались от скрининга на носительство болезни Тея-Сакса в подростковом возрасте.
Анализ фермента показал, что как муж, так и жена имеют чрезвычайно низкую активность гексозаминидазы А. Последующий молекулярный анализ мутаций, преобладающих у евреев ашкенази, подтвердил, что у жены имеется патогенная мутация, тогда как у мужа только аллель псевдонедостаточности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Болезнь Тея-Сакса
У некоторых детей после рождения может развиться редкая генетическая болезнь Тея-Сакса, которая постепенно разрушает нейроны или нервные клетки в головном и спинном мозге. Это расстройство пока неизлечимо, но в ближайшем будущем ученые рассчитывают найти лекарство и делают большие ставки на трансплантацию костного мозга и генную терапию.
Что такое болезнь Тея-Сакса?
Обычно ганглиозиды непрерывно расщепляются ферментом гексозаминидазой А для поддержания соответствующего баланса. Но при болезни Тая-Сакса этот фермент (необходимый для удаления избытка ганглиозидов) отсутствует. Это приводит к накоплению ганглиозидов в головном мозге, что затрудняет работу нервов и приводит к появлению симптомов расстройства.
Различные формы болезни Тея-Сакса
Другие формы этого заболевания встречаются довольно редко.
Существует также поздняя ювенильная или взрослая форма этого расстройства, симптомы которой проявляются в зрелом возрасте. Она встречается крайне редко. Продолжительность жизни людей с этим расстройством может отличаться.
Причины болезни Тея-Сакса
Причины болезни Тея-Сакса могут заключаться в следующем:
Симптомы болезни Тея-Сакса
Некоторые из распространенных симптомов инфантильной болезни Тея-Сакса являются:
Симптомы других форм болезни Тея-Сакса
Симптомы других форм болезни Тея-Сакса могут сильно варьироваться. Некоторые из них:
Диагностика и тесты
Для диагностики болезни Тея-Сакса проводится пренатальный тест между 10 и 12 неделями беременности на забор ворсинок хориона (CVS), во время которого из плаценты извлекают образцы клеток.
Генетическое тестирование родителей проводится для того, чтобы определить, являются ли они носителями болезни Тея-Сакса. В том случае, если у ребенка появляются симптомы заболевания, врач может сначала поинтересоваться семейным анамнезом. Он также может провести физический осмотр глаз ребенка, чтобы проверить наличие вишнево-красного пятна, которое является одним из характерных симптомов расстройства болезни Тея-Сакса.
Также ребенку могут назначить сдачу ферментативного анализа тканей или образцов крови, который исследует наличие и уровень гексозаминидазы А. При болезни Тея-Сакса эти показатели отсутствуют или снижены..
Лечение болезни Тея-Сакса
От болезни Тая-Сакса нет лекарства. Однако некоторые методы помогают справиться с ее симптомами. Так, например, для контроля тремора используются противосудорожные препараты.
В комплекс терапии входит также массаж, который помогает сохранить гибкость суставов и мышц.
Профилактика болезни Тея-Сакса
Предотвратить возникновение инфантильной болезни Тея-Сакса сложно, поскольку она является наследственной.
Скрининговые тесты, такие как амниоцентез или CVS беременных женщин, могут оказаться полезными для выявления носителей этого расстройства.
В случае, если у пары имеется расстройство Тея-Сакса в семейном анамнезе, перед планированием ребенка необходимо обратиться за консультацией генетика.
Болезнь Тея-Сакса – это генетическое заболевание, характеризующееся недостаточностью фермента гексозаминидазы А, скоплением липоидных макромолекул в нейронах, нарушением функций головного и спинного мозга. Проявляется деградацией физических навыков и психических функций: распадом глотательного рефлекса, речи и произвольных движений, утратой слуха и зрения, снижением интеллекта. Развиваются судорожные приступы, атрофия мышц, паралич, деменция. Специфические методы диагностики – офтальмоскопия глазного дна, исследование количества гексозаминидазы в крови и нейронах. Лечение паллиативное, нацелено на облегчение симптомов.
МКБ-10
Общие сведения
Синонимы болезни Тея-Сакса (БТС) – ганглиозидоз GM2, идиотия Тея-Сакса, ранняя детская амавротическая идиотия. Является одним из вариантов лизосомных болезней накопления. Названа по фамилиям двух врачей – невропатолога из США Бернарда Сакса и офтальмолога из Великобритании Уоррена Тея. В 80-е годы XIX века они впервые опубликовали независимые описания данной патологии. Ее распространенность крайне низка, в общей популяции средняя частота носителей рецессивного измененного гена составляет около 0,3%. Эпидемиологические показатели наиболее высоки в группе евреев ашкенази (носительство мутации определяется у 3%), а также у франкоканадцев и каджунов. Пик заболеваемости приходится на возраст от полугода до 2 лет, реже симптомы дебютируют у подростков и взрослых.
Причины
Метаболические нарушения, составляющие основу заболевания, вызваны мутацией гена HEXA, который находится на длинном плече 15 хромосомы. Он кодирует альфа-субъединицу фермента лизосом бета-N-ацетилгексозаминидазы А. Болезнь Тея-Сакса наследуется по аутосомно-рецессивному принципу – для возникновения симптоматики необходимо присутствие в хромосоме двух мутированных генов. Риск болезни у ребенка существует, только если оба супруга являются носителями мутации, составляет 25%. Таким образом, патология может проявиться в любом поколении независимо от того, когда произошла мутация. Носительство долгое время может оставаться скрытым – в этом случае доминантный «здоровый» ген в состоянии обеспечить организм производством фермента на 50% и более, что достаточно для нормального протекания биохимических реакций.
К началу 2000-х годов выявлено более 100 различных мутаций в генах HEXA: вставки в пары оснований, делеции пар оснований, сплайс-сайт мутации, точечные мутации и другие варианты изменений структуры гена. Каждая из этих мутаций определенным образом влияет на строение фермента и подавляет его активность. Разнообразие мутаций пары генов – компаундная гетерозиготность – определяет наличие нескольких форм болезни. Одинаково мутировавшие гены в аллели вызывают полную инактивацию катаболизма ганглиозидов. Наследование разных (не одинаковых) мутаций в паре генов чаще проявляется уменьшением активности фермента, а не полной инактивацией.
Патогенез
Основой развития болезни является отсутствие или недостаточная активность гексозаминидазы A – лизосомального фермента, катализирующего биодеградацию макромолекул ганглиозидов, олигосахаридов, гликозаминогликанов и гликолипидов. Ганглиозиды – тип жирных кислот, липидные компоненты мембран нейронов и глиальных клеток. Они обеспечивают активность нервных клеток: влияют на скорость и интенсивность нейропередачи, проведение нервных импульсов, распределение и хранение информации, формирование памяти. В норме ганглиозиды производятся, выполняют свои функции и быстро расщепляются в процессе многоступенчатой реакции с участием ферментов. Для гидролиза этих сложных липидов необходимы три компонента: альфа- и бета-субъединицы гексозаминидазы А, белок-активатор GM2A. При недостаточности альфа-гексозаминидазы А процесс биодеградации замедляется или становится полностью невозможным. Ганглиозиды накапливаются в лизосомах клеток головного, спинного мозга, приводят к их дисфункции и гибели.
Классификация
В зависимости от особенностей генетического дефекта, сохранности функций гексозаминидазы заболевание имеет быстропрогрессирующее или медленно прогрессирующее течение, проявляется в раннем детстве, подростничестве или во взрослом возрасте. Согласно этим характеристикам выделено 3 формы болезни:
Симптомы болезни Тея-Сакса
Клиническая картина болезни отражает процессы поражения ЦНС. При инфантильной форме первые симптомы становятся заметными к 3-5 месяцам, до этого развитие соответствует норме: ребенок держит голову, переворачивается на живот и обратно, агукает, улыбается при виде взрослого, устанавливает визуальный контакт. К 6 месяцам снижается заинтересованность окружающим миром. Малыш подолгу смотрит в сторону, апатичен, малоподвижен, чувствителен к громким звукам, яркому свету. Он перестает узнавать близких людей, с трудом фокусирует взгляд на любимых игрушках.
После полугода задержка психического и физического развития становится еще более заметной. Нарастает мышечная гипотония, утрачиваются ранее приобретенные навыки: удерживание головы и корпуса в вертикальном положении, переворачивание в положении лежа на горизонтальной поверхности, сидение (попытки сидения), захват игрушки и перекладывание ее из руки в руку. К 8-10 месяцам усиливаются старт-рефлексы – реакции на внезапные звуковые, световые, тактильные и обонятельные раздражители. Интерес к происходящим вокруг событиям почти полностью исчезает. К 12 месяцам нарушается способность глотать, заметно снижается слух и зрение, затрудняется цикл дыхания. Мышцы подвергаются атрофии, развивается паралич, судороги в форме тонико-клонических генерализованных и парциальных приступов. На втором году жизни возникают явления децеребрационной ригидности, бульбарно-псевдобульбарного синдрома.
Ювенильная форма дебютирует менее явными симптомами. На начальном этапе несколько усиливается эмоциональная неустойчивость, при выполнении сложных двигательных комплексов – беге, ходьбе, быстром письме – появляется едва заметная дискоординация движений. Через некоторое время неуклюжесть и неловкость нарастают, замечаются окружающими и самим ребенком. К подростковому возрасту походка становится шаткой, неустойчивой. Формируются гиперкинезы – внезапные непроизвольные движения различных групп мышц. Нарушения координации не позволяют продолжать школьное обучение. Параллельно появляются расстройства речи сложного мозжечково-дизартрического характера: теряется плавность и ритмичность, произношение становится медленным, смазанным, невнятным. Поздние стадии болезни характеризуются частыми эпилептическими приступами, стойким снижением интеллектуальных функций (деменцией), утратой произвольности движений, параличом.
Хроническая форма заболевания имеет менее выраженные симптомы, течение сравнительно легкое. У пациентов наблюдаются перепады настроения, неуклюжесть, ухудшается произношение. На протяжении нескольких лет снижаются интеллектуальные функции: утрачивается способность к абстрактному мышлению, сравнению и анализу явлений и предметов, нарастает забывчивость и рассеянность. Спустя несколько лет после начала болезни развиваются психические расстройства: больные неадекватны в поведении, аффективно возбудимы, склонны к состояниям ажитации и глубокой депрессии, подвержены психозам с галлюцинациями и бредом. При длительном течении формируется органическая деменция.
Осложнения
В число симптомов БТС входят эпилептические приступы, представляющие собой результат внезапных вспышек аномальной биоэлектрической активности мозга. При их высокой частоте физическая и психическая деградация происходит быстрее. Во время приступа больные падают, бьются в конвульсиях, что сопровождается высоким риском удушья (западение корня языка), получения смертельных травм. Основным осложнением острой инфантильной формы заболевания являются инфекции: у детей снижены функции иммунной системы, поражение органов дыхания носит рецидивирующий характер, протекает крайне тяжело. Распространенная причина смерти – пневмония.
Диагностика
Обследование проводится детским неврологом, офтальмологом, генетиком, психиатром. Процесс постановки диагноза начинается со сбора клинико-анамнестических данных. Как правило, выявляются случаи БТС у родственников, наличие периода нормального развития пациента, затем деградация – распад приобретенных навыков, сформировавшихся функций. Дифференциальная диагностика направлена на исключение дегенеративных заболеваний ЦНС, ювенильной идиотии, эпилепсии. Для подтверждения диагноза выполняются следующие процедуры:
Лечение болезни Тея-Сакса
В настоящее время эффективные способы терапии отсутствуют. Медицинская помощь больным нацелена на устранение симптомов и поддержание жизнедеятельности. Паллиативное лечение включает переход на зондовое питание, поскольку у пациентов утрачивается глотательный рефлекс, применение антибиотиков, противовирусных и иммуностимулирующих препаратов для борьбы с сопутствующими инфекционными заболеваниями. Терапия противоэпилептическими средствами не приносит положительного результата.
Поиск возможных способов лечения БТС продолжается. Исследования ведутся в трех направлениях: изучаются возможности ферментозаместительной, генной и субстратредуцирующей терапии. Замена отсутствующего фермента оказывается неэффективной из-за большого размера молекул гексозаминидазы, неспособных пройти сквозь гематоэнцефалический барьер и оболочку нейронов. Среди методов генотерапии опробовано введение нового генетического материала в клетки при помощи вирусного вектора и трансплантации стволовых клеток. Но положительных результатов не получено, исследования продолжаются. Наиболее перспективной считается субстратредуцирующая терапия с использованием фермента сиалидазы, который стимулирует катаболизм GM2 ганглиозидов. Ожидается разработка фармакологического препарата, повышающего экспрессию лизосомальных сиалидаз внутри нейронов.