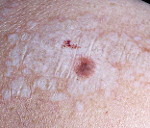
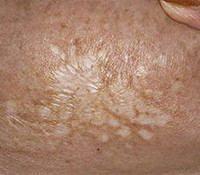
Склероатрофический лихен
В 1885 чешский гинеколог Август Брейски (August Breisky) описал lichen sclerosus et atrophicus — хронический неинфекционный дерматоз с очаговой атрофией кожи и слизистых
В структуре дерматологических болезней эта патология составляет меньше 1%, однако в последние годы отмечена тенденция к росту заболеваемости.
За 130 лет lichen sclerosus et atrophicus приобрел немало различных названий. Среди них:
Виды лихена
В зависимости от локализации высыпаний принято различать следующие формы:
Экстрагенитальная
Генитальная.
Если спонтанное излечение не происходит, то генитальный склероатрофический лихен переходит в крауроз (от греч. krauros — сухой, хрупкий) вульвы или крайней плоти — головки полового члена для которого характерно развитие склерозирования с потерей подвижности тканей. При краурозе поверхность пораженных участков сухая, блестящая, плотная. При поражении вульвы обычен интенсивный зуд и телеангиоэктазии. Если не лечить заболевание, в дальнейшем развиваются атрофия малых и больших половых губ, лейкоплакия и, нередко, рак. Крауроз полового члена проявляется в виде хронической атрофии и сморщивания головки полового члена и внутреннего листка крайней плоти, приводить к фимозу и сужению отверстия мочеиспускательного канала. В противоположность краурозу вульвы, при поражениях полового члена зуд отсутствует, и болезнь не осложняется раком.
Генитальную форму разделяют на:
Клиническая картина
Склероатрофический лихен не относится к заболеваниям, передаваемым половым путем.
Течение заболевания волнообразное — площадь и интенсивность высыпаний могут уменьшаться и увеличиваться. Нередко склероатрофический лихен осложняется присоединением грибковой и/или бактериальной инфекциии.
Возникновение лихена
Возникновение склероатрофического лихена связывают также с частой травматизацией слизистых, воздействием раздражающих веществ, нарушениями метаболизма, эндокринные, нейрогенные и иные факторы.
Доминируют 2 теории возникновения склероатрофического лихена:
Аутоиммунная
Аргументы: наличие семейного анамнеза, связь с определенными классами HLA, наличие аутоантител, сочетание с очаговой и системной склеродермией, витилиго, красным плоским лишаем, другой аутоиммунной патологией кожи и/или слизистых оболочек.
Инфекционная
Аргументы: в половине случаев заболевание формируется на фоне острых или хронических инфекционных заболеваний, отмечена связь с лаймской болезнью (боррелиозом). Во время диагностики часто удается выявить высокий титр антител к спирохетам Бургдорфера, а клиническая картина существенно улучшается после лечения пенициллином.
Специфические меры профилактики не разработаны. Традиционно рекомендуют: обеспечить бережный и мягкий уход за больными местами, использовать белье из хлопка и выбирать модели, не оказывающие давления на очаги поражения, регулярно и обильно использовать средства для смягчения и увлажнение слизистых, а туалет проводить с использованием нейтральных моющих средств.
Лечение лихена
Лечение склероатрофического лихена направлено на осуществление следующих задач:
Комплекс лечебных мероприятий определяется тремя доминирующими патогенетическими механизмами:
Фармакодинамика препарата Лонгидаза ® обусловлена фибринолитической активностью гиалуронидазы, усиленной и пролонгированной за счет фиксации на высокомолекулярном носителе.
Соответственно, медикаментозное лечение проводят:
Кортикостероидами
(оказывают ингибирующее влияние на функции клеточного и гуморального иммунитета); длительная терапия стероидами в форме кремов и мазей может приводить к истончению кожи и вызвать дискомфорт.
Ингибиторами кальциневрина
— подавляют активацию Т-лимфоцитов, блокируя выработку в T-хелперах 1 и 2 типа провоспалительных цитокинов, таких как интерлейкины IL-2, −4, −5, −10, фактор некроза опухоли TNF и гранулоцитарно-макрофагальный колониестимулирующий фактор GM-CSF. Такролимус — мазь Протопик 0,03% и 0,1%. Среди нежелательных эффектов этого препарата: ощущение жжения и зуда, покраснение, боль, раздражение, сыпь в месте нанесения, развитие фолликулита и акне. Зарегистрированы единичные случаи малигнизации (кожные и другие виды лимфом, рак кожи). Пимекролимус — крем Элидел 1%. Среди побочных эффектов жжение в месте нанесения крема, развитие импетиго и кожных инфекций, ринит, крапивница.
Ферментными препаратами
(способствуют рассасыванию рубцов): гиалуронидаза, трипсин, хемотрипсин.
Лечебное действие препарата Лонгидаза ®
В диапазоне рекомендуемых доз Лонгидаза ® селективно разрушает измененную по составу и структуре соединительную ткань в области фиброза, не влияя на морфологию и функцию нормальной соединительной ткани.
Высокомолекулярный носитель не только стабилизирует гиалуронидазу, но и связывает (инактивирует) высвобождающихся в ходе гидролиза матрикса продукты (ионы железа, меди, гепарин и т.п.), способные одновременно и ингибировать гиалуронидазу, и стимулировать синтез соединительной ткани.
Таким образом, Лонгидаза ® не только избирательно деполимеризует матрикс фиброзно-гранулематозных образований, но и блокирует попытку организма компенсаторно нейтрализовать последствия этой деполимеризации путем усиления синтеза коллагена.
Лонгидаза ® подавляет гиперплазию соединительной ткани, контролируя патологический процесс на всех стадиях его развития.
Лонгидаза ® не обладает антигенными свойствами, мутагенной активностью, не оказывает аллергизирующего, эмбриотоксического, тератогенного и канцерогенного действия.
Лечение СКЛЕРОЗИРУЮЩЕГО ЛИХЕНА (ЛИШАЯ) У ЖЕНЩИН – Рекомендации Британской ассоциации дерматологов (перевод и адаптация проф. Святенко)

Какова цель этой статьи?
Эта статья была написана, чтобы помочь Вам больше узнать о склерозирующем лихене. Она расскажет Вам, что это такое, что его вызывает, что можно сделать по этому поводу, и где Вы можете узнать об этом больше.
Что такое склерозирующий лихен?
Склерозирующий лихен – хроническое воспалительное состояние кожи, которое может поражать любую часть кожи, но чаще всего поражает кожу половых органов (вульву) и кожу вокруг ануса. Это может начаться в детстве или в зрелом возрасте (обычно после менопаузы) и поражать девочек или женщин любого возраста.
Что вызывает склерозирующий лихен?
Причина склерозирующего лихена до конца не понята. Это состояние может быть связано с другими заболеваниями, при которых иммунная система организма атакует нормальные ткани, такими как щитовидная железа (вызывая гиперактивную или гипоактивную функцию щитовидной железы) или инсулин-продуцирующие клетки поджелудочной железы (вызывая диабет), но и не было доказано, что это аутоиммунное состояние само по себе.
Склерозирующий лихен не связан с инфекцией – болезнь не заразна и не может распространяться через контакт, в том числе и половой акт.
Трение или повреждение кожи вызывает склерозирующий лихен и ухудшает его. Эта реакция называется «ответом Кёбнера». Проблему могут ухудшить раздражение от подтекания мочи, ношение прокладок для страдающих недержанием или прокладки для белья.
Является ли склерозирующий лихен наследственным?
Неизвестно, является ли склерозирующий лихен наследственным, но изредка встречается у родственников.
Каковы симптомы склерозирующего лихена?
Наиболее распространенным симптомом склерозирующего лихена вульвы является зуд, который может быть тяжелым и очень болезненным, если кожа истончается или трескается. Процесс образования рубцов в области гениталий может стянуть кожу, что может помешать мочеиспусканию и половому акту. Стягивание кожи вокруг ануса может вызвать дискомфорт при прохождении каловых масс кишечника и усугубить любую тенденцию к запорам, особенно у детей.
На участках вне кожи гениталий редко появляются какие-либо симптомы.
Как выглядит склерозирующий лихен?
В областях, удаленных от кожи половых органов, склерозирующий лихен похож на небольшие области, слегка окрашенные в цвет слоновой кости, которые могут соединяться между собой. Через некоторое время поверхность пятен может выглядеть как белая морщинистая салфетка. Наиболее распространенными местами являются изгибы запястий, верхняя часть грудной клетки, области вокруг груди, шеи и подмышек.
Как диагностировать склерозирующий лихен?
Диагноз обычно может быть поставлен по типичному виду состояния кожи. Если есть какие-либо сомнения, небольшой образец кожи можно взять и осмотреть под микроскопом, чтобы подтвердить диагноз, особенно если беспокоит боль или утолщенная область кожи. Эта диагностическая манипуляция известно как биопсия кожи и требует местной анестезии и, возможно, зашивания для закрытия раны, что приводит к небольшому рубцу.
Можно ли вылечить склерозирующий лихен?
Не существует полного излечения склерозирующего лихена, но симптомы и признаки болезни можно хорошо контролировать с помощью применения кремов для пораженной кожи. Если он начинается в детстве, он обычно успокаивается примерно в период полового созревания.
Как можно лечить лихен?
Для склерозирующего лихена предлагаются различные виды лечения:
Самостоятельный уход
Будьте здоровы и привлекательны!
Обращайтесь только к профессионалам.
Используйте при изучении информации о вашей проблеме только данные доказательной медицины, такие, как приведены в этой статье.
Склероатрофический лишай
Склероатрофический лишай – дерматологическое заболевание неясной этиологии, при котором наблюдается атрофия различных участков кожи, в основном в области половых органов, реже других регионов тела. Симптомом этого состояния является образование светлых, почти белых бляшек и папул вокруг гениталий, изредка на шее и около подмышечных впадин, которые со временем трансформируются в атрофические очаги. Диагностика склероатрофического лишая осуществляется на основании результатов дерматологического осмотра больного, в спорных случаях может производиться биопсия кожных покровов в области поражения с последующим гистологическим исследованием. Этиотропное лечение заболевания не разработано, назначают общеукрепляющие средства, витаминотерапию и лекарства для улучшения микроциркуляции. Имеются указания на положительный эффект от использования противомалярийных средств.
Общие сведения
Склероатрофический лишай (болезнь белых пятен, каплевидная склеродермия, крауроз вульвы/полового члена) – атрофическое заболевание кожи неопределенного генеза, которое преимущественно поражает зону гениталий, но может располагаться и на иных участках кожных покровов. Это состояние было впервые описано еще в 1889 году французским дерматологом Франсуа Аллопо, принявшем заболевание за разновидность обычного плоского лишая. Лишь дальнейшие исследования позволили определить, что патология, описанная Аллопо, разделяется на два типа – первичный склероатрофический лишай и последствия красного плоского лихена (стадия атрофии). Это дерматологическая заболевание в несколько раз чаще встречается у женщин, особенно экстрагенитальные формы – последние практически никогда не наблюдаются у мужчин. Наблюдения по поводу возрастного распределения несколько разнятся – по одним данным, склероатрофический лишай в основном поражает лиц старшего возраста и крайне редко возникает у девочек в подростковый период. Согласно мнению иных исследователей, нередки случаи развития этого состояния у молодых женщин – такие различия в описании многих специалистов объясняют путаницей, при которой за болезнь белых пятен принимают застарелые формы красного плоского лишая.
Причины склероатрофического лишая
Этиология и патогенез склероатрофического лишая в данный момент изучены недостаточно, имеется лишь несколько гипотез по поводу развития этого дерматологического заболевания. Наибольшим признанием пользуется патогенетическая теория – описаны как наследственные случаи данного состояния, так и их схожее развитие у однояйцовых близнецов. Однако при этом ни дефектные гены, ни другие молекулярные механизмы возникновения склероатрофического лишая не изучены. Другая популярная теория указывает на аутоиммунные факторы развития этой патологии, поскольку ее проявления схожи с другими поражениями кожи подобного типа (склеродермией, некоторыми формами псориаза). Но и эта версия не объясняет все проявления склероатрофического лишая, кроме того, заболевание очень слабо реагирует на лечение иммуносупрессивными средствами.
Имеются указания на роль инфекционных факторов, например, боррелиоза (болезни Лайма). После перенесенной инфекции такого типа у ряда лиц возникают типичные проявления склероатрофического лишая. Не исключено влияние и других вирусных или бактериальных инфекций, также эта теория некоторыми дерматологами сочетается с аутоиммунной по причине возможной перекрестной реакции на антигены возбудителей и собственных тканей человека. Практически доказано, что предрасполагающую роль в развитии склероатрофического лишая играют гормональный дисбаланс, поражения эндокринной системы, частые психоэмоциональные стрессы. Изучение этого заболевания, попытки объяснения причин его возникновения и использования этих данных в лечении патологии продолжаются до сих пор.
Симптомы склероатрофического лишая
Большинство случаев склероатрофического лишая регистрируется у женщин в возрасте 35-50 лет, иногда наблюдается развитие заболевания у молодых девушек и даже подростков. Высыпания могут локализоваться на шее, груди, около подмышечных впадин, на лобке, бедрах и в области половых органов – при этом так называемые экстрагенитальные формы болезни белых пятен (наличие высыпаний на теле при отсутствии их на вульве и близлежащих участках) составляют только 20% от всех случаев. Наиболее часто склероатрофический лишай проявляется именно поражением генитальной области и собственно вульвы. Для начала заболевания характерно появление на поверхности кожных покровов папул белого цвета, которые достаточно быстро трансформируются в светлые или розовые бляшки. Поверхность бляшек несколько приподнята над здоровой кожей, шелушится, из субъективных симптомов отмечается выраженный зуд. При дальнейшем развитии склероатрофического лишая на месте бляшек образуются гипопигментированные атрофические участки кожи, поверхность которых напоминает папиросную бумагу.
Мужчины страдают от этой патологии в несколько раз реже, при этом у них практически всегда наблюдается поражение кожных покровов в области половых органов (в 90% случаев поражается крайняя плоть и поверхность головки полового члена). В остальном развитие кожных проявлений склероатрофического лишая не имеет особенностей, отмечается появление бляшек или папул с дальнейшей атрофией кожи и появлением белых пятен. Поражение крайней плоти может приводить к развитию рубцового фимоза. Как у мужчин, так и у женщин генитальные формы склероатрофического лишая могут осложняться вторичной инфекцией бактериального или вирусного генеза. Также эта форма заболевания опасна тем, что является предраковым состоянием – по статистике, примерно в 3-5% случаев болезнь белых пятен перерождается в плоскоклеточный рак кожи или половых органов.
Диагностика склероатрофического лишая
Выявление склероатрофического лишая в дерматологии не представляет особой сложности из-за выраженных проявлений заболевания – белых атрофических участков кожи, локализующихся вокруг половых органов и на вульве. При осмотре могут обнаруживаться относительно свежие очаги патологии в виде светло-розовых папул или бляшек. Однако дифференциальная диагностика склероатрофического лишая несколько затруднена, поскольку схожими проявлениями обладают склеродермия, застарелые формы красного плоского лишая, некоторые разновидности псориаза. Главной особенностью патологии является преимущественная локализация высыпаний вокруг и на половых органах, поэтому при экстрагенитальных формах наиболее часто возникают диагностические ошибки.
Патогистологические изменения при склероатрофическом лишае неодинаковы на различных стадиях процесса. На начальных этапах выявляют выраженный отек дермы, умеренную лимфогистиоцитарную инфильтрацию, расширение кровеносных сосудов. Эпидермис утолщен, наблюдается нарушение процессов ороговения, роговые массы могут забивать волосяные фолликулы, протоки потовых и сальных желез. При дальнейшем развитии склероатрофического лишая определяется атрофия эпидермиса, гомогенность коллагеновых волокон дермы. На поздних этапах в некоторых случаях могут наблюдаться признаки метаплазии клеток и начальных проявлений плоскоклеточного рака.
Лечение склероатрофического лишая
Из-за неясности причин склероатрофического лишая этиотропного лечения этого дерматологического заболевания на сегодняшний день не существует. Применяют различные симптоматические методы терапии, а также препараты, относительная эффективность которых была доказана эмпирическими клиническими наблюдениями. Из наружных средств назначают иммуносупрессивные мази (на основе кортикостероидов или такролимуса), однако они могут уменьшить выраженность симптомов лишь на стадии развития бляшек и папул. Аналогично в лечении склероатрофического лишая используют и противомалярийные средства – их не назначают при развившейся атрофии кожи. Препараты, улучшающие местное кровоснабжение и процессы микроциркуляции (например, на основе витаминов), также позволяют значительно уменьшить выраженность симптомов. Некоторые специалисты указывают на необходимость лечения основного заболевания, которое могло быть провоцирующим для склероатрофического лишая – эндокринных нарушений, сахарного диабета и пр.
Иногда в терапии болезни белых пятен применяют хирургические методики. Операции могут производиться как по эстетическим показаниям (устранение чрезмерно больших участков атрофии и дальнейшая пластика), так и по медицинским. В тяжелых случаях склероатрофического лишая возникают спайки, приводящие к сращению малых половых губ, сужению мочеиспускательного канала, фимозу. Все эти осложнения могут быть устранены только хирургическим путем – пластикой вульвы и мочеиспускательного канала, обрезанием (циркумцизио) у мужчин. Кроме того, хирургическое лечение показано при трансформации склероатрофического лишая в плоскоклеточный рак кожи.
Прогноз и профилактика склероатрофического лишая
Большинство дерматологов склонны относить склероатрофический лишай к заболеваниям с относительно неблагоприятным прогнозом. Это связано с неопределенным генезом патологии, в результате чего, несмотря на все терапевтические мероприятия, у больных остаются атрофические участки кожи различного размера. Всегда имеется риск таких осложнений, как развитие спаек, сужение мочеиспускательного канала, вторичная инфекция, злокачественное перерождение. Больные склероатрофическим лишаем должны каждые 2-3 месяца посещать дерматолога или онколога с целью как можно более раннего выявления вышеперечисленных грозных осложнений.
Что такое склероатрофический лишай
«Баланит ксеротический облитерирующий» теперь рассматривается как синоним склероатрофического лихена, а «крауроз вульвы» теперь распознается как склероатрофический лишай вульвы. Термин «лейкоплакия» не является диагностическим симптомом и носит описательный характер, поскольку некоторые заболевания могут быть представлены белыми бляшками. Термин «склероатрофический лишай» был сокращен до «склеротического лихена», поскольку некоторые случаи связаны с гипертрофическим, а не атрофическим эпителием.
Склероатрофический лишай у взрослых женщин
Склероатрофический лишай у девочек
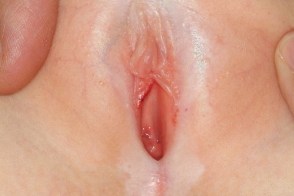 Поражения аналогичны тем, что у взрослых женщин, но экхимоз может быть более выраженным и потенциально ошибочным в качестве доказательства сексуального насилия.Милия также может временно присутствовать при лечении и лечении без лечения.Перианальные очаги часто встречается у молодых девушек, вызывая запор из-за болезненных трещин в этой области. Поражения аналогичны тем, что у взрослых женщин, но экхимоз может быть более выраженным и потенциально ошибочным в качестве доказательства сексуального насилия.Милия также может временно присутствовать при лечении и лечении без лечения.Перианальные очаги часто встречается у молодых девушек, вызывая запор из-за болезненных трещин в этой области. |
Склероатрофический лишай у взрослых мужчин
Склероатрофический лишай у мальчиков
Экстрагенитальная форма
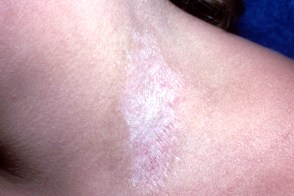 Классическими местами для экстрагенитальных поражений являются верхняя часть туловища, подмышечные впадины, ягодицы и боковые бедра, и это чаще всего встречается у взрослых женщин. Более редкие локализации включают рот, лицо, кожу головы, руки, ноги и ногти. Типичными поражениями являются фарфоро-белые бляшки, которые могут иметь фолликулярные пробки и участки экхимоза, похожие на генитальные поражения. Экстрагенитальную форму СЛ трудно отличить от ограниченной склеродермии. Клинические типы экстрагенитальных поражений включают обширную буллезную форму, а также кольцевидные, блашкоидные и кератотические варианты. Коэбнеризация очень распространена на участках давления, старых хирургических и лучевых рубцах и на месте травмы. Классическими местами для экстрагенитальных поражений являются верхняя часть туловища, подмышечные впадины, ягодицы и боковые бедра, и это чаще всего встречается у взрослых женщин. Более редкие локализации включают рот, лицо, кожу головы, руки, ноги и ногти. Типичными поражениями являются фарфоро-белые бляшки, которые могут иметь фолликулярные пробки и участки экхимоза, похожие на генитальные поражения. Экстрагенитальную форму СЛ трудно отличить от ограниченной склеродермии. Клинические типы экстрагенитальных поражений включают обширную буллезную форму, а также кольцевидные, блашкоидные и кератотические варианты. Коэбнеризация очень распространена на участках давления, старых хирургических и лучевых рубцах и на месте травмы. |
Осложнения
Биопсия целесообразна, если есть атипичные признаки или диагностическая неопределенность и является обязательным, если есть подозрение на неопластические изменения. Пациентам, находящимся под наблюдением, требуется биопсия, если:
Скрининг аутоантител для поиска ассоциированного аутоиммунного заболевания полезен, если есть клинические признаки, указывающие на аутоиммунное расстройство. В частности это заболевания щитовидной железы.
Микробиологическое исследование показано при эрозивной форме болезни для исключения простого герпеса или кандидоза, которые могут осложнять течение заболевания.
Имеются противопоказания.Проконсультируйтесь с врачом
Что такое склероатрофический лишай
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Склероатрофический лихен вульвы: современный взгляд на проблему
Журнал: Российский вестник акушера-гинеколога. 2018;18(6): 41-50
Зароченцева Н. В., Джиджихия Л. К. Склероатрофический лихен вульвы: современный взгляд на проблему. Российский вестник акушера-гинеколога. 2018;18(6):41-50.
Zarochentseva N V, Dzhidzhikhiia L K. Lichen sclerosus et atrophicus: modern view on the problem. Russian Bulletin of Obstetrician-Gynecologist. 2018;18(6):41-50.
https://doi.org/10.17116/rosakush20181806141
Московский областной НИИ акушерства и гинекологии
Представлены современные данные литературы об этиологии, патогенезе, особенностях развития, диагностике и основных методах консервативной терапии склероатрофического лихена вульвы в разные возрастные периоды. Полиэтиологичность, недостаточная изученность причин возникновения, наличие спорных вопросов патогенеза, поздняя диагностика, низкая эффективность существующих схем лечения обусловливают диагностические и лечебные сложности, способствуют затяжному течению заболевания с развитием тяжелых осложнений. Поиск и внедрение новых, эффективных методов лечения склероатрофического лихена являются актуальной проблемой современной гинекологии.
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Проблема профилактики и лечения рака вульвы относится к одному из малоизученных вопросов гинекологии. До настоящего времени не разработана концепция патогенеза данного заболевания, остается много спорных моментов в трактовке доброкачественных дистрофических и предраковых состояний. Злокачественные заболевания чаще всего развиваются на фоне длительно существующих дистрофических процессов [1, 2]. Особую группу в структуре гинекологической патологии занимают неопухолевые поражения вульвы, именовавшиеся ранее хроническими дистрофическими заболеваниями. В течение долгого времени данная патология считалась прерогативой женщин климактерического и постменопаузального периода [1, 2]. Однако за последние десятилетия прослеживается тенденция ее «омоложения», так как дистрофические заболевания вульвы диагностируются в репродуктивном возрасте. Риск их малигнизации колеблется от 10 до 35%. Ранее подобные изменения классифицировали как «крауроз» и «лейкоплакию», позже их выделили в группу «вульварной дистрофии», нозологическими формами которой являются склероатрофический лишай (lichen sclerosus) и плоскоклеточная гиперплазия (squamous cell hyperplasia).
Склероатрофический лихен вульвы
Склероатрофический лихен вульвы (САЛВ) — один из медленно развивающихся хронических воспалительных дерматозов с выраженной очаговой атрофией кожи и слизистых оболочек, наиболее часто поражающих вульву и приводящих к деформации вульвы и обусловленным ею функциональным нарушениям [1, 2].
Историческая справка. Впервые склероатрофический лихен был описан в 1885 г. A. Breisky [3, 4] для характеристики белесоватых изменений на вульве у пациенток в постменопаузе. Медицинскому сообществу САЛВ был «представлен» в 1887 г. H. Hallopeau. В течение всего периода изучения и наблюдения было предложено много названий данного заболевания — каплевидная склеродермия, болезнь «белых пятен», белый лишай Цумбуша, крауроз вульвы [5]. В зарубежной литературе САЛВ чаще встречается под названием lichen sclerosus.
Согласно определению ВОЗ, САЛВ — это хроническое воспалительное заболевание вульвы неизвестной этиологии с периодами обострений и ремиссий. Выделяют два пика заболеваемости САЛВ: девочки до периода полового созревания и женщины в постменопаузальном периоде. Средний возраст дебюта заболевания у девочек — 5,4 года, а у женщин — 55,1 года.
Эпидемиология. Распространенность у женщин в среднем составляет 1,7%, а в детском возрасте — около 0,1% из числа обследованных; при этом распространенность САЛВ колеблется в пределах от 1:30 до 1:1000 у женщин, 1:900 у девочек [2]. Единой классификации заболевания нет, и в российских федеральных клинических рекомендациях для дерматовенерологов САЛВ рассматривается в разделе «Локализованная склеродермия», шифр которого по МКБ10 — L94.0.
Классификация
Разнообразие клинических проявлений послужило причиной выделения следующих форм САЛВ:
— папулезная — характеризуется наличием отдельных плоских папул, располагающихся на внутренней поверхности больших половых губ без распространения на перианальную область и оставляющих после себя белесоватые участки поверхностной атрофии (субъективные ощущения обычно выражены слабо);
— эритематозно-отечная — сопровождается наличием участков атрофии кожи белесоватого цвета на фоне выраженной гиперемии и отека больших половых губ, иногда с распространением на перианальную область, характерна для пациенток с отягощенным аллергологическим анамнезом;
— витилигинозная является довольно распространенной формой, которая проявляется очагами поверхностной атрофии и депигментации, трещинами слизистой оболочки, часто ошибочно расценивается как лейкоплакия или витилиго, также протекает без субъективных ощущений;
— атрофическая форма определяется наличием четко отграниченной атрофии слизистой оболочки по типу «папиросной» бумаги с радиальной складчатостью тканей и частым вовлечением перианальной области, протекает либо без субъективных ощущений либо с жалобами на сухость и дискомфорт в области наружных половых органов;
— буллезная форма характеризуется упорным течением с возникновением субэпидермальных пузырей с серозным и/или геморрагическим содержимым на фоне атрофии и гиперемии слизистой оболочки, у пациенток появляются жалобы на жжение, зуд;
— эрозивно-язвенная — отличается спонтанным образованием кровоточащих болезненных эрозий или язвенных дефектов на фоне гиперемии и атрофии слизистой оболочки без предшествующего образования пузырей.
Предложенная классификация основана лишь на клинических проявлениях и не является официально принятой [6].
Этиология
Этиология САЛВ остается невыясненной. Поражение вульвы и перианальной зоны зачастую появляется без определенных причин. По результатам немногочисленных исследований предположена мультифакторность данного состояния, включающая в том числе влияние аутоиммунных, инфекционных и гормональных предикторов возникновения. Так, к примеру, показана связь клинических проявлений САЛВ и дебюта аутоиммунных заболеваний у взрослых пациенток. В литературе представлены указания на наличие высоких уровней аутоантител как у взрослых, так и у детей с САЛВ. Описаны поражения САЛВ у членов одной семьи — девочки-близнецы, мать и дочь, отец и дочь. При этом авторами описано выявление одинаковых HLA-антигенов у родственников и однотипных склероатрофических поражений вульвы, особенно у девочек-близнецов [2, 6].
Развитие заболевания обусловлено множеством составляющих — наследственных, относящихся к клеточному иммунитету, и аутоиммунных, гормональных, инфекционных, местных. Роль гормональных факторов подтверждается тем, что заболевание чаще начинается на фоне дефицита эстрогенов в детстве и постменопаузе, а также на фоне расстройства метаболизма андрогенов. Однако этиологическая роль гормонов не доказана в полной мере.
Развитие склероатрофического лихена связывают с присутствием патогенных микроорганизмов, особенно спирохеты Borrelia burgdorferi, но истинным возбудителем она не является. Также сомнений в значении местных воздействий — от расчесов до радиоактивного облучения как пусковых факторов заболевания нет [1, 2, 5].
Жалобы
На начальных стадиях заболевания женщин беспокоят парестезии с легким покалыванием и ощущением «ползающих мурашек». Вариант первого проявления САЛВ — ярко выраженный зуд в области наружных половых органов. Ведущим симптомом является спорадически проявляющийся (чаще в ночное время суток) упорный, длительный зуд вульвы. Длительное течение заболевания может приводить к истощению нервной системы, тяжелым нервно-психическим расстройствам, потере трудоспособности, диспареунии. Большинство женщин отмечают вульводинию — болезненность, жжение, чувство сухости, напряжения и стягивания кожно-слизистых покровов вульвы [7—11]. Нередко САЛВ может протекать бессимптомно.
Клиническая картина
Клинические проявления САЛВ у молодых и у пожилых женщин отличаются. У девочек чаще всего обнаруживается гиперемия кожи вульвы и перианальной области в сочетании со спонтанным появлением петехий и язв, что зачастую ошибочно воспринимается специалистами как последствия травмы.
Для САЛВ характерны истончение и депигментация кожи, образование рубцов, повышенная чувствительность кожи, дизурия, диспареуния. При осмотре выявляют типичные белые атрофические сморщенные папулы и бляшки в области преддверия влагалища с захватом клитора, малых половых губ, внутренней поверхности больших половых губ и кожи вокруг ануса в форме так называемой «восьмерки». Визуально отмечается локальная бледность, наличие тонких, белесоватых, морщинистых бляшек (лихенификация), что ведет к отеку и сморщиванию структур вульвы. Позднее наступает утрата пигментации, появляется мраморно-белая окраска, истончение и атрофия кожных покровов [2, 12].
В 98% наблюдений выявлено поражение всех структур вульвы. Одновременное поражение промежности отмечается в 48% наблюдений. Из-за прогрессирующей атрофии постепенно уменьшаются и исчезают клитор и малые половые губы. В конечной стадии заболевания вход во влагалище сужается и даже полностью закрывается. При этом кожа мацерированная, тонкая, «пергаментообразная», легко трескается, становится похожей на смятую «папиросную бумагу» [2]. Поражение промежности может быть очаговым, в виде немногочисленных изолированных белых папул или отдельно мелких бляшек. Реже отмечается диффузная гиперемия с трещинами, диффузная гипопигментация или витилиго, наиболее редко развивается буллезная форма. Часто эти варианты сочетаются. Расчесы приводят к вторичным изменениям — кровоизлияниям, эрозиям, ссадинам, трещинам, коркам. Обусловленная расчесами травма способствует расширению области поражения в промежности. Возникает утолщение кожи, иногда — бородавчатые разрастания. Глубокие ссадины, кровоизлияния и рубцы на вульве детей иногда ошибочно расценивают как следы изнасилования [1, 2].
Диагностика
Диагноз ставят на основании клинической картины и подтверждают гистологическими результатами, полученными после проведения биопсии вульвы. В свою очередь своевременная диагностика и корректный подбор терапии неоспоримо важны у юных и молодых пациенток для улучшения их самочувствия и профилактики риска развития плоскоклеточного рака вульвы при упорном или часто обостряющемся течении заболевания. Так, по данным разных авторов, у 60% женщин при отсутствии инфицирования ВПЧ плоскоклеточный рак вульвы ассоциировался с длительно существующим САЛВ.
Несмотря на яркие клинические проявления и достаточно серьезные возможные последствия, спектр методов уточняющей диагностики ограничен. Ведущими методами продолжают оставаться клинический осмотр, микроскопическое и молекулярно-генетическое исследование вульварных и вагинальных мазков-соскобов, реже — вульвоскопия с использованием стандартной увеличительной оптики. Следует учитывать, что САЛВ может маскироваться под любые бактериальные, грибковые, аллергические и даже травматические сопутствующие поражения вульвы [2, 6]. После проведения биопсии вульвы могут быть выявлены следующие гистологические изменения: атрофия эпидермиса с гиперкератозом и гидропической дистрофией базального слоя, отек верхнего слоя дермы, гомогенизация коллагена, в нижнем слое — мононуклеарная воспалительная инфильтрация [12].
Дифференциальная диагностика
Дифференциальный диагноз на ранних стадиях следует проводить со следующими заболеваниями [1, 2, 13—15]:
— при нейродермите — эпителий утолщен, уплотнен, суховат, кожный рисунок усилен с воспалительными папулами коричневато-розового цвета, кожа гиперемирована, шагреневидная, зуд проявляется и на других участках тела;
— для витилиго типично отсутствие пигментации, иногда легкий зуд, отсутствуют атрофические изменения;
— для красного плоского лишая — множественные сгруппированные папулезные высыпания с атрофическими изменениями или склерозированием с образованием келлоидоподобных рубцов;
— при сахарном диабете — выраженный зуд вульвы, ткани наружных половых органов отечны, имеют «тестоватую» консистенцию, резко гиперемированы.
Как хронический воспалительный дерматоз с длительным течением циклов «зуд—расчесы—зуд» и образованием рубцов САЛВ является пусковым фактором канцерогенеза или способствует ему. По-видимому, к развитию злокачественного новообразования вульвы предрасполагает также нарушение регуляции иммунных процессов.
Одной из первоначальных мер является устранение раздражающих факторов, бережный уход за вульвой, лечение вторичной инфекции, местное применение эстрогенов, препятствующее атрофии вульвы и влагалища. Это заключается в соблюдении диеты (исключение острой, соленой, сладкой пищи, кофеинсодержащих продуктов, алкоголя) и правил интимной гигиены (ограничение/исключение мылосодержащих средств, дезодорантов, синтетического белья, прокладок, тампонов). При выраженных проявлениях зуда рекомендовано назначение десенсибилизирующей терапии и седативных средств [2].
Наиболее широко распространенным и рекомендуемым «золотым стандартом» лечения САЛВ является местное применение мазей с ультрапотентными кортикостероидами [16], особенно 0,05% мази клобетазола пропионата. Противовоспалительные свойства клобетазола наиболее эффективны в лечении САЛВ, что выражается в уменьшении воспаления и предотвращении прогрессирования состояния и последующего рубцевания. Топические ультрапотентные кортикостероиды являются терапией первой линии при лечении САЛВ (мометазона фуроат, клобетазола проприонат (Ib, A). В опубликованных в 2014 г. клинических рекомендациях Американской ассоциации детских и подростковых гинекологов предложено в качестве препаратов первой линии использовать глюкокортикоидные препараты высокой степени активности в длительном режиме. Они обладают следующими эффектами:
— антигиперпластическое воздействие на пролиферирующие поверхностные слои кожи;
— антиаллергические, местноанальгезирующие и противозудные свойства;
— ингибирующее влияние на функции клеточного и гуморального иммунитета.
Суммируя рекомендации по лечению САЛВ у детей с учетом уровня доказательности, американские коллеги представили их следующим образом:
1. Терапия у пациенток с САЛВ должна начинаться с использования глюкокортикоидных препаратов высокой степени активности. Уровень II-2 B.
2. Существуют ограниченные данные, обосновывающие возможность использования иммуномодуляторов как при неэффективности лечения, так и при отказе пациенток от препаратов с глюкокортикоидами. Уровень II-3 B.
3. САЛВ следует подозревать у детей при наличии жалоб на различные нарушения мочеотделения и дефекации, в том числе дизурию и дисхезию. Уровень C.
У пациенток с САЛВ необходимо исключить аутоиммунные заболевания. Следует также отметить, что диагностика САЛВ у детей и подростков не требует обязательного проведения биопсии вульвы. Биопсия кожных покровов вульвы может проводиться лишь при наличии подозрительных на атипию участков кожи вульвы и перианальной области и/или при стойкой резистентности к терапии.
Пациентки с САЛВ требуют обязательного наблюдения каждые 6—12 мес для оценки жалоб, исключения изменений архитектоники вульвы и перианальной области, а также в целях профилактики возможного риска малигнизации [6].
Как было уже отмечено, при лечении САЛВ используют сверхмощные кортикостероиды клобетазол или галобетазол в виде 0,05% мазей. Поскольку рецидивы могут быть частыми, длительными и могут привести к атрофии и рубцеванию, рекомендуется долгосрочная поддерживающая терапия, считающаяся более безопасной. Поскольку рандомизированных контролируемых исследований, сравнивающих потенцию стероидов, нет, то частоту применения и длительность лечения каждому пациенту подбирают на индивидуальной основе. По результатам исследования М. Gurumurthy и соавт. [17] сообщили, что при испытании мази клобетазола пропионата полной ремиссии удалось достигнуть у 66% пациенток и у 30% был получен частичный ответ на лечение. Рубцы не прогрессировали. И, наоборот, улучшения не было у 75% пациенток без лечения, а прогрессирование рубцов наблюдалось у 35% женщин [17].
В зависимости от выраженности клинического эффекта современные топические кортикостероиды (ТКС) разделяют на четыре группы [3, 18, 19] (табл. 1):

— препараты слабой активности (гидрокортизон 1%, преднизолон 0,5%, фторцинолона ацетонид 0,0025%);
— препараты умеренного действия (алклометазона дипропионат 0,05%, бетаметазона валерат 0,025%, клобетазола бутират 0,05%, дезоксиметазон 0,05%, флуметазона пивалат 0,02 и 2%);
— препaраты сильного действия (бетаметазона валерат 0,1%, бетаметазона дипропионат 0,025 и 0,5%, бутезонид 0,25%, фторлоролона ацетонид 0,025%, фторциноид 0,05%, фторцинолона ацетонид 0,025%, триамцинолона ацетонид 0,02, 0,1% и 2%, метилпреднизолона ацепонат 0,1%, гидрокортизона 17-бутират 0,1%, мометазона флуорат 0,1%);
— препараты с очень сильной активностью (клобетазола пропионат 0,05%, дифторкортолона валерат 0,05%, галцинонид 0,1%).
Среди кортикостероидов выделяют галогенизированные (фторированные) и негалогенизированные [18—20]. Фторированные кортикостероиды (дексаметазон, бетаметазон, флуметазон, триамцинолон, клобетазол, флутиказон, флуоцинолон, флуметазон), как правило, обладают большей противовоспалительной активностью, но чаще приводят к возникновению побочных эффектов. К негалогенизированным кортикостероидам относят производные преднизолона (мометазона фуорат, метилпреднизолона ацепонат, гидрокортизона ацетат и гидрокортизона 17-бутират) [3, 20].
Слизистые оболочки вульвы относительно устойчивы к стероидам, что предполагает для достижения хорошего эффекта использование мазей с максимальной стероидной потенцией. На протяжении 2—3 мес их накладывают ежедневно, далее 3 раза в неделю тонким слоем на вульву. В окружности заднего прохода, где кожа тоньше, мазь ежедневно накладывают 4 нед с последующим переходом на трехразовое введение в неделю, а позднее — однократное или двукратное применение в неделю. Об эффективности лечения свидетельствует значительное уменьшение количества трещин, эрозий, кровоизлияний и утолщенных белых очагов. Полностью, даже при эффективном лечении, они исчезают не всегда.
Режимы дозирования могут быть использованы различные. Один из самых частых — ежедневное использование стероидов высокой и максимальной степени активности: один раз в день в течение 3 мес. У детей для избежания атрофии кожи ТКС используются еженедельно в течение 3 мес.
Применение ТКС дважды в день имеет дополнительную пользу в дебюте склероатрофического лихена. Проактивная поддерживающая терапия с двукратным использованием мази мометазона фуроата 0,1% эффективна и безопасна при поддержании ремиссии и может помочь предотвратить возникновение злокачественных изменений (Ib, A). Применение 30 г стероида максимальной степени активности должно продолжаться 3 мес.
В постменопаузе необходимо длительное, на протяжении 6 мес., применение кортикостероидов максимальной активности. За 12 нед в 77—90% наблюдений удается добиться значительного улучшения и исчезновения жалоб, а в 23% наблюдений — полного исчезновения изменений кожи. Длительное лечение позволяет поддержать ремиссию заболевания надолго. Больная должна находиться под наблюдением всю жизнь. При утолщенных гипертрофированных, резистентных к лечению очагах может быть эффективно введение в них триамцинолона [1]. Применение ТКС в сочетании с антибактериальными и противогрибковыми средствами, например гентамицином или фузидиновой кислотой и нистатином или азольными противогрибковыми средствами, может быть целесообразным при присоединении вторичной инфекции. Они могут быть использованы на короткий период времени для элиминирования инфекции (IV, C).
Аллергическая реакция к любой кортикостероидной мази может проявиться после длительного использования. Следует учитывать, что ТКС способны изменять проявления некоторых заболеваний кожи, что может затруднить постановку диагноза. Кроме того, применение ТКС может быть причиной задержки заживления ран [21].
При проведении долгосрочной местной терапии кортикостероидами в аногенитальной области выявляются серьезные побочные эффекты:
— реакция «рикошета», возникающая при внезапном прекращении терапии и проявляющаяся в форме дерматита с интенсивным покраснением кожи и ощущением жжения;
— развитие грибковых инфекций;
— подавление функции надпочечников в результате системной абсорбции.
Согласно результатам исследований [2], было доказано, что все побочные эффекты быстро разрешаются по мере уменьшения активности топических кортикостероидов и кратности их применения.
Подбор лечебной тактики САЛВ базируется на теоретических предположениях. Терапия пациенток, страдающих САЛВ, связана с полипрагмазией, так как должна помочь устранить одновременно явления атрофии, гиперкератоза, уменьшить микроциркуляторные нарушения, воспаление, улучшить заживление эрозий на коже вульвы и промежности. Однако нецелевое использование антисептиков, антибиотиков, противовирусных и иных групп препаратов зачастую усиливает активность патологического процесса и распространение САЛВ. При склероатрофическом лихене для предупреждения нарастающего рубцевания и раннего выявления злокачественного новообразования, риск которого не велик, но реален, необходимо длительное наблюдение. Как правило, лечение приводит к длительной ремиссии. Ее отсутствие — повод усомниться в диагнозе. Возможно осложнение контактным дерматитом как реакция на местное лечение или избыточно тщательное соблюдение гигиены, инфекцией, развитием рака вульвы. Неэффективность местной кортикостероидной терапии часто связана с нарушением режима ее применения пациенткой, в том числе в связи с непониманием или невозможностью полноценного нанесения мази из-за ожирения или артрита. Рубцы могут быть болезненными.
По данным European guideline for the management of vulval conditions 2016 г., пациентки с САЛВ нуждаются в лечении [21]. Около 10% пациенток не имеют зуда, но у них есть клинические признаки склероатрофического лихена, и они должны также лечиться (IV, C).
В последние годы ведется дискуссия среди специалистов о необходимости продолжения дальнейшего лечения при купировании первоначальных симптомов. Это связано с тем, что нет данных об активности заболевания на тот момент. Однако указано, что САЛВ может развиваться дальше и приводить к рубцеванию, несмотря на недостаток симптомов после профилактического лечения, пациентам показана непрерывная терапия в течение многих лет для предотвращения прогрессирования (IV, C).
Срок длительности наблюдения в течение 5 лет показал, что непрерывное лечение индивидуально подобранным кортикостероидом предотвращает прогрессирование симптомов, дальнейшее рубцевание и развитие карциномы соответственно в 58% наблюдений против 93,3%, в 40% против 3,4% и в 0% против 4,7% [21].
Одним из представителей современного поколения ТКС является отечественный комбинированный препарат для наружного применения — тетрадерм (табл. 2).

Фармакодинамика
Активность препарата обусловлена фармакологическими свойствами компонентов, входящих в его состав.
Гентамицин — антибиотик широкого спектра действия из группы аминогликозидов. Обладает бактерицидным действием, активен в отношении грамотрицательных микроорганизмов: Pseudomonas aeruginosa, Aerobacter aerogenes, Escherichia coli, Proteus vulgaris, Klebsiella pneumoniae; грамположительных микроорганизмов: Staphylococcus aureus (коагулазоположительные, коагулазоотрицательные и некоторые штаммы, продуцирующие пенициллиназу).
Декспантенол — производное пантотеновой кислоты. Стимулирует регенерацию кожи, нормализует клеточный метаболизм, ускоряет митоз и увеличивает прочность коллагеновых волокон. Проникает во все слои кожи. Оказывает при этом слабое противовоспалительное действие.
Мометазон — синтетический КС, оказывает местное противовоспалительное, противозудное и антиэкссудативное действие, индуцирует выделение белков, ингибирующих фосфолипазу А2 и липокортины, которые контролируют биосинтез медиаторов воспаления (простагландины и лейкотриены, клеточные медиаторы воспаления) путем торможения высвобождения их общего предшественника — арахидоновой кислоты.
Эконазол — синтетическое производное имидазола. Оказывает противогрибковое и антибактериальное действие, тормозит биосинтез эргостерола, регулирующего проницаемость клеточной стенки микроорганизмов. Он легко растворяется в липидах и хорошо проникает в ткани, активен в отношении дерматофитов Trichophyton, Microsporum, Epidermophyton, дрожжеподобных грибов рода Candida, Corynebacterium minutissimum, а также Malassezia furfur (Pityrosporum orbiculare), вызывающего отрубевидный лишай, и некоторых грамположительных бактерий (стрептококки, стафилококки).
Показания к применению препарата Тетрадерм
Лечение дерматозов воспалительного генеза с сопутствующей бактериальной и микотической инфекцией или высокой вероятностью присоединения вторичной инфекции (простой и аллергический дерматиты, атопический дерматит (в том числе диффузный нейродермит), ограниченный нейродермит, экзема, дерматомикозы (дерматофития, кандидоз, разноцветный лишай), особенно при локализации в паховой области и крупных складках кожи; простой хронический лишай (ограниченный нейродермит).
Способ применения и дозы
Наружно. Крем наносят на пораженные участки кожи тонким слоем, осторожно втирая, 2 раза в сутки до достижения положительного клинического результата. Длительность лечения индивидуальна, зависит от размера, локализации поражения и тяжести заболевания и обычно составляет 1—2 нед. Более 4 нед применять тетрадерм не рекомендуется.
Препараты второй линии терапии САЛВ
Топические ингибиторы кальциневрина (ТИК) — пимекролимус, такролимус — оказывают дерматотропное, иммунодепрессивное, противовоспалительное местное действие, специфично связываются с цитозольным рецептором макрофилином-12 Т-лимфоцитов и ингибируют кальцийзависимую фосфатазу — кальциневрин. В настоящее время ТИК рекомендуются в качестве терапии второй линии при САЛВ. Крем пимекролимус 1% является иммунодепрессантом, который ингибирует активацию Т-клеток, блокируя транскрипцию ранних цитокинов, и таким образом значительно уменьшает зуд, жжение и воспаление, связанное с САЛВ. Кроме того, предотвращает высвобождение провоспалительных цитокинов, медиаторов воспаления из тучных клеток in vitro в ответ на стимуляцию антигеном IgE, не влияет на кератиноциты, фибробласты и эндотелиальные клетки.
Несмотря на тот факт, что ТИК могут обеспечить эффективное облегчение симптомов, топический клобетазол превосходит пимекролимус в плане уменьшения воспаления и улучшения клинической картины. Однако крем пимекролимус имеет более приемлемый профиль безопасности и не вызывает кожной атрофии, хотя его использование связано с повышенным риском развития осложнений из-за подавления местного иммунитета. В результате ТИК следует назначать под наблюдением специалиста, который может контролировать потенциальный риск озлокачествления САЛВ. Учитывая доказанную эффективность и безопасность топических кортикостероидных средств, эксперты сходятся во мнении, что ТИК должны быть зарезервированы для случаев САЛВ, не отвечающих на терапию топическими кортикостероидами [2].
ТИК применяют наружно 2 раза в сутки, наносят тонким слоем на пораженные участки кожи и осторожно втирают до полного впитывания. Лечение продолжают до полного исчезновения симптомов. При первых признаках рецидива терапию следует возобновить. При сохранении симптомов заболевания в течение 6 нед следует провести повторную оценку состояния больного.
Наиболее известные формы ТИК:
1. Такролимус — мазь Протопик 0,03 и 0,1%. Среди нежелательных эффектов этого препарата: ощущение жжения и зуда, покраснение, боль, раздражение, сыпь в месте нанесения, развитие фолликулита и акне. Зарегистрированы единичные случаи малигнизации (кожные и другие виды лимфом, рак кожи).
2. Пимекролимус — крем Элидел 1%. Из побочных эффектов отмечают жжение в месте нанесения крема, развитие импетиго и кожных инфекций, ринит, крапивница.
Наиболее актуальным представляется 0,03% мазь такролимуса для эффективного лечения детей с аногенитальным склероатрофическим лихеном 2 раза в неделю, при этом возможно сокращение рецидивов (ІІІА, B). Сравнение препаратов пимекролимуса (1% крема) и клобетазола пропионата (0,05%) крема показало улучшение симптомов зуда, жжения, боли через 12 нед после появления склероатрофического лихена вульвы, при этом клобетазол был использован для быстрого купирования воспалительного процесса (Ib, A). Другие исследования пимекролимуса показали, что 42% пациенток находились в «полной ремиссии» после 6 мес применения (IIb, B). Местное раздражение было наиболее распространенным побочным эффектом при использовании такролимуса и пимекролимуса. Долгосрочные риски применения ТИК должны быть еще изучены, так как существуют опасения по поводу возможности повышения риска злокачественного развития местной иммуносупрессии при длительной терапии САЛВ [21].
Эмолленты
Одним из важных компонентов терапии САЛВ являются эмолленты (англ. emollient — смягчающий) смягчающие и увлажняющие средства. Эти средства не содержат потенциальные аллергены, такие как пропиленгликоль и ланолин, могут минимизировать местное воспаление, увеличивают содержание влаги в роговом слое кожи, усиливают ослабленную барьерную функцию кожи и уменьшают субклиническое воспаление [2].
Согласно результатам исследования, проведенного T. Simonart и соавт. [22], выявлено, что более 50% женщин, использовавших ежедневный увлажняющий крем вместе с топическими кортикостероидами, сохраняли ремиссию на протяжении 58 мес. А более 2/3 женщин прекратили использование топических кортикостероидов оставаясь длительно на эмоллентах.
По источнику происхождения эмолленты делятся на растительные (натуральные), химические и синтетические. Растительные эмолленты — это, прежде всего, натуральные масла. Они смягчают кожу и защищают ее, делают упругой. Они абсолютно безвредны. Сюда можно отнести популярные косметические масла: персиковое, оливковое, жожоба. К химическим эмоллентам относят парафин, вазелин и мази на его основе («Прополисная», «Календула»), минеральные масла. Синтетические эмолленты получают в промышленных условиях путем проведения различных реакций и смешивания жирных кислот, эфиров и других составляющих. Это циклометиконы, диметиконы и синтетические масла. Наиболее известными и изученными являются средства линейки эмолиум, локобейз рипеа, липикар.
Эффекты воздействия эмоллентов:
— начинают действовать сразу после нанесения на кожу, снижая испарение влаги за счет эффекта окклюзии;
— при дальнейшем проникновении в роговой слой липиды замещают недостающие липиды эпидермиса и сохраняют влажность кожи на протяжении нескольких часов (среднесрочное воздействие);
— липиды достигают более глубоких слоев кожи и поступают в опустевшие «кладовые» — пластинчатые тельца, при необходимости высвобождаются для поддержания водно-липидного баланса кожи (долгосрочное воздействие).
Эстрогенсодержащие препараты
Данная группа средств обладает пролиферативным действием, не оказывая системного эффекта на эндометрий и молочные железы [23, 24]. Крем Орниона — один из самых современных отечественных препаратов, который содержит эстриол — аналог естественного женского гормона. Эстриол применяется для коррекции дефицита эстрогенов у женщин в период пре- и постменопаузы. Эффективен при лечении урогенитальных нарушений. В случае атрофии эпителия влагалища и шейки матки, что имеет место при САЛВ, эстриол купирует эти нарушения, способствует восстановлению нормальной микрофлоры и физиологического рН влагалища, тем самым повышая устойчивость эпителия влагалища к инфекционным и воспалительным процессам. В отличие от других эстрогенов, эстриол взаимодействует с ядрами клеток эндометрия в течение небольшого промежутка времени, благодаря чему при ежедневном применении рекомендованной суточной дозы не происходит пролиферации эндометрия. Таким образом, нет необходимости в циклическом дополнительном назначении прогестагенов, а в постменопаузальном периоде не наблюдается кровотечений «отмены».
Показания к применению:
— заместительная гормональная терапия (ЗГТ) для лечения атрофии слизистой оболочки нижних отделов мочевыводящих и половых путей, связанная с дефицитом эстрогенов у женщин в постменопаузе;
— пред- и послеоперационная терапия у женщин в постменопаузе, которым предстоит или уже проведена операция влагалищным доступом;
— с диагностической целью при неясных результатах цитологического исследования эпителия шейки матки на фоне атрофических изменений (как вспомогательное средство).
Противопоказания к применению:
— установленная повышенная чувствительность к активному веществу или к любому из вспомогательных веществ препарата;
— нелеченная гиперплазия эндометрия;
— установленный, имеющийся в анамнезе или подозреваемый рак молочной железы;
— диагностированные эстрогенозависимые опухоли или подозрение на них (например, рак эндометрия);
— кровотечение из влагалища неясной этиологии;
— тромбозы (венозные и артериальные) и тромбоэмболии в настоящее время или в анамнезе (в том числе, тромбоз глубоких вен, тромбоэмболия легочной артерии, инфаркт миокарда, инсульт), цереброваскулярные нарушения;
— состояния, предшествующие тромбозу (в том числе транзиторные ишемические атаки, стенокардия) в настоящее время или в анамнезе;
— врожденная или приобретенная предрасположенность к развитию артериальных или венозных тромбозов, например дефицит протеина С, протеина S или антитромбина III;
— заболевание печени в острой стадии или заболевание печени в анамнезе, после которого показатели функции печени не вернулись к норме;
— беременность и период грудного вскармливания.
Способ применения и дозы
Крем Орниона следует вводить во влагалище перед сном при помощи калибровочного аппликатора. Одна доза (при заполнении аппликатора до кольцевой метки) содержит 0,5 г крема Орниона, что соответствует 0,5 мг эстриола. Курс лечения заключается в назначении эстриола в дозе 500 мкг в сутки в течение 2—3 нед ежедневно, далее переход на поддерживающую дозу 1—2 раза в неделю. Небольшая часть разовой дозы наносится непосредственно на вульву, а остальная во влагалище дозатором. При отслоении гиперпластических бляшек — усиление болевых ощущений, которые являются быстропроходящими.
Крем Орниона может применяться как у женщин с гистерэктомией в анамнезе, так и у женщин с интактной маткой. При проведении ЗГТ для лечения атрофии слизистой оболочки нижних отделов мочевыводящих и половых путей, связанной с дефицитом эстрогенов у женщин в постменопаузе, проводится одно внутривлагалищное введение крема ежедневно в течение не более двух недель до облегчения симптомов. Далее доза постепенно снижается до поддерживающей в зависимости от клинической картины (например, одно введение 2 раза в неделю).
При пред- и послеоперационной терапии у женщин в постменопаузе, которым предстоит или уже проведена операция влагалищным доступом, пр