что такое синдром торс
SARS (Severe Acute Respiratory Syndrome), или ТОРС (тяжелый острый респираторный синдром)
Тяжелый острый респираторный синдром — ТОРС (Severe Acute Respiratory Syndrome, SARS) — термин, предложенный ВОЗ, вместо принятого ранее — «атипичная пневмония». В конце 2002 г. — в ноябре-декабре — в западных провинциях Китая, в Гонконге
Тяжелый острый респираторный синдром — ТОРС (Severe Acute Respiratory Syndrome, SARS) — термин, предложенный ВОЗ, вместо принятого ранее — «атипичная пневмония».
В конце 2002 г. — в ноябре-декабре — в западных провинциях Китая, в Гонконге, Вьетнаме, Сингапуре были отмечены первые случаи тяжелых острых респираторных заболеваний, привлекшие внимание врачей, обративших внимание на необычное течение данной воспалительной реакции дыхательных путей. Раньше в этой географической зоне были описаны вспышки микоплазменной пневмонии. Здесь высок процент заболеваний легких (бронхиальная астма, другие легочные болезни). В 97-99 гг. прошлого века были описаны спорадические случаи заболевания, которое в настоящее время трактуется как «тяжелый острый респираторный синдром». Тяжелый — так как у болезни плохой прогноз; острый — потому что начинается остро, как грипп; респираторный — потому что затронуты дыхательные пути; синдром, так как человек умирает не от пневмонии, а от отека легких. Удалось идентифицировать, что эти случаи вызваны коронавирусом.
Общая летальность составляет около 4%, с резкими колебаниями в разных возрастных группах.
Возбудитель SARS — один из представителей коронавирусов. Он был идентифицирован 17 марта 2003 г. По материалам ВОЗ было установлено, что возбудитель SARS представляет собой новый тип коронавируса.
Коронавирусы — крупные РНК, содержащие вирусы, способные вызывать заболевания у людей и животных. По антигенным свойствам разделяются на три группы. К первой принадлежат респираторный коронавирус человека 229Е, коронавирусы кошек, собак, свиней. Ко второй — человеческий вирус ОС43, вирус гепатита мышей и коронавирус телят. Третья группа включает в себя кишечные коронавирусы человека и вирусы инфекционного бронхита птиц.
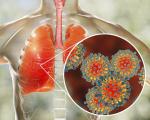
Официально установлено, что SARS вызывает новый коронавирус, который ранее никогда не встречался у человека и животных. Новый вирус назвали SARS-ассоциированным коронавирусом. Изображение его получено с помощью электронной микроскопии.
Вирионы имеют сферическую форму диаметром 80–160 нм. Поверхность вириона покрыта булавовидными отростками, длиной около 20 нм, придающими вирионам форму короны.
Вирионы содержат плюс-цепь полиаденилированной РНК длиной 16–30 kb (коронавирусы обладают самым большим геномом, превосходящим геном других вирусов в три раза). Геномная нить (+) РНК коронавирусов, состоящая из одной цепочки, способна транслироваться на рибосомах клетки хозяина. Вирионы образуются почкованием от мембран шероховатого эндоплазматического ретикулума или аппарата Гольджи. Зрелые вирионы формируются внутри клеток до того, как вирусные белки будут экспрессированы на поверхности клеток. Вышедшие вирионы способны вновь сорбироваться на поверхности клеток, вызывая их слияние и стимулируя иммунный ответ хозяина. Основными клетками-мишенями являются клетки альвеолярного эпителия.
Вирус обнаружен в мокроте, плазме (в остром периоде); в фекалиях — в период реконвалесценции. Обладает относительно высокой устойчивостью в окружающей среде. Сохраняется на открытых поверхностях до трех часов. Быстро инактивируется дезинфицирующими средствами. Официально эпидемия SARS началась в феврале 2003 г. К апрелю 2003 г. очаги инфекции были зарегистрированы в 32 странах мира. Общее число заболевших составляет около 8,5 тыс. Причем 5 тыс. пациентов зарегистрировано в Китае. Хотя к концу мая 2003 г. официально эпидемия закончилась, но спорадические случаи по-прежнему регистрируются. Основной путь передачи воздушно-капельный, но не исключена и возможность передачи при прямом контакте. Восприимчивость невысокая, о чем свидетельствует небольшое число заболевших. Болезнь зарегистрирована только среди взрослых. Наибольшему риску заражения подвергаются лица пожилого возраста.
Коронавирусы обладают широким тропизмом и могут поражать помимо дыхательных путей печень, почки, кишечник, нервную систему, сердце и глаза. Типичная коронавирусная инфекция клинически проявляется гриппоподобным синдромом и/или кишечными расстройствами. При коронавирусной инфекции поражается альвеолярный эпителий. Коронавирусы, обладая способностью к индукции апоптоза, вызывают некроз пораженных тканей, а у пациентов после выздоровления остаются фиброзные рубцы в легких. Коронавирусы, индуцируя слияние клеток оказывают сильное воздействие на проницаемость клеток, что приводит к нарушению водно-солевого баланса и транспорта белков. Вероятно, в этих условиях развиваются недостаточность сурфактанта (антиателектатический фактор), что приводит к коллапсу альвеол, и легочный дистресс-синдром. Наиболее опасным свойством коронавирусов является их способность поражать макрофаги. Вероятнее всего, заболевание в особо тяжелой форме развивается на фоне блокирования основных звеньев иммунного ответа.
Клиническая картина
Инкубационный период от трех до пяти, максимум до 10 суток. Болезнь начинается остро, как грипп: высокая температура, головная боль, кашель, артралгии, миалгии. Начальная фаза может длиться от трех до семи суток. Заболевания средней тяжести и тяжелые формы связаны с развитием коронавирусной пневмонии. На фоне не очень тяжелых катаральных явлений процесс быстро поражает нижний отдел респираторного тракта и характеризуется развитием долевой, многоочаговой или сливной пневмонии. Клинически это проявляется резким ухудшением состояния больного. Температура снижается до субфебрильных цифр, потом резко повышается до 39-40°С, появляются упорный непродуктивный кашель, затруднение дыхания, нарастают симптомы дыхательной недостаточности, которая прогрессирует. В ряде случаев физикальные изменения не определяются, но могут выслушиваться мелкопузырчатые хрипы и определяться участки притупления перкуторного звука. В 80% случаев дальнейшее состояние больного улучшается и наступает выздоровление, а в 10—20% болезнь прогрессирует. Развивается острый респираторный дистресс-синдром. Отмечено, что для SARS не характерны реакция корней легких, увеличение медиастинальных лимфатических узлов, выпот в плевральную полость и распад легочной ткани. От SARS погиб один из вирусологов, представитель ВОЗ, итальянец Карло Урбани, умер профессор-патологоанатом из Китая, производивший вскрытие погибшего от SARS жителя Вьетнама. Раньше предполагали, что человек от человека этим заболеванием заразиться не может. Эта точка зрения не подтвердилась. Однако родственники, находившиеся рядом с больными, не заболевали. Значит, для заражения необходим очень тесный контакт с пациентом, особому риску в связи с этим подвергаются врачи, медицинские сестры, технический персонал, проводившие определенные манипуляции на дыхательных путях.
На основании одной лишь клинической картины SARS можно только заподозрить. Важно отметить, что в клинической картине отсутствуют сыпь, полиаденопатия, гепатолиенальный синдром, острый тонзиллит, поражение нервной ткани.
Общий анализ крови выявляет лимфопению, лейкопению, тромбоцитопению. Биохимический анализ крови показывает высокий уровень ЛДГ, АСТ. R-логически у большинства больных обнаруживаются множественные очаги просветления неправильной формы, склонные в дальнейшем к слиянию. Очаги в легочной ткани имеют место у всех пациентов. При клиническом ухудшении очаги поражения быстро увеличиваются. SARS рентгенологически может быть неотличим от других тяжелых форм пневмонии. Используется ПЦР-диагностика. ИФА может быть задействован только для ретроспективного анализа.
При исследовании биопсийного материала обнаруживалась картина интерстициального воспаления с разрушением альвеолярных пневмоцистов. Постмортальные гистологические изменения соответствовали патоморфологической картине респираторного дистресс-синдрома.
При исследовании печени — мелкодисперсная жировая инфильтрация, точечный некроз гепатоцитов, селезенки — обширные поля ишемического некроза.
Врачам и медицинскому персоналу рекомендуется соблюдать правила санитарно-эпидемического режима, работать в перчатках, маске, съемном халате, защитных очках.
Среди мер защиты особое место принадлежит выявлению не только больных, но и контактировавших с ними лиц, людей, прибывших из регионов, признанных очагами этой инфекции, с последующей изоляцией до 10 суток под медицинским наблюдением.
Скрининг за предполагаемыми случаями тяжелого острого респираторного синдрома для выбывающих из областей, представляющих эпидемиологическую опасность
Рекомендациями ВОЗ установлена система взаимодействия с операторами аэропортов и другим персоналом: пассажиры, депортируемые по интернациональным линиям из опасных областей, опрашиваются (предпочтительно работниками здравоохранения) в пункте отправления до прохождения контроля. В ходе опроса следует установить:
Лица, в отношении которых имеется подозрение на атипичную пневмонию, должны быть направлены в инфекционную больницу. Люди, у которых отмечается только лихорадка, должны быть отделены от остальных пассажиров, после чего за ними устанавливается медицинское наблюдение.
Если у пассажира, следующего из эпидемиологически неблагополучной зоны, выявляется заболевание, сопровождающееся респираторными синдромами и лихорадкой, рекомендуется:
Рекомендации для пассажиров, находившихся в непосредственном контакте с больным
Если медицинские службы устанавливают, что больной пассажир имеет подозрительные симптомы, все остальные пассажиры направляются в местные медицинские службы для последующего наблюдения.
Если у пассажира имеются симптомы, указывающие на возможность наличия SARS, необходимо выполнить следующие действия.
Методы лечения SARS
Способов высокоэффективного лечения SARS в настоящее время не существует. Лица с симптомами SARS подлежат лечению в стационаре под постоянным контролем врача и полной изоляции от других пациентов. Из-за тяжести заболевания лечение следует начинать как можно скорее, по симптоматическим показателям, до подтверждения диагноза (см. таблицу 1).
Противовирусные препараты (рибавирин орально или внутривенно). Рибавирин — это пуриновый нуклеозид с широким спектром действия и антивирусной активностью, имеет сходство с гуанозином. Доказана активность этого препарата в отношении большого числа РНК-содержащих вирусов. Из-за относительно высокой токсичности рибавирина его применения следует избегать у лиц с дефектами иммунной системы (новорожденные, люди старше 65 лет, реципиенты органов и костного мозга, ВИЧ-положительные больные), а также у пациентов, проходящих курс терапии с использованием других препаратов — нуклеозидных аналогов (ацикловир, ганцикловир и т. д.).
Антибактериальные препараты. Антибиотики не действуют на коронавирус — этиологический агент SARS, но предотвращают присоединение вторичной бактериальной флоры, а также могут воздействовать на бактерии, вызывающие нетипичные пневмонии невирусного происхождения, эти средства могут использоваться до постановки окончательного диагноза.
Индукторы интерферона, в частности циклоферон, рекомендуются для профилактики и лечения SARS.
Стероидные гормоны орально или внутривенно применяют для снятия воспалительных симптомов и предупреждения отека легкого.
Может назначаться также легочный сурфактант BL.
Комбинированная терапия рибавирином и глюкокортикостероидами основана на положительном клиническом эффекте от их применения. Наилучший результат получен врачами госпиталя в Гонконге при назначении пациентам больших доз комбинированной терапии рибавирином и глюкокортикостероидами.
Наиболее эффективной признана следующая схема лечения больных с подтвержденным и предполагаемым диагнозом тяжелого острого респираторного синдрома.
Антибактериальная терапия
Комбинации рибавирина и метилпреднизолона назначаются при наличии следующих условий.
Пульс-терапия метилпреднизолоном
Условие — наличие двух признаков из нижеперечисленных:
Необходимой терапевтической процедурой при SARS является применение бронходилататоров с помощью небулайзера (альбутерол 0,5 мг через небулайзер совместно с кислородом в объеме 6 л в минуту, четыре раза в день, на протяжении семи дней). В качестве диагностических и лечебных процедур в этом случае рассматриваются также бронхоскопия, эндотрахеальная интубация для проведения искусственной вентиляции легких в случае гипоксемии без признаков левожелудочковой недостаточности.
Вакцины для профилактики коронавирусной инфекции
Несмотря на распространенность коронавирусов, разработка вакцин против инфекций, вызываемых ими, фактически не проводилась. Ни одна из стран не обладает даже ограниченным опытом конструирования и лабораторных испытаний коронавирусных вакцин.
Стратегия создания коронавирусных вакцин должна базироваться на следующих положениях.
Разработка инактивированной вакцины на основе коронавируса SARS или близких к нему изолятов.
Получение субъединичной вакцины с использованием поверхностных антигенов коронавирусов SARS.
Получение рекомбинантов с ослабленной вирулентностью путем генно-инженерного конструирования плазмидных ДНК-вакцин.
В настоящее время в НИИ гриппа РАМН подготовлены базы данных и материалы для конструирования ДНК-вакцины против коронавирусной инфекции, вызванной SARS.
Литература
Н. В. Астафьева, кандидат медицинских наук, доцент
Е. Г. Белова, кандидат медицинских наук
МГМСУ, Москва
Что такое синдром торс
ТОРС – это воспалительная патология легочной ткани вирусной этиологии. Характеризуется нарастающей тяжелой дыхательной недостаточностью вследствие респираторного дистресс-синдрома. Клиническая картина также включает в себя лихорадку, сухой кашель, выраженную одышку. Диагностика осуществляется с помощью молекулярно-генетических методов (выявление возбудителя) и серологических исследований (поиск антител). Лечение заболевания преимущественно патогенетическое и симптоматическое, этиотропного препарата с доказанной вирулицидной эффективностью в настоящее время не разработано.
МКБ-10
Общие сведения
ТОРС (тяжелый острый респираторный синдром, SARS, ранее – атипичная пневмония) является инфекционной патологией нижних дыхательных путей. Впервые сообщения о болезни начали поступать из больниц провинции Гуандонг (Китай) в 2002г. SARS быстро распространился по стране, во Вьетнаме, Сингапуре, Гонконге. К маю 2003г. инфекцией были охвачены все континенты, ВОЗ объявила о пандемии ТОРС. Возбудитель – новый коронавирус – был открыт в апреле 2003г. Наиболее подвержены заражению оказались пожилые люди, гендерной разницы выявлено не было. Особенностью данной пандемии было большое число нозокомиальных заражений.
Причины ТОРС
Характеристика воздудителя
Возбудитель инфекции – РНК-содержащий коронавирус SARS–CoV. Представляет собой сферический микроорганизм с шиповидными выростами, тропизмом к клеткам альвеол, печени, кишечника, также почек, сердца, глаза. Резервуар инфекции в дикой природе – летучие мыши, источник – больной или бессимптомный носитель. Основной путь передачи – воздушно-капельный, также передача вируса может осуществляться контактным и гораздо реже ‒ фекально-оральным путем.
Факторы риска
Основные факторы риска: возраст старше 65 лет, иммунные дефициты, связанные с ВИЧ-инфекцией, онкологическими болезнями, приемом системных кортикостероидов. К уязвимой группе относят лиц с заболеваниями легких, сердечно-сосудистой системы, сахарным диабетом, ожирением. Высока вероятность заболевания у медицинских работников, лиц, осуществляющих уход за больными дома.
Патогенез
При попадании на слизистую рото- и носоглотки коронавирусы колонизируют эпителий. Они имеют различные механизмы связи с рецепторами. Так, с эпителиальными клетками взаимодействие происходит посредством аминопептидазы. Ведущая роль в механизме связывания с рецепторами клеток человека принадлежит гликопротеину шиповидных отростков. Вышедшие вирионы способны вновь сорбироваться на поверхности клеток, вызывая их слияние и стимулируя иммунный ответ хозяина.
Основными клетками-мишенями являются клетки альвеолярного эпителия, макрофаги. Коронавирусы, обладая способностью к индукции апоптоза, вызывают некроз пораженных тканей. Индуцирование слияния клеток оказывает сильное воздействие на их проницаемость, приводит к нарушению водно-солевого баланса и транспорта белков. В этих условиях развивается недостаточность сурфактанта, возникают симптомы легочного дистресс-синдрома.
Симптомы ТОРС
Первые симптомы тяжелого острого респираторного синдрома возникают после инкубационного периода, который составляет 5 дней (от 2 до 10 суток). Обычно пациенты предъявляют жалобы на гриппоподобный синдром: лихорадку более 38,5°C, ознобы, головную боль. Отмечается выраженная слабость, боли в мышцах, снижение работоспособности. К концу первой недели болезни или к началу второй появляется сухой мучительный кашель, который при коронавирусной инфекции обычно беспокоит больных по ночам.
Наиболее грозным проявлением ТОРС является одышка. Пациенты отмечают нарастающее чувство нехватки воздуха, особенно в ночные часы, при разговоре или натуживании, затруднение, как вдоха, так и выдоха. Позднее больные вынуждены принимать позу с опорой на руки, дыхание становится хриплым, шумным, кожа приобретает багрово-синюшный оттенок. Параллельно могут возникать першение, сухость в горле, симптомы диареи.
Осложнения
Наиболее частые осложнения ТОРС возникают из-за прогрессирующей дыхательной недостаточности. Самые грозные последствия ‒ тромбоэмболия легочной артерии, миокардит, перикардит, спонтанный пневмоторакс, сердечная недостаточность и нарушения ритма сердца. Также наблюдаются повторные пневмонии, фиброзные изменения в легких. Имеются сообщения об обнаружении коронавирусов в ликворе у больных рассеянным склерозом.
Диагностика
Диагностика коронавирусной инфекции, её лечение осуществляется совместно врачами-инфекционистами, пульмонологами, реаниматологами. Другие медицинские специалисты привлекаются по показаниям. Важен сбор эпидемиологического анамнеза, включая данные о путешествиях в эндемичные районы, семейных, рабочих контактах больного. Основные клинические, инструментальные и лабораторные методы диагностики ТОРС:
Дифференциальная диагностика
Схожие клинические симптомы наблюдаются при гриппе, респираторно-синцитиальной вирусной патологии, MERS, что требует их лабораторной верификации. Необходимо дифференцировать ТОРС с пневмониями, вызванными Haemophilus influenzae, Mycoplasma pneumoniae, Chlamydia species, реже Legionella species, Сoxiella burnetii, пневмококком. Дифференциальный диагноз проводится с ХОБЛ, бронхоэктатической болезнью, анафилаксией.
Лечение ТОРС
Симптомы SARS, выявляемые у пациента, являются показанием к госпитализации, за исключением легких случаев, когда допускается амбулаторное лечение с соблюдением правил самоизоляции, обязательным медицинским контролем состояния. Стационары должны быть оборудованы палатами интенсивной терапии, реанимационными отделениями. Специфической диеты нет, питьевой режим вне противопоказаний не ограничивается.
Консервативная терапия
Стандартизированное лечение ТОРС отсутствует. Предпочтительна симптоматическая терапия: жаропонижающие, препараты сурфактанта, дезинтоксикационные и иные средства. Использование системных кортикостероидов увеличивает риск внутрибольничных инфекций ‒ диссеминированных грибковых заболеваний, нарушений обмена веществ, остеонекроза. Данные препараты, назначаемые на ранних стадиях ТОРС, могут пролонгировать виремию.
Вирус ТОРС склонен к нозокомиальному распространению, поэтому использование небулайзеров, спейсеров и кислородотерапии через назальные катетеры либо маску должно быть запрещено или строго ограничено. При нарастании дыхательной недостаточности, респираторных симптомов дистресс-синдрома пациент переводится на ИВЛ. По показаниям применяется ЭКМО.
Экспериментальное лечение
Лечение с использованием рибавирина не доказало своей эффективности при ретроспективном исследовании. Применение высоких доз препарата приводило к задокументированному снижению гемоглобина у 59% пациентов, среди 36% больных регистрировался гемолиз, были отмечены гепатотоксичные, кардиотоксичные эффекты. Сочетание с лопинавиром/ритонавиром снижало частоту интубаций, а также общую смертность до 2,3%.
Лопинавир, бустированный ритонавиром, является препаратом для терапии ВИЧ-инфекции. Лечение с введением данного средства при ТОРС показало снижение вирусной нагрузки коронавируса, позволяло уменьшить дозу метилпреднизолона. Ингибирующим эффектом на возбудителя также обладал интерферон альфакон-1, однако исследование проводилось всего на 9 пациентах, сопровождалось приемом кортикостероидов и не было контролируемым.
Лечение при помощи пассивной иммунизации с помощью плазмы выздоровевших больных использовалось на небольшом числе пациентов, однако имело эффект в виде значительного снижения смертности по сравнению с плацебо либо отсутствием терапии. Наилучшие результаты получены в группе инфицированных ТОРС, которым вводили плазму не позднее 14-го дня болезни. Также предлагалась концепция человеческих моноклональных антител.
Прогноз и профилактика
Прогноз при своевременном выявлении, отсутствии соматической декомпенсированной патологии благоприятный. Летальность ТОРС составляет около 4%, варьирует от 0 до 40% в зависимости от исходного состояния заболевшего. Специфическая профилактика (вакцина) находится в стадии разработки. Неспецифические меры: использование масок заболевшими, частое мытье рук с мылом, кашлевой этикет, в медицинских учреждениях – строгое соблюдение санитарных норм.
Литературный обзор Тяжёлый острый респираторный синдром (ТОРС), вызываемый коронавирусом.
С.В. Нетёсов, В.М. Блинов, Т.Ю. Иванькина, Г.М. Игнатьев, М.И. Кисурина,
Г.Г. Онищенко, Л.С. Сандахчиев.
Заболевание «атипичная пневмония» или тяжёлый острый респираторный синдром (ТОРС) или Severe Acute Respiratory Syndrome (SARS) является вновь выявленным заболеванием, которое впервые возникло в китайской провинции Гуандун, в середине ноября 2002 года и было первоначально описано доктором Карло Урбани в Гонконге. К настоящему времени по данным ВОЗ больные атипичной пневмонией зарегистрированы в 28 странах мира. При этом общее число заболевших на 17 мая 2003 года составило 7761 человек, в том числе 623 смертельных исхода. Заболевание зарегистрировано в 32 странах, наибольшее количество в Китае, Сингапуре, Канаде.
Рис.1 Эпидемическая кривая возможных случаев SARS с 1 января по 22 апреля 2003 года по дате начала болезни [2]
Классификация инфекционного агента.
В состав семейства Коронавирусов входят род Коронавирусы и род Торовирусы. Род Коронавирусы объединяет большие, оболочечные, позитивные одноцепочечные РНК-содержащие вирусы, которые вызывают широко распространенные заболевания человека и животных. Его представители могут быть выделены в три серологические подгруппы (Таблица 2). Внутри каждой серогруппы вирусы классифицированы согласно их естественным хозяевам, нуклеотидным последовательностям и серологическим взаимосвязям [6].
Серотипы и хозяева коронавирусов.
| Антигенная группа | Вирус | Хозяин |
| Human coronavirus 229E (HcoV-229E) Porcine Transmissible gastroenteritis virus (TGEV) Porcine respiratory coronavirus (PRCoV) Canine Coronavirus (CcoV) Feline enteric coronavirus (FECoV) Feline infectious peritonitis virus (FIPV) Rabbit coronavirus (RbCoV) | Человек Свиньи Свиньи Собаки Кошки Кошки Кролики | |
| Human coronavirus OC43 (HcoV- OC43) Murine hepatitis virus (MHV) Sialodacryoadenitis virus (SDAV) Porcine hemagglutinating encephalomyelitis (HEV) Bovine coronavirus (BcoV) Turkey coronavirus (TcoV) | Человек Мыши Крысы Свиньи Крупный рогатый скот Индюки | |
| Avian infectious bronchitis virus (IBV) Turkey coronavirus (TcoV) | Курицы Индюки |
Секвенирование генетического материала коронавируса, выделенного у больных ТОРС (SARS), было впервые проведено одновременно и независимо в лабораториях американских Центров по контролю и профилактике заболеваний (CDC) и канадского «Vanderbild University Medical Center». По полученным данным размер генома возбудителя ТОРС (SARS) составляет 29727 п.о. и 29736 п.о. соответственно [8, 9].
Также получены данные по секвенированию нескольких изолятов вируса SARS китайскими исследователями (Institute of Microbiology and Epidemiology of the Academy of Military Medical Sciences and the Beijing Genomics Institute of Chinese Academy of Sciences) [10]. Сравнение последовательностей этих изолятов с данными, представленными американскими и канадскими учеными, позволяет предположить, что вирус может быстро мутировать [11].
По мнению исследователей из Bernard Nocht Institute of Tropical Medicine в Гамбурге, вирус ТОРС (SARS) по нуклеотидным последовательностям отличается на 50-60 % от трёх известных групп коронавирусов, но, несомненно, является типичной вариацией среди существующих групп 2 и 3 коронавирусов [12].
Филогенетический анализ, проведенный различными исследователями на основании сравнения нуклеотидных и аминокислотных последовательностей участков гена полимеразы, представлен на Рисунках 2, 3.
Рисунок 2. Филогенетическое дерево с максимально возможной достоверностью, построенное на основе выравненных последовательностей 405 нуклеотидов открытой рамки считывания 1b гена полимеразы коронавируса (номера нуклеотидов с 15173 по 15578 на основе полного генома коронавируса крупного рогатого скота инвентарный номер NC_003045), для сравнения коронавируса SARS с другими коронавирусами человека и животных.
На дереве видны три основные антигенные группы в Роду коронавирусов (I, II и III), представленные человеческим коронавирусом 229E (HcoV-229E), собачьим коронавирусом (CcoV), вирусом инфекционного кошачьего перитонита (FIPV), вирусом инфекционного гастроэнтерита свиней (TGEV), вирусом эпидемической диареи свиней (TGEV), человеческим коронавирусом OC43 (HcoV-OC43), коронавирусом крупного рогатого скота (BcoV), гемагглютинирующим вирусом энцефаломиелита свиней (HEV), вирусом крысиного сиалодакриоаденита (SDAV), вирусом гепатита мышей (MHV), коронавирусом индюков (TcoV) и вирусом инфекционного бронхита птиц (IBV). Значения бутстрепов для автоматической компенсации погрешностей (на основе 100 повторов), полученные из дерева консенсуса на основе 50 % принципа большинства, показаны на основных внутренних ветвях филограммы. Длины ветвей пропорциональны количеству нуклеотидных межштаммовых замен.[13]
Рисунок 3. Филогенетический анализ частичной белковой последовательности (215 аминокислот) коронавируса SARS [14].
Cравнение полных геномов коронавирусов не позволяет выявить наиболее близкий к вирусу SARS геном, хотя наибольшее число совпадающих линий наблюдается между SARS и бычьим коронавирусом 2-ого типа (рис. 4). Поэтому эволюционные сравнения необходимо проводить по кластерам генов (рис. 5-7). Хотя и здесь разбиение на кластеры также сопряжено с трудностями. В некоторых участках генома вируса SARS наблюдается наибольшее сходство с бычьим коронавирусом, в других участках генома вируса SARS, наоборот, сходство между птичьим коронавирусом и вирусом SARS выше. Правда, при этом степень гомологии очень низка со всеми известными коронавирусами. Блочный тип эволюции (и возможные точки рекомбинации) можно просчитать более точно, но для этого необходимо время и информация по структуре большего числа штаммов коронавирусов.
Ниже приводится сравнение аминокислотных последовательностей генов полимеразы (POL), матриксного (M) и оболочечного (VGL) белков; для других белков выравнивать последовательности практически невозможно, поскольку сходство между ними меньше 20 %. Для двух известных короновирусов человека (штамм 229E и OC43)- ситуация уникальная: наиболее близкий к вирусу SARS штамм OC43 (но для этого штамма нет полной структуры генома), а штамм 229E настолько не похож на вирус SARS, что говорить о каком-то сходстве вообще нельзя. С одной стороны имеется группа короновирусов (бычий/мышиный/человеческий OC43), с другой стороны группа (свиной/кошачий/собачий/человеческий 229E) и наконец группа (птичьи) и все эти три группы равноудалены от вируса SARS. Говорить о блочной рекомбинационной природе агента SARS пока можно только для мышиных коронавирусов, для которых известны структуры 6 полных геномов, для них существуют, по крайней мере, четыре точки рекомбинации в одном геноме. Для остальных коронавирусов такой информации пока нет.
Как видно из приведенных на Рис.4 матриц сравнения и филогенетических деревьев, возбудитель SARS (ТОРС) наиболее близок к бычьему коронавирусу. Известно, что так называемые «бычьи» вирусы, как правило, оказываются также и вирусами мелких грызунов и даже кошек, живущих вместе или рядов с коровами. Поэтому гипотеза о кошачьей природе возбудителя ТОРС (SARS) имеет законные права на существование.
Рис. 4. Матрица сравнения полного генома вируса SARS c геномами других коронавирусов другими коронавирусами
Рис. 5. Матрица сравнения POL гена вируса SARS c геномами других коронавирусов
Рис. 6. Матрица сравнения M гена вируса SARS c геномами других коронавирусов
Рис. 7. Матрица сравнения VGL гена вируса SARS c геномами других коронавирусов.
При доказательстве этиологической роли коронавируса SARS, как возбудителя «атипичной пневмонии» все исследования в 13 лабораториях проводились с учетом постулатов Коха: возбудитель должен обнаруживаться у всех больных с данным заболеванием; он должен быть выделен из хозяина и культивирован в чистой культуре; и культура выделенная таким образом должна воспроизводить болезнь у других организмов, с подъемом уровня специфических антител после заражения.
Как удалось в настоящее время выяснить, коронавирусы были обнаружены у более чем 50 % больных, значительная часть изолятов была культивирована в чистой культуре, у больных с выявленным агентом ТОРС был обнаружен подъем антител, и заражение обезьян этим возбудителем дало клиническую картину, характерную для ТОРС [5].
Клиника и лечение «атипичной пневмонии».
С момента возникновения «атипичной пневмонии» уже собрано много материала, который позволяет представить клиническую картину этого заболевания. В совместной публикации ВОЗ, СDC и Health Canada были суммированы данные историй болезни пациентов с диагнозом ТОРС (SARS) начиная с середины февраля 2003 [15].
26 марта ВОЗ были опубликованы результаты проведения виртуального круглого стола, в котором участвовали 80 клиницистов из 13 стран занимающихся исследованием «атипичной пневмонии» [16].
По мнению специалистов, клиническая картина ТОРС(SARS) выглядит следующим образом.
Инкубационный период обычно 2-7 дней; однако в отдельных случаях может достигать 10 дней.
Клинические признаки в начале заболевания неспецифические. Начало болезни в подавляющем большинстве случаев характеризуется высокой температурой > 38° С, сопровождающейся ознобом, миалгией, головными болями и сухим кашлем. Сыпь, неврологические или желудочно-кишечные признаки обычно отсутствуют, однако в некоторых случаях отмечалась диарея в начальном периоде во время лихорадочного состояния.
Через 3-7 дней наступает стадия, связанная с поражением нижних дыхательных путей и появлением характерного сухого кашля, одышки, которая может сопровождаться прогрессирующей гипоксимией. На этой стадии больные разделяются на две группы. У большинства, 80-90 % заболевших, в течение последующих 6-7 дней наблюдается улучшение состояния и симптоматики. Во второй, меньшей группе проявляется более тяжелая форма «атипичной пневмонии» у многих пациентов развивается острый респираторный дистресс синдром и требуется искусственная вентиляция лёгких. Смертность во второй группе высока, и может быть связана с наличием у больных, кроме ТОРС, других заболеваний. Характерные изменения на рентгеновских снимках лёгких могут отмечаться уже через 3-4 дня после появления первых симптомов заболевания, но в некоторых случаях рентгеновские снимки могут оставаться нормальными в течение первой недели и даже всего заболевания.
При прогрессировании болезни рентгенологические исследования показывают у большинства больных двусторонние изменения в виде внутритканевых инфильтратов (жидкость накапливается между клетками в лёгких), которые развиваются в более генерализованные образования. Эти инфильтраты дают на рентгеновских снимках специфическую картину лёгких, испещренных пятнами.
Лабораторные тесты часто показывают лимфопению, среднюю тромбоцитопению и повышенный уровень печеночных ферментов.
При отсутствии диагностических тест систем на ТОРС (SARS), и сложности дифференцированной диагностики атипичной пневмонии в начале заболевания, в CDC были разработаны критерии для выявления подозрительных и предполагаемых случаев.
К «подозрительным случаям» следует относить респираторные заболевания неизвестной этиологии и соответствующие следующим критериям:
· Повышение температуры выше 38° С
· Наличие одного или более клинических признаков респираторного заболевания (кашель, учащенное или затрудненное дыхание, гипоксия)
· Путешествие в течение 10 дней в пораженные SARS районы мира или общение с больными подозрительными по данной болезни.
При выявлении «предполагаемых» случаев следует учитывать такие критерии как:
· Подтверждение пневмонии на рентгеновских снимках или респираторный дистресс синдром
· Данные аутопсии, соответствующие респираторному дистресс синдрому без идентифицируемых причин [18].
Кстати, очень неплохие результаты были получены нашими учеными при использовании тетрациклина для лечения вирусного клещевого энцефалита, что отчасти связано с его иммуномодулирующими свойствами. Это позволяет предположить, что препарат может рассматриваться и испытываться, как потенциальное средство в терапии ТОРС (SARS) [19].
В качестве основного противовирусного препарата для лечения ТОРС (SARS) наиболее широко врачами в очагах заболевания используется рибавирин, один или в сочетании со стероидными препаратами. Показано, что он обладает противовирусной активностью, в том числе и по отношению к коронавирусам. Однако, некоторые исследователи высказывают критическое отношение к применению этого препарата, отмечая случаи ухудшения состояния больных при его приёме, хотя давно известны негативные побочные эффекты этого препарата [17]. В отсутствие контролируемых испытаний препаратов, у CDC в настоящее время нет четких рекомендаций как о возможности использования рибавирина и путях его введения (внутрь, внутривенно и/или в виде аэрозоля), так и о необходимости терапии гликокортикоидами [20].
Видимо, применение интерферона и других препаратов этой группы в первые три дня должно снижать тяжесть заболевания, хотя это также требует доказательства.
Таким образом, на настоящий момент терапия ТАРС (SARS) является главным образом патогенетической и симптоматической.
В начале апреля в газетах появились сообщения об использовании гонконгскими врачами в качестве лекарственного препарата против вируса SARS плазмы крови пациентов, благополучно перенесших инфекцию. Врачи из Госпиталя Принца Уэльского (Гонконг) с помощью переливания плазмы крови переболевших людей больным смогли спасти жизни как минимум 20 больных, находившихся до переливания плазмы в критическом состоянии [21]. К сожалению пока не найдено других источников, более подробно описывающих этот опыт.
Сложная ситуация, обусловленная недавним появлением и быстрым распространением по всему миру ТОРС (SARS), побудила исследователей различных стран направить свои усилия на разработку быстрых и точных лабораторных методов диагностики этого возбудителя. Однако разработка диагностических тестов для этого заболевания продемонстрировала большую проблематичность, чем ожидалось.
В настоящее время ряд диагностикумов разработан, и они уже использовались в разных странах для идентификации возбудителя этого заболевания. Однако, по мнению ВОЗ, до тех пор, пока эти тесты не пройдут соответствующие полевые испытания, и их надежность не будет доказана, диагностика ТОРС (SARS) будет продолжать зависеть от клинических данных, подтверждающих, что атипическая пневмония не вызвана какой-либо другой причиной и контактом с пациентом, предположительно или вероятно больного SARS, или с выделениями из его респираторного тракта и других физиологических жидкостей. Это требование отражено в современном определении предполагаемого и вероятного случая ТОРС (SARS), данном ВОЗ [22] Тем не менее, в некоторых странах (Канада, Франция, Германия, Гонконг, Япония, Нидерланды, Сингапур, Великобритания и США) с помощью этих тестов в экспериментальных условиях исследуются образцы предполагаемых или вероятных больных SARS.
По мнению ВОЗ, при интерпретации результатов тестов следует учитывать ряд моментов. Позитивные результаты теста показывают, что ТОРС (SARS) пациенты являются, или недавно были инфицированы SARS вирусом. В данном случае необходимо установить специфичность различных тестов.
Негативные результаты теста на SARS вирус не должны быть утверждением, что пациент не имеет SARS вируса. Причинами для негативных результатов у пациентов с ТОРС (SARS) может быть следующее:
— Пациент не инфицирован SARS вирусом; заболевание вызывается другим инфекционным агентом (вирусом, бактерией, грибами) или неинфекционной причиной.
— Некорректные результаты теста («false-negative»). Используемый тест необходимо дальше доработать для улучшения его чувствительности.
— Образцы не были собраны в то время, когда вирус или его генетический материал присутствовал (при использовании метода RT-PCR или культур клеток). Вирус и его генетический материал может присутствовать в человеке очень короткий промежуток времени, в зависимости от типа тестируемого образца.
— Образцы были собраны до развития заболевания и до того момента, как стали нарабатываться антитела (относится к ELISA и иммунофлюоресцентному анализам).
Для улучшения понимания процесса ТОРС (SARS) заболевания ВОЗ рекомендует клиницистам проводить последовательный сбор образцов от пациентов с ТОРС (SARS) и сохранять их для тестирования до того момента, когда станут доступными диагностические тесты. Это особенно важно для первичного случая, который выявляется в стране ранее не докладывавшей о ТОРС (SARS) заболевании. Рекомендации по сбору и транспортировке образцов можно найти на web-сайте CDC (США) [23].
Согласно рекомендациям ВОЗ, имеется ряд лабораторных тестов, с помощью которых можно выявить, какой вирус является причиной заболевания у человека, и в настоящее время они апробируются при диагностике ТОРС (SARS). Однако все эти тесты имеют определенные ограничения для использования в случае контролировании ситуации с ТОРС (SARS).
1. Тестирование антител.
Тестирование антител проводится методами ELISA или IFA. Метод ELISA достоверно выявляет антитела в сыворотке ТОРС (SARS) пациентов, начиная с 21-го дня после появления клинических симптомов заболевания. Следовательно, этот тест не может быть использован для выявления вирусов на ранней стадии инфекции, до того, как вирус может распространить инфекцию от одного человека к другому. Иммунофлюоресцентный метод выявляет антитела в сыворотке пациентов через десять дней после появления клинических симптомов и заболевания. Однако этот метод требует наработки в клеточной культуре SARS вируса, проведение работ в противочумной лаборатории или лаборатории BSL-3 уровня иммунофлюоресцентный микроскоп и опытного микроскописта, на что уйдет 2-4 дня.
2. Молекулярные тесты (PCR).
ОТ-ПЦР-тест позволяет выявлять генетический материал SARS-вируса из различных образцов пациента (крови, стуле, респираторных секретов или тканевых жидкостей) и на очень ранних стадиях инфекции. Более того, праймеры, которые являются ключевыми для PCR-теста, сейчас сделаны доступными сетью лабораторий ВОЗ на web сайте ВОЗ и уже используются лабораториями многих стран по всему миру. Существующие ПЦР-тесты являются весьма специфичными, но они пока что недостаточно чувствительны и дают много ложноотрицательных результатов, по которым нельзя исключить наличие SARS-вируса у пациента. Сеть лабораторий ВОЗ работает над своими протоколами и праймерами, чтобы улучшить их достоверность и надежность [23].
Результаты PCR, использующие эти праймеры, могут быть использованы в качестве дополнительной клинической оценки. Однако тесты не утверждены лицензионнно на подтверждение или исключение случаев заболевания.
В настоящее время для диагностики ТОРС (SARS) на сайте ВОЗ различными исследовательскими центрами представлены следующие данные по праймерам, которые могут быть использованы в PCR-диагностикумах.
1. Bernhard-Nocht Institute (Bernhard-Nocht Str. 74 D-20359 Hamburg, Germany).
BNIoutS/BNoutAs: sense ATGAAT TAC CAA GTC AAT GGT TAC
antisense CAT AAC CAG TCG GTA CAG CTA C
FraGment lenGth 195 bp
BNIinS/BNIAs: sense GAA GCT ATT CGT CAC GTT CG
antisense CTGTAGAAA ATC CTA GCT GGA G
Fragment length 110 bp
SAR1s/SAR1as: sense CCT CTC TTG TTC TTG CTC GCA
antisense TAT AGT GAG CCG CCA CAC ATG
Fragment length 150 bp
Amplicon sequence (BNI-1, Bernhard-Nocht Institute, Hamburg, Germany)
TACCGTAGACTCATCTCTATGATGGGTTTCAAAATGAATTACCA
AGTCAATGGTTACCCTAATATGTTTATCACCCGCGAAGAAGCTAT
TCGTCACGTTCGTGCGTGGATTGGCTTTGATGTAGAGGGCTGTCAT
GCAACTAGAGATGCTGTGGGTACTAACCTACCTCTCCAGCTAGGA
TTTTCTACAGGTGTTAACTTAGTAGCTGTACCGACTGGTTATGTTGA
CACTGAAAATAACACAGAATTCACCAGAGTTAATGCAAAACCTCC
ACCAGGTGACCAGTTTAAACATCTTATACC
2. Centers for Disease Control & Prevention (National Centers for Infectious Diseases,
Atlanta GA 30333 1600 Clifton Road, NE, MS-C12 United States)
SARS-specific primers:
Cor-p-F2 (+) 5’CTAACATGCTTAGGATAATGG 3′,
Cor-p-F3 (+) 5’GCCTCTCTTGTTCTTGCTCGC 3′,
Cor-p-R1 (-) 5’CAGGTAAGCGTAAAACTCATC 3′,
Product size:
Cor-p-F2/Cor-p-R1 :368 bp
Cor-p-F3/Cor-p-R1 :348 bp
COR-1,COR-2: sense 5′ CAC CGT TTC TAC AGG TTA GCT AAC GA 3′
antisense 5′ AAA TGT TTA CGC AGG TAA GCG TAA AA 3′
Product size: 310 bp
HKU: sense 5′ TACACACCTCAGCGTTG 3′
antisense 5′ CACGAACGTGACGAAT 3′
Product size 182 bps [23]
Лабораториям, занимающимся ТОРС (SARS) специфическими PCR-тестами, ВОЗ рекомендует принимать на вооружение качественные контрольные процедуры и объединить свои усилия, как внутри своей страны, так и с исследовательскими лабораториями ВОЗ, с целью перепроверки положительных результатов и использования положительного опыта.
Вирус в образцах ТОРС (SARS) пациентов (респираторные секреты, кровь и стул) может быть также выявлен при помощи инфицирования культур клеток и последующей наработки вируса. Выделенный вирус может быть идентифицирован как SARS вирус дополнительными тестами. Культура клеток является очень требовательным методом, однако в то же время и единственным способом показать наличие живого вируса [24,25].
По сообщениям газеты Reuters [26] немецкая биотехнологическая компания «Artus GmbH» начала распространение разработанного ее сотрудниками экспресс-теста для диагностики ТОРС (SARS). Согласно заявлению представителей компании, на разработку этого теста ушло всего две недели. Разработанная «Artus GmbH» совместно с «Bernhard-Nocht Institute for Tropical Medicine» тест-система представляет собой комплект реагентов для проведения полимеразной цепной реакции для выявления РНК коронавируса, предположительно вызывающего ТОРС (SARS). В качестве объекта для диагностики может использоваться любой биологический материал – кровь, мокрота, кал, моча, мазки со слизистой носоглотки. Собственно процедура анализа занимает не более четырех часов, причем положительные результаты могут быть получены не через две недели после инфицирования, как в случае обычных иммунологических тестов, а практически сразу же после попадания вируса в ткани.
В настоящее время компания «Artus GmbH» бесплатно поставляет тест-комплекты в страны Азии, наиболее пострадавшие от вспышки SARS, а также в Австралию, США, Скандинавские страны и Германию, где были зарегистрированы отдельные случаи заболевания [26]
В течение последней недели ученые из Канады, Гонконга, Сингапура и Атланты в США сообщили о полном секвенировании генома ТОРС (SARS) вируса [11]. Исследователи надеются, что эти знания могут стать основой для разработки более чувствительных диагностикумов и даже терапевтических средств. В геноме SARS-вируса содержится более чем 29000 нуклеотидов. Имеющиеся ОТ-ПЦР-диагностикумы пока что детектируют только 200-500 из этих нуклеотидов. Остается определить, какая область генома может быть оптимальной мишенью для диагностического реагента. Это является сейчас основной задачей для исследователей.
Для того чтобы тест стал хорошим, прежде всего, необходимо усиление его биохимической специфичности. Это способ, когда используемые реагенты должны реагировать только с мишенями вируса. В случае ДНК-диагностического теста для SARS вирусных генов, нет сомнений, что специфичность имеется. Во-вторых, необходимо, чтобы тест был высокочувствительным. Используя современные ДНК-диагностические подходы, мы можем выявлять вплоть до 500-1000 частиц в миллилитре. Биохимическая специфичность и чувствительность является реально высокой и в настоящий момент может быть обеспечена. Однако трудности заключаются в особенностях вируса. Количество выделяемого вируса, фактически, может варьировать до 10000 раз у одного пациента и до миллиона раз между пациентами. Пока неясно, где и как вирус депонируется, но известно, что имеется небольшой промежуток времени, когда вирус может быть выявлен в различных жидкостях тела, прежде всего, в слюне, затем в крови и, в заключение, в стуле [27].
Согласно официальному отчету института Beijing Genomics Китайской академии наук SARS вирус очень быстро мутирует, поэтому необходимо тщательно изучить много штаммов, чтобы создать точные диагностические тесты и эффективные способы лечения [28]. Однако, по мнению американских исследователей в настоящее время не имеется очевидных данных, которые бы показывали, что SARS вирус быстро мутирует. По их мнению, коронавирусы обладают потенциалом изменяться больше, чем другие РНК-вирусы, главным образом, потому, что их геном значительно больше и высокая частота рекомбинации является их особенностью. Они считают, что рекомбинация, вероятно, ограничивается лишь обменом фрагментами генома с близкородственными вирусами. В случае с SARS-вирусом необходимо провести тщательный филогенетический анализ для определения того, приобрел ли этот вирус какую-нибудь генетическую информацию путем рекомбинации с хорошо известными коронавирусами животных [29].
Таким образом, имеющаяся на сегодняшний день информация по последним диагностическим разработкам и по динамике развития эпидемии вселяет определенную надежду на то, что борьба c вирусной SARS-инфекцией будет успешной. Ключевыми моментами здесь, конечно, стали достаточно быстрая идентификация возбудителя вновь возникшего заболевания, секвенирование его генома и принятие жестких противоэпидемических мер в странах-очагах. Главными задачами теперь являются использование полученных знаний для лучшего понимания самой инфекции, вызывающей ТОРС (SARS), для совершенствования диагностических тестов и для скорейшей разработки методов специфического лечения и профилактики этого заболевания.
Авторы выражают благодарность сотрудникам ГНЦ ВБ «Вектор» А.В.Миронову, В.А.Терновому, Н.А.Маркович за полезные замечания, техническую помощь и участие в сборе информации для данного обзора.
Список использованной литературы
1. Cumulative Number of Reported Probable Cases of Severe Acute Respiratory Syndrome (SARS). 2003. Сайт ВОЗ. http://www.who.int/csr/sarscountry/2003_04_26/en/
3. Coronavirus never before seen in humans is the cause SARS. 2003
Сайт ВОЗ. http://www.who.int/mediacentre/releases/2003/pr31/en/print.html
6. Lai M.M.C., Holmes K.V. Coronaviridae: The viruses and their replication. Fields’ virology. vol.1. [ed. D. M. Knipe, P.M. Howley, D.E. Griffin.- 4th ed,] 2001. Lip.Wil.&Wilkins. USA. p.1163.
7. Enterz. NC_002645; NC_001846; NC_003045; NC_001451.
8. Bellini W.J., Campagnoli R.P., Icenogle J.P., et al. SARS coronavirus (SARS-CoV), Urbani strain. Unpublished. 2003. http://www.cdc.gov/ncidod/sars/pdf/nucleoseq.pdf
11. Two SARS-associated viral genomes were sequenced in Beijing. 2003. http://www.genomics.org.cn:8080/bgi/news/zhongxin/news030416-2.htm;
12. Drosten C., Gunther S., Preiser W., et al.. Identification of a Novel Coronavirus in Patients with Severe Acute Respiratory Syndrome. //N. Engl. J. Med. 2003. www.nejm.org http://content.nejm.org/cgi/reprint/NEJMoa030747v2.pdf
13. Ksiazek TG, Erdman D, Goldsmith CS et al. A Novel Coronavirus Associated with Severe Acute Respiratory Syndrome. // N. Engl. J. Med. 2003. www.nejm.org http://content.nejm.org/cgi/reprint/NEJMoa030781v3.pdf
14. Peiris J S M, Lai S T, Poon L L M, et al. Coronavirus as a possible cause of severe acute respiratory syndrome. // THE LANCET • Published online. 2003. http://image.thelancet.com/extras/03art3477web.pdf
15. Preliminary Clinical Description of Severe Acute Respiratory Syndrome.// MMWR Weekly. 2003. V.52. N12. P. 255-256. http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5212a5.htm
16. Clinical hold virtual conference on management of SARS patients. Сайт ВОЗ. 2003. www.who.int/csr/clinicansconference/en.print.html
17. Hsu L-Y, Lee C-C, Green JA, et al. Severe acute respiratory syndrome (SARS) in Singapore: clinical features of index patient and initial contacts. // Emerg. Infect. Dis. [serial online] 2003. http://www.cdc.gov/ncidod/EID/vol9no6/03-0264.htm)
18. Updated Interim U.S. Case Definition of Severe Acute Respiratory Syndrome (SARS). 2003. http://www.cdc.gov/ncidod/sars/casedefinition.htm
19. Atrasheuskaya A.V., Fredeking T.M., Ignatyev G.M. Changes in immune parameters and their correction in human cases of tick-borne encephalitis. // Clin. Exp. Immunol. 2003. V.131.
P. 148-154.
21. HK Doctors Use Antibodies to Treat Pneumonia Victims. 2003. http://www.reuters.com/newsArticle.jhtml?type=scienceNews&storyID=2477221
22. Case Definitions for Surveillance of Severe Acute Respiratory Syndrome (SARS). Сайт ВОЗ. 2003. http://www.who.int/csr/sars/casedefinition/en/
23. PCR primers for SARS developed by WHO Network Laboratories. 2003. Сайт ВОЗ. http://www.who.int/csr/sars/primers/en/
24. Heymann D. L. Status of the global SARS outbreak and lessons for the immediate future. 2003. Сайт ВОЗ. http://www.who.int/csr/sarsarchive/2003_04_11/en/tests
25. SARS: Availability and use of laboratory testing. 2003. Сайт ВОЗ. http://www.who.int/csr/sars/testing2003_04_18/en/
26. Blenkinsop P. German Firm Distributes First Sars Test Worldwide. 2003. http://www.nlm.nih.gov/medlineplus/news/fullstory_12350.html
27. Testing for the SARS virus: hopes and realities //Strait Times Interactive. 2003.
http://straitstimes.asis1.com.sg
28. Progress in genome sequencing of Chinese isolates of SARS virus. 2003.
http:// www.gpbjournal.org/sars.jsp
29. Shared mutations in the genomes of SARS coronaviruses. 2003.
http://www.biomedcentral.com/news/20030416/04