что такое синдром пфайффера
Что такое синдром пфайффера
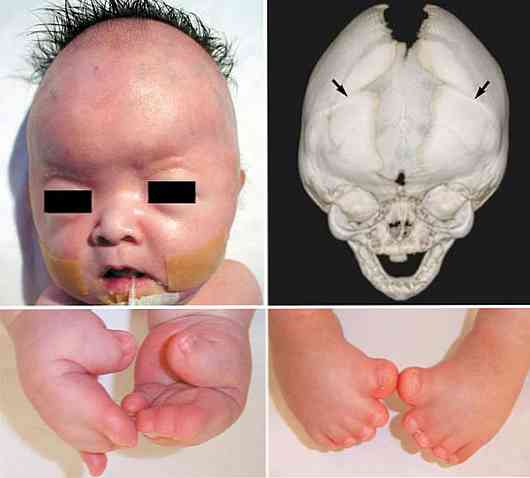
Врожденное заболевание, описанное R. Pfeiffer в 1964 году, которое характеризуется акроцефалической формой черепа, синдактилией пальцев кистей и стоп и гипертрофией больших пальцев кистей. Синдром подразделяется на три типа.
• Тип I характеризуется классическим внешним видом, проявляющимся краниосиностозом, широкими большими пальцами кисти и синдактилией, а также нормальным умственным развитием. Данная форма совместима с жизнью.
Распространенность. Неизвестна. Со времени опубликования первого описания имеются сообщения приблизительно о 30 клинических наблюдениях.
Этиология. Тип I имеет аутосомно-доминантное наследование или возникает вследствие новых мутаций. Типы II и III встречаются спорадически.
Риск рецидива. Различный, зависит от этиологии. В тех случаях, когда заболевания наследуются аутосомно-доминантно, то риск составляет 50%. Если же синдром возникает вследствие новых мутаций, то риск рецидива очень низок.
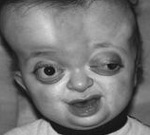
Диагностика. Эхографические признаки синдрома Пфайффера (Pfeiffer) включают черепно-лицевые аномалии (брахицефалия, акроцефалия, краниосиностоз за счет преждевременного закрытия коронарного шва, гипертелоризм, маленький нос и глубокая переносица), аномалии кистей и стоп (частичная синдактилия II и III пальцев кисти; II, III и IV пальцев стопы; широкие большие пальцы кистей и гипертрофия больших пальцев стопы).
Генетические нарушения. Синдром Пфайффера (Pfeiffer) генетически гетерогенен. Некоторые случаи связаны с мутациями гена FGFR1, локализованного в хромосоме 8р11.22-р12. Также имеются сообщения о мутациях гена FGFR2, который располагается в хромосоме 10q25-q26.
Дифференциальный диагноз. Основной дифференциальный диагноз проводится с синдромами, которые характеризуются краниосиностозами (синдром Апера (Apert), Карпентера (Carpenter), Крузона (Crouzon), аномалия Kleeblattschadel и танатофорная дисплазия).
Прогноз. Прогноз зависит от тяжести сочетанных аномалий, особенно от степени выраженности неврологическоих поражений. При типе I в большинстве случаев прогноз благоприятный, в то время как типы II и III практически несовместимы с жизнью и приводят к ранней гибели.
Акушерская тактика. Если принято решение о пролонгировании, рекомендуется проведение ультразвукового обследования в динамике для оценки степени выраженности патологии и особенно аномалий развития ЦНС.
Пфайффера синдром
OMIM 101600
Наша команда профессионалов ответит на ваши вопросы
Выделяют три типа ACS5. Классический ACS5 относится к типу 1. Тип 2 характеризуется черепом в форме клеверного листа и руками и ногами Пфайффера, а также анкилозом локтей. Тип 3 похож на тип 2, но у больных череп обычной формы. У больных отмечается тяжелый глазной проптоз, короткое переднее основание черепа. Также для типа 3 характерны различные лицевые изменения. Раннее отставание в развитии отмечается при типах 2 и 3. Эти типы описаны только как спорадические случаи.
В ряде семей было обнаружено сцепление ACS5 с 8р11.2-р11.1, где расположен ген рецептора фактора роста фибробластов-1 (FGFR1, MIM 136350). В нем найдена мутация p. 252 Pro>Arg, приводящая к ACS5. Описано несколько семей с характерными изменениями ног. Изменения черепа могут присутствовать, однако их может и не быть. Большой палец ног широкий и плоский, он обычно отклонен в сторону, также отмечается синдактилия второго и третьего пальцев. Предполагают, что при этих характерных изменениях ног даже в изолированных случаях без краниосиностоза надо проводить поиск мутации p. 252 Pro>Arg в экзоне 7a гена FGFR1.
Кроме того мутации в гене рецептора фактора роста фибробластов-2 FGFR2 (fibroblast growth factor receptor 2; MIM 176943) приводят к ACS5. Ген FGFR2 локализован на хромосоме 10q26 и состоит из 20 экзонов. Известно 26 мутаций, в основном располагающихся в экзонах 7 и 9 гена, приводящих к развитию заболевания. Однако описаны семьи, в которых отсутствует сцепление как с локусом FGFR1 на хромосоме 8, так и с локусом FGFR2 на хромосоме 10. Ряд мутаций в гене FGFR2, приводящих к ACS5, встречаются при синдроме Крузона (MIM 123500). Мутация р. 290 Trp>Cys описана при ACS5. Но в кодоне 290 описаны мутации p.290 Trp>Arg, приводящая к классической форме синдрома Крузона, и p.290 Trp>Gly, выявленная у больного атипически мягкой формой синдрома Крузона. Т.о. кодон 290 может быть основной «горячей точкой» в гене FGFR2. Другой «горячей точкой» является цистеин в положении 342. Эти два кодона локализованы в экзонах 7 и 9, кодирующих иммуноглобулинподобный домен рецептора. Отмечается эффект возраста отца при образовании мутации de novo. При исследовании происхождения мутаций de novo с помощью внутригенных полиморфных маркеров во всех информативных случаях показано их отцовское происхождение.
В Центре Молекулярной генетики проводится поиск мутаций в экзонах 7 и 9 гена FGFR2 и экзоне 7a гена FGFR1 методом прямого автоматического секвенирования.
Синдром Пфейффера, симптомы, причины, лечение
Синдром Пфейффера Это очень редкое генетическое заболевание, для которого характерно раннее слияние костей черепа с деформациями головы и лица. Эта аномалия определяется как краниосиностоз, который дает вид выпученных глаз. Кроме того, у пострадавших наблюдаются изменения в руках, такие как отклонения в пальцах и ступнях..
Он получил свое название от Рудольфа Артура Пфайффера, немецкого генетика, который в 1964 году описал 8 пациентов одной семьи, у которых были аномалии рук, ног и головы.
Он входит в группу заболеваний, которые являются результатом мутаций в генах FGFR. Например, синдром Аперта, синдром Крузона, синдром Беара-Стивенсона или синдром Джексона-Вейсса.
Типы синдрома Пфайффера
Классификация, которая была широко признана для синдрома Пфайффера, была опубликована в 1993 году Майклом Коэном. Он предположил, что три типа могут быть даны в зависимости от их серьезности, так что типы II и III являются наиболее серьезными.
Тем не менее, у этих трех типов есть общее представление о увеличенных больших пальцах рук и ног, брахидактилия (пальцы короче, чем обычно) и синдактилия (порок развития, характеризующийся врожденным соединением некоторых пальцев друг с другом)..
Совсем недавно, в частности, в 2013 году, Грейг и его коллеги разработали новую систему классификации синдрома Пфейффера, также с точки зрения степени тяжести. Они изучили 42 пациента, основываясь на их классификации по оценке неврологического статуса, дыхательных путей, глаз и ушей..
Кроме того, эти оценки проводились до и после хирургических вмешательств, чтобы наблюдать, как они развивались. Результаты указали 3 типа:
Эта последняя классификация полезна, поскольку она поощряет междисциплинарное лечение.
Какова его частота?
Синдром Пфейффера затрагивает оба пола в равной степени и приблизительно встречается в 1 из каждых 100 000 рождений.
Каковы его причины?
Синдром Пфайффера представляет собой паттерн аутосомно-доминантного наследования. Это означает, что для того, чтобы вызвать заболевание, требуется только одна копия пораженного гена, которую может внести любой из родителей. Риск передачи аномального гена от одного из родителей ребенку составляет 50% при каждой беременности..
Однако это также может быть результатом новой мутации (как мы видели в типах I и II).
Типология I связана с мутациями как в FGFR1, так и в FGFR2, тогда как в типах II и III они связаны с дефектами в гене FGFR2..
Он тесно связан с мутациями в гене рецептора-1 фактора роста фибробластов (или FGFR1), который находится в хромосоме 8, или в гене 2 (FGFR2) в хромосоме 10. Задача этих генов заключается в кодировании рецепторов фактора роста фибробластов, которые необходимы для правильного развития кости.
Также считается, что способствующим возникновению этой болезни является то, что отец имеет преклонный возраст на момент зачатия, поскольку Увеличение мутаций в сперме.
Каковы ваши симптомы?
Генетическая и аллельная гетерогенность этого синдрома, по-видимому, объясняет представленную фенотипическую изменчивость (Cerrato et al., 2014)
— Главным образом, характерные черты лица и черепа: аномальный рост головы, слияние костей черепа (краниосиностоз), лобная выпуклость, выпуклые глаза (проптоз) и гипертелоризм (орбиты более разделены, чем обычно). Также распространено иметь заостренную головку или турибрахицефалию и недоразвитие в медиальной трети лица..
— Во втором типе показана голова в форме клевера, которая часто связана с гидроцефалией (расширение желудочков из-за скопления спинномозговой жидкости)..
— Гипоплазия верхней челюсти или неразвитая верхняя челюсть с выраженной нижней челюстью.
— Потеря слуха у 50% пострадавших.
— Нарушения в верхних конечностях, в частности, пороки развития в области больших пальцев рук и ног. Они большие, расширенные и / или изогнутые. Клинодактилия или ангуляция одного из пальцев.
— Как уже упоминалось, чрезмерно короткие пальцы рук и ног (брахидактилия) или сустав пальцев (синдактилия или синофалангизм).
— Все пациенты с аномалиями в верхних конечностях также имели другие более легкие аномалии в конечностях, согласно Cerrato et al. (2014)
— Недостаток подвижности (анкилоз) и аномальная фиксация локтевых суставов.
— Пороки развития органов брюшной полости в тяжелых случаях.
— Проблемы с дыханием.
— Если это тип II или III, могут возникнуть проблемы с неврологическим и умственным развитием из-за возможного повреждения головного мозга или гипоксии (из-за затрудненного дыхания, которое есть у некоторых из пострадавших). Напротив, у людей типа I интеллект обычно находится в пределах нормы.
— Более серьезные случаи: потеря зрения, вторичная к увеличению внутричерепного давления.
Возможные осложнения
Очевидно, что наиболее серьезными являются случаи, которые будут развиваться хуже (типы II и III). Так как они подвержены риску неврологических изменений и респираторных осложнений, которые могут привести к преждевременной смерти. Напротив, субъекты с синдромом Пфайффера I типа заметно улучшаются после лечения.
Сопутствующие расстройства
Как это диагностируется?
Диагноз синдрома Пфайффера можно поставить при рождении, наблюдая преждевременное соединение черепно-лицевых костей, а также длину и ширину больших пальцев рук и ног..
Следует отметить, что точная пренатальная диагностика усложняется, поскольку признаки этого синдрома можно спутать с таковыми при других расстройствах, упомянутых выше (Детская черепно-лицевая ассоциация, 2010).
Как это можно лечить?
Очень важно, чтобы лечение проводилось на ранней стадии, чтобы у детей с этим синдромом не наблюдалось снижения их потенциала..
Лечение будет сосредоточено на симптомах, которые влияют на каждого человека в частности. То есть они должны быть индивидуализированы и направлены в соответствии с типом и серьезностью клинической картины..
Обычно это требует междисциплинарного и исчерпывающего подхода с согласованными усилиями группы специалистов. Среди них было бы необходимо включить педиатров, хирургов, отоларингологов (врачей, которые лечат проблемы с ушами, носом и горлом), неврологов, аудиологов (для проблем со слухом), среди других..
Хирургическое лечение рекомендуется для устранения краниосиностоза, так как оно может вызвать другие проблемы, такие как гидроцефалия. В последнем случае может быть необходимо выполнить вмешательство, вставив трубку внутрь черепа, чтобы отвести избыток спинномозговой жидкости из мозга. Это может также быть помещено в другие части тела, это уместно для того, чтобы это было извлечено.
Хирургия может также использоваться в качестве правильного и реконструктивного метода у детей, чтобы помочь смягчить последствия пороков развития черепа, таких как гипоплазия медиальной области лица, аномалии носа или глазной проптоз..
Результаты этого типа вмешательства могут быть переменными. В исследовании Clark et al. (2016) подчеркивает успех реконструктивной пластической хирургии в лечении проптоза и типичные офтальмологические осложнения у тех, кто страдает этим синдромом.
Таким образом, специалисты советуют, что в течение первого года жизни ранняя хирургическая процедура может помочь разделить закрытые черепные швы и таким образом позволить черепу и мозгу нормально расти..
Вы можете сделать то же самое с глазницами, с целью поддержания хорошего зрения.
В более позднем возрасте целесообразно исправить половину лица с помощью операции, чтобы улучшить ее внешний вид и положение верхней и нижней челюсти (Детская черепно-лицевая ассоциация, 2010).
В некоторых случаях вы можете выбрать операцию, чтобы помочь исправить пороки развития уха. В других случаях для улучшения слуха можно использовать специализированные слуховые аппараты..
Хирургическое вмешательство, по-видимому, также проводится пациентам с синдактилией или другими пороками развития скелета, чтобы улучшить функционирование и увеличить подвижность..
Необходимо отметить, что хирургические процедуры для исправления нарушений, связанных с заболеванием, будут зависеть от тяжести, состояния и местоположения указанных аномалий и симптомов, которые вызывают.
В других случаях, когда есть проблемы с зубами, целесообразно обратиться в ортодонтическую клинику. В любом случае рекомендуется обратиться к стоматологу в возрасте 2 лет..
Другим вариантом для улучшения подвижности пострадавших является посещение физиотерапии или выбор ортопедических мер..
Генетическая консультация рекомендуется для семей пострадавших. Это особенно полезно, если есть подозрение на наличие этого синдрома, и в семье уже были случаи этого заболевания. Адекватная клиническая оценка в этих случаях определит любой признак или симптом, а также физические особенности, которые могут быть связаны с этим состоянием..
В любом случае, мы отмечаем, что по мере развития науки разрабатываются новые и более эффективные способы вмешательства в эту болезнь..
Синдром Пфайффера
Синдром Пфайффера – генетическое заболевание с аутосомно-доминантным механизмом наследования, характеризующееся нарушением формирования костей черепа и конечностей. Симптомами являются деформации черепа (в результате краниосиностоза), костей пальцев рук и ног. Некоторые формы заболевания характеризуются глухотой, нарушением интеллектуального развития, стоматологическими патологиями. Диагностика синдрома Пфайффера производится на основании данных настоящего статуса больного, рентгенологических исследований, молекулярно-генетических анализов. Специфическое лечение отсутствует, применяют паллиативные мероприятия для предотвращения тяжелых осложнений (в том числе и хирургического характера) и симптоматическую терапию.
Общие сведения
Синдром Пфайффера – врожденное генетически обусловленное нарушение формирования черепа и конечностей, которое характеризуется краниосиностозом, деформацией лица, расширением и укорочением пальцев, частыми синдактилиями. Впервые это заболевание было описано в 1964 году немецким педиатром Рудольфом Пфайффером, в дальнейшем было выявлено несколько клинических форм патологии.
По данным современной генетики, синдром Пфайффера является аутосомно-доминантным состоянием с полной пенетрантностью, половое распределение больных не имеет особенностей – с одинаковой частотой болеют как мальчики, так и девочки. Встречаемость точно не определена, по некоторым данным она составляет примерно 1:100 000 новорожденных. Каких-либо национальных или расовых особенностей в распределении этого заболевания также не выявлено. В отношении синдрома Пфайффера крайне важна ранняя диагностика, так как от времени начала паллиативного лечения во многом зависит прогноз заболевания и качество дальнейшей жизни больного.
Причины синдрома Пфайффера
Несмотря на то, что синдром Пфайффера является наследственным заболеванием с аутосомно-доминантным механизмом передачи, большинство случаев этой патологии являются следствием спонтанных герминативных мутаций в половых клетках родителей. При этом за развитие состояния отвечают дефекты двух генов, кодируемые ими белки обладают сходными функциями.
По причине того, что вышеуказанные белки обладают очень похожими функциями, патогенез синдрома Пфайффера при дефектах гена FGFR1 и FGFR2 тоже весьма схож. В результате миссенс-мутаций изменяется структура экспрессируемого белка, из-за чего полученный рецептор становится неспособен полноценно связываться с веществом-стимулятором (фактором роста фибробластов) и передавать информацию внутрь клетки. Так как фибробласты активно участвуют в процессах остеогенеза в эмбриональный период и в первые годы жизни ребенка, такое изменение рецепторов ведет к разнообразным костным патологиям.
Доказательством этого является тот факт, что дефекты гена FGFR1, помимо синдрома Пфайффера, приводят к тригоноцефалии 1-го типа и ряду других нарушений, а FGFR2 – к неспецифическому краниосиностозу, синдрому Крузона и иным похожим патологиям. При синдроме Пфайффера происходит преждевременное сращение костей черепа, что становится причиной деформации головы и лица, повышения внутричерепного давления – это, в свою очередь, способно вызывать ряд вторичных нарушений от нейросенсорных расстройств до глубокой умственной отсталости.
Классификация и симптомы синдрома Пфайффера
На сегодняшний день выделяют как минимум три клинические формы синдрома Пфайффера, которые различаются между собой выраженностью нарушений, течением и прогнозом заболевания. Причина такого различия лежит в молекулярно-генетических механизмах развития патологии – 1-й тип обусловлен единственной мутацией гена FGFR1 (252Pro-Arg) и некоторыми нарушениями структуры FGFR2, тогда как 2-й и 3-й типы вызваны различными вариантами дефектов только гена FGFR2.
Более тонкие особенности патогенеза каждой формы заболевания в настоящее время находятся в стадии изучения. Благодаря характерной клинической картине, специалисты могут определить разновидность синдрома Пфайффера, основываясь только на симптомах патологии. Молекулярно-генетический анализ во многих случаях необходим лишь для окончательного подтверждения диагноза.
Синдром Пфайффера 1-го типа является наиболее распространенным и благоприятным в прогностическом отношении вариантом заболевания. При этом состоянии уже с самого рождения ребенка отмечаются аномалии развития лица – гипертелоризм, недоразвитие верхнечелюстных костей, расширенные плоские переносица и спинка носа. Иногда могут отмечаться расщепление твердого нёба и экзофтальм. При этой форме синдрома Пфайффера характерные изменения формы черепа сводятся к увеличению его высоты и длины, очень редко отмечается асимметрия. В дальнейшем могут возникать аномалии зубов – искривление зубного ряда, гипоплазия, склонность к кариесу. Деформации костей конечностей сводятся к расширению фаланг первых пальцев на руках и ногах, может отмечаться частичная синдактилия.
Синдром Пфайффера 2-го типа – более тяжелая форма заболевания, проявляющаяся значительной выраженностью сращения костей черепа между собой и рядом других аномалий. Голова из-за краниосиностоза приобретает характерную форму «трилистника» или «листка клевера», наблюдается значительная гипоплазия средней трети лица. По причине грубого нарушения формирования черепа данный тип синдрома Пфайффера характеризуется выраженной умственной отсталостью и рядом неврологических нарушений. Пороки развития конечностей сводятся к расширению первых пальцев, синдактилии, анкилозу локтевых суставов. Кроме того, синдром Пфайффера 2-го типа часто сопровождается различными пороками развития внутренних органов. Все вышеперечисленные нарушения могут стать причиной летального исхода в раннем возрасте.
Такое различие в клинической картине и прогнозе различных вариантов синдрома Пфайффера накладывает свой отпечаток на наследование этого заболевания. Так как 1-й тип, особенно в случае своевременного выявления и правильного лечения, характеризуется сохранением нормального уровня интеллекта, фертильности и выживаемости больных, возможна аутосомно-доминантная передача патологии потомству. Более тяжелые 2-й и 3-й типы чаще всего приводят к ранней смерти или глубокой инвалидизации больных, эти варианты синдрома Пфайффера возникают только в результате спонтанных мутаций.
Диагностика
Своевременная диагностика синдрома Пфайффера крайне важна, так как она позволяет вовремя составить схему паллиативного лечения, тем самым избежать осложнений и значительно улучшить качество жизни больного. Но это справедливо лишь в отношении 1-го типа заболевания, так как при других вариантах патологии комплекс пороков развития настолько тяжел, что практически не оставляет шансов на сохранение интеллекта, а в дальнейшем – жизни больных.
Для выявления синдрома Пфайффера используют ультразвуковые методики (в том числе и в качестве пренатальной диагностики), рентгенографию, молекулярно-генетические анализы. На профилактических УЗИ во время беременности при наличии этого заболевания у ребенка во 2-3 триместре можно выявить нарушение формирования черепа, синдактилию, пороки развития внутренних органов.
Рентгенологические методы редко используют при ранней диагностике синдрома Пфайффера у детей – в основном, производят исследование черепа, которое обнаруживает наличие краниосиностоза различной степени выраженности, гипоплазию верхнечелюстных костей, изменение формы глазниц. Также на рентгене можно определить изменение формы костей больших пальцев рук и ног.
Молекулярно-генетическая диагностика производится врачом-генетиком – в этом случае при подозрении на наличие синдрома Пфайффера 1-го типа производят поиск точечной мутации 252Pro-Arg методом прямого секвенирования экзона 7а гена FGFR1. В других случаях выполняют секвенирование 7-го и 9-го экзонов гена FGFR2 – именно там возникает большинство дефектов, приводящих к развитию синдрома Пфайффера. Вспомогательную роль в диагностике заболевания могут играть методы медицинской визуализации, направленные на определение аномалий развития внутренних органов.
Лечение синдрома Пфайффера
Лечение синдрома Пфайффера только симптоматическое и паллиативное – специалисты стараются устранить повышенное внутричерепное давление, обеспечить нормальное развитие нервной системы, снизить выраженность нарушений со стороны внутренних органов. Для этого широко применяют хирургические методики – разделение пальцев, пластику черепа и ряд других. Также назначают препараты, направленные на улучшение питания нервной ткани – ноотропные средства, витамины. При своевременно начатом лечении синдрома Пфайффера 1-го типа выживаемость больных значительно увеличивается. К сожалению, объем медицинской помощи зачастую недостаточен для полноценного лечения больных синдромом Пфайффера 2-го и 3-го типов.
Прогноз и профилактика
Прогноз синдрома Пфайффера определяется вариантом этого заболевания. Первый тип характеризуется относительно благоприятным прогнозом, который зависит от своевременности выявления патологии и правильности подобранного лечения. В благоприятных условиях больные сохраняют нормальный интеллект, доживают до преклонного возраста и способны иметь потомство – при этом риск передачи заболевания детям составляет минимум 50%.
Однако синдром Пфайффера 2-го и 3-го типов обладает крайне неблагоприятным прогнозом – совокупность неврологических и других нарушений часто становится причиной летального исхода в раннем детстве. Даже при выполнении паллиативных мероприятий у больных наблюдается выраженная олигофрения и глубокая инвалидизация. Профилактика синдрома Пфайффера, учитывая часто спонтанный механизм развития этого заболевания, возможна только в рамках пренатальной диагностики ультразвуковыми или генетическими методами.