что такое синдром адамса
Cиндром Морганьи-Адамса-Стокса
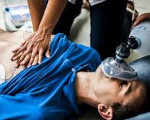
Синдром Морганьи-Адамса-Стокса_- это внезапный обморок, в результате резкого снижения сердечного выброса и острого нарушения сердечного ритма, вызывающего ишемию мозга. Нарушения сердечного ритма может выражаться блокадами, пароксизмальной тахикардией, фибрилляцией желудочков и др. Обморок может сопровождаться судорогами, нарушением дыхания.
Симптомы синдрома Морганьи-Адамся-Стокса
Симптомы синдрома Морганьи-Адамся-Стокса выражаются внезапным головокружением, потемнением в глазах, шумом в ушах и последующей потерей сознания. Затем появляются судороги, кожа становится бледной, кончики пальцев, губы, нос, уши приобретают синюшный оттенок. Пульс плохо прощупывается, Артериальное давление не удается измерить. Зрачки расширяются. В подобных ситуациях следует оказать соответствующую помощь, восстанавливающую нормальную сократительную работу сердца, после чего пациент приходит в сознание. Обморок может быть вызван стрессами, чувством тревоги или резким изменением положения тела. Во время приступа применяются экстренные реанимационные мероприятия. В случае длительного кислородного голодания, которое длится дольше 5 минут, может существенно пострадать нервная система, интеллект. Прогноз будет тем хуже, чем чаще возникают приступы МАС.
Лечение синдрома Морганьи-Адамса-Стокса
Лечение синдрома Морганьи-Адамса-Стокса наши специалисты проводят после предварительного обследования пациента с целью определения характера нарушений, которые провоцируют проявление этого заболевания. При диагностировании используются современные методы исследования, включающие и суточный мониторинг. Применение антиаритмических препаратов и электрокардиостимуляция являются основными направлениями в лечении синдрома МАС. Своевременное диагностирование и соответствующее лечение позволяют значительно улучшить качество жизни больного.
Публикации в СМИ
Синдром Морганьи–Адамса–Стокса
Синдром Морганьи–Адамса–Стокса (синдром МАС) — нарушение сознания, обусловленное резким снижением сердечного выброса и ишемией головного мозга вследствие остро возникшего нарушения сердечного ритма
Классификация
• Брадиаритмическая форма (см. Блокада атриовентрикулярная, Синдром слабости синусно-предсердного узла). Тяжесть синдрома МАС зависит от двух факторов: •• длительности асиситолии ••• при длительности 4–4,5 с чёткой симптоматики может не быть ••• 5–9 с — головокружение, потемнение в глазах ••• 10–15 с — потеря сознания; •• состояния мозгового кровообращения (каждый больной имеет свой индивидуальный порог начала приступа).
• Тахиаритмическая форма — возникает при высокой частоте сердечного ритма (200 в минуту и более), особенно при сниженной сократительной функции миокарда. Высокая частота сердечного ритма часто возникает при наличии дополнительных проводящих путей с коротким эффективным рефрактерным периодом (>270 мс), при развитии фибрилляции, трепетания предсердий, реципрокной АВ-тахикардии (см. Синдром Вольффа–Паркинсона–Уайта, Фибрилляция предсердий, Трепетание предсердий, Тахикардия желудочковая, Синдром удлинения интервала Q–T).
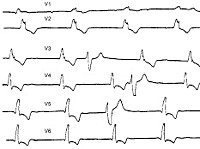
Клинические проявления • Внезапное головокружение или потеря сознания • Бледность • Артериальная гипотензия • Тоникоклонические судороги (при асистолии желудочков длительностью более 15 с) • Резкая брадикардия или тахикардия.
Специальные исследования • ЭКГ • Суточное мониторирование ЭКГ • ЭхоКГ • Электрофизиологическое исследование
ЛЕЧЕНИЕ
Брадиаритмическая форма • Временная эндокардиальная или трансторакальная наружная ЭКС • Медикаментозная терапия позволяет выиграть время для подготовки к проведению ЭКС •• Атропин — 1 мг в/в, повторяют через 3–5 мин до получения эффекта или достижения общей дозы 0,04 мг/кг •• При отсутствии эффекта — аминофиллин в/в струйно медленно в дозе 240–480 мг •• При отсутствии эффекта — либо допамин в дозе 100 мг, либо эпинефрин в дозе 1 мг (изопреналин 1 мг) в 250 мл 5% р-ра глюкозы в/в, постепенно увеличивая скорость инфузии до достижения минимально достаточной ЧСС • Хирургическое лечение — показана имплантация ЭКС.
Тахиаритмическая форма • Купирование пароксизма тахикардии электроимпульсной терапией. При синдроме удлинённого интервала Q–T, осложнённого желудочковой тахикардией типа «пируэт», показано внутривенное введение препаратов магния (см. Тахикардия желудочковая, Синдром удлинения интервала Q–T) • Хирургическое лечение •• При синдроме Вольффа–Паркинсона–Уайта — абляция дополнительных проводящих путей •• При фибрилляции и трепетании предсердий — абляция пучка Хиса с имплантацией ЭКС (в режиме VVI) •• При желудочковой тахикардии — имплантация кардиовертера-дефибриллятора.
Синонимы • Синдром Адамса–Стокса • Синдром Адамса–Морганьи–Стокса • Синдром Спенса • Синдром Стокса.
МКБ-10 • I45.9 Нарушение проводимости неуточнённое
Код вставки на сайт
Синдром Морганьи–Адамса–Стокса
Синдром Морганьи–Адамса–Стокса (синдром МАС) — нарушение сознания, обусловленное резким снижением сердечного выброса и ишемией головного мозга вследствие остро возникшего нарушения сердечного ритма
Классификация
• Брадиаритмическая форма (см. Блокада атриовентрикулярная, Синдром слабости синусно-предсердного узла). Тяжесть синдрома МАС зависит от двух факторов: •• длительности асиситолии ••• при длительности 4–4,5 с чёткой симптоматики может не быть ••• 5–9 с — головокружение, потемнение в глазах ••• 10–15 с — потеря сознания; •• состояния мозгового кровообращения (каждый больной имеет свой индивидуальный порог начала приступа).
• Тахиаритмическая форма — возникает при высокой частоте сердечного ритма (200 в минуту и более), особенно при сниженной сократительной функции миокарда. Высокая частота сердечного ритма часто возникает при наличии дополнительных проводящих путей с коротким эффективным рефрактерным периодом (>270 мс), при развитии фибрилляции, трепетания предсердий, реципрокной АВ-тахикардии (см. Синдром Вольффа–Паркинсона–Уайта, Фибрилляция предсердий, Трепетание предсердий, Тахикардия желудочковая, Синдром удлинения интервала Q–T).
Клинические проявления • Внезапное головокружение или потеря сознания • Бледность • Артериальная гипотензия • Тоникоклонические судороги (при асистолии желудочков длительностью более 15 с) • Резкая брадикардия или тахикардия.
Специальные исследования • ЭКГ • Суточное мониторирование ЭКГ • ЭхоКГ • Электрофизиологическое исследование
ЛЕЧЕНИЕ
Брадиаритмическая форма • Временная эндокардиальная или трансторакальная наружная ЭКС • Медикаментозная терапия позволяет выиграть время для подготовки к проведению ЭКС •• Атропин — 1 мг в/в, повторяют через 3–5 мин до получения эффекта или достижения общей дозы 0,04 мг/кг •• При отсутствии эффекта — аминофиллин в/в струйно медленно в дозе 240–480 мг •• При отсутствии эффекта — либо допамин в дозе 100 мг, либо эпинефрин в дозе 1 мг (изопреналин 1 мг) в 250 мл 5% р-ра глюкозы в/в, постепенно увеличивая скорость инфузии до достижения минимально достаточной ЧСС • Хирургическое лечение — показана имплантация ЭКС.
Тахиаритмическая форма • Купирование пароксизма тахикардии электроимпульсной терапией. При синдроме удлинённого интервала Q–T, осложнённого желудочковой тахикардией типа «пируэт», показано внутривенное введение препаратов магния (см. Тахикардия желудочковая, Синдром удлинения интервала Q–T) • Хирургическое лечение •• При синдроме Вольффа–Паркинсона–Уайта — абляция дополнительных проводящих путей •• При фибрилляции и трепетании предсердий — абляция пучка Хиса с имплантацией ЭКС (в режиме VVI) •• При желудочковой тахикардии — имплантация кардиовертера-дефибриллятора.
Синонимы • Синдром Адамса–Стокса • Синдром Адамса–Морганьи–Стокса • Синдром Спенса • Синдром Стокса.
МКБ-10 • I45.9 Нарушение проводимости неуточнённое
Синдром Морганьи-Адамса-Стокса
Синдром Морганьи-Адамса-Стокса – это комплекс симптомов, обусловленных резким снижением сердечного выброса и ишемией головного мозга у больных, страдающих выраженными нарушениями ритма. Проявляется в виде приступов синкопе, судорог, фибрилляции желудочков, асистолии. Диагноз устанавливается по наличию характерной клинической картины, изменениям на электрокардиограмме, результатам суточного мониторирования. Заболевание дифференцируют с эпилепсией, истерическим припадком. Лечение состоит из реанимационных мероприятий в момент развития симптоматики и последующего терапевтического восстановления нормальной работы сердца.
МКБ-10
Общие сведения
Впервые синдром Морганьи-Адамса-Стокса был описан итальянским анатомом и врачом Д. Морганьи в 1761 году. В период с 1791 по 1878 г заболевание изучалось ирландскими кардиологами Р. Адамсом и В. Стоксом. С учетом вклада всех специалистов синдром был назван их именами. Патология распространена среди пациентов, страдающих сердечными болезнями, в первую очередь – блокадами внутрисердечной проводимости и синдромом слабости синусового узла. Чаще диагностируется у людей старше 45-55 лет, мужчины составляют около 60% от общего числа больных. Максимальное количество случаев регистрируется в развитых странах, жители которых склонны к гиподинамии и подвержены воздействию кардиотоксических веществ. В государствах «третьего мира» синдром встречается сравнительно редко.
Причины
К развитию болезни приводят врожденные органические изменения в строении проводящей системы, а также нарушения, возникающие под влиянием внешних патогенетических факторов. К их числу относят передозировку антиаритмическими средствами (новокаинамид, амиодарон), профессиональную интоксикацию хлорорганическими соединениями (винилхлорид, четыреххлористый углерод), дистрофические и ишемические изменения миокарда, затрагивающие крупные узлы системы автоматизма (синатриальный, атриовентрикулярный). Кроме того, синдром может формироваться в результате возрастной дегенерации АВ-центра. Непосредственно приступ имеет следующие причины:
Патогенез
В основе лежит резкое сокращение сердечного выброса, которое становится причиной замедления кровотока, недостаточного снабжения органов и тканей кровью, кислородом, питательными веществами. Первоначально от гипоксии страдают нервные структуры, в том числе головной мозг. Работа ЦНС нарушается, происходит потеря сознания. Чуть позже возникают судорожные мышечные сокращения, свидетельствующие о выраженном кислородном голодании тканей. Длительные приступы, особенно обусловленные фибрилляцией желудочков, могут привести к постгипоксической энцефалопатии, полиорганной недостаточности. При сохранении минимального кровотока (блокады, аритмии) заболевание протекает легче. Приступы в большинстве случаев не приводят к отсроченным последствиям.
Классификация
Патогенетическая систематизация, учитывающая причины и механизмы формирования приступа, используется при плановом лечении и выборе мер профилактики. При оказании экстренной помощи синдром Морганьи-Адамса-Стокса удобнее классифицировать по виду нарушения коронарного ритма, поскольку это позволяет быстро определить оптимальную тактику лечения. Различают следующие виды патологии:
Симптомы
Классический припадок характеризуется быстрым развитием и определенной последовательностью изменений. В течение 3-5 секунд с момента возникновения аритмии или блокады у пациента формируется предобморочное состояние. Внезапно появляется головокружение, головная боль, дискоординация, дезориентация, бледность. На коже выступает обильный холодный пот. При пальпаторной оценке пульса обнаруживается резко выраженная тахикардия, брадикардия или неровный ритм.
Возможно абортивное течение приступа с редукцией симптоматики в течение очень короткого временного промежутка. Кора мозга не успевает подвергнуться выраженной гипоксии. Основными симптомами, наблюдаемыми при этом варианте патологии, являются головокружение, слабость, преходящее нарушение зрения, помрачение сознания. Проявления исчезают за несколько секунд без медицинского вмешательства. Подобные разновидности МАС крайне сложно диагностировать, поскольку аналогичная симптоматика выявляется при множестве других состояний, в т. ч. при цереброваскулярной болезни.
Осложнения
Диагностика
Первичную диагностику осуществляют сотрудники СМП, прибывшие на вызов. Окончательный диагноз устанавливает кардиолог, основываясь на результатах электрокардиографии и холтеровского мониторирования. Дифференциальную диагностику проводят с эпилептическим припадком, истерией. Отличительной особенностью истинной эпилепсии является смена тонических судорог клоническими, гиперемия лица, предшествующая аура. При истерическом происхождении патологии утраты сознания не происходит, присутствует синусовый сердечный ритм. Признаками болезни МАС считаются наличие аритмии того или иного характера, стремительное развитие клинической картины. В процессе диагностического поиска используют следующие методы:
Неотложная помощь
Помощь при синдроме МАС включает непосредственное купирование приступа и профилактику рецидивов. При развивающемся припадке спасательные мероприятия производит присутствующий медицинский работник независимо от его профиля и специализации. Осуществляются комбинированные реанимационные мероприятия. Лечение включает:
Прогноз и профилактика
Прогноз благоприятный при быстром купировании приступа и при его абортивном варианте. Нормализация сердечного ритма и кровоснабжения головного мозга в течение 1 минуты с момента формирования клинической картины не сопровождается отсроченными последствиями. Длительный период асистолии или фибрилляции желудочков снижает вероятность благополучного восстановления коронарного ритма и повышает риск ишемического поражения головного мозга. Специфические меры профилактики не разработаны. Общие рекомендации по предотвращению кардиологических болезней включают отказ от курения и алкоголя, исключение гиподинамии, занятия спортом, соблюдение принципов здорового питания. При появлении первых признаков нарушений в работе сердца следует обратиться к врачу для обследования и лечения.
Нормотензивная гидроцефалия (синдром Хакима-Адамса)
Нормотензивная гидроцефалия (НТГ) – синдром, характеризующийся сочетанием деменции, нарушений ходьбы и недержания мочи при выраженном расширении желудочковой системы и нормальном давлении цереброспинальной жидкости (ЦСЖ).
Этиология
В основе развития заболевания лежит дисбаланс между секрецией и резорбцией ЦСЖ, а также нарушение ликвородинамики.
Клинические проявления
Для НТГ характерно постепенное развитие триады Хакима-Адамса – деменции (слабоумие), нарушений ходьбы и недержания мочи. В большинстве случаев нарушение ходьбы является первым симптомом, затем возникает деменция и позднее присоединяются тазовые расстройства. Возможна флуктуация выраженности симптомов, однако это не характерно для НТГ.
Основной жалобой пациентов с данной патологией на приеме у невролога является головокружение, которое они описывают как ощущение неустойчивости при движении, резких поворотах туловища. В данном случае в основе головокружения лежит постуральная неустойчивость и дисбазия, свойственная заболеванию. Нарушения ходьбы при НТГ включают в себя элементы апраксии ходьбы в виде шаркающей походки короткими шажками на широко расставленных ногах и потерю контроля над равновесием. При НТГ не отмечается каких-либо изменений движений руками при ходьбе, что отличает ее от болезни Паркинсона. На ранних стадиях при минимальной поддержке изменение походки у больных с НТГ может быть незначительным. При этом пациенты с НТГ могут имитировать движения ногами, которые они должны совершать при ходьбе, в положении лежа или сидя.
Другим важным проявлением НТГ является деменция. Для пациентов характерно наличие мории, дезориентированности (больше во времени, нежели чем в месте). Часто больным трудно изложить историю своего заболевания. У некоторых возможно развитие галлюцинаций, мании, депрессии.
Уже на ранних стадиях НТГ при активном, целенаправленном расспросе удается выявить жалобы больных на учащенное мочеиспускание и никтурию (позывы на мочеиспускание по ночам). По мере прогрессирования заболевания присоединяются императивные позывы и периодическое недержание мочи. Больные перестают чувствовать позывы к мочеиспусканию и индифферентно относятся к факту непроизвольного мочеиспускания, что характерно для лобного типа тазовых расстройств. Недержание кала встречается редко, как правило, у пациентов на поздней стадии НТГ.
Диагностика
Одним из основных способов диагностики НТГ является “tap-test” – люмбальная пункция с выведением некоторого количества ЦСЖ (однократно 20-50 мл или по 30 мл в течение 3 дней). Более сложной модификацией “tap-test” является, т.н. “drainage test” – люмбальный дренаж, обеспечивающий временный (1-5 суток) и контролируемый отток ликвора (10 см3/час). Особенно важным является оценка динамики основных симптомов триады Хакима-Адамса после проведения этих тестов в течение нескольких суток. Даже кратковременное клиническое улучшение позволяет считать тест положительным и свидетельствует о необходимости консультации нейрохирурга для решения вопроса о проведении шунтирующей операции.
Огромное значение для диагностики НТГ имеют результаты нейровизуализационных методов исследования (компьютерная и магнитно-резонансная томография), позволяющие выявлять резко расширенные желудочки головного мозга, в то время как корковые борозды остаются в пределах нормы или незначительно расширены.
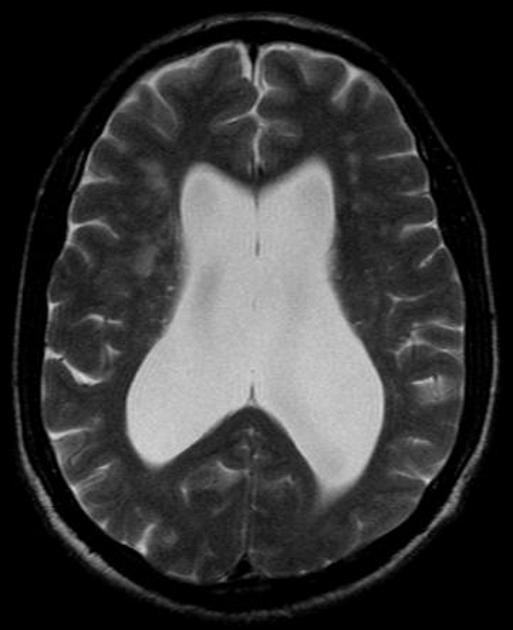
при отсутствии значимой атрофии вещества головного мозга
С помощью этих методик можно исключить иные причины гидроцефалии.
Лечение
Основу лечения составляют шунтирующие операции с наложением вентрикулоперитонеального и люмбоперитонеального шунтов, при которых положительный эффект достигается у 60% больных. В далеко зашедших стадиях болезни, когда имеются уже необратимые изменения в мозге, прогноз оперативного лечения ухудшается. У части больных, среди которых не отмечалось значительное улучшение после люмбальной пункции, операция шунтирования также может оказаться эффективной. Осложнения после шунтирования (субдуральные гематомы, синдром ликворной гипотензии) отмечаются у 30-40% больных. Летальность составляет около 6-7%. Для профилактики осложнений рекомендуется индивидуальный подбор шунта.
Что такое синдром адамса
ГБОУ ВПО «Дагестанская государственная медицинская академия» Минздрава РФ, Махачкала
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2015;115(9): 49-53
Шамов И. А. Синдром Хакима—Адамса. Журнал неврологии и психиатрии им. С.С. Корсакова. 2015;115(9):49-53.
Shamov I A. Hakim—Adams syndrome. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2015;115(9):49-53.
https://doi.org/10.17116/jnevro20151159149-53
ГБОУ ВПО «Дагестанская государственная медицинская академия» Минздрава РФ, Махачкала
Синдром Хакима—Адамса — малоизвестное, хотя и достаточно часто встречающееся состояние. Этиология его не полностью ясна. Патогенетические механизмы включают блокаду оттока цереброспинальной жидкости (ЦСЖ) по верхнелатеральной поверхности мозга, развитие гидроцефалии с расширением желудочков мозга при сохранении нормотензии ЦСЖ. Основные клинические проявления: развитие атаксии, апраксии, явления деменции и нарушения мочеиспускания, вплоть до недержания мочи. Диагностика основывается на данных клинической симптоматики, люмбальной пункции с пробным извлечением жидкости и нейровизуализации. Основным способом лечения является наложение вентрикулоперитонеального шунта для отведения ЦСЖ. Своевременное проведение хирургического вмешательства дает хорошие результаты, улучшает качество жизни пациентов.
ГБОУ ВПО «Дагестанская государственная медицинская академия» Минздрава РФ, Махачкала
Синдром Хакима—Адамса (СХА), или нормотензивная гидроцефалия, описан в 1964—1965 гг. [1]. Он включает в себя классическую триаду симптомов: нарушение походки в результате атаксии или апраксии, или лобной дисбазии, деменцию и недержание мочи. Заболевание встречается редко, его часто принимают за ригидную форму болезни Паркинсона (БП), болезнь Альцгеймера (БА) и распознают с трудом [2].
За рубежом заболевание известно широко и оперативному лечению подвергнуты сотни тысяч больных. В России оно известно меньше [3].
Сведения о распространенности противоречивы. Наиболее часто СХА встречается после 60 лет. По данным D. Jaraj и соавт. [4], заболевание встречается в 0,2% случаев в возрасте 70—79 лет и в 5,9% — 80 лет и старше. Авторы полагают, что реальные показатели значительно выше. C. Iseki и соавт. [5] выявили, что в японской популяции заболеваемость лиц старше 70 лет равна 1,2 на 1000 человек в год. Различия между мужчинами и женщинами не отмечены.
СХА у взрослых может быть следствием субарахноидального и внутрижелудочкового кровоизлияния, черепно-мозговой травмы, воспалительного процесса, перинатального поражения головного мозга и мозговых оболочек, объемных интракраниальных образований (опухоли, аневризмы мозговых сосудов), аномалий развития мозга, перенесенных операций на головном мозге и других ситуаций, создающих механические препятствия нормальной циркуляции цереброспинальной жидкости (ЦСЖ) [3]. Однако в большинстве случаев болезнь развивается без видимых причин.
Представляют интерес данные о возможности участия генетических факторов в развитии болезни [6]. Ряд симптомов СХА встречался среди родственников с частотой 7,1%, тогда как в контрольной популяции — лишь у 0,7%.
Причина клинических проявлений СХА до конца неизвестна. Возможно, они обусловлены растяжением волокон лучистого венца головного мозга.
Вероятный патогенетический механизм, лежащий в основе заболевания, — дисбаланс секреции и резорбции ЦСЖ и нарушение ликвородинамики [7]. Основным местом резорбции ЦСЖ у человека являются конвекситальные субарахноидальные пространства в области верхнего сагиттального синуса. При СХА возникают блокада оттока ЦСЖ по верхнелатеральной поверхности мозга, а также затруднение ее всасывания в кровь. Происходит увеличение объема ликворного пространства (размеры желудочков) с соответственным уменьшением объема мозговой ткани [8]. Изменения в субарахноидальном пространстве предшествуют расширению желудочков [5]. Причиной таких явлений может быть окклюзия ликворных путей в пределах желудочков (окклюзионная форма) или нарушение резорбции ЦСЖ из субарахноидального пространства через арахноидальные ворсины в дуральные полости мозга, являющиеся основными путями оттока венозной крови из мозга (открытая форма). Как уже указывалось, окклюзия и нарушение резорбции жидкости могут вести к растяжению проводящих путей лучистого венца.
Для СХА характерно постепенное развитие симптоматики — нарушений походки (моторные изменения), признаков органического поражения мозга (деменция, потеря памяти, дезориентация) и тазовых расстройств (дизурия, недержание мочи) [3].
Моторные нарушения развиваются медленно, появляются затруднения при ходьбе, создается впечатление повышения тонуса мышц. Больные ходят медленно, мелкими шажками, походка становится шаркающей, семенящей, на широко расставленных ногах. Отмечаются плохой контроль равновесия, неустойчивость при поворотах. Теряется осанка, появляется сгорбленная поза.
Больные сообщают, что затруднения возникают из-за того, что появляется тяжесть в икроножных мышцах, ноги становятся «тяжелыми», больным трудно их поднимать. Вследствие этого ходьба ограничивается по длительности и дальности. Могут отмечаться постуральный тремор, проявления типа акинетико-ригидного синдрома (феномен «застывания»). Такие проявления сближают заболевание с ригидной формой БП (этот диагноз довольно часто выставляется первоначально). Однако при детальном обследовании ригидность мышц не выявляется. У ряда пациентов встречается псевдобульбарный синдром.
В большинстве случаев нарушения ходьбы являются первым симптомом, затем возникает деменция и позднее присоединяются тазовые расстройства.
Нарушения когнитивных функций в целом напоминают таковые при Б.А. Наиболее значительными могут быть выпадение как кратко-, так и долговременной памяти, дезориентированность во времени, реже они проявляются совместно. Пациенты с трудом излагают историю своей болезни [1]. Появляются проблемы в исполнительной функции: планировании, сосредоточении, абстрактном мышлении [9].
Возникают нарушения семантической памяти. Оскудевает эмоциональная сторона, появляются апатия, благодушие [10]. Возможны явления агнозии: нарушение различных видов восприятия (зрительное, слуховое, тактильное). Замедляется скорость психических процессов и психомоторных реакций. Эти явления считают характерными для дисфункции передних отделов головного мозга и подкорковой деменции [2, 11, 12]. Степень нарушений когнитивных функций различна. На ранних этапах изменения не столь выражены, однако при длительном течении болезни приближаются к таковым при БА.
Тазовые нарушения появляются в последнюю очередь. Однако при целенаправленном расспросе уже на ранних стадиях СХА удается выявить жалобы больных на учащенное мочеиспускание и никтурию. Постепенно к этим симптомам присоединяются императивные позывы к мочеиспусканию, а затем недержание мочи. У пациентов теряется запирательный рефлекс, и на фоне когнитивных нарушений они начинают индифферентно относиться к данному факту, что характерно для лобного типа тазовых расстройств.
Диагностика СХА является сложной задачей, поскольку он может имитировать многие другие неврологические заболевания. Так, начальные проявления болезни напоминают ригидную форму БП, а более поздние — Б.А. При детальном обследовании БП исключается более или менее легко [13]. Магнитно-резонансная (МРТ) и компьютерная томография (КТ) головного мозга дают возможность исключить Б.А. Дифференциальной диагностике помогает также то, что при СХА после шунтирования наступает регресс симптомов [14]. МРТ является методом выбора в диагностике гидроцефалии.
При МРТ головного мозга выявляют расширение III и боковых желудочков. Особенно значительно расширены III желудочек, височные и фронтальные рога боковых желудочков. Гидроцефалия при этом синдроме является сообщающейся, так как сильвиев водопровод проходим.
В диагностике используются также люмбальная пункция и исследование ЦСЖ. Давление ЦСЖ в спинномозговом канале бывает в пределах нормы (что отражает и название болезни — нормотензивная гидроцефалия). Начальное давление должно быть менее 180 мм вод. ст. Имеются также количественные методы оценки ЦСЖ [15], в том числе автоматизированные. Показано, что объем ЦСЖ при СХА ниже, чем при БА [16] и у здоровых.
Есть исследования, показавшие, что в ЦСЖ при этом синдроме снижается уровень простагландин D-синтазы, что может быть использовано в диагностике [17]. Иногда проводится цистернография с использованием радиоактивного 99-m технеция или другого изотопа. Она позволяет установить замедление всасывания ЦСЖ на верхнелатеральной поверхности мозга. Специфичность и чувствительность метода требуют уточнения, и результаты спорны, поэтому методика используется редко. Другие методы исследования (М-ЭХО-ЭГ и ЭЭГ) малоинформативны. Диагностическими критериями СХА считают увеличение переднерогового индекса (индекс Эванса) более 30% и расширение височных рогов боковых желудочков более 2 мм [3].
Одним из диагностических приемов является пробное извлечение 30—50 мл ЦСЖ. Пока окончательно не решено, когда и как оценивать результаты этого теста. В основном оценка производится через 1 сут. При СХА после такой процедуры походка и когнитивные функции временно улучшаются. Однако K. Kang и соавт. [18] описали пациента, у которого через 1 сут отклика не было, но улучшение наступило через 7 сут. Пациент был шунтирован с хорошим послеоперационным исходом.
Имеются единичные работы, посвященные поиску средств консервативного лечения болезни. Так, N. Alperin и соавт. [19] выявили, что малые дозы ацетазоламида уменьшали объем перивентрикулярной жидкости и у 5 из 8 пациентов привели к улучшению походки. Показано также, что психотропные препараты второго поколения оказывают положительное влияние на клинические проявления [20].
Основным способом лечения признается хирургический, заключающийся в выполнении ликворошунтирующих операций [21]. Рекомендуется проводить оперативное лечение сразу после установления диагноза [22].
Одним из наиболее часто применяемых методов является вентрикулоперитонеальное шунтирование. Проксимальный отдел катетера устанавливают в боковом желудочке мозга, а периферический — отводят в брюшную полость. Считается, что за 1 сут в брюшную полость может попасть около 300 мл ЦСЖ. Однако она не доставляет особых беспокойств и утилизируется путем всасывания брюшиной (или слизистой оболочкой).
Существует несколько вариантов шунтирующих систем. Имеется простой дренажный катетер. Более технологически совершенными являются специальные катетеры для шунтирования. Как правило, они снабжены клапанами, регулирующими отток в зависимости от количества жидкости в системе желудочков головного мозга и препятствующими обратному току жидкости из брюшной полости в головной мозг. Система для шунтирования включает также резервуар, позволяющий при необходимости забирать жидкость на исследование и вводить лекарственные вещества. Имеются исследования, продемонстрировавшие, что отдаленные результаты операции при применении разных шунтовых систем примерно одинаковы [23]. Ряд авторов [24, 25] находили преимущества у систем с гравитационным регулированием клапана шунта. Метаанализ работ по шунтированию показывает, что у адекватно диагностированных пациентов шунтирование приводит к длительным положительным результатам.
Исходы тем лучше, чем моложе пациент, чем меньше у него коморбидных заболеваний и нет поражения белого вещества [26]. Эффективность шунтирования выше при меньшей длительности заболевания. У больных с нарушениями походки улучшение наступает в 77% случаев. Однако проведенные контролируемые исследования методами актиграфии показали, что при этом активность пациентов значительно не возрастает [27]. M. Poca и соавт. [28] показали, что после шунтирования у 79,3% пациентов наступило улучшение походки, у 82,4% — тазовых нарушений и у 63,7% — уменьшение когнитивных расстройств.
Неврологические расстройства при СХА могут полностью или в значительной степени регрессировать после своевременно проведенной шунтирующей операции. По данным разных авторов [2], хирургическое лечение оказывается эффективным в 1/3 —¾ случаев. В работе, оценивавшей исходы через 1 год после шунтирования [29], было показано, что у 69% пациентов наступило значительное улучшение и клинических проявлений (способность жить самостоятельно), и рентгенологических данных. Стадия болезни и коморбидность не влияли на степень улучшения. Однако другие авторы [30] нашли, что бо́льшая коморбидность влияет на успех операции: при наличии до шести сопутствующих заболеваний шунтирование не приводит к улучшению.
Осложнения встречаются у 31—38% пациентов. Основными являются синдром ликворной гипотензии, проявляющийся головными болями при вставании, в редких случаях — субдуральная гематома вследствие быстрого уменьшения размера желудочков. По данным M. Poca и соавт. [28], смертность составляет 0,8%. Ранние послеоперационные осложнения были у 5,3% оперированных. Через 6 мес бессимптомные гигромы отмечены у 3,4%. В последующем у 3% выявлены субдуральные гематомы. Для профилактики осложнений рекомендуют индивидуальный подбор шунта.
Приводим краткие описания собственных наблюдений.
Пациент М., 74 года, работник умственного труда. Несколько лет назад появились затруднения при ходьбе, шаркающая походка. Нарушения прогрессировали, стало трудно ходить пешком на работу (примерно 1 км). В дальнейшем стали беспокоить частые позывы к мочеиспусканию. Недержания мочи не отмечает. Когнитивные нарушения не проявлялись, хотя стал отмечать некоторое снижение памяти, трудности сосредоточения при умственной работе.
Анализы: общие анализы крови, мочи в норме.
Глюкоза крови 5,99 ммоль/л, инсулин 2,37 мкед/мл, пролактин 285 мкг/л; Т3 свободный 12,6 нмоль/л; тиреотропный гормон 3,66 мкМЕ/мл; Nа + 148 ммоль/л; K + 4,8 ммоль/л; Ca ++ 1,16 ммоль/л, лактатдегидрогеназа 212 ЕД/л.
Консультация окулиста: глазное дно без застойных явлений. МРТ головного мозга: мозговые структуры не смещены, желудочки умеренно расширены. Боковые желудочки симметричны, несколько увеличены, увеличение симметричное. III желудочек 13 мм, боковые — 24—25 мм. В белом веществе очаги микроглиоза 3—6 мм, интенсивность сигналов повышена. Микроангиопатия. Визуализируется расширение периваскулярных пространств в области базальных вен. Субарахноидальное пространство умеренно расширено в конвекситальных областях лобно-теменных долей. Гипофиз 3—3,4 мм, не увеличен. Области интенсивных сигналов в его структуре не выявляются. Ножка гипофиза распределена срединно. Стволовые структуры без особенностей. Позвоночные артерии несколько асимметричны по калибру.
Заключение: единичные очаги микроглиоза в белом веществе головного мозга как проявления микроангиопатии. Умеренное расширение боковых и III желудочков, ликворных пространств в области сильвиевых щелей. Проявления атрофических изменений головного мозга.
Диагноз: СХА, ранняя стадия.
При люмбальной пункции повышения давления ЦСЖ не отмечено. Удалено 30 мл ЦСЖ. Анализ в норме. После пункции почувствовал облегчение при ходьбе.
Операция была проведена в НИИ нейрохирургии им. Н.Н. Бурденко: с правой стороны установлен шунт, проксимальный конец в IV желудочке, дистальный — в брюшной полости в подпеченочном пространстве. Степень устойчивости 90% по шкале Карновского. Операция прошла успешно, заживление ранок первичным натяжением. Самочувствие улучшилось, голова «прояснилась», ходить стало легче. Рекомендовано в течение 1 мес исключить физические нагрузки, работу, требующую наклона головы, туловища, затем постепенно расширять режим.
Состояние пациента значительно улучшилось. Переносимость физических нагрузок значительно увеличилась — может быть на ногах до 3 ч без признаков тяжести, усталости. Стал активнее физически и психически — улучшилась умственная деятельность, активно занимается научной деятельностью и преподаванием.
Пациент: А., 62 года. Болеет около 2 лет. Появились непонятная слабость, когнитивные нарушения — стал «заговариваться», снизилась память, возникли конфликты на работе, в связи с чем вынужден был уйти со службы. Постепенно возникли затруднения при ходьбе, появилась боль в икрах обеих голеней, походка стала семенящей, замедленной. Установлен диагноз паркинсонизма, ригидная форма. Проводилось лечение мадапаром, пронораном, ПК-мерц, но без эффекта. Отмечалось нарастание симптоматики.
При обследовании все анализы в норме.
МРТ: в обеих полушариях головного мозга определяются участки изменения интенсивности МР-сигнала, гиперинтенсивные на Т2 и FLAIR, гипоинтенсивные на Т1-взвешенных изображениях, без признаков объемного воздействия. Боковые желудочки мозга симметричные, передние рога умеренно расширены. III желудочек до 10 мм, IV — не изменен.
Субарахноидальные пространства и сильвиевы щели расширены. Хиазмально-селлярная область без особенностей. Гипофиз имеет однородную интенсивность сигнала. В придаточных пазухах носа определяется усиление сигнала. Миндалины мозжечка расположены на уровне линии Чемберлена. Зрительные бугры, зрительные и слуховые нервы не изменены.
На МР-ангиограммах, выполненных в режиме 3D TOF, визуализируются мозговые, внутренние сонные, позвоночные, основная артерии и их интракраниальные ветви. Со стороны сосудов головного мозга определяется снижение сигнала от позвоночной артерии справа. Сосуды симметричны, диаметр остальных не изменен, артериовенозные анастомозы отсутствуют. Венозные синусы свободно проходимы.
Заключение. МР-признаки дисциркуляторной энцефалопатии. Умеренная смешанная заместительная гидроцефалия.
Диагноз: СХА, начальная стадия.
От операции пока воздерживается.
Таким образом, СХА — малоизвестное, хотя и достаточно часто встречающееся заболевание, этиология которого не полностью ясна. Основные клинические проявления синдрома включают развитие атаксии, апраксии, явления деменции и нарушения мочеиспускания, вплоть до недержания мочи. Диагностика основывается на данных клинической симптоматики, люмбальной пункции с пробным извлечением жидкости и нейровизуализации. Основным способом лечения является наложение вентрикулоперитонеального шунта для отведения ЦСЖ. Своевременное проведение хирургического вмешательства дает хорошие результаты, улучшает качество жизни пациентов.