Репликация вирусов
Репликация вирусов
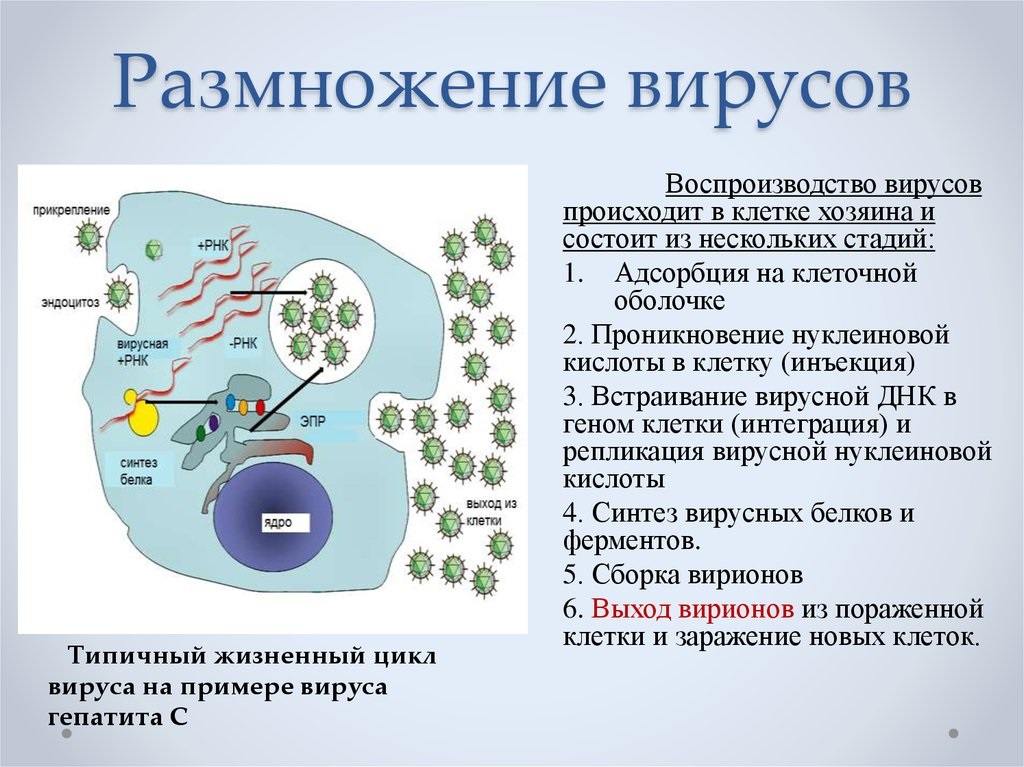
Размножение вируса, или репликация, является весьма характерным процессом, свойственным только обитателям этого особого мира природы. Как известно, рост организмов растительного и животного мира природы невозможен без деления клеток. Вирус же вообще не увеличивается в размерах. Вирусные частицы появляются сразу «взрослыми» в результате своеобразного процесса, названного репликацией. Но самое поразительное — то, что в продуцировании новых вирусных частиц участвует только одна нить: одинарная цепочка нуклеиновой кислоты.
Проследим за нуклеиновой кислотой бактериофага, проникшей в клетку бактерии. Первым делом ДНК выключает жизненно важные для клетки хозяина процессы. Затем начинают образовываться специфические вещества ферменты, идущие на строительство молекул ДНК, точно таких же, какие были и у бактериофага. Примерно через 8 мин образование ферментов замедляется и начинают образовываться белки капсидов. На строительство цепочек нуклеиновых кислот потомства кроме ферментов идет часть родительской ДНК бактериофага и разбитая ДНК хозяина. Капсиды новых бактериофагов строятся из вновь образованных белков; сюда же идет часть белков разрушенной клетки и старого бактериофага.
Примерно через 15 мин после инфицирования в клетке бактерий образуется столько вирусных частиц, что им становится тесно. Они разрывают оболочку хозяина и вырываются наружу, заражают новые клетки бактерий и т. д.
Репликация вирусов как сборочный конвейер
Часто процесс репликации вирусов сравнивают с заводским сборочным конвейером, действующим по заранее разработанному технологическому процессу. Сначала под руководством ДНК идет изготовление строго определенных элементов деталей. Далее ДНК вырабатывает белки своей сферы и ядрышко, вокруг которого белки под влиянием электростатических сил собираются в сферу. Ядрышко уничтожается, после того как образовалась головка-сфера. Один из ответственейших моментов сборки — заполнение сферы цепочкой ДНК. К этому моменту из отдельных участков «цеха сборки» к «главному конвейеру» подаются недостающие детали бактериофага: стержень, сократительные кольца, пластинки, нити. Эти детали друг за другом прикрепляются к сфере.
Интересно, что «рабочие» операции по сборке вирусов сходны с процессами зарождения и развития более сложных организмов. Не заимствованы ли эти приемы из мира вирусов?
Кстати, технические приемы репликации различных видов вирусов не только состоят из общих операций, но имеют и некоторые особенные черты. Так, вирусы оспы размножаются в цитоплазме, а вирусы группы герпеса и аденовирусы — в ядре. В процессе построения нуклеиновых кислот участвуют разрушенные системы клетки хозяина. Следовательно, вирусам оспы и аденовирусам придется использовать различный строительный материал. Эти вирусы относятся к группе крупных вирусов. Например, в молекуле ДНК вируса осповакцины закодировано около 500 белков. Цикл размножения длится более 20 ч. Можно представить, как сложно контролировать процесс репликации вируса! И если системы, отвечающие за последовательность сборки, хоть раз ошибутся, вирусу не удастся «самособраться». Запомните это уязвимое место в процессе репликации.
Репликация компетентного вируса как важного источника смещения в моделях латентности ВИЧ с использованием однократных вирусных конструкций
Модель Т-клеток центральной памяти (ТСМ) формирует уникальную модель латентности ВИЧ-1, основанную на первичных клетках, которые очень напоминают TCM in vivo. Вирус, используемый в этой модели, основан на сконструированном векторе, неспособном к репликации после первичной инфекции. Мы показываем, что, несмотря на эту стратегию, реплицированные компетентные вирусные частицы высвобождаются в культуральную среду из-за рекомбинации между перекрывающимися последовательностями env удаленного генома ВИЧ, который совместно трансфицируется интактным env. Этот вывод подчеркивает необходимость тщательного анализа и интерпретации данных, если используются подобные конструкции, и настоятельно призывает к дополнительной осторожности во время лабораторных работ.
Онлайн-версия этой статьи (doi: 10.1186 / s12977-014-0070-3) содержит дополнительный материал, доступный для авторизованных пользователей.
Недавний интерес к латентности ВИЧ привел к разработке моделей клеток, которые повторяют вирусную латентность in vitro. Модель TCM, опубликованная Bosque и Planelles [1], представляет собой широко используемый метод. Эта модель, основанная на дифференцированных in vitro центральных ячейках памяти в сочетании с вирусом с дефицитом репликации, создает большое количество латентно инфицированных первичных клеток. Здесь мы показываем, что вирусная конструкция, используемая в этой модели, может стать репликацией, соответствующей рекомбинации. Мы наблюдали распространение инфекции и высокую изменчивость между повторными экспериментами с использованием этой модели TCM (дополнительный файл 1: рисунок S2). Это требует повторного анализа данных и представляет собой важную проблему биобезопасности в отношении использования подобных вирусных конструкций.
Первоначально используемую вирусную конструкцию получали с помощью вирусного вектора ВИЧ-1NL4.3-DHIV, содержащего 600 bp-делецию в рамке считывания env. Эту плазмиду совместно трансфицируют плазмидой pLET-LAI, содержащей последовательность env дикого типа из HIV-1LAI. Наши данные показывают, что вирусный супернатант состоит из смеси одиночных круглых векторов и грамотных вирусов репликации, генерируемых рекомбинацией между последовательностями env (рисунок 1, дополнительный файл 1). Рисунок 1
ПЦР и NGS-подтверждение рекомбинации между конструкциями DHIV и pLET-LAI как источник вируса, способного к репликации. Чтобы генерировать вектор, способный только к одному раунду репликации, вектор, используемый в исходной модели TCM, создается с помощью конструкции ENV с дефицитом DHIV, ко-трансфицированной интактным env. Рекомбинация между перекрывающимися последовательностями этих плазмид восстанавливает интактную последовательность env в вирусном геноме и продуцирует репликационно-компетентный вирус. (cfr. Дополнительный файл 1). А-С. Данные на основе ПЦР A. Праймерные пары, используемые в исследовании, выровнены с геном огибающей конструкции DHIV. Правая пара ENV выравнивается с общей последовательностью env DHIV и полной длины env, пара праймеров DEL выравнивается с интактной env-последовательностью в удаленной части (пунктирная линия) DHIV. ДО НАШЕЙ ЭРЫ. Электрофоретическое разделение продуктов ПЦР на плазмидной ДНК-NL4.3-IRES-HSA-E * и DHIV (B) и на ДНК из клеток, инфицированных указанными вирусами (C). Положительный сигнал в клетках, инфицированных DHIV + pLET-LAI, указывает на наличие полноразмерной env-последовательности в вирусной ДНК. D-F. Экспрессия РНК ВИЧ в скрытой модели TCM, полученная из анализа РНК-Seq 4 донорных клеток, инфицированных DHIV + pLET-LAI. D. Сюжет, представляющий количество раз, когда отдельные нуклеотиды были сопоставлены с геномом ВИЧ. Очерченная область указывает область env, удаленную в исходном DHIV. Большое количество отображаемых чтений указывает, что полная последовательность env выражена. E-F. Сюжет, представляющий считывания, охватывающий удаление в области env DHIV в начале (E) и конце (F) удаления. В совокупности электрофоретический анализ интегрированной провирусной ДНК и выравнивание NGS-считываний в области, первоначально содержащей делецию в env, показывают, что интактная последовательность env была восстановлена в конструкции.
Эти результаты могут быть неудивительными, учитывая строгие меры предосторожности, предпринятые в области лентивирусной трансдукции, требующие трех или четырех (до 7 а в суперраздельной системе [2]) отдельных плазмид для котрансфекции [3,4]. Однако в базовых исследованиях по ВИЧ все еще используются две векторные конструкции. В текущих выводах подчеркивается забота о биобезопасности лабораторий, работающих с векторами, которые предположительно являются репликацией, но могут стать полностью компетентными вирусами. Более того, эти данные побуждают к повторному анализу опубликованных данных, полученных из модели TCM, а также из данных с использованием аналогичных конструкций.
В оригинальной статье, описывающей модель TCM [1], NFAT характеризовался как основной фактор транскрипции, опосредующий реактивацию скрытых вирусов после стимуляции антигенами. Учитывая текущие данные, роль NFAT следует переоценить из-за его потенциального участия в двух разных явлениях: реактивации от латентности и повышении кинетики вирусной репликации, как описано ранее [5]. Нужны ли NF-κB или NFAT для реактивации скрытых вирусов в TCM. В соответствии с этим выводы о том, что путь JAK-STAT [6] или PIM-1 [7] необходимы для репликации вируса, все еще сохраняются, но данные не могут определить, является ли эффект результатом ингибирования реактивации или ингибирования репликации вируса кинетика.
В отличие от ранних интерпретаций [8], клеточное позитивное окрашивание p24 после стимуляции антигена не является однозначным признаком реактивированного вируса, а скорее комбинацией этого и распространением вирусной репликации. Поэтому количество латентно инфицированных клеток должно быть ниже, чем изначально предполагалось. Это, вероятно, повлияет на глубокие последовательности и транскриптомические эксперименты.
В недавнем исследовании сравнивались сайты интеграции между индуцированными и неиндуцированными провирусами по пяти латентным моделям, включая модель TCM [9]. Был использован вирус env (-), в котором nef был заменен GFP. После инфицирования клетки GFP (-) (предположительно, латентно инфицированные) сортировали и культивировали в течение 9 дней до анализа интеграционного сайта [9]. Несмотря на то, что стратегия сортировки исключала клетки, производящие ВИЧ, незначительная доля инфицированных клеток ранней стадии, которые еще не начали производить GFP, могла присутствовать и приводить к смещению данных. Использование антиретровирусной терапии, которая блокирует интеграцию, возможно, обеспечило количественную оценку степени этого смещения.
Интересно, что в модели TCM наблюдается явное увеличение p24 положительных клеток между образцами, обработанными ингибиторами интегразы, за которыми следует антигенная стимуляция, и образцы, которые не стимулируются. Это указывает на то, что часть инфицированных клеток скрыто инфицирована, несмотря на продолжающуюся репликацию. Таким образом, эта модель продолжает оставаться ценной для исследований по латентности ВИЧ. Это подтверждается результатами, которые были подтверждены в последующих или параллельных исследованиях с использованием альтернативных моделей.
В исследовании, характеризующем опосредованную IL-7 гомеостатическую пролиферацию [10], клетки инфицировали вирусом, кодирующим GFP, и делящиеся и не делящие GFP (-) клетки сортировали с использованием красителя для пролиферации. Оба подмножества переносили интегрированную ДНК ВИЧ и способны индуцировать вирусную продукцию после стимуляции антигена. Вывод о том, что клетки могут подвергаться гомеостатической пролиферации при отсутствии вирусного продуцирования, сохраняется, особенно учитывая стратегию сортировки. Этот механизм был поддержан данными in vivo [11]. Кроме того, данные, показывающие, что Pam3CSK4 [12] могут реактивировать ВИЧ-1, подтверждались двумя экспериментами ex vivo от ВИЧ-инфицированных авиремических пациентов. Аналогично, эффект ромадипсина на реактивацию ВИЧ, обнаруженный на экране лекарственного средства с использованием модели TCM, был подтвержден в модели ex vivo с использованием памяти пациента и покоящихся CD4 + Т-клеток [13].
Увеличение содержания p24 из-за реактивации после латентности после интеграции происходит быстро. Однако увеличение p24 из-за вирусной репликации происходит сравнительно медленнее, поскольку каждый цикл репликации требует входа, обратной транскрипции и интеграции. Следовательно, смещения в экспериментальных измерениях будут меньше при более коротких временах считывания (например, через 24 часа после реактивации), по сравнению с более длительными временами (например, через 72 часа после реактивации).
Репликационные компетентные вирусы, созданные в простых системах совместного трансфекции, могут влиять на результаты исследований в области биобезопасности и смещения. Исследователи должны предоставить доказательства, свидетельствующие о некомпетентности репликации новых конструкций. Полученные результаты влияют на ранние представления, связанные с моделью TCM, и поэтому вирус, первоначально включенный как часть этой модели, не может использоваться, как изначально описано [1]. Тем не менее, модель может по-прежнему быть пригодной для понимания латентности ВИЧ-1 при условии внесения определенных модификаций. Здесь есть два возможных варианта. Можно предпринять усилия, чтобы избежать рекомбинации путем внедрения генов огибающей, происходящих из не-ВИЧ-видов (например, VSV-G) [14], с использованием расколотых векторных систем, таких как эти, используемые в генной терапии, или более сложные системы совместной трансфекции с проверенным отсутствие рекомбинации. Альтернативно, модель может использоваться с компетентными вирусами репликации в сочетании с антиретровирусными препаратами, чтобы ограничить распространение инфекции. Наконец, мы хотели бы заявить, что мы уверены, что культивируемый TCM, сгенерированный, как описано Bosque и Planelles [1], по-прежнему является подходящей и подходящей моделью клеток для исследований ВИЧ-инфекции и латентности / реактивации, и что результаты описанные здесь, не влияют на способы получения таких клеток или их использование в лаборатории.
Дополнительный файл 1:
Экспериментальные результаты, подтверждающие рекомбинацию и исключение лабораторного загрязнения в качестве источника грамотного вируса репликации в модели Tcm, а также материалы и методы, связанные с исследованием.
На эту работу в равной степени внесли вклад Павел Бончковский и Уорд Де Шпигелере.
Авторы заявляют, что у них нет конкурирующих интересов.
PB, WDS, AB и LV разработали и спроектировали эксперименты. PB, AB, EM, MK и AVN провели эксперименты. PB, LV, WDS, AB, BV и VP проанализировали данные. CHW и CHW генерировали и анализировали данные NGS. LV, WDS, AVN, WT, JV, WW и BV предоставили техническую экспертизу на протяжении всего эксперимента. PB, WDS и LV написал рукопись. Все авторы прочитали и утвердили окончательную рукопись.
Лентивирусные векторы: как они стали лучшими векторами для терапии ex vivo
Лентивирусные векторы: как они стали лучшими векторами для терапии ex vivo
Иногда самый безопасный и эффективный вариант генной терапии — не вводить вектор непосредственно пациенту, а наоборот, выделить клетки пациента, произвести с ними генно-инженерные манипуляции и ввести обратно ему же. В таком случае непревзойденный инструмент — лентивирусные векторы. Рисунок в полном размере.
Автор
Редакторы
Генная и клеточная терапии
Спецпроект о генной и клеточной терапиях, тернистом пути их развития, первых успехах и надеждах, а также о сложностях регулирования, производства и изучения этих новейших методов лечения.
Партнер спецпроекта — Департамент разработки генотерапевтических препаратов одной из крупнейших российских биотехнологических компаний — BIOCAD. BIOCAD заслужил серьезные позиции на мировом фармацевтическом рынке благодаря выпуску лекарственных препаратов на основе антител.
Со времени зарождения генной терапии — начиная с самых первых исследований и клинических испытаний — дорога к ее широкому внедрению была тернистой. Впечатляющие успехи чередовались с досадными провалами, отбросившими на новое лечение порочащую тень, что в какой-то момент резко затормозило развитие области [1].
Вы читаете пятую статью спецпроекта «Генная и клеточная терапии». Ранее мы уже информировали вас, как вообще устроены лекарства будущего [2], а также достаточно подробно останавливались на аденоассоциированных вирусах [3] как важном инструменте «генных терапевтов».
Подробнее о тернистом пути разработки и производства генного лечения читайте в статье: «Генные и клеточные лекарства: сложное регулирование для сложных продуктов» [4]; ну а об экономических перипетиях при внедрении сверхдорогих инновационных лекарств (да и не только их) расскажет статья: «Фармакоэкономика: лечить или экономить?» [5].
Однако генная терапия по-прежнему более чем актуальна, ведь она предлагает регулирование молекулярных процессов на новом уровне, тем самым позволяя подбирать ключи к лечению ранее неприступных болезней.
Существующие ныне генные терапии в основном работают по принципу внедрения нужного генетического материала в определенные клетки пациента, что и позволяет модулировать происходящее в организме с лечебными целями. Поэтому для такого лечения критически важна успешная доставка требуемого гена в целевые клетки и ткани, что чаще всего осуществляют с использованием особых носителей — векторов.
In vivo vs Ex vivo
В предыдущих статьях нашего цикла о генной терапии уже были довольно подробно разобраны имеющиеся ныне решения. Не будем сильно повторяться, но отметим особо важные для дальнейшего повествования моменты.
Терапия in vivo — это прямой перенос векторов в организм пациента путем внутривенной инфузии раствора, содержащего такие носители. В такой доставке наилучшим образом проявили себя аденоассоциированные векторы, поскольку имеют широкий тропизм — специфичность к различным типам клеток, а также низкий уровень генотоксичности и соответственно бóльшую безопасность [3].
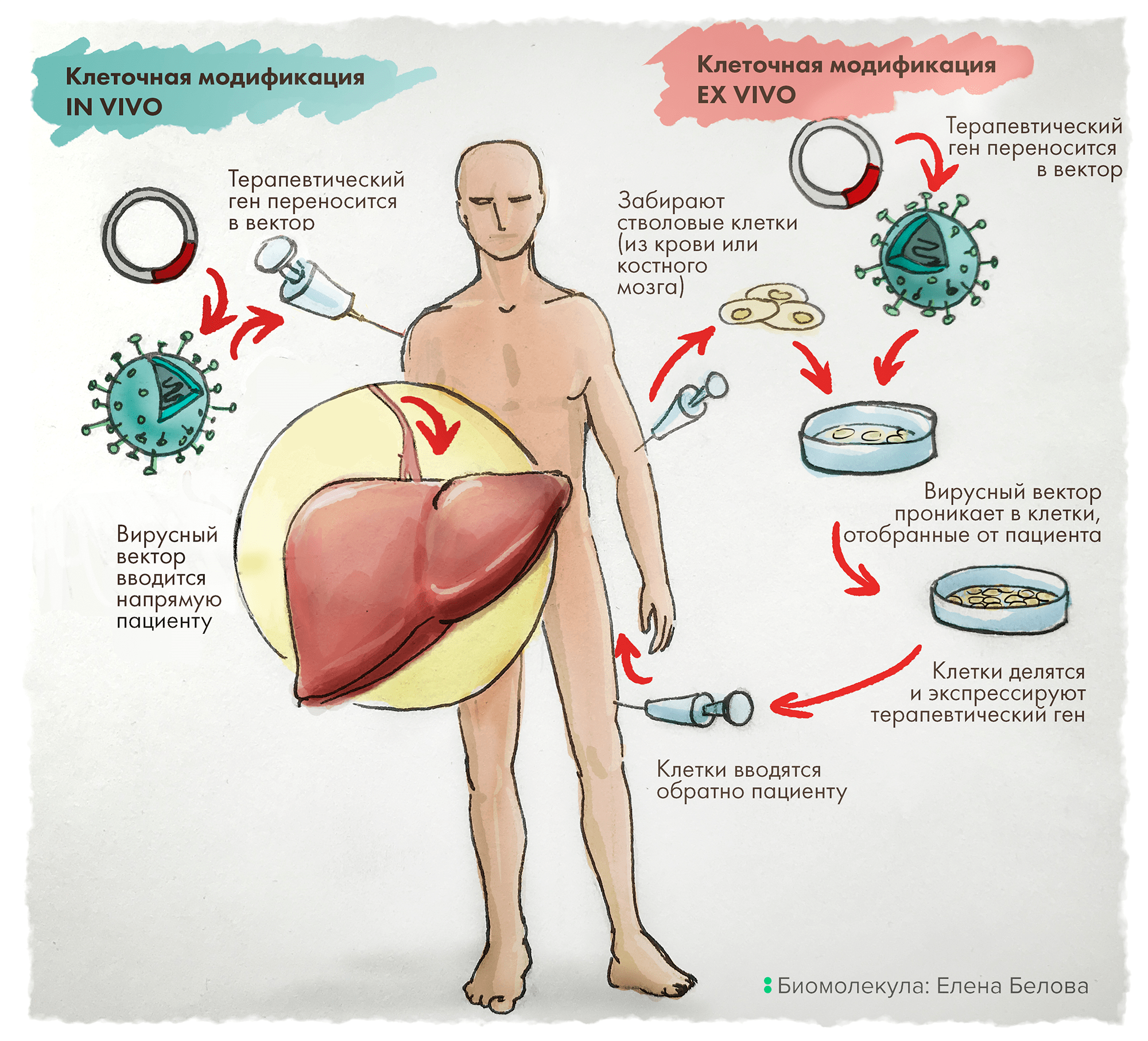
Альтернативно терапевтический ген может быть доставлен ex vivo: для этого клетки сначала отбирают у пациента, генетически модифицируют и культивируют вне организма. И только после этого такие несущие целевые (читай — терапевтические) гены клетки вводят путем инфузии обратно пациенту (рис. 1) [6].
Рисунок 1. In vivo vs Ex vivo. Терапия in vivo заключается в прямой доставке в организм пациента векторов, содержащих терапевтические гены. В отличие от этого, подход ex vivo включает предварительный отбор клеток у пациента, их генетическую модификацию in vitro (это, как правило, внедрение нужного — лечебного — гена), затем отбор эффективно трансдуцированных клеток с последующим размножением и введением такой культуры клеток обратно пациенту.
Для клинических приложений терапии ex vivo изначально были особо интересны γ-ретровирусы и лентивирусы, — ведь они способны перманентно интегрировать свой генетический материал в геном клеток организма-хозяина, что подразумевает передачу генов интереса при делении в ряду клеточных поколений, а значит, низкую элиминацию и долгоиграющую экспрессию.
Однако по сравнению с γ-ретровирусными векторами лентивирусы оказались безопаснее в доклинических исследованиях, а потому сейчас преимущественно используются именно они [7]. Лентивирусные векторы способны еще и трансдуцировать как постмитотические, так и неделящиеся клетки, в то время как для эффективного инфицирования с использованием других ретровирусных платформ требуется, чтобы клетка активно делилась [6]. Дело в том, что среди всех ретровирусов только лентивирусы способны проникать через ядерную мембрану.
Серьезными плюсами лентивирусных векторов являются также относительно низкая стоимость и возможность масштабирования производства. Эта платформа была выбрана для создания одной из наиболее многообещающих ныне генных терапий ex vivo: онколечения с использованием CAR-T-клеток [8], — и используется сегодня при разработке таких препаратов наряду с γ-ретровирусами. К этому мы еще вернемся.
Лентивирусы в природе: что они собой представляют?
Строение
Под положительной (+) РНК понимают геномную нуклеиновую кислоту вируса, похожую на мРНК, благодаря чему информация в ходе трансляции — синтеза полипептидной цепи вирусного белка в зараженной клетке — может считываться непосредственно с нее. Такую (+)РНК называют также смысловой. В отличие от этого, антисмысловая (−) РНК комплементарна мРНК, и для перевода в аминокислотную цепочку ее требуется сначала реплицировать в (+)-форму с помощью фермента РНК-репликазы.
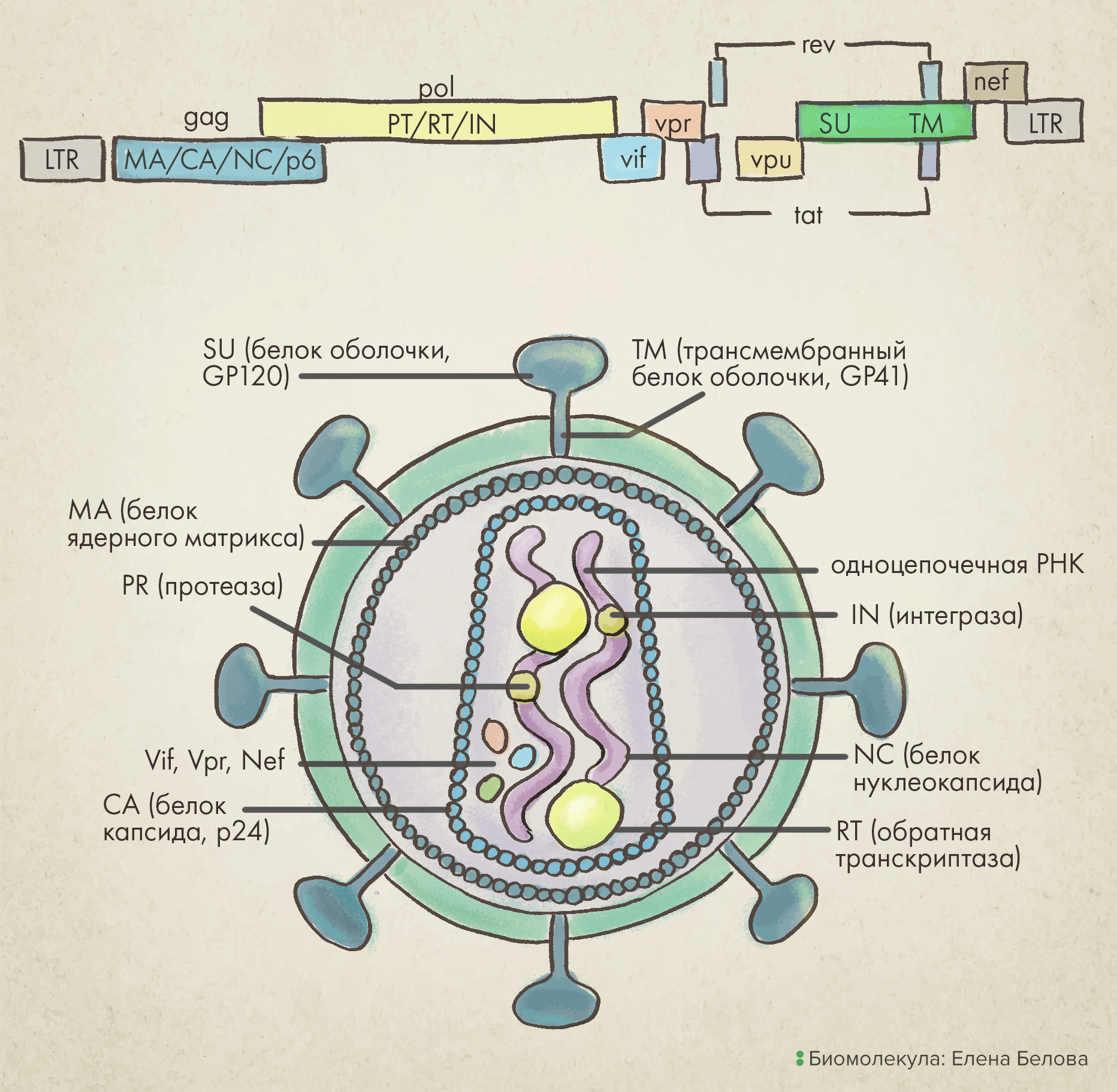
Рисунок 2. Лентивирус: геномная карта и структура вириона. Важный для проникновения в клетку ген env обозначен зеленым цветом.
Ген gag первым транскрибируется в незрелую пре-мРНК, которая затем расщепляется на отдельные транскрипты, кодирующие три белка вирусного кора:
Ген pol кодирует ферменты, необходимые для репликации генетического материала: вирусную протеазу (PRO), обратную транскриптазу (RT) и интегразу (IN).
Наконец, ген env кодирует белок вирусной поверхности: гликопротеин gp160, который в процессе созревания вирусной частицы расщепляется на белок поверхности вириона gp120 (SU) и трансмембранный белок gp41 (TM).
Кроме того, вирусный геном содержит регуляторные гены (tat и rev), которые после инфицирования вирионом экспрессируются первыми и нужны для ускорения продукции мРНК, а также четыре вспомогательных гена (vif, vpr, vpu, и nef) [10].
Жизненный цикл лентивирусов
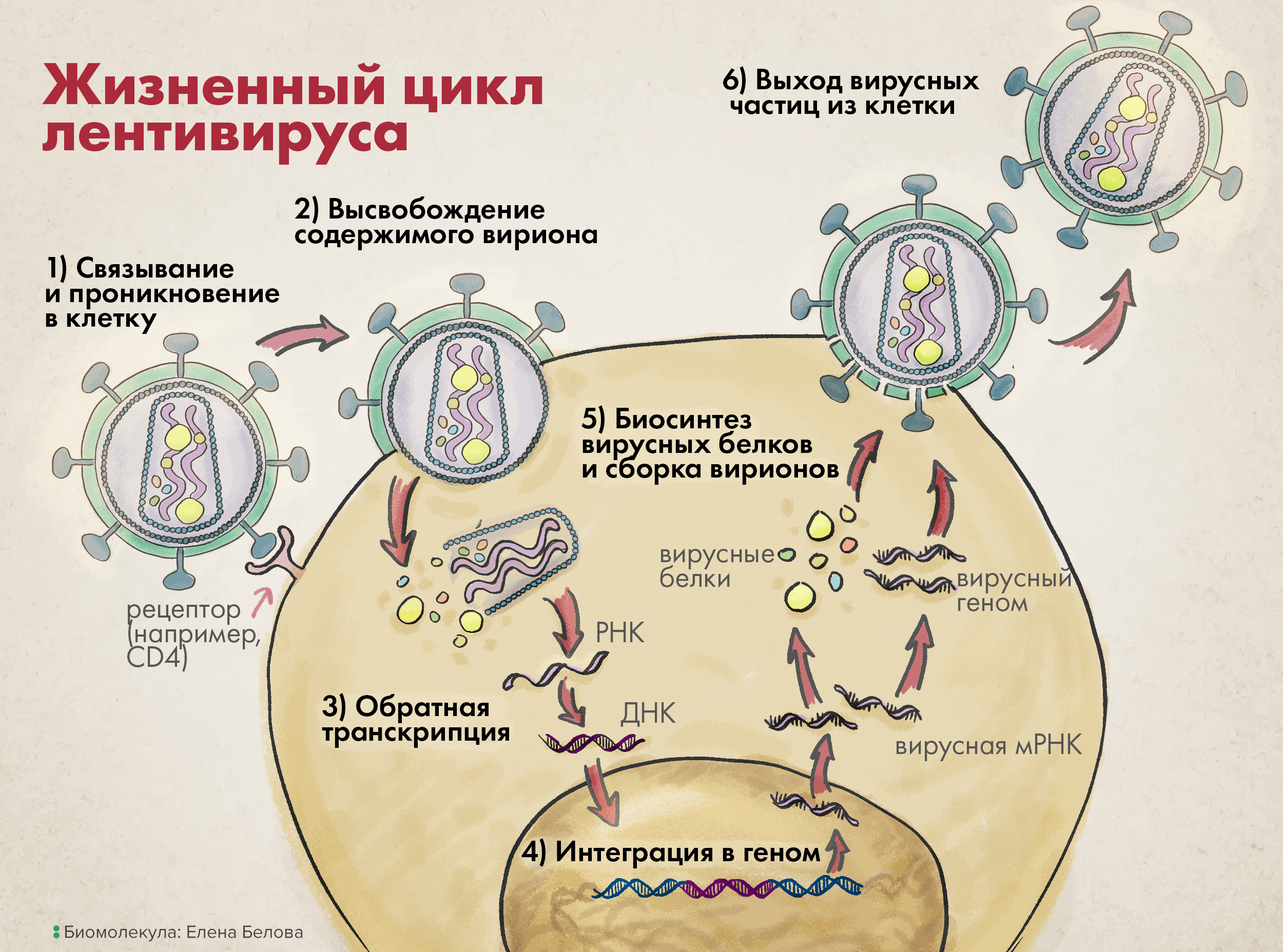
Жизненный цикл лентивируса можно немного обобщить и представить в виде шести основных шагов (рис. 3).
На первой стадии вирион связывается со своей клеткой-мишенью через взаимодействие между белком вирусной оболочки gp120 (SU) и особым рецептором клеточной поверхности.
Существование этих поверхностных и специфичных белков-рецепторов собственно и определяет особую способность вирусов инфицировать строго определенные типы клеток (известную также как тропизм).
Рисунок 3. Жизненный цикл лентивируса. 1. Связь с клеточной поверхностью и проникновение в клетку. 2. Высвобождение содержимого вириона во внутриклеточную среду. 3. Обратная транскрипция. 4. Интеграция в геном. 5. Биосинтез вирусных белков и сборка вирионов. 6. Выход вирусных частиц из клетки.
При инициации цикла заражения вирусом ВИЧ, помимо взаимодействия гликопротеина SU с первичным рецептором СD4 на поверхности лимфоцитов Т-хелперов (что и определяет патогенез ВИЧ-инфекции), происходит также его связывание с корецепторами: CXCR4 или CCR5.
Затем вирусные трансмембранные белки (TM) изменяют свою конформацию, чтобы сблизить вирион и клетку, что приводит к слиянию их мембран и проникновению вируса в клетку (этап 1 на рисунке 3).
После входа в клетку матрикс вируса — то есть все его содержимое, кроме слившегося с мембраной клетки суперкапсида, — распределяется в цитоплазме на составляющие элементы: структурные белки капсида, нуклеиновые кислоты вирусного генома, а также ферменты, необходимые для успешной репродукции генетического материала (этап 2 на рисунке 3).
Используя вирусную РНК как шаблон, а также нуклеотиды зараженной клетки, обратная транскриптаза начинает синтезировать комплементарную вирусную ДНК, а точнее — провирусную ДНК (этап 3 на рисунке 3); последняя затем импортируется в клеточное ядро, вставляясь там с использованием вирусной интегразы в геном клетки-мишени (этап 4).
Дальнейшая репродукция генетического материала идет уже как по нотам: в соответствии с центральной догмой молекулярной биологии. Из последовательности провируса в геноме транскрибируются одноцепочечные (+)РНК, затем с них транслируются вирусные белки (этап 5); они упаковывают вирусные нуклеиновые кислоты так, чтобы в одном вирионе таких последовательностей было две (этап 5).
После этого сформированные вирусные частицы, прорывая цитоплазматическую мембрану, выходят из клетки, формируя из ее фрагментов свой суперкапсид (этап 6 на рисунке 3). Ну а такие новые вирионы заражают уже другие клетки, и весь описанный цикл повторяется [10].
Создание лентивирусных векторов
Теперь мы знаем, как структурно устроены лентивирусы, каков их жизненный цикл, но пока еще не разобрались, что собой представляют лентивирусные векторные системы, — как они работают и как их производят. Что же, рассмотрим и этот вопрос.
Безопасность превыше всего
Рекомбинация
Лентивирусы имеют высокую частоту рекомбинации (обмена частями генома между двумя вирусами) и быстро мутируют. Отсюда естественные опасения, что векторы на их основе смогут самопроизвольно воспроизводиться в организме человека и благодаря дальнейшей «перетасовке генов» приводить к появлению суперинфекций. Чтобы снизить подобные риски при разработке векторных систем, основные гены исходных вирусов стали распределять в отдельные плазмиды. При этом полученные векторы (уже неспособные к репликации) — далее еще и последовательно улучшали: на сегодняшний день сменилось уже три поколения таких частиц.
Инсерционный мутагенез
Помимо образования репликационно компетентного вируса, вторым основным риском при применении ретровирусных векторов является онкогенез, возникающий за счет так называемого инсерционного мутагенеза. Критически важно оценивать такие риски, ведь γ-ретровирусы имеют тенденцию встраиваться вблизи генных регуляторных последовательностей, что представляет большую опасность. В частности, в клинических исследованиях с использованием таких частиц фиксировались случаи смерти от развившегося лейкоза [11].
Именно поэтому в поле генной терапии наблюдается постепенное смещение в пользу преимущественного использования лентивирусных векторов, которые намного безопаснее [12]. Они предпочитают транскрипционно активные регионы, но интегрируются в основном в «тело гена» (преимущественно в интроны), избегая энхансеров и промоторов, — что и снижает (и довольно существенно) риски онкогенеза [11], [12].
Поскольку инсерция в транскрипционно активные регионы все же может быть генотоксичной, для усиления биобезопасности разработали так называемые самоинактивирующиеся векторы (self-inactivating, SIN). Они обладают делецией в регионе 3′-LTR вирусного генома: во время обратной транскрипции эта делеция переносится на 5′-LTR провирусной ДНК, что подавляет транскрипционную активность.
Это предотвращает продукцию полноразмерного вируса (после интеграции векторного генома в геном клетки-хозяина), минимизируя тем самым вероятность возникновения репликационно активных вирусных частиц [13]. Более того, такая делеция снижает вероятность, что клеточные кодирующие последовательности, в которые встроился вектор, будут аберрантно экспрессироваться в связи с активностью промотора или через энхансерный эффект. Наконец, дизайн SIN предотвращает потенциальную транскрипционную интерференцию между LTR и промотором, управляющим экспрессией трансгена [13].
Другая повышающая безопасность модификация заключается во включении синтетического инсулятора хроматина в лентивирусные векторы, что снижает взаимодействия между трансгеном и ближайшими к нему генами, также уменьшая возможность аберрантной экспрессии.
Кроме того, правильный подход к дозированию векторов позволяет избегать множественных интеграционных событий в клетке. В идеале требуется подобрать такую дозу, чтобы интеграция происходила в среднем один раз на клетку [12].
В совокупности, все перечисленные меры снижают риск генотоксичности, однако говорить о том, что он сведен на нет, пока еще рано. В нескольких последних исследованиях с использованием лентивирусных векторов были зафиксированы случаи возникновения онкологических заболеваний. В двух из них после проведения расследования испытания продолжили, так как вероятность связи генной терапии и онкозаболеваний посчитали пренебрежимо малой.
Три поколения векторов
Первые лентивирусные векторные системы содержали три плазмиды: трансферную (transfer), оболочечную (envelope), и упаковочную (packaging).
Упаковочная плазмида содержала бóльшую часть генома исходного вируса: структурные, ферментативные, регуляторные и вспомогательные последовательности, — и не включала гены, кодирующие поверхностные белки вириона. А ведь именно они нужны для связи с клеткой и проникновения в нее, что является ключевым этапом репликативного цикла. Поэтому такие векторные системы (с удаленным геном env) — к репликации уже неспособны, однако уметь проникать в клетку они ведь все же должны — иначе как же они доставят туда целевые гены?
За это отвечает оболочечная плазмида, несущая последовательность вирусного гликопротеина (такого как оболочечный гликопротеин G вируса везикулярного стоматита VSV-G) для помощи векторной частице в связывании с рецепторным белком на поверхности клетки.
Эта технология, основанная на общем свойстве большинства ретровирусов, — возможности формировать так называемые псевдотипы (частицы, в оболочку которых включается поверхностный белок какого-то другого вируса) — позволила расширить диапазон поражаемых ими клеток. Псевдотипированные белком VSV-G векторы обладают уникальными преимуществами: большей стабильностью, а также способностью связываться с рецепторами LDL (липопротеинов низкой плотности), присутствующим на поверхности множества клеток, — что и определяет широкий тропизм этих частиц [10]. Существуют и другие варианты псеводтипирования векторов, расширяющие их тропизм (табл. 1).
| Лентивирусные псевдотипы | Исходный вирус (у которого «позаимствован» поверхностный гликопротеин вирусной оболочки) | Клеточный рецептор, с которым связывается псевдотип | Клеточный тропизм | Эффективность |
|---|---|---|---|---|
| VSV-G | Вирус везикулярного стоматита | LDL-R | Широкий тропизм в не первичных (подвергнутых хотя бы одному пассивированию) культурах клеток | Высокая |
| BaEV | Эндогенный ретровирус павиана | ASCT-1 ASCT-2 | CD34+ клетки | 30% |
| Наивные Т-клетки | До 80% | |||
| Наивные В-клетки | 40% | |||
| В-клетки памяти | 20% | |||
| Натуральные киллеры | 40% | |||
| Ранние тимоциты | До 80% | |||
| RD114 | Эндогенный ретровирус кошек | ASCT-2 | Наивные Т-клетки | До 60% |
| Наивные В-клетки | До 30% | |||
| H/F | Вирус кори | SLAM CD46 | CD34+ клетки | ── |
| Покоящиеся Т-клетки памяти | ── | |||
| Наивные Т-клетки | До 50% | |||
| Покоящиеся В-клетки | ||||
| Покоящиеся гемопоэтические стволовые клетки | До 70% | |||
| Дендритные клетки | ||||
| G/F | Вирус Нипах | EphinB2/B3 | Перициты | 20–40% |
| Клетки эндотелия опухоли | ||||
| COCV | Везиколовирус Кокал | LDL-R | Стимулированные клетки CD34+ | До 80% |
Наконец, последний компонент векторной системы первого поколения — трансферная плазмида — несет целевой трансген, а также так называемую последовательность пси-петли (ψ-петли), — и все это в обрамлении длинных терминальных повторов (long terminal repeats, LTRs). Последние два элемента необходимы для упаковки вирусной РНК в вирион (рис. 4).
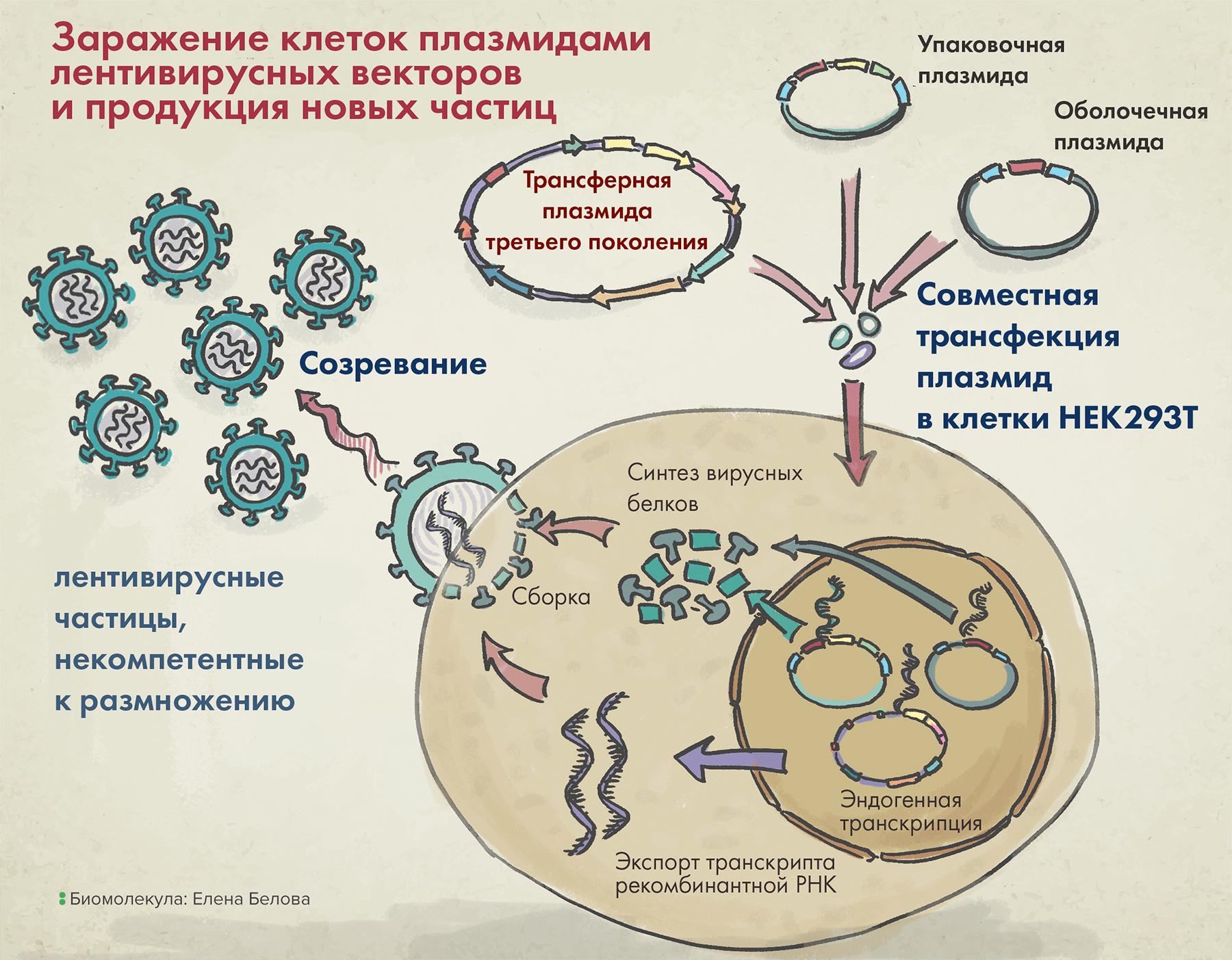
Рисунок 4. Упаковка лентивирусных векторов в клетке (на примере третьего поколения таких систем).
После заражения клеток тремя вышеназванными плазмидами в них происходит сборка вирусных частиц, а затем уже их выход наружу. Высвобождаемые векторы содержат VSV-G (он помогает им впоследствии проникать в клетки), но внутри них нет гена, кодирующего этот белок. Так происходит потому, что в кодирующей VSV-G плазмиде отсутствуют генетические последовательности, необходимые для сборки белковой вирусной оболочки, а значит, все ее содержимое запаковаться в вирион уже не сможет.
Поэтому такие частицы умеют доставлять гены в клетку, но не способны размножаться. Чтобы они вдруг снова научились этому, необходима рекомбинация между нашими векторами и, например, природными лентивирусами. Гипотетически это возможно, хоть и маловероятно, — ведь для восстановления репликативно компетентного генома должно многое совпасть: одновременное заражение клеток и вектором, и вирусом, а также прицельный обмен между ними генетическим материалом, — что в силу случайного характера рекомбинации вряд ли случится.
Тем не менее чтобы обезопаситься еще больше, исследователи стали менять исходный геном лентивируса еще сильнее: разбивать его на большее число плазмид, удалять еще больше нецелевых генов, а также модифицировать все необходимые в векторе нативные последовательности. Такие стратегии легли в основу создания лентивирусных векторов второго и третьего поколений (табл. 2).
| Характеристика | Второе поколение | Третье поколение |
|---|---|---|
| Количество плазмид | 3 | 4 |
| Наличие делеции в области U3 в 3′ LTR — для создания самоинактивирующегося вектора (Self-INactivation, SIN) | Нет | Да |
| 5′ LTR | Дикого типа (5′ LTR) | Химерные (RSV) |
| Количество упаковочных плазмид | 1 | 2 |
| Вспомогательные гены: vif, vpr, vpu, nef | Отсутствуют | Отсутствуют |
| tat и rev гены | В упаковочной плазмиде | Ген tat удален, rev в отдельной упаковочной плазмиде |
| gag и pol гены | В упаковочной плазмиде, вместе с tat и rev | Вместе в отдельной плазмиде |
| Псевдотипирование | Псевдотипированы (VSV-G) | Псевдотипированы (VSV-G) |
| Количество рекомбинационных событий, необходимых для генерации репликационно компетентных вирусов | 3 рекомбинации | 4 рекомбинации |
Производство
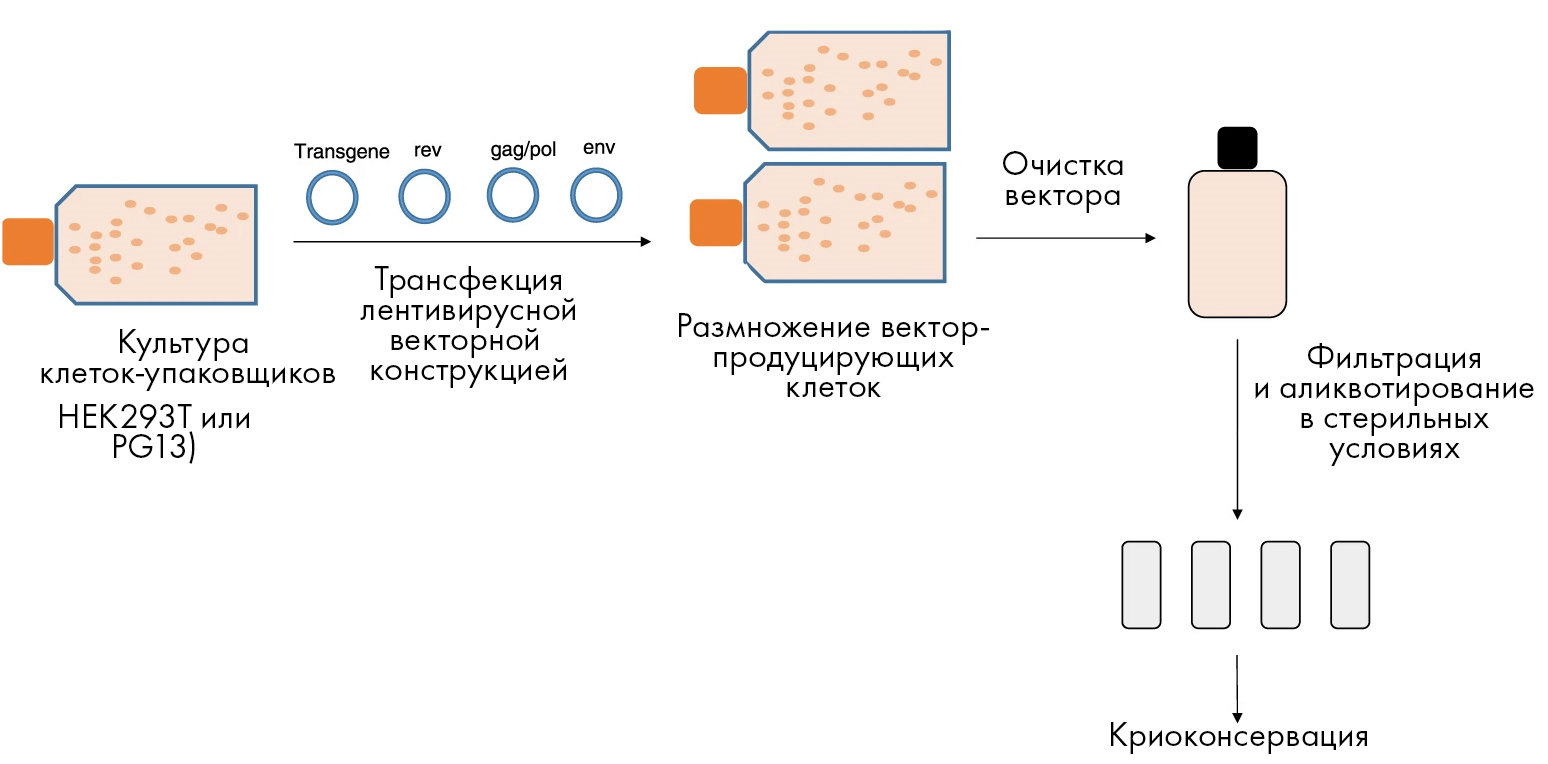
Создание эффективных векторных систем — это лишь первый этап к достаточной продукции нужного материала. Не менее важна разработка технологии производства и ее последующее масштабирование на большие объемы, — чтобы можно было получать требуемые частицы в нужных количествах. При этом в современном мире продукция вирусных частиц для лечебного применения должна идти по Правилам надлежащей производственной практики (известной также как GMP). На рисунке 5 даны основные стадии производства лентивирусных векторов.
Рисунок 5. Основные этапы продукции вирусных векторов на современном производстве, работающем в соответствии с принципами GMP. Все начинается с культуры специальных «клеток-упаковщиков» (таких как HEK293T или PG13). Эти особые упаковочные линии культивируют в течение нескольких дней, заражают плазмидами третьего поколения лентивирусного вектора, и затем уже такие вектор-продуцирующие клетки снова размножают в культуре. После этого векторы выделяют и очищают от остатков клеток (т.н. дебриса: различных клеточных органелл, плазмалеммы и т.д.), а также других загрязняющих примесей. После очистки содержащий векторы полупродукт фильтруют через мембрану с определенным размером пор, не пропускающюю микроорганизмы (что позволяет достичь стерильности). Далее полученный сток асептично распределяют по отдельным аликвотам и криоконсервируют. Сообщалось, что такие замороженные при −80 °С векторы могут сохранять свою стабильность до 9 лет после криоконсервации. Стоит также отметить, что в течение всего описанного процесса очень важен контроль качества, ведь, например, не до конца удаленный из стоков вектора клеточный дебрис может вызывать воспалительные реакции, что было показано в исследованиях как in vitro, так и in vivo [15].
Альтернатива: стабильные упаковщики
Еще один способ получать лентивирусные векторы, помимо временной трансфекции плазмидами, — создание стабильных линий клеток-упаковщиков. Для этого геном клеток (чаще всего это клетки почки человеческого эмбриона HEK293T) модифицируют так, чтобы они смогли стабильно экспрессировать бóльшую часть вирусного генетического материала.
Такие клетки-упаковщики, как правило, экспрессируют гены gag, pol и rev, а зачастую также ген капсида VSV-G. Далее для использования в качестве продуцентов векторов их нужно заразить плазмидой, несущей целевой ген.
Пока что такие стабильные линии используют реже чем «стандартные» клетки-продуценты, ─ но перспективы расширения их применения весьма заманчивы. Они могут осуществлять долгоиграющую экспрессию, что крайне желательно, ─ так как позволит упростить производство, снизив тем самым и его стоимость [16].
Применение лентивирусных векторов в клинике
С момента первых применений лентивирусные векторы стали одним из основных инструментов арсенала генной и клеточной терапии с заметными успехами в клинических исследованиях [17]. Одна из причин — они изначально обладали большим потенциалом благодаря способности эффективно трансдуцировать CD34 + стволовые клетки. Из последних, как известно, в процессе гемопоэза появляются все остальные типы кровяных клеток [18], а потому их генетическая модификация была крайне привлекательна. Ведь после дифференциации эти измененные клетки теоретически смогут остановить (или хотя бы притормозить) патогенез самых разных связанных с ними болезней.
Ученым и медикам оставалось лишь проверить эту теорию практикой, и вскоре перенос генов с использованием лентивирусного вектора в CD34+ стволовые клетки был осуществлен для лечения нескольких генетических заболеваний. Среди них: бета-талассемия, серповидноклеточная анемия, Х-сцепленная адренолейкодистрофия, метахроматическая лейкодистрофия, синдром Вискотта—Олдрича и др. При этом о наличии каких-либо связанных с вектором серьезных нежелательных явлениях в этих исследованиях заявлено не было (о первом тревожном сигнале, связанным с онкогенезом, рассказано выше) [15].
Ранние успехи подстегнули развитие такого лечения, и, согласно регистру клинических испытаний ClinicalTrials.gov, функциональность лентивирусного вектора сейчас уже тестируют более чем в 4000 исследований. При этом известно, что и количество подобных испытаний непрерывно и экспоненциально растет, например: в 2017 г. их было около 200, в 2020-м — более 600 [19], ну а сегодня, как видим, — уже на порядок больше. Из такого обширного поля настоящими прорывами можно назвать уже одобренное лечение, — а это пока что два генных продукта:
Заключение и перспективы
Одно из направлений улучшения генной терапии — разработка новых векторов-носителей. В частности, представляют интерес не интегрирующиеся лентивирусные векторы (non-integrating lentiviral vectors, NILVs) — они привлекательны в плане снижения вероятности инсерционного мутагенеза. В них выключен фермент вирусная интеграза (как мы помним, отвечающая за внедрение провирусной последовательности в геном клетки) — и они точно так же умеют инфицировать как делящиеся, так и неделящиеся клетки. При этом вирусный геном остается в клетке в виде эписомы, а не интегрируется в геномную ДНК [15].
NILVs стабильно экспрессируют трансгены из эписомальной ДНК в неделящихся клетках, и временно — если клетки-мишени размножаются. Было показано, что такие векторы имеют широкий тропизм ко множеству различных типов клеток и тканей, что вкупе с повышенной безопасностью делает их идеальными кандидатами для использования в вакцинации и иммунотерапии.
Это также открывает перспективы использования NILVs как инструмента для доставки компонентов CRISPR/Cas9 — революционной технологии, которая ныне широко используется в исследованиях генного редактирования. Она включает так называемую направляющую РНК, помогающую распознавать нужные участки генома в клетке для связи с ними нуклеазы Cas9. Последняя начинает в этом месте расщеплять спираль ДНК, создавая двухцепочечные разрывы, которые затем могут быть репарированы определенным образом — с удалением (делецией) каких-либо «поломанных» генов, или внедрением в этом месте каких-то новых кодирующих последовательностей.
Сегодня существуют лентивирусные системы, умеющие доставлять в клетку как направляющие РНК, так и нуклеазу Cas9 (точнее кодирующие их последовательности — для последующей экспрессии).
Лентивирусные векторы также часто используют в исследовательских целях для изменения экспрессии генов посредством использования короткой шпилечной РНК или антисмысловой РНК [23], — что является частью уже известного механизма РНК-интерференции (об этом интересном феномене «Биомолекула» писала уже не раз).
Конечно, пока что большинство из таких перспективных подходов все еще находится на ранних стадиях разработки, и необходимы дальнейшие исследования, чтобы определить, насколько лентивирусные векторы по настоящему «жизнеспособны» — как инструмент для терапевтической доставки компонентов редактирования/регуляции экспрессии тех или иных генов [15].