что такое рекомбинантная векторная вакцина
Что такое рекомбинантная векторная вакцина
Генно-инженерные вакцины содержат Аг возбудителей, полученные с использованием методов генной инженерии, и включают только высокоиммуногенные компоненты, способствующие формированию защитного иммунитета (более подробно см. главу 7). Возможны несколько вариантов создания генно-инженерных вакцин.
• Внесение генов вирулентности в авирулентные или слабовирулентные микроорганизмы.
• Внесение генов вирулентности в неродственные микроорганизмы с последующим выделением Аг и его использованием в качестве иммуногена.
• Искусственное удаление генов вирулентности и использование модифицированных организмов в виде корпускулярных вакцин.
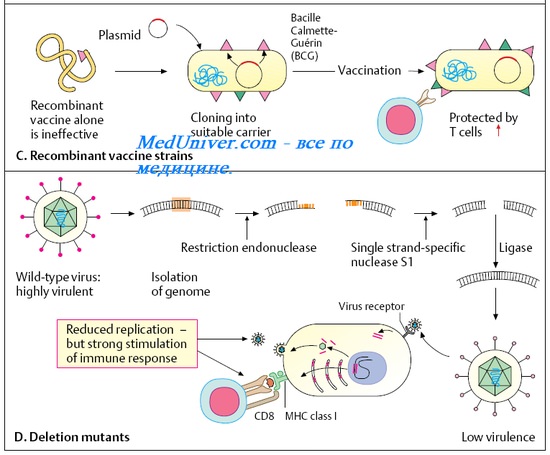
Ряд современных противовирусных вакцин сконструирован путём введения генов, кодируюших основные Аг патогенных вирусов и бактерий в геном вируса осповакцины (HBsAg вируса гепатита В) и непатогенных для человека сальмонелл (HBsAg вируса гепатита В и Аг токсина столбнячной палочки). Другим примером служит введение генов возбудителя туберкулёза в вакцинный штамм БЦЖ, что придаёт ему большую активность в качестве дивергентной вакцины. Такие препараты известны как векторные вакцины.
Для активной иммунопрофилактики гепатита В также предложена вакцина, представляющая собой HBsAg вируса. Его получают из дрожжевых клеток, в которые введён вирусный ген (в форме плазмиды), кодирующий синтез HBsAg. Препарат очищают от дрожжевых белков и используют для иммунизации. В качестве метода более быстрой и дешёвой наработки бактериальных экзотоксинов в настоящее время разработаны методы их получения при помощи неприхотливых микроорганизмов, в геном которых искусственно внесены гены токсинообразования (например, в виде плазмид).
Синтетические вакцины
Принцип конструирования вакцин включает синтез или выделение нуклеиновых кислот или полипептидных последовательностей, образующих Aг-детерминанты, распознаваемых нейтрализующими AT. Непременные компоненты таких вакцин — сам Аг, высокомолекулярный носитель (винилпирролидон или декстран) и адъювант (повышающий иммуногенность вакцин). Подобные препараты наиболее безопасны в плане возможных поствакцинальных осложнений, но их разработке мешают две проблемы. Во-первых, не всегда имеется информация об идентичности синтетических эпитопов естественным Аг. Во-вторых, низкомолекулярные синтетические пептиды обладают низкой иммуногенностью, что приводит к необходимости подбора соответствующих адъювантов.
С другой стороны, введение синтетических вакцин в комбинации с адъювантами и иммуномодуляторами перспективно у лиц с нарушениями иммунного статуса. Особые перспективы имеет использование нуклеиновых кислот для иммунопрофилактики инфекций, вызываемых внутриклеточными паразитами. В эксперименте показано, что иммунизация организма РНК и ДНК многих вирусов, малярийного плазмодия или возбудителя туберкулёза приводит к развитию стойкой невосприимчивости к заражению.
Национальный Фармацевтический журнал
Войти на сайт
ВАКЦИНЫ ПРОТИВ COVID-19 И АДЪЮВАНТЫ, УЛУЧШАЮЩИЕ ИХ СВОЙСТВА.

Новый адъювант для профилактических вакцин компании SEPPIC

• вакцины на основе цельного (полногеномного) ослабленного вируса;
• инактивированные вакцины на основе полностью нежизнеспособного вируса;
• векторные вакцины;
• генетические вакцины (ДНК и РНК вакцины);
• субъединичные вакцины на основе отдельных компонентов патогена, таких как белки, пептиды или генетический материал (например, белковые или рекомбинантные вакцины). Разработчики из различных стран на основании накопленных знаний и имеющихся у них результатов и методов исследований выбирают для разработки тот тип вакцины, который считают наиболее действенным для обеспечения эффективной защиты людей от вируса SARS-CoV-2 (Рис.1).
На настоящий момент среди вакцин-кандидатов против COVID-19, зарегистрированных в списке ВОЗ, можно найти практически все из вышеназванных типов вакцин. Коротко напомним, что представляет собой каждый из них и чем они отличаются друг от друга.

Векторные вакцины – это также вакцины на основе живых вирусов, однако здесь есть небольшой, но очень важный нюанс: это вакцины на основе хорошо изученных и достаточно безобидных для человека вирусов («векторов» или вспомогательных транспортных вирусов) с встроенными в них фрагментами генома «злого вируса» (Рис. 3). В случае векторных вакцин в геном хорошо изученного и, в целом, безобидного вируса, например, аденовируса («вектора»), путём генетических модификаций встраивается небольшой ген – участок генома SARS-CoV-2. При вводе в организм такой векторной вакцины генетически модифицированные вспомогательные вирусы провоцируют такой же сильный иммунный ответ на белки-антигены SARS-CoV-2, как в случае «живой» полногеномной вирусной вакцины.
Преимущество указанных вакцин, по замыслу разработчиков, в той же высокой эффективности, что и у вакцин на основе живых ослабленных вирусов, но в большей управляемости в связи с достаточной изученностью и предсказуемостью «вектора»-носителя. Векторные вакцины начали разрабатываться и изучаться относительно недавно, поэтому к массовому применению вакцин этого типа ученые также подходят с должной и необходимой осторожностью.

Еще два перспективных типа вакцин против COVID-19, разрабатываемые мировым сообществом, – вакцины на основе нуклеиновых кислот, а именно, ДНК- и РНК-вакцины. В случае ДНК-вакцины нуклеотидная последовательность, кодирующая антиген SARS-CoV-2, встраивается в вектор – бактериальную плазмиду – небольшую стабильную кольцевую молекулу ДНК, способную к автономной репликации. Сама по себе плазмида не вызывает нужного специфического иммунного ответа, для этого, собственно, в неё и вшивают гены иммуногенных белков. Указанный модифицированный геном направляется в клетку, встраивается в ее ядро и образует вирусный белок (антиген), индуцирующий иммунный ответ.
Согласно замыслу разработчиков, ДНК-вакцины не могут вызвать заражение SARS-Cov-2, однако иммунитет, который они обусловливают, должен оказаться таким же сильным, как в случае «живых» вакцин. Тем не менее, влияние ДНК-вакцин на живые организмы изучено еще в меньшей степени, чем влияние векторных вакцин, поэтому вряд ли в ближайшее время ДНК-вакцины будут допущены к массовому применению на людях. 
В случае применения РНК-вакцины получается двойной иммунный ответ: с одной стороны, выработку антител вызывают вирусные белки, с другой стороны, сами липидные частицы с мРНК могут стимулировать иммунный ответ, так как «похожи на вирус» и воспринимаются организмом соответственно. Разработчики предполагают, что при вакцинации РНК-вакцинами из-за их «двойного действия» в организме быстро возникнет сильный и стойкий иммунитет.
В случае генетических вакцин преимуществом является их относительно быстрое и экономически выгодное производство: небольшую молекулу мРНК можно довольно быстро воссоздать, наработка нужного антигена обойдется недорого. Это делает вакцину доступной широким массам. Тем не менее иммунологи очень осторожно относятся к РНК-вакцинам, так как из-за малого периода их изучения никто не знает наверняка, как именно мРНК будет вести себя в живом, особенно в репродуктивном, организме.

Одним из самых безопасных типов вакцин в настоящее время считаются субъединичные вакцины, то есть вакцины на основе белков или фрагментов вируса (Рис. 6), не имеющих в своем составе ни ДНК, ни РНК как, например, белковые вакцины.
Попадая в организм при вакцинации, смесь фрагментов вирусных белков-антигенов также способна вызывать иммунный ответ. При этом такая вакцина абсолютно безопасна, здесь невозможны мутации вируса, поэтому вызвать у человека заболевание COVID-19 такая вакцина не может. Недостатком субъединичных вакцин является довольно длительный и сложный процесс наработки и очистки – получить достаточное для вакцинации очищенное количество вирусного белка не так легко. Кроме того, в чистом виде белковые вакцины не вызывают сильный иммунный ответ, поэтому недостаточно эффективны. В связи с этим при разработке белковых вакцин очень важно:
а) усилить иммунный ответ, вводя в состав белковых вакцин соединения, усиливающие их эффективность (эти вещества называют адъюванты),
б) увеличить количество нарабатываемой вакцины также за счет добавления к наработанному вирусному белку существенного количества того же адъюванта.

Наконец, мы подошли к еще одному безопасному и перспективному типу вакцин – инактивированным вакцинам. Здесь так же, как и в случае «живых» вакцин на основе ослабленного вируса используется цельный геном SARS-Cov-2, но в случае инактивированных вакцин вирус полностью деактивирован либо высокой температурой, либо дезинфицирующими составами, либо определенным видом излучения, что делает его совершенно нежизнеспособным. Этот инактивированный вирус никогда не сможет инфицировать клетку. Тем не менее по структуре «неживой» инактивированный вирус остается полным аналогом «живого» вируса и поэтому вызывает в организме иммунный ответ. Проблема в том, что в чистом виде инактивированные вирусы индуцируют существенно более низкий иммунный ответ, нежели живые, пусть даже и ослабленные вирусы. В связи с этим в составах инактивированных вакцин так же, как и в случае субъединичных вакцин используют адъюванты – вещества, которые значительно усиливают иммунный ответ, делая эти вакцины схожими по эффективности с живыми.
Основываясь на вышесказанном, мы склоняемся к выводу, что наиболее безопасными для человека являются субъединичные и инактивированные вакцины. Для повышения эффективности указанных безопасных вакцин до уровня более иммуногенных «живых», векторных или генетических вакцин необходимо применение в их составах современных адъювантов. Что же такое адъюванты и какова их роль в вакцинах?

Адъювант (от лат. adjuvans – «помогающий, поддерживающий») – соединение или комплекс веществ, используемых для усиления иммунного ответа при введении одновременно с антигеном.
Адъюванты на протяжении десятилетий применяются для улучшения иммунного ответа на вакцинные антигены. Включение адъювантов в состав вакцин направлено на усиление, ускорение и продление специфического иммунного ответа до желаемого уровня. Таким образом, адъюванты играют ключевую роль в получении эффективного и длительного иммунитета.
Использование адъювантов в вакцинах позволяет:
• Усилить краткосрочный иммунный ответ;
• Увеличить продолжительность иммунитета, то есть сократить частоту требуемых бустерных иммунизаций;
• Направить иммунный ответ (гуморальный или клеточный иммунитет);
• Уменьшить антигенную нагрузку при сохранении эффективности вакцины;
• Улучшить иммунный ответ у ослабленных или иммунокомпроментированных вакцинируемых лиц;
• Снизить себестоимость вакцины;
• Повысить стабильность вакцины.
Интерес к адъювантам для вакцин резко возрос в 2000-е годы. Ведущие фармацевтические компании-производители путем применения адъювантов разработали более эффективные и безопасные вакцины против гриппа.
В последние годы появляется все больше и больше новых вакцин-кандидатов как для профилактики инфекционных заболеваний, так и для терапии самых тяжелых заболеваний человечества. В связи с низкой иммуногенностью таких вакцин во многих случаях требуется введение в их состав адъювантов. Новые достижения в области аналитической биохимии, очистке макромолекул, технологии рекомбинантной ДНК, улучшенное понимание иммунологических механизмов и патогенеза заболевания позволили улучшить техническую основу разработки и применения адъювантов.
В настоящее время известно довольно много эффективных адъювантов, которые классифицируются по природе происхождения, механизму действия и физическим или химическим свойствам.
Так, в современных вакцинах широко применяются гели гидроксида алюминия, фосфаты алюминия или кальция, препараты на основе масляных эмульсий и ПАВ, дисперсные адъюванты, например, виросомы, структурные комплексы сапонинов и липидов и многие другие типы адъювантов.
Как уже упоминалось выше, наиболее эффективно и поэтому чаще всего адъюванты используются в следующих категориях вакцин:
• вакцины на основе белков (рекомбинантные субъединичные);
• инактивированные;
• векторные вакцины (для уменьшения дозы).
Для каждой вакцины адъювант подбирается таким образом, чтобы получить оптимальное соотношение эффективности указанной вакцины (получение сильного и продолжительного иммунного ответа) и ее безопасности для человека (минимальная реактогенность и отсутствие побочных эффектов).
К сожалению, немаловажным аспектом уже зарегистрированных в настоящее время адъювантов является их недоступность широкому кругу разработчиков. Практически все имеющиеся на настоящий момент современные адъюванты, применяемые в профилактических вакцинах, за исключением соединений алюминия, являются собственностью крупнейших фармацевтических компаний (см. табл. 2). В первую очередь, к ним относятся адъюванты для приготовления эмульсионных вакцин. Эти адъюванты на настоящий момент считаются наиболее перспективными в профилактических вакцинах, но остаются при этом и наименее доступными, так как были специально разработаны крупными биофармацевтическими компаниями исключительно для вакцин собственного производства.
Эти недоступные широкому кругу разработчиков адъюванты ведущих фармацевтических компаний отлично зарекомендовали себя в составах готовых вакцин указанных производителей. К примеру, эмульсионные адъюванты масло-в-воде MF59, AS03 и AF03 продемонстрировали высокую эффективность в вакцинах против гриппа. Сегодня вакцинами на их основе провакцинировано >120 миллионов человек, их профиль безопасности и иммуногенности тщательно и глубоко изучен и подтвержден на значительном количестве клинических испытаний (см. табл. 3).

Франсуа Бертран, руководитель направления разработки и производства адъювантов компании Seppic, в своем выступлении по поводу выпуска адъюванта SEPIVAC TM SWE на мировой рынок сказал: «Указанная разработка иллюстрирует наше общее стремление привнести готовый эффективный и общедоступный адъювант в мировое сообщество разработчиков вакцин. Мы твердо верим, что SEPIVAC TM SWE ускорит разработку новых профилактических вакцин для людей и будет способствовать более здоровому будущему человечества во всем мире».
Какими бывают вакцины от COVID-19 и как они защищают нас от инфекции, «Доктору Питеру» рассказала заместитель управляющего по качеству НИЦ «Эко-безопасность», инфекционист, клинический фармаколог Гульнара Ислямовна Сыраева.
Такой разный иммунитет
Смысл любой вакцинации – так или иначе воздействовать на иммунную систему. Изначально понятие «иммунитет» подразумевало только способность организма противостоять внешним инородным агентам: бактериям, вирусам, простейшим. Потом оно стало шире. В современном понимании – это сложная, многогранная система, которая направлена в том числе на поддержание внутренней целостности и слаженной работы организма. В свое время Илья Мечников и Пауль Эрлих получили Нобелевскую премию за открытие иммунитета. Мечников разработал теорию клеточного иммунитета, Эрлих — гуморального. На момент своих разработок ученые друг друга критиковали, но в итоге жизнь показала, что они оба были правы. На сегодня две их теории не исключают, а дополняют друг друга. За клеточный иммунитет отвечают так называемые Т-клетки, которые поглощают чужеродные микроорганизмы, а также презентируют их — они носят на себе их фрагменты и показывают другим клеткам, после чего запускается выработка антител — специальных белковых комплексов в крови (иммуноглобулины IgА, IgМ, IgG), которые нейтрализуют и поглощают чужеродные микроорганизмы. Антитела отвечают за гуморальный иммунитет.
Любое вещество, которое организм человека воспринимает как чужеродное и потенциально опасное для себя, называется антигеном. Новый коронавирус SARS-CoV-2 относится к РНК-содержащим вирусам, и антигеном может быть как внутренняя его часть (нуклеиновые кислоты), так и внешняя (поверхностная оболочка, которая представлена сложными полипептидами – белками).
Помимо того, что иммунитет бывает клеточным и гуморальным, он подразделяется еще на естественный или искусственный.
Естественный иммунитет, в свою очередь, бывает врожденным (как выяснилось, у человека нет врожденного, генетически обусловленного иммунитета к новой коронавирусной инфекции) или приобретенным (он формируется после перенесенной болезни, в некоторых случаях даже на всю жизнь, как после ветрянки).
Искусственный иммунитет бывает активным и пассивным. Если человек уже болеет, у него вырабатываются антитела, но их недостаточно для выздоровления, тогда речь идет о необходимости пассивного иммунитета. Это не что иное, как переливание плазмы крови уже переболевших. Так происходит, например, при заражении клещевым энцефалитом: человеку в течение 72 часов вводят специальные противоклещевые иммуноглобулины. Вакцинация помогает создать активный искусственный иммунитет. Мы вводим человеку вакцину, в которой есть антигены, — на них организм начинает формировать иммунный ответ, но при этом они не вызывают заболевания.
В зависимости от использованных антигенов и принципа создания вакцины делятся на несколько видов. Расскажу об основных из них.
Векторные рекомбинантные вакцины. «Спутник V», «Конвидеция»
К плюсам векторных вакцин можно отнести высокую иммуногенность — при их введении формируется достаточно высокий титр защитных антител. По сути, это самые современные технологии создания вакцин — генная инженерия в чистом виде. Но как раз в ее новизне кроется и минус — они применялись на небольшом проценте популяции и еще мало изучены. Мы пока не можем говорить о долгоиграющих перспективах — сформируется ли пожизненный иммунитет? Или что будет, если вирус мутирует и ген, который использовали в создании вакцины, «в природе» немного изменит свою кодировку — состыкуется ли с ним антительный ответ после вакцинации? Кроме того, при введении такой вакцины организм может также отреагировать на вирус-вектор, что помешает главной цели – формированию стойкого иммунитета против целевого вируса. Именно поэтому для вектора важно выбрать оптимальный вариант — тот, на который реакция организма будет минимальной.
К векторным относится первая российская вакцина против коронавируса «Спутник V», разработанная НИЦ эпидемиологии и микробиологии им. Гамалеи. Разработчики «Спутник V» встроили ген, кодирующий информацию о структуре S-белка шипа коронавируса — он формирует всем известную «корону» и отвечает за связывание вируса с клетками человека. В качестве вектора они использовали давно и хорошо изученный аденовирус, который вызывает сезонную ОРВИ. Над векторными вакцинами трудятся и другие разработчики. В частности, регистрируемая китайская вакцина «Конвидеция» тоже векторная и тоже на основе аденовируса. Заявку на ее регистрацию подала биофармацевтическая компания «Петровакс» (входит в холдинг «Интеррос» Владимира Потанина). Сейчас она проходит 3-ю фазу клинического исследования, в которой только наш центр задействует 300 добровольцев из Петербурга.
До «Спутника V» в России в широкой клинической практике векторные вакцины не применялись. В 2015 году была зарегистрирована подобная вакцина против лихорадки Эбола, разработанная тем же Центром им. Гамалеи. Векторная вакцина против другой разновидности коронавируса – ближневосточного респираторного синдрома (MERS) – еще одна разработка Центра им. Гамалеи с использованием вектора на основе аденовируса, но она пока не зарегистрирована.
Есть еще одна разновидность генно-инженерных вакцин последнего поколения — на основе нуклеиновых кислот (ДНК- и РНК-вакцины). В них также используются модификации генетического материала, но, в отличие от векторных вакцин, этот материал синтезируют искусственно. Иначе говоря, собирают необходимую нуклеиновую последовательность в лаборатории и с ней работают. Это технология завтрашнего дня — пока в России нет ни одной такой вакцины, испытанной на людях.
Цельновирионные вакцины
На цельновирионных вакцинах человечество выросло — это классика. Для создания таких вакцин вирус используется целиком, а не какая-то его часть. Они бывают живыми ослабленными или инактивированными (в них вирус «убит» термически либо воздействием химических агентов, например, с помощью формалина или ацетона).
Для приготовления инактивированных вакцин используется большой спектр возбудителей — бактерий и вирусов. Такие вакцины защищают нас от бешенства (антирабическая), коклюша, гепатита А, гриппа, клещевого энцефалита, брюшного тифа.
Цельновирионную инактивированную вакцину против коронавируса, к примеру, разработал Научный центр им. Чумакова (по словам президента Путина, она уже «на подходе»). Сейчас она проходит стадию клинического исследования. 19 октября на базе научно-исследовательского центра «Эко-безопасность» стартовал второй этап — в нем участвуют 30 добровольцев. Чтобы «подхлестнуть» иммунитет и повысить уровень антител, вакцину вводят двукратно – с разницей в 10 дней. Кстати, дважды вводят и «Спутник V».
Для цельновирионных вакцин с живым, но ослабленным вирусом обычно достаточно одного введения. В них вирус сохраняет возможность размножаться в организме человека. Такие препараты нуждаются в регулярном изучении генетической стабильности, чтобы не вызвать заболевания при иммунизации. Бывают, к примеру, живые вакцины против кори, полиомиелита, гриппа, но их сейчас практически не применяют.
Субъединичные вакцины. «ЭпиВакКорона»
Такие препараты создаются на основе различных антигенных компонентов – субъединиц. Можно взять, к примеру, часть оболочки вируса — белки, которые отвечают за проникновение вируса в клетку. У коронавируса это S-белок. И хотя антитела при введении такой вакцины будут вырабатываться непосредственно на белок, уровень иммунного ответа и качество защитных антител, скорее всего, будет ниже, чем на векторную или цельновирионную вакцины. На целый вирус или кусочек генома вырабатываются более сложные по структуре антитела, чем на изолированный белок. Но надо понимать, что, говоря «белок», мы немного утрируем — там может использоваться много структур, включая поверхностную и внутреннюю мембрану, белки-носители и так далее.
В чем минусы таких вакцин? Поверхностный белок может со временем мутировать, и будет ли вакцина эффективна, скажем, через год — вопрос. Для усиления иммунного ответа в них так же, как и в цельвирионных, используются адъюванты. Плюс же в том, что субъединичные вакцины проще в производстве, чем, например, векторные.
К субъединичным относятся вакцины против пневмококковой и менингококковой инфекций, брюшного и сыпного тифа, холеры.
Вакцины на основе вирусоподобных частиц
Для производства этих вакцин берут пустую белковую оболочку вируса – без «нутра». Вирусоподобные частицы имитируют структуру вируса, но не содержат его генетического материала. В их состав также могут входить адъюванты и иммуностимуляторы.
Из плюсов. Они безопасны и способны вырабатывать высокий иммунный ответ, при этом эффективны даже в виде капель для носа – так они сразу активируют иммунитет слизистых оболочек, которые обычно становятся «входными воротами» для вирусов. В то же время такие вакцины технологически сложны для массового производства и требуют больших финансовых вложений. Опять же, даже при незначительной мутации вируса поверхностный белок может поменять свою конфигурацию, и тогда вакцина попросту может не сработать.
На сегодня такие вакцины созданы для профилактики гриппа, гепатита С.