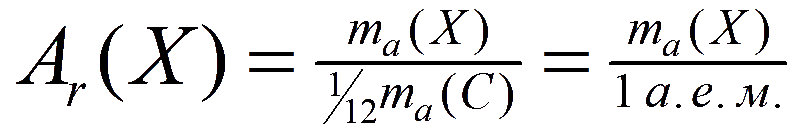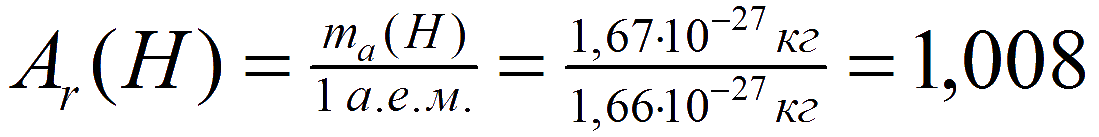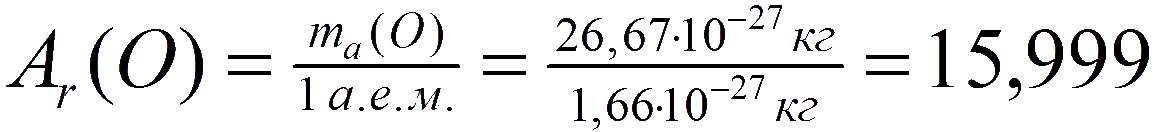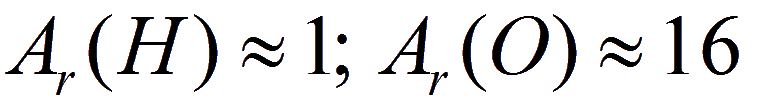§ 1.3. Размеры атомов разных химических элементов, их абсолютные и относительные массы
Мы уже знаем, что атомы химических элементов могут отличаться друг от друга по составу и, очевидно, что это должно влиять на их массу, поскольку чем больше в ядре атома суммарное количество протонов и нейтронов, тем он тяжелее. Электроны практически не влияют на массу атома, поскольку обладают крайне малой по сравнению с нейтронами и протонами массой (mp/me
Так как количество протонов в каждом атоме всегда равно количеству электронов, а электроны, если рассматривать строение атома упрощенно, движутся вокруг ядра на значительном от него удалении, то радиус атома равен радиусу орбиты наиболее удаленного от ядра электрона. Следовательно, должна быть некоторая зависимость радиуса атома от количества таких орбит, которая в какой-то степени связана с количеством электронов.
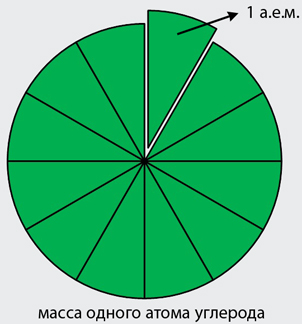
99 %). Одну двенадцатую массы атома данного изотопа углерода было принято обозначать 1 а.е.м., что расшифровывается как «атомная единица массы». Одна атомная единица массы равно примерно 1,66·10 −27 кг.
Графическое представление смысла одной атомной единицы массы представлено на рисунке 2.
Таким образом, мы подошли к определению нового термина – относительной атомной массы:
Определение: относительная атомная масса химического элемента равна отношению его абсолютной массы к одной двенадцатой абсолютной массы атома углерода или к массе одной атомной единицы массы.
Относительную атомную массу обозначают символом Ar (индекс r означает сокращение от английского слова relative, что переводится как «относительный»). Таким образом, обозначив в общем виде химический элемент символом Х, мы получаем следующую формульную запись представленного выше определения:
Относительная атомная масса — величина безразмерная, так как в числителе и знаменателе находятся значения, измеряемые в одинаковых единицах массы (кг, г или др.). Согласно представленной выше формуле, например, относительная атомная масса водорода равна:
а относительная атомная масса кислорода:
В большинстве расчетных задач, с которыми приходится иметь дело химикам, используются значения относительных атомных масс, округленные до целочисленных значений, т.е. применительно к водороду и кислороду:
Следует отметить, что атомную массу хлора округляют до 35,5. Это связано с тем, что у данного элемента наиболее распространенные в природе изотопы имеют относительные атомные массы 35 и 37, а их содержание в смеси близко к 3:1 в пользу более легкого.
Основы строения атома. Просто о сложном
Все в мире состоит из атомов. Но откуда они взялись, и из чего состоят сами? Сегодня отвечаем на эти простые и фундаментальные вопросы. Ведь многие люди, живущие на планете, говорят, что не понимают строения атомов, из которых сами и состоят.
Естественно, уважаемый читатель понимает, что в данной статье мы стараемся изложить все на максимально простом и интересном уровне, поэтому не «грузим» научными терминами. Тем, кто хочет изучить вопрос на более профессиональном уровне, советуем читать специализированную литературу. Тем не менее, сведения данной статьи могут сослужить хорошую службу в учебе и просто сделать Вас более эрудированными.
Атом – это частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, которая является носителем его свойств. Иными словами, это мельчайшая частица того или иного вещества, которая может вступать в химические реакции.
История открытия и строение
Понятия атома было известно еще в Древней Греции. Атомизм – физическая теория, которая гласит, что все материальные предметы состоят из неделимых частиц. Наряду с Древней Грецией, идеи атомизма параллельно развивался еще и в Древней Индии.
Не известно, рассказали тогдашним философам об атомах инопланетяне, или они додумались сами, но экспериментально подтвердить данную теорию химики смогли много позже – только в семнадцатом веке, когда Европа выплыла из пучины инквизиции и средневековья.
Долгое время господствующим представлением о строении атома было представление о нем как о неделимой частице. То, что атом все-таки можно разделить, выяснилось только в начале двадцатого века. Резерфорд, благодаря своему знаменитому опыту с отклонением альфа-частиц, узнал, что атом состоит из ядра, вокруг которого вращаются электроны. Была принята планетарная модель атома, в соответствии с которой электроны вращаются вокруг ядра, как планеты нашей Солнечной системы вокруг звезды.
Ядро атома имеет положительный электрический заряд, а электроны, вращающиеся по орбите – отрицательный. Таким образом, атом электрически нейтрален.
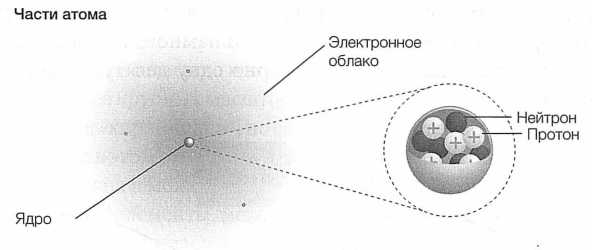
Ниже приведем элементарную схему строения атома углерода.
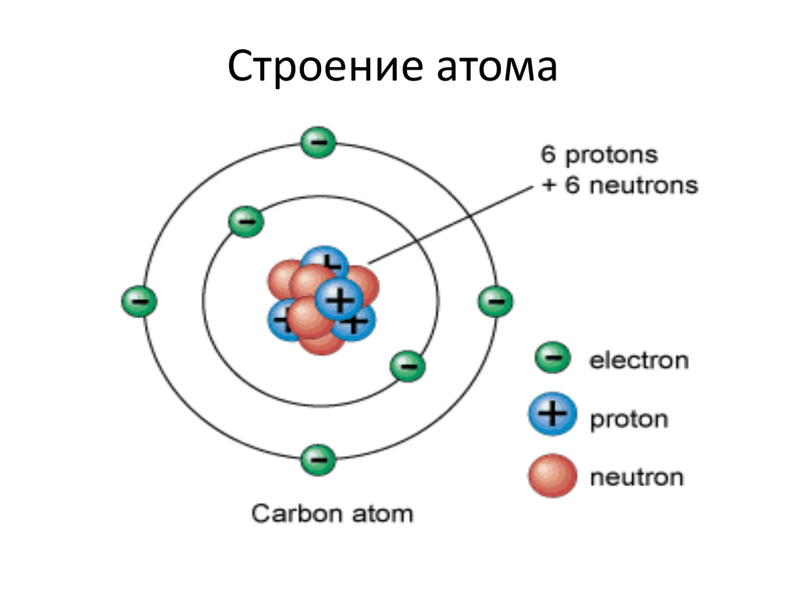
Свойства атомов
Масса
Массу атомов принято измерять в атомных единицах массы – а.е.м. Атомная единица массы представляет собой массу 1/12 части свободно покоящегося атома углерода, находящегося в основном состоянии.
В химии для измерения массы атомов используется понятие «моль». 1 моль – это такое количество вещества, в котором содержится число атомов, равное числу Авогадро.
Размер
При этом, масштабы вещей таковы, что, по сути, атом на 99% состоит из пустоты. Ядро и электроны занимают крайне малую часть его объема. Для наглядности, рассмотрим такой пример. Если представить атом в виде олимпийского стадиона в Пекине (а можно и не в Пекине, просто представьте себе большой стадион), то ядро этого атома будет представлять собой вишенку, находящуюся в центре поля. Орбиты электронов при этом находились бы где-то на уровне верхних трибун, а вишня весила бы 30 миллионов тонн. Впечатляет, не так ли?

Откуда взялись атомы?
В самом начале формирования Вселенной никаких атомов не было и подавно, существовали лишь элементарные частицы, под воздействием огромных температур взаимодействующие между собой. Как сказал бы поэт, это был настоящий апофеоз частиц. В первые три минуты существования Вселенной, из-за понижения температуры и совпадения еще целой кучи факторов, запустился процесс первичного нуклеосинтеза, когда из элементарных частиц появились первые элементы: водород, гелий, литий и дейтерий (тяжелый водород). Именно из этих элементов образовались первые звезды, в недрах которых проходили термоядерные реакции, в результате которых водород и гелий «сгорали», образуя более тяжелые элементы. Если звезда была достаточно большой, то свою жизнь она заканчивала так называемым взрывом «сверхновой», в результате которого атомы выбрасывались в окружающее пространство. Так и получилась вся таблица Менделеева.

Так что, можно сказать, что все атомы, из которых мы состоим, когда-то были частью древних звезд.
Почему ядро атома не распадается?
В физике существует четыре типа фундаментальных взаимодействий между частицами и телами, которые они составляют. Это сильное, слабое, электромагнитное и гравитационное взаимодействия.
Именно благодаря сильному взаимодействию, которое проявляется в масштабах атомных ядер и отвечает за притяжение между нуклонами, атом и является таким «крепким орешком».
Не так давно люди поняли, что при расщеплении ядер атомов высвобождается огромная энергия. Деление тяжелых атомных ядер является источником энергии в ядерных реакторах и ядерном оружии.

Итак, друзья, познакомив Вас со структурой и основами строения атома, нам остается только напомнить о том, что наши авторы готовы в любой момент прийти Вам на помощь. Не важно, нужно Вам выполнить диплом по ядерной физике, или самую маленькую контрольную – ситуации бывают разные, но выход есть из любого положения. Подумайте о масштабах Вселенной, закажите работу в Zaochnik и помните – нет поводов для беспокойства.
Что такое размеры атома
Атом состоит из атомного ядра и электронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом.В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам.
Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Число Z также определяет суммарный положительный электрический заряд (Ze) атомного ядра и число электронов в нейтральном атоме, задающее его размер.
По определению, любые два атома с одним и тем же числом протонов в их ядрах относятся к одному химическому элементу. Атомы с одним и тем же количеством протонов, но разным количеством нейтронов называют изотопами данного элемента. Например, атомы водорода всегда содержат один протон, но существуют изотопы без нейтронов (водород-1, иногда также называемый протием — наиболее распространённая форма), с одним нейтроном (дейтерий) и двумя нейтронами (тритий). Известные элементы составляют непрерывный натуральный ряд по числу протонов в ядре, начиная с атома водорода с одним протоном и заканчивая атомом унуноктия, в ядре которого 118 протонов. Все изотопы элементов периодической системы, начиная с номера 83 (висмут), радиоактивны.
Поскольку наибольший вклад в массу атома вносят протоны и нейтроны, суммарное число этих частиц называют массовым числом. Массу покоя атома часто выражают в атомных единицах массы (а. е. м.), которая также называется дальтоном (Да). Эта единица определяется как 1⁄12 часть массы покоя нейтрального атома углерода-12, которая приблизительно равна 1,66·10−24 г. Водород-1 — наилегчайший изотоп водорода и атом с наименьшей массой, имеет атомный вес около 1,007825 а. е. м. Масса атома приблизительно равна произведению массового числа на атомную единицу массы Самый тяжёлый стабильный изотоп — свинец-208 с массой 207,9766521 а. е. м.
Так как массы даже самых тяжёлых атомов в обычных единицах (например, в граммах) очень малы, то в химии для измерения этих масс используют моли. В одном моле любого вещества по определению содержится одно и то же число атомов (примерно 6,022·1023). Это число (число Авогадро) выбрано таким образом, что если масса элемента равна 1 а. е. м., то моль атомов этого элемента будет иметь массу 1 г. Например, углерод имеет массу 12 а. е. м., поэтому 1 моль углерода весит 12 г.
Атомы не имеют отчётливо выраженной внешней границы, поэтому их размеры определяются по расстоянию между ядрами соседних атомов, которые образовали химическую связь (Ковалентный радиус) или по расстоянию до самой дальней из стабильных орбит электронов в электронной оболочке этого атома (Радиус атома). Радиус зависит от положения атома в периодической системе, вида химической связи, числа ближайших атомов (координационного числа) и квантово-механического свойства, известного как спин. В периодической системе элементов размер атома увеличивается при движении сверху вниз по столбцу и уменьшается при движении по строке слева направо. Соответственно, самый маленький атом — это атом гелия, имеющий радиус 32 пм, а самый большой — атом цезия (225 пм). Эти размеры в тысячи раз меньше длины волны видимого света (400—700 нм), поэтому атомы нельзя увидеть в оптический микроскоп. Однако отдельные атомы можно наблюдать с помощью сканирующего туннельного микроскопа.
Малость атомов демонстрируют следующие примеры. Человеческий волос по толщине в миллион раз больше атома углерода. Одна капля воды содержит 2 секстиллиона (2·1021) атомов кислорода, и в два раза больше атомов водорода. Один карат алмаза с массой 0,2 г состоит из 10 секстиллионов атомов углерода. Если бы яблоко можно было увеличить до размеров Земли, то атомы достигли бы исходных размеров яблока.
Учёные из Харьковского физико-технического института представили первые в истории науки снимки атома. Для получения снимков учёные использовали электронный микроскоп, фиксирующий излучения и поля (field-emission electron microscope, FEEM). Физики последовательно разместили десятки атомов углерода в вакуумной камере и пропустили через них электрический разряд в 425 вольт. Излучение последнего атома в цепочке на фосфорный экран позволило получить изображение облака электронов вокруг ядра.
АТОМНЫЙ МАСШТАБ
Уйдя от механики биосистем и опускаясь глубже по шкале линейных размеров, чтобы разобраться уже в базовых физических элементах, мы остановимся ненадолго на размере атома — около 100 пикометров, что в 10 тысяч миллионов (10 10 ) раз меньше метра. Точный размер атома определить трудно, поскольку в его составе присутствуют электроны, которые циркулируют вокруг ядра, но никогда не застывают на месте. Традиционно, однако, в качестве размера атома указывают среднее расстояние от электрона до ядра.
Говоря о физических процессах, протекающих на этих крошечных расстояниях, нередко прибегают к наглядным изображениям, но необходимо помнить, что все они основаны на аналогиях. У нас нет другого выхода, и для описания непривычных структур, которые ведут себя странно с точки зрения здравого смысла, приходится привлекать описания объектов, с которыми мы сталкиваемся в обычной жизни.
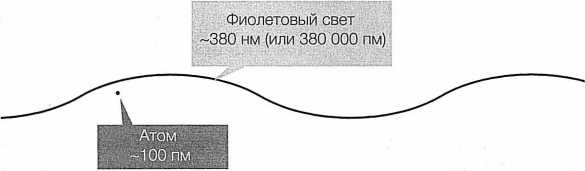
Корректно изобразить внутреннее строение атома невозможно — ведь рассчитывать при этом мы можем лишь на собственные физиологические качества, а именно чувства и двигательные способности, применимые только в человеческом масштабе. Человеческое зрение, к примеру, опирается на явления, которые видимыми делает свет, то есть электромагнитное излучение. Световые волны — те, что попадают в оптический диапазон — имеют длину волны примерно от 380 до 750 нм. Это намного больше размера атома, который составляет примерно одну десятую нанометра (рис. 14).
РИС. 14. Отдельный атом — всего лишь крохотная точка по сравнению даже с самой маленькой длиной волны видимого света
Это означает, что исследовать внутреннюю структуру атома при помощи видимого света, пытаясь увидеть его глазами, так же бесполезно, как вдевать нитку в иголку в варежках. Длины волн, о которых идет речь, буквально «размывают» объекты более мелких размеров, и получить с их помощью четкую картинку невозможно, не хватит разрешения. Поэтому, когда мы хотим по–настоящему «увидеть» кварки или даже протон, мы хотим невозможного. У нас просто нет инструмента, который позволил бы точно визуализировать то, что происходит внутри атома.
Но путать способность человека увидеть некие явления и нашу уверенность в том, что эти явления существуют, — серьезная ошибка, которую ученые не могут себе позволить. Тот факт, что мы не только не видим эти явления, но и не имеем их мысленного образа, не означает, что мы не можем логически вычислить физические элементы и процессы, которые имеют место на соответствующих масштабах.
Гипотетически в масштабе атома окружающий мир показался бы нам невероятным, потому законы физики в этом мире резко отличаются от тех, к которым мы привыкли и которые действуют там, где мы бодро отмеряем расстояния при помощи линеек. Мир атома совершенно не похож на тот образ, что возникает в нашем сознании при мысли о материи (рис. 15).
РИС. 15. Атом состоит из электронов, обращающихся вокруг центрального ядра, которое, в свою очередь, состоит из положительно заряженных протонов (заряд каждого из них равен единице) и нейтральных нейтронов (их заряд равен нулю)
Это совсем не то, что мы видим и чувствуем, когда стучимся в дверь или пьем прохладную жидкость через соломинку. Чувства подсказывают нам, что вещество непрерывно. Тем не менее на атомном уровне мы обнаруживаем, что вещество по большей части не содержит ничего «вещественного», просто наши чувства усредняют все, что имеет меньшие размеры; за счет этого вещество кажется нам твердым и непрерывным. На атомном уровне оно совсем не такое.
Почти полная пустота — не единственное, что удивило бы нас при взгляде на вещество в атомном масштабе. В свое время мир физики был буквально потрясен тем, что на этих крошечных расстояниях нарушаются даже самые фундаментальные основы ньютоновой физики. Понять свойства электронов в атоме невозможно без представления о двух вещах: волновой природе вещества и принципа неопределенности — ключевых элементах квантовой механики. Электроны в атоме вовсе не летают по простым кривым, описывающим конкретные орбиты, изображение которых мы так часто видим. Согласно квантовой механике никто не в состоянии измерить одновременно положение и импульс частицы с бесконечной точностью, а без этого невозможно и проследить точный путь частицы во времени. Принцип неопределенности, выдвинутый Вернером Гейзенбергом в 1926 г., утверждает, что точность, с которой измерены координаты частицы, ограничивает максимальную точность, с которой можно измерить ее импульс[21]. Если бы электроны двигались по классическим траекториям, мы могли бы в любой момент точно сказать, где находится данный конкретный электрон, а также с какой скоростью и в каком направлении он движется; следовательно, мы могли бы точно сказать, где он будет находиться в любой момент в будущем. Это, однако, противоречит принципу Гейзенберга.
Квантовая механика учит нас, что электроны не занимают в атоме строго определенного положения, как следовало бы из классической картины мира. Вместо этого мы имеем распределение вероятностей, из которого следует, какие у нас шансы в данный момент обнаружить электрон в данном конкретном месте; вероятности — это все, что у нас есть. Мы можем предсказать среднее положение электрона как функцию времени, но любое конкретное измерение подчиняется принципу неопределенности.
Имейте в виду, что эти распределения не произвольны. У электронов может быть далеко не любое распределение энергий или вероятностей. В классической теории не существует внятного способа описать орбиту электрона — ее можно описать только в терминах теории вероятностей. Тем не менее распределение вероятностей — вполне конкретная функция. В квантовой механике мы можем записать уравнение, описывающее волновое решение для электрона, и это уравнение даст нам вероятность нахождения электрона в конкретной точке пространства.
Еще одно свойство атома, замечательное с точки зрения классической ньютоновой физики, заключается в том, что электроны в атоме могут занимать только фиксированные квантованные энергетические уровни. Орбиты электронов зависят от их энергий, и конкретные энергетические уровни и связанные с ними вероятности должны соответствовать правилам квантовой механики.
Без квантованных уровней электронов невозможно разобраться в атоме. В начале XX в. физики начали понимать, что классические правила придется радикально пересматривать: дело в том, что с точки зрения классической физики электроны, обращающиеся вокруг ядра, нестабильны. По идее они должны были бы излучать энергию и быстро падать на ядро. Такая система не только ничем не напоминала бы атом, но и не допускала бы существование структуры вещества, основанной на стабильных атомах, какими мы их знаем.
Нильс Бор в 1912 г. оказался перед непростым выбором — отказаться от классической физики или отказаться от веры в достоверность наблюдаемых данных. Бор мудро выбрал первый вариант и предположил, что на малых расстояниях, разделяющих электроны в атоме, классические законы неприменимы. Этот вывод стал одним из ключевых факторов, приведших к созданию квантовой физики.
Отказавшись от законов Ньютона, Бор смог постулировать, что электроны в атоме могут занимать только фиксированные энергетические уровни в соответствии с предложенным им условием квантования; условие это было связано с величиной, известной как орбитальный угловой момент электрона (он же момент импульса). По Бору, принципу квантования подчинялось все в атомном масштабе. Вообще, в этом масштабе действовали совсем иные правила, нежели те, что применимы в привычном для нас макроскопическом мире и по которым, к примеру, Земля обращается вокруг Солнца.
Технически квантовая механика применима и в макроскопических системах. Но ее действие здесь слишком слабо, чтобы мы смогли его измерить или хотя бы заметить. Когда вы наблюдаете движение Земли — или, вообще говоря, любого другого макроскопического объекта по орбите, — квантово–механическими эффектами можно пренебречь. В подобных системах они усредняются таким образом, что любое предсказание, сделанное на основе квантовой механики, полностью совпадает с предсказанием, сделанным на базе классической физики. Как уже говорилось в главе 1, для измерений в макроскопическом масштабе классические предположения, как правило, дают чрезвычайно хорошие результаты — настолько хорошие, что заметить действие законов квантовой механики, которые лежат в основе всего этого, невозможно. Проведем следующую аналогию. Текст и изображения на экране компьютера даже с самым хорошим разрешением состоят из точек; точки — аналог квантово–механической атомной структуры. Но нам, как правило, достаточно видеть лишь текст и изображения.
Квантовая механика, безусловно, представляет собой изменение научной парадигмы, однако очевидным оно становится только в атомном масштабе. Несмотря на радикальность предложенной модели, Бору не пришлось отказываться от всего, что было прежде. Он вовсе не считал, что физика Ньютона неверна; он всего лишь предположил, что к электронам в атоме классические законы механики неприменимы. В макроскопическом масштабе вещество состоит из такого количества атомов, что квантовые эффекты выделить невозможно, и в целом оно подчиняется законам Ньютона, по крайней мере на том уровне, на котором можно оценить правильность сделанных на их основе предположений. Ньютоновы законы верны, и мы признаем их справедливость в тех масштабах, где они применимы. Однако на атомном уровне законы Ньютона с неизбежностью отказывают — и отказывают весьма наглядным образом, который и позволил ученым разработать квантовую механику.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Читайте также
МАСШТАБ НЕИЗВЕСТНОГО
МАСШТАБ НЕИЗВЕСТНОГО Немецкий поэт Райнер Мария Рильке точно ухватил парадокс, который остро ощущает всякий человек при встрече лицом к лицу с совершенством: «С красоты начинается ужас./Выдержать это начало еще мы способны;/Мы красотой восхищаемся, ибо она
Атомный вес
Атомный вес В настоящее время атомный или молекулярный вес измеряется сравнением веса атома данного вещества с атомом водорода. Вес атома водорода удобно считать приблизительно одной единицей атомной массы (вес одной атомной массы 1,66?10—24 г), так, вес атома углерода 12.
Размер и масса атома
Размер атома определяется радиусом его внешней электронной оболочки. Размеры всех атомов
Атомы очень маленькие и очень легкие. Атом во столько раз легче яблока, во сколько раз яблоко легче земного шара. Если мир «потяжелеет» так, что атом станет весить как капля воды, то люди в таком мире станут тяжелыми, как планеты: дети — как Меркурий и Марс, а взрослые — как Венера и Земля.
Рассмотреть атом нельзя даже с помощью микроскопа. Лучшие оптические микроскопы позволяют различить детали объекта, если расстояние между ними
0,2 мкм. В электронном микроскопе это расстояние удалось уменьшить до
2-3 Å. Различить и сфотографировать отдельные атомы впервые удалось с помощью ионного проектора. Но никто не видел, как устроен атом внутри. Все данные о строении атомов получены из опытов по рассеянию частиц.
Масса атомного ядра в несколько тысяч раз больше массы его электронной оболочки. Это связано с тем, что ядра атомов состоят из очень тяжелых, по сравнению с электроном, частиц — протонов p и нейтронов n. Их массы почти одинаковы и примерно в 2000 раз больше массы электрона. При этом протон — положительно заряженная частица, а нейтрон — нейтральная. Заряд протона по величине равен заряду электрона. Число протонов в ядре равно числу электронов в оболочке, это и обеспечивает электрическую нейтральность атома. Число нейтронов может быть различным, в ядре атома легкого водорода нейтронов нет совсем, а в ядре атома углерода их может быть и 6, и 7, и 8.
Масса атома меньше суммы масс ядра и электронов на величину Δm, называемую дефектом масс, который возникает из-за кулоновского взаимодействия ядра и электронов. Дефект масс у атомов (в отличие от ядер) очень мал, и, хотя он увеличивается с ростом Z, ни у одного атома не превышает массы электрона. Материал с сайта http://worldofschool.ru