Что такое постинфекционный иммунитет
Иммунитет
Иммунная система осуществляет защиту организма от инфекционных и неинфекционных чужеродных агентов. При появлении и накоплении в организме клеток, отличающихся генетически, запускается каскад иммунных реакций и формируется иммунный ответ.
Основное назначение иммунной системы — это обезвреживание потенциально опасного антигена и формирование резистентности к нему.
Строение
Иммунная система состоит из совокупности лимфоидных органов и тканей, суммарная масса которых составляет 2% от массы тела и которые разрознены между собой в анатомическом смысле. Однако благодаря наличию медиаторов, сигнальных молекул и клеток, способных к миграции в различные органы и ткани, иммунная система представляет четко организованную структуру в функциональном смысле.
Иммунная система включает центральные и периферические органы. К центральным относят тимус и костный мозг. В этих органах начинается созревание зрелых лимфоцитов.
Периферические органы объединяют селезенку, лимфатические узлы и лимфоидную ткань, печень, кровь, лимфу. Наиболее известными структурами являются миндалины и пейеровы бляшки.
Лимфоциты — основные функциональные клетки иммунной системы. Они образуются в костном мозге, а затем проходят созревание. В зависимости от того, в каком органе лимфоциты проходят созревание, они подразделяются на две гетерогенные популяции: Т-лимфоциты (тимус) и В-лимфоциты (лимфоузлы). Т-лимфоциты ответственны за клеточный иммунитет, В-лимфоциты отвечают за гуморальный. В-лимфоциты являются предшественниками антителообразующих клеток.
Благодаря существованию механизма «иммунологической памяти», иммунный ответ при повторном взаимодействии с теми же антигенами возникает в более короткие сроки и имеет более яркое выражение. Индукция иммунитета является благоприятным исходом иммунных реакций и ведет к восстановлению гомеостаза организма.
Виды иммунитета
Состояние иммунитета обеспечивают наследуемые и индивидуально формируемые механизмы.
К первому относится невосприимчивость человека или определенных видов животных к возбудителям некоторых инфекционных болезней. Например, люди невосприимчивы к возбудителю чумы собак, многие животные — к вирусу кори, гонококку и т.д. Устойчивость к соответствующей инфекции наследуется, как видовой признак, и проявляется у всех представителей данного вида. Это врожденный иммунитет или видовой.
Приобретенный иммунитет формируется в течение всей жизни индивидуума. Примером естественного приобретенного иммунитета является невосприимчивость к инфекции после перенесенного заболевания. Так называемый постинфекционный иммунитет. Например, ветряная оспа.
Приобретенный иммунитет может быть активным и пассивным. Активно приобретенный иммунитет возникает в результате перенесенного инфекционного заболевания или введения в организм вакцины. Пассивно приобретенный иммунитет формируется при передаче антител от матери к плоду или может быть искусственно создан путем парентерального введения в организм готовых иммунореагентов. К ним относят специфические иммуноглобулины, иммунные сыворотки и лимфоциты, способные защитить организм от антигенов.
Иммунитет может быть генерализованным и местным. При местном иммунитете происходит защита покровов организма, которые контактируют с внешней средой: слизистые оболочки мочеполовых органов, желудочно-кишечного тракта и т.д.
Иммунный статус
Характеристику состояния иммунной системы организма, выраженную количественными и качественными показателями ее компонентов, называют иммунным статусом. Определение иммунного статуса проводят с целью правильной постановки диагноза заболевания, прогнозирования его течения и выбора метода лечения.
Постинфекционный иммунитет к SARS-CoV-2
По всей видимости, Т-клеточный ответ играет важную роль в контроле инфицирования SARS-CoV-2, однако он остается достаточно плохо изученным. В настоящее время появились сведения о том, что у большинства инфицированных людей развивается стойкий и длительный Т-клеточный иммунитет. Эти данные значимы с точки зрения сохранения долговременного иммунитета и разработки вакцин.
Инфекция SARS-CoV-2 приводит к различным клиническим исходам, начиная от бессимптомного течения и заканчивая развитием тяжелой формы заболевания и смертью. Учитывая приспособленность этого вируса к человеческому организму на данный момент и его возможную устойчивость к механизмам противовирусной защиты, важно понимать степень выраженности и длительность иммунологической памяти, стимулируемой самой инфекцией. Хотя в нескольких исследованиях сообщалось, что у людей после перенесенной инфекции развивается устойчивый во времени ответ Т-клеток памяти, специфичных к SARS-CoV-2 [1,2,3,4,5], остается неясной степень корреляции между такой иммунной реакцией и клиническими исходами. В текущем выпуске Nature Immunology Zuo с соавт. [6] описывают стойкость и разнообразие Т-клеточного ответа, возникающего после бессимптомного течения или легкой формы заболевания COVID-19.
Авторами был изучен Т-клеточный ответ спустя шесть месяцев после перенесенной инфекции у 100 человек (средний возраст которых составил 41 год), среди которых у 56 лиц инфекция протекала в относительно легкой форме, а у 44 — бессимптомно. Чтобы подсчитать Т-клетки, способные распознавать SARS-CoV-2, их стимулировали пептидами из вирусных белков, взятыми от людей, ранее перенесших коронавирусную инфекцию — это позволяло получить цитокиновый ответ. Затем осуществляли подсчет Т-клеток, способных реагировать на SARS-CoV-2, основываясь на секреции провоспалительного цитокина интерферона (IFN)-γ, которая оценивалась с помощью анализа ELISpot (от англ. enzyme-linked immune absorbent spot assay). Почти у всех доноров в этом анализе был выявлен Т-клеточный ответ на SARS-CoV-2. Однако степень выраженности ответа в границах когорты сильно различалась, и коррелятом ответа было наличие симптомов на ранней стадии инфекции. У людей, перенесших инфекцию SARS-CoV-2 с четко выраженными симптомами, Т-клеточный ответ, определенный по синтезу IFN-γ, спустя шесть месяцев после инфицирования проявлялся в большей степени, чем у тех, кто переболел в бессимптомной форме. Хотя лица с тяжелой формой заболевания не включались в исследование, в другой недавней статье не было засвидетельствовано каких-либо значительных различий в степени Т-клеточного ответа, специфичного к SARS-CoV-2, между госпитализированными и не госпитализированными пациентами [5]. Важно отметить, что иммунный ответ Т-клеток, продуцирующих IFN-γ, не коррелировал с возрастом субъектов в когорте. Вместе с другой работой, в которой было обнаружено увеличение интенсивности Т-клеточного ответа у пациентов с COVID-19 [7], эти данные свидетельствуют в пользу того, что устойчивый Т-клеточный ответ может быть индуцирован инфекцией SARS-CoV-2 вне зависимости от возраста.
Далее Zuo с соавт. исследовали, коррелирует ли интенсивность Т-клеточного ответа (в виде синтеза IFN-γ) спустя шесть месяцев после перенесенной инфекции с выработкой антител с течением времени. Важным достоинством этого исследования стала ежемесячная оценка содержания антител после постановки диагноза. Это позволило провести кинетический анализ значений IgG к S-белку SARS-CoV-2 и его нуклеопротеину (N). Эти значения оказались крайне неоднородными среди участников исследования. В среднем антительный ответ в виде выработки IgG начинал ослабевать примерно через два месяца, но при этом оставался значительно выше предела обнаружения [с помощью тестов] у большинства субъектов на пятом месяце. Интересно, что большая величина Т-клеточного ответа, специфичного к S-белку, спустя шесть месяцев коррелировала с более высокими пиковыми концентрациями антител к S- и N-белкам и устойчивым антительным ответом к N-белку. Остается определить, связан ли Т-клеточный ответ с другими характеристиками антител (например, с их нейтрализующей способностью и/или другими эффекторными функциями) и/или связаны ли другие особенности Т-клеточного ответа (к примеру, продукция IL-2 CD4+ Т-клетками) с пиковым ответом антител.
Хотя в этом исследовании оценка Т-клеточного ответа проводилась спустя шесть месяцев после болезни, остается неясным, был ли кто-то из участников исследования за это время повторно инфицирован. Это маловероятно, если брать во внимание то, что в течение ближайших шести месяцев после перенесенной первичной инфекции SARS-CoV-2 частота реинфекций крайне мала, но, тем не менее, влияние ее на измерения у некоторых участников исключать нельзя [8]. Кроме того, хотя авторы оценивали Т-клеточный ответ по отношению к более раннему антительному ответу, в будущем необходимо оценить, предвосхищает ли Т-клеточный ответ CD4+ лимфоцитов выраженный и/или устойчивый антительный ответ по прошествии времени. К примеру, считается, что фолликулярные Т-хелперы (TFH) играют решающую роль, оказывая помощь В-клеткам в формировании гуморальной иммунной памяти. Также была выявлена корреляция между популяциями циркулирующих клеток памяти и выработкой нейтрализующих противовирусных антител [9]. В недавней работе показано, что концентрация циркулирующих TFН-клеток с фенотипом CD40L+OX40+, специфичных для SARS-CoV-2, оставалась стабильной в течение нескольких месяцев [5]. Кроме того, необходимо выяснить, можно ли на основе содержания или степени сродства антиген-специфических циркулирующих TFH-клеток или других типов клеток на ранних стадиях болезни предсказать последующие параметры антител — такие как устойчивость во времени и/или степень сродства с антигеном.
То, что большинство Т-клеток с фенотипами CD4+ и CD8+ активировалось эпитопами вируса, отличными от S-белка, имеет значение для вакцинации популяций, ранее перенесших инфекцию SARS-CoV-2. Чтобы задействовать такие Т-клетки, которые образовались во время болезни, в вакцины можно включать другие белки помимо шипикового; это могло бы усилить нейтрализующие и иные реакции антител, вызывая более устойчивый CD4+ Т-клеточный ответ и задействуя более усиленный CD8+ Т-клеточный ответ, который был запущен во время предшествующей инфекции. Выявление более устойчивых антител и CD8+ Т-клеточного ответа против эпитопов, отличных от S-белка, может оказаться важным для вакцинации по следующей причине. Вероятно, для иммунитета существуют иные мишени помимо S-белка, что способствует благоприятному разрешению инфекции и может опосредовать широкий спектр иммунных реакций против различных вариантов SARS-CoV-2.
Один из главных вопросов, связанных с иммунитетом против SARS-CoV-2, заключается в том, обеспечивает ли инфекция создание резервуара клеток памяти против данного патогена, способных противостоять последующему заражению. Данное исследование внушает надежду, так как у большинства людей, заразившихся шестью месяцами ранее, даже если у них инфекция протекала в бессимптомной или в легкой форме, были выявлены признаки наличия клеточного иммунитета против коронавируса. Однако наблюдалась выраженная гетерогенность Т-клеточного ответа, и поэтому целью будущих исследований станет определение того, свидетельствует ли ранний Т-клеточный ответ о высоком сродстве антител к вирусу, и какие факторы (вируса или организма хозяина), помимо исходной тяжести заболевания, свидетельствуют о выраженности и/или длительности иммунитета к SARS-CoV-2. Это может лечь в основу понимания иммунных коррелятов защиты от долгосрочных клинических последствий, таких как постковидный синдром и/или повторное заражение, в том числе иными вариантами SARS-CoV-2 (см. рис. 1).
Самые частые вопросы о прививках. Часть 1. Общие вопросы
Опубликовано в журнале:
Практика педиатра, ноябрь-декабрь, 2017
А. С. Боткина, к.м.н., доцент, ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, г. Москва
Ключевые слова: дети, инфекционные заболевания, вакцины, вакцинация, безопасность, эффективность
Keywords: children, infectious diseases, vaccines, vaccination, safety, efficacy
Среди множества разнообразных болезней человека особое место занимают заболевания, вызываемые патогенными микроорганизмами и передающиеся здоровому человеку от больных людей или животных. Эти болезни в середине XIX в. получили название инфекционных (лат. Inficere – заражать). Ежегодно рождаются более 150 млн детей, из которых 12 млн умирают от инфекционных заболеваний, причем 4 млн смертей могли быть предупреждены вакцинацией [1].
Желание победить болезнь, а лучше – предотвратить ее возникновение занимало умы врачей во все времена. С этой целью применялось множество различных средств: от заговоров и заклинаний до лекарственных препаратов. Однако несмотря на усилия человека, микроскопические патогены побеждали. Впервые для профилактики болезни сам патоген стали применять в Древнем Китае, когда для создания искусственной невосприимчивости к натуральной оспе вводили в нос и втирали в кожу здоровым людям растертые в порошок корочки оспенных пустул. Однако метод не получил широкого распространения, так как часто вызывал тяжелые формы заболевания и гибель привитых.
Началом успешной борьбы с инфекционными болезнями можно считать 1796 г., когда английский врач и ученый Э. Дженнер предупредил заражение человека натуральной оспой. Он привил 8-летнего мальчика содержимым пустулы, взятым от заболевшей коровьей оспой молочницы. Привитой перенес слабую форму инфекции и приобрел устойчивость к инокуляции содержимого пустулы больных натуральной оспой. Материал, использованный для этой цели, был назван вакциной (от лат. Vacca – корова), а сам метод прививки – вакцинацией. Так родилась первая вакцина и начала свою историю наука о вакцинации.
С момента первого опыта Дженнера прошло уже более 200 лет. Ликвидирована натуральная оспа, практически ликвидированы паралитический полиомиелит, дифтерия, резко сократилось количество коклюша, кори, эпидемического паротита и др. Однако, несмотря на видимые преимущества, споры о целесообразности вакцинации не прекращаются, а порой усиливаются, выливаются в конфликты и активную антипрививочную кампанию [2]. И даже у активных приверженцев вакцинации, родителей и врачей, постоянно возникает множество вопросов. В статье мы постараемся осветить наиболее часто задаваемые из них.
Вопрос 1: нужно ли прививать ребенка: насколько эффективна вакцинация?
Вакцинация – введение антигенного материала с целью вызвать иммунитет к болезни, который предотвратит заражение или ослабит его отрицательные последствия. В нашем кишащим патогенами мире речь не идет об отмене вакцинации, а лишь о грамотном ее применении [3]. Благодаря вакцинопрофилактике удалось ликвидировать и существенно уменьшить количество более 40 различных инфекционных заболеваний, что снизило смертность населения и продлило жизнь человека. По данным ВОЗ, благодаря развернутым по всему миру программам вакцинации ежегодно удается сохранить 6 млн детских жизней и 750 тыс. детей не становятся инвалидами. Вакцинация ежегодно дарит человечеству 400 млн дополнительных лет жизни [4; 5]. Количество осложнений, возникающих после перенесенного инфекционного заболевания, в сотни раз превышает аналогичные после вакцинации. Кроме того, вакцины не только создают специфическую защиту от конкретных инфекций, они оказывают сильное неспецифическое действие, стимулируя многочисленные факторы естественной резистентности. Таким образом, вакцинация является самым эффективным и экономически выгодным профилактическим мероприятием, известным в современной медицине [6; 7].
Вопрос 2: какой иммунитет «лучше»: после перенесенной болезни или вакцинации?
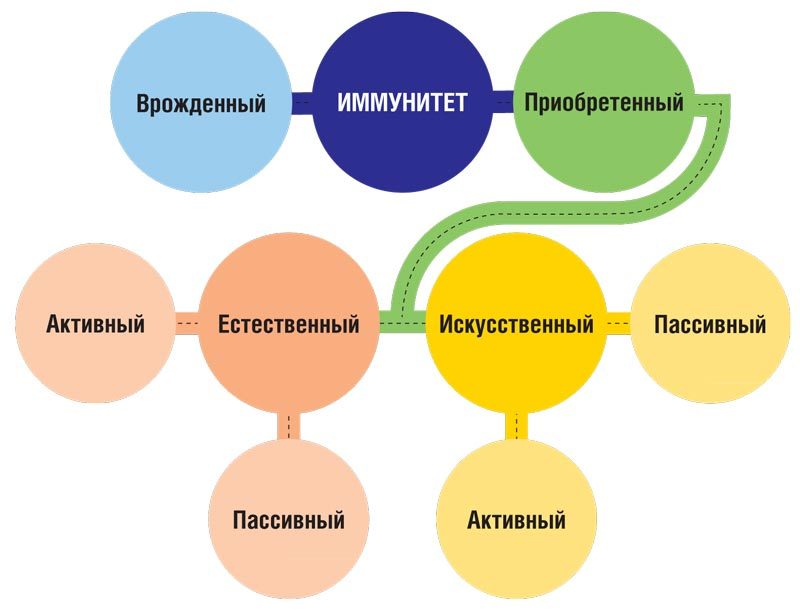
Часто можно слышать от родителей, а порой и от самих врачей, фразу: «Пусть переболеет: иммунитет крепче (лучше) будет». Так ли это? Термин «иммунитет» произошел от лат. immunitas, что в переводе означает «свобода от податей». В настоящее время под иммунитетом понимают защиту организма, направленную против проникновения генетически чужеродных патогенов и веществ с антигенными свойствами. Иными словами, основная задача иммунной системы – защита и сохранение генетического постоянства человека. Иммунитет подразделяется на врожденный, тот с которым человек появляется на свет и приобретенный, возникающий в результате контакта с патогенами (см. рис. 1).
Рис. 1. Виды иммунитета
Приобретенный естественный активный иммунитет возникает при контакте с циркулирующими в окружающей среде дикими штаммами возбудителя (инфекционное заболеваний), а пассивный – при поступлении в организм ребенка материнских антител трансплацентарно и с молоком (активен до 3–4 мес.). Искусственный приобретенный иммунитет формируется в результате введения в организм человека вакцины (активный) или иммунных сывороток и иммуноглобулинов (пассивный). При контакте с возбудителем, естественно или искусственно попавшим в организм, включаются одни и те же механизмы иммунного ответа [8].
Искусственный (поствакцинальный) иммунитет отличается от естественного, возникающего под влиянием перенесенной инфекции, меньшей напряженностью и напрямую зависит от вида вакцин (см. рис. 2).
Рис. 2. Иммуногенность вакцин (увеличение)
Обусловлено это тем, что при инфекции и введении живой или цельноклеточной вакцины организм отвечает на весь комплекс антигенов, входящих в состав микроорганизмов, тогда как при введении субъединичной вакцины иммунитет формируется под влиянием только отдельных антигенов (столбнячного, дифтерийного анатоксинов, Нbs-антигена и др.). Этим обуславливается и некоторое различие в длительности поствакцинального и постинфекционного иммунитета (табл. 1).
Таблица 1. Продолжительность постинфекционного и поствакцинального иммунитета
| Заболевание | Постинфекционный иммунитет | Поствакцинальный иммунитет |
| Гепатит В | Пожизненный | До 10 лет |
| Полиомиелит | Пожизненный типоспецифический | Пожизненный |
| Дифтерия | 5-10 лет | 5-10 лет |
| Столбняк | Практически не формируется | До 10 лет |
| Коклюш | Вероятно пожизненный | До 5 лет |
| Корь | Пожизненный | 20-25 лет |
| Краснуха | Пожизненный | 20-25 лет |
| Паротит | Пожизненный | 20-25 лет |
Однако в процессе формирования естественного иммунитета возникает гораздо больше рисков от осложнений, вплоть до летального исхода. Так что в одних случаях целесообразнее перенести инфекцию, а других сделать прививку.
Вопрос 3: содержат ли современные вакцины токсические примеси, такие как алюминий и ртуть? Опасно ли это для здоровья ребенка?
Вакцины – это биологические препараты, применяемые для активной иммунизации с целью специфической профилактики инфекций. В состав вакцин входят:
Идеальная вакцина должна быть высокоэффективной и безопасной. Эффективность зависит от реактивности макроорганизма и свойств антигена, используемого для вакцинации. Но повышение безопасности зачастую сопровождается понижением эффективности, так как чем выше степень очистки антигена, тем ниже его иммуногенная активность. Именно поэтому вакцинный препарат требует введения неспецифических иммуностимуляторов – адъювантов [9]. Механизм действия адъювантов сводится либо к стимуляции иммунной системы макроорганизма, либо к изменению структуры антигена, усиливая тем самым ответ на его внедрение. Кроме того, применение адъювантов позволяет получить надежный иммунитет даже на малые дозы антигена, уменьшить количество инъекций и снизить лекарственную нагрузку на организм. Наиболее часто в качестве адъюванта (только в инактивированные вакцины!) добавляют соли алюминия.
Алюминий является одним из самых распространенных металлов в природе. Он присутствует во многих тканях нашего организма (головной мозг – 0,02 мг/г, легкие – 0,59 мг/г), поступает к нам с водой и пищей, содержится в грудном молоке (0,01 мг/мл), применяется в качестве лекарственных препаратов (антациды). Случаи хронической интоксикации алюминием связаны, прежде всего, с пищей, водой или вдыханием алюминиевой пыли. Повышенное поступления растворимых солей алюминия оказывает выраженное токсическое действие на весь организм [10]. В качестве адъюванта используют нерастворимые соли алюминия с практически нулевой биодоступностью, следовательно, опасения все беспочвенны [11]. В силу своей нерастворимости и депонирования в месте инъекции системные реакции на введение вакцины исключены, а местные закономерны и не требуют дополнительного лечения.
Для обеспечения высокой безопасности, препятствия контаминации препарата микробной флорой обязательно введение и консервантов. Наиболее широкое применение нашли антибактериальные препараты. Для исключения лекарственной непереносимости рекомендуется тщательный сбор анамнеза, а в случае невозможности – проведение лекарственной пробы. Большой страх вызывает тиомерсал ртути, в незначительных количествах содержащийся в ограниченном перечне вакцин. Ртуть также является достаточно распространенным в природе элементом и в незначительных количествах содержится практически во всех тканях и органах нашего организма (0,3–2,0 мг/кг). Даже в крови новорожденных детей, до введения какой-либо вакцины, количество ртути составляет 0,1–4,5 нг/мл. Ежедневно человек массой тела 70 кг усваивает с пищей около 2,5–17 мкг ртути. Соли ртути оказывают выраженное токсическое действие на все живые организмы, что и послужило причиной использования ее в качестве консерванта. Содержание тиомерсала ртути в вакцинном препарате ничтожно мало – 0,3–0,5 мкг на дозу, а через 24 ч после введения вакцины снижается до 2,8 нг [12]. На сегодняшний день нет ни одного исследования, подтвердившего системное токсическое действие тиомерсала (при применении в стандартных дозах) или причастность его к развитию аутизма [13]. Так, в Канаде при обследовании почти 30 000 детей было выявлено, что среди получивших вакцинный препарат, содержащий мертиолят ртути, случаев аутизма было меньше, чем у детей, получавших вакцину без этого препарата [14]. Аналогичные данные были получены и в других странах, однако с 2003 г. ни одна педиатрическая вакцина не содержит солей ртути.
Практически все вакцины по основным показателям безопасности и эффективности соответствуют требованиям ВОЗ, но почти каждая нуждается в дальнейшем улучшении. И в заключение хочется напомнить, что токсическим при определенных условиях может стать практически любой химический элемент, даже кислород.
Вопрос 4: насколько часты осложнения после вакцинации?
Вопрос безопасности вакцин является, пожалуй, самым частым на приеме у педиатра. Необходимость вакцинации как наиболее эффективного средства предупреждения инфекций не вызывает сомнений. В то же время известно, что в поствакцинальном периоде, иногда даже в день прививки, могут возникать разнообразные заболевания. В таких случаях родители, а также сами врачи часто связывают заболевания детей с введенной вакциной, и это служит причиной отказа от дальнейшей вакцинации, снижает доверие и дискредитирует вакцинацию. Сразу нужно подчеркнуть, что не существует абсолютно безопасных вакцин. Вакцина – это лекарственный препарат, а медицина не знает ни одного лекарства даже от аллергии, у которого не было бы побочных эффектов.
Прежде, чем говорить об осложнениях, необходимо разобраться в терминологии. Различают три принципиально различных события:
Побочное действие вакцины – это способность вакцины вызывать функциональные и морфологические изменения в организме, выходящие за пределы физиологических колебаний и не связанные с формированием иммунитета. По сути, является отражением реактогенности вакцин. Клинически проявляется в виде незначительного недомогания, лихорадки, нерезко выраженных местных реакций, которые в большинстве случаев разрешаются самостоятельно.
Поствакцинальные реакции – клинические и лабораторные признаки временных патологических изменений в организме, связанные с вакцинацией. Это закономерные, ожидаемые процессы в поствакцинальном периоде, указанные в инструкциях к вакцинам. Различают:
В зависимости от степени выраженности все поствакцинальные реакции разделяют на слабые (лихорадка до 37,5°С, размер инфильтрата не превышает 3 см), средние (лихорадка до 38,5°С, размер инфильтрата не превышает 6 см) и сильные (лихорадка более 38,5°С, размер инфильтрата более 6–8 см). Все проявления обычного вакцинального процесса кратковременны и разрешаются обычно в течение 3–5 дней.
Поствакцинальные осложнения – клинические проявления стойких патологических изменений в организме, связанные с вакцинацией и не свойственные обычному вакцинальному процессу [15]. Выделяют следующие поствакцинальные осложнения.
Серьезные поствакцинальные осложнения встречаются крайне редко – реже, чем при применении других лекарственных средств и намного реже, чем при инфекционных заболеваниях [16–18] (см. табл. 2, 3).
Таблица 2. Сравнительная частота поствакцинальных осложнений и неблагоприятных реакций на ЛС
| Осложнение | Вакцина | Лекарственный препарат |
| Анафилактический шок | Один случай на 1 000 000 доз и реже | Один случай на 5 000 доз антибиотика (пенициллиновый ряд). Один случай на 100 000 доз рентгеноконтрастного вещества |
| Судороги | Один случай на 3-15 000 доз | Пенициллины 2-20% от всех введений |
| Тромбоцитопения | Один случай на 40 000 доз противокоревой вакцины | До 25% от всех госпитализаций |
Таблица 3. Сравнительная частота осложнений при вакцинации и заболевании у детей
| Вакцина | Заболевание | Частота осложнений от вакцинации (на 100 тыс. привитых) | Частота осложнений при заболевании (на 100 тыс. заболевших) |
| БЦЖ | Диссеминированный туберкулез | 0,1 | 1 000-3 000 |
| ОПВ | Паралитическая форма | 0,1-0,3 | 500-1 000 |
| АКДС | Судороги | 0,3-90 | 600-8 000 |
| Коревая вакцина | Энцефалит Пневмония Летальный исход | 0,1 – 0,02-0,3 | 50-400 4 000-7 000 10-1 000 |
| Паротитная вакцина | Энцефалит Орхит Воспаление околоушной железы | – – 10-100 | 25 20 000 80 000 |
Выявить причинно-следственную связь между вакцинацией и патологией, появившейся в вакцинальный период, бывает трудно. Зачастую связь может быть кажущейся, совпадающей по времени. Патологические процессы, регистрируемые при вакцинации, могут быть следствием:
Таким образом, постулат о том, что вакцинация представляет угрозу для жизни, – не более, чем выдумка. Многолетний опыт использования вакцин подтверждает, что вакцинация все же лучше, чем риск заболевания или его осложнения [19].
Вопрос 5: какие противопоказания к вакцинации имеются?
До недавнего времени количество противопоказаний к проведению вакцинации было очень велико. Поводом не прививать ребенка служили различные, даже самые минимальные проявления аллергии, риниты, информация о когда-то перенесенном тяжелом заболевании, страх «перегрузить иммунитет» грудного ребенка и просто неведение родителей и врачей об истинных противопоказаниях к вакцинации. Прежде всего, нужно четко подразделять противопоказания к проведению вакцинации на истинные, на которые должны ориентироваться врачи, и ложные, являющиеся результатом невежества и мракобесия. К ложным противопоказаниям относятся:
Список истинных противопоказаний в настоящее время весьма невелик и сформулирован на основании Приказа Минздрава России № 375 от 18.12.97 в соответствии рекомендациям ВОЗ [20]. Они включают в себя постоянные (абсолютные) и временные (относительные) противопоказания (см. табл. 4).
Таблица 4. Истинные противопоказания к проведению вакцинации
| Вакцина | Абсолютные противопоказания | Относительные противопоказания |
| Для всех вакцин | Сильные реакции и осложнения на предыдущую дозу препарата | Острые заболевания и обострение хронических болезней. Вакцинацию можно проводить в период ремиссии хронической патологии или через 2-4 недели после выздоровления от острого заболевания |
| Для всех живых вакцин | ПИД, глубокая иммуносупрессия, злокачественное новообразование, беременность | |
| БЦЖ | Масса тела ребенка менее 2000 г, реакция в виде келоидного рубца на предыдущую дозу вакцины | |
| АКДС | Прогрессирующее заболевание нервной системы, афебрильные судороги в анамнезе | |
| Корь, краснуха, паротит | Тяжелые реакции на аминогликозиды, анафилактические реакции на гетерологичный белок | Введение иммуноглобулинов, плазмы или крови человека. Иммуносупрессивная терапия. Беременность |
| Вакцина от гепатита В | Тяжелая аллергическая реакция на пекарские дрожжи | Беременность |
Таким образом, необходимо помнить, что существует лишь небольшое число истинных медицинских противопоказаний к вакцинации, которые применимы не более чем к 1% детей в РФ.
Вопрос 6: можно ли прививать детей с аллергическими заболеваниями?
В настоящее время аллергические заболевания принимают размах эпидемии: по статистике, более 25% жителей планеты имеют симптомы аллергических заболеваний. К аллергическим относят такие заболевания, как атопическая бронхиальная астма, атопический дерматит (экзема), аллергический риноконъюнктивит, крапивница аллергическая. Все эти заболевания, если находятся в периоде ремиссии, не являются противопоказанием для проведения плановой вакцинации. Исключение составляют анафилактические реакции, возникшие на введение предыдущих доз вакцин.
Необходимо помнить, что антигены вакцины редко бывают причиной возникновения аллергической реакции. Наиболее часто она развивается на различные примеси и добавки, содержащиеся в вакцинах (см. табл. 5):
Таблица 5. Компоненты вакцин, вызывающие аллергические реакции
| Компонент | Вакцина |
| Аминогликозиды | Гриппозные вакцины, коревая, краснушная, паротитная вакцины |
| Белок куриного яйца | Гриппозные вакцины, коревая и паротитная вакцины зарубежного производства, вакцина против желтой лихорадки |
| Пекарские дрожжи | Вакцина от гепатита В |
| Желатин | Вакцина от ветряной оспы |
Для успешной и безопасной вакцинации пациентов аллергическими заболеваниями необходимо соблюдение некоторых правил:
В заключение необходимо добавить, что у детей, страдающих аллергическими заболеваниями, достаточно высока сенсибилизация к бактериальным патогенам. Известно, что многие инфекционные заболевания (коклюш, корь, грипп) являются триггерами обострений бронхиальной астмы, атопического дерматита, аллергического ринита [21]. Следовательно, вакцинация играет важную роль не только в защите от инфекционного заболевания, но и в профилактике обострения основного заболевания.
Вопрос 7: как вакцинировать детей с первичным иммунодефицитом?
По классификации ВОЗ выделяют следующие виды иммунодефицитных состояний:
Первичные иммунодефициты (ПИД) – это генетически детерминированные заболевания, обусловленные нарушением сложного каскада реакций, необходимых для элиминации чужеродных агентов из организма и развития адекватных воспалительных реакций. Типичными проявлениями ПИД являются тяжело протекающие бактериальные, вирусные и грибковые инфекции, аутоиммунные заболевания и повышенная склонность к развитию злокачественных новообразований. В настоящее время опровергнуто заблуждение в чрезвычайной редкости данной патологии: ПИД встречаются с частотой от 1 : 1000 до 1 : 5 000 000 (в среднем 1 : 10 000) и могут проявиться в любом (!!) возрасте [22; 23]. Если диагноз иммунодефицита подтвержден лабораторно, возникает вопрос не об отмене вакцинации, а о разумном ее назначении. Дело в том, что для большинства детей с ПИД инфекция представляет бо´льшую опасность, чем прививка. Чтобы вакцинация у таких пациентов была успешной и безопасной, необходимо придерживаться ряда правил:
К сожалению, порой первые признаки ПИД (БЦЖ-ит, ВАПП) проявляются как раз после, прививки, что снижает приверженность вакцинации в целом. Решение проблемы кроется в ведении в РФ скрининга на ПИД у всех новорожденных детей.
В заключение необходимо еще раз подчеркнуть, что профилактика болезни является самым эффективным и экономически выгодным способом сохранения здоровья людей. Современная вакцинопрофилактика является ярким примером преимущества превентивных способов охраны здоровья населения [24; 25].