Подвижность ионов и электронов
Полезное
Смотреть что такое «Подвижность ионов и электронов» в других словарях:
ПОДВИЖНОСТЬ ИОНОВ И ЭЛЕКТРОНОВ — 1) в газе и н и з к о т е м п е р а т у р н о й плазме отношение ср. скорости v направленного движения эл нов или ионов (в результате действия электрич. поля) к напряжённости этого поля Е: m=v/E. Зависимость v от Е в принципе даётся решением… … Физическая энциклопедия
ПОДВИЖНОСТЬ НОСИТЕЛЕЙ ЗАРЯДА — отношение скорости направленного движения носителей заряда в веществе под действием электрического поля к напряженности этого поля. 1) В газе подвижность ионов и электронов обратно пропорциональна давлению газа, массе частиц и их средней… … Большой Энциклопедический словарь
ПОДВИЖНОСТЬ НОСИТЕЛЕЙ ЗАРЯДА — отношение скорости направленного движения носителей заряда в веществе под действием электрического поля к напряженности этого поля. 1) В газе подвижность ионов и электронов обратно пропорциональна давлению газа, массе частиц и их средней… … Большой Энциклопедический словарь
подвижность носителей заряда — отношение скорости направленного движения носителей заряда в веществе под действием электрического поля к напряжённости этого поля. 1) В газе подвижность ионов и электронов обратно пропорциональна давлению газа, массе частиц и их средней… … Энциклопедический словарь
ПОДВИЖНОСТЬ — электронов и ионовв газе и низкотемпературной плазме коэф. пропорциональности в соотношении связывающем величину скорости дрейфа v др электронов (ионов)в газе с величиной напряжённости электрич. поля Е, вызывающего этотдрейф. Понятие П.… … Физическая энциклопедия
ПОДВИЖНОСТЬ НОСИТЕЛЕЙ ТОКА — величина, характеризующая электрические свойства (см.) и полупроводников (см.), равная отношению средней установившейся скорости движения носителей тока (электронов, уст ионов, дырок) в направлении действия электрического поля к напряжённости Е… … Большая политехническая энциклопедия
ПОДВИЖНОСТЬ — носителей тока хар ка электрич. св в проводников и полупроводников, равная отношению ср. скорости упорядоч, движения носителей тока (электронов, ионов, дырок), возникающего под действием электрич. поля, к напряжённости этого поля. Понятие П.… … Большой энциклопедический политехнический словарь
ПЕРЕЗАРЯДКА ИОНОВ — взаимодействие положит. ионов с нейтр. атомами (молекулами) или поверхностью тв. тела, сопровождающееся обменом эл нами между взаимодействующими ч цами. П. п. в газах и жидкостях происходит по схеме А++В°+А°+В+ (верхние индексы указывают заряд ч… … Физическая энциклопедия
СТОЛКНОВЕНИЯ АТОМНЫЕ — элементарные акты соударения двух ат. ч ц (атомов, молекул, эл нов или ионов), при к рых структура и строение ядер не изменяются. С. а. делятся на упругие и неупругие. При у п р у г о м С. а. суммарная кинетич. энергия соударяющихся ч ц остаётся… … Физическая энциклопедия
ПОДВИЖНОСТЬ ИОНОВ



Свяжем электропроводность электролита со скоростью движения его ионов в электрическом поле. Для вычисления электропроводности надо подсчитать число ионов, проходящих через поперечное сечение электролитического сосуда в единицу времени. Так как электричество переносится ионами различных знаков, движущимися в противоположных направлениях, то общая сила тока складывается из количеств электричества, перенесенных катионами (I+) и анионами (I—) :
Подсчитаем количество катионов, проходящих через поперечное сечение электролита в 1 секунду. За это время через сечение пройдут все катионы, находившиеся на расстоянии не более чем u¢ см от выбранного сечения, т.е. все катионы в объеме u¢q :
Т.к. каждый г-экв ионов несет согласно закону Фарадея F =96485 к электричества, то сила тока (в А) :
Аналогично для анионов :
Для суммарной силы тока (с+ = с— = с¢) :
u¢ = u 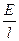
По закону Ома I = E/R = E×K = E×k
Отсюда k = (u + v)c¢qF/S = (u + v)c¢F (т.к. q º S)
l = 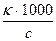
Для сильных электролитов : l = l+ + l—
Т.о., для всех электролитов можно записать :
Движение иона можно уподобить движению макроскопического шарика в вязкой среде и применить в этом случае формулу Стокса :
u =

Связь иона с молекулами растворителя ионно-дипольная, а так как напряжённость поля на поверхности иона лития гораздо больше, чем на поверхности иона калия, то степень гидратации иона лития больше степени гидратации иона калия. Согласно формуле Стокса многозарядные ионы должны обладать большей подвижностью, чем однозарядные. Однако скорости движения многозарядных ионов мало отличаются от скоростей движения однозарядных, что, очевидно, объясняется большей степенью их гидратации.
Что такое подвижность ионов
Электропроводность электролитов зависит от числа ионов в единице объема и от подвижности ионов.
Подвижность ионов определенного сорта выражается скоростью их перемещения в растворителе под действием электрического поля с падением потенциала в I в на I см.
Движение ионов можно обнаружить, например, проводя электролиз бесцветного раствора азотнокислого калия 




Рис. 134. Прибор для демонстрации движения ионов при электролизе.
В подобных опытах можно непосредственно измерить подвижность различных окрашенных (или окрашивающих индикаторы) разновидностей ионов. Однако удобнее пользоваться другими, окольными, но более точными методами измерения подвижностей. Результаты этих измерений представлены в таблице на стр. 186. Численные значения экстраполированы для бесконечно больших разведений соответствующих электролитов. (Иногда подвижностью ионов называют произведение приведенных в данной таблице чисел на заряд, равный фарадею, т. е. на 96 500 кулонов.)
Как видно из таблицы, подвижности различных ионов независимо от знака и величины их зарядов имеют близкие значения (несколько десятитысячных долей сантиметра в секунду, или, что тоже,
Подвижности 
доли миллиметра в минуту для поля 1 в/см). Но подвижности гидроксония 




Рис. 135. Фиктивное движение ионов гидроксония при электролизе.
Покажем, как при помощи таблицы подвижностей ионов вычисляется электропроводность растворов, настолько разбавленных, чтобы ионы были достаточно удалены друг от друга и вследствие этого, с одной стороны, не сцеплялись в молекулы, а с другой, — не тормозили движения друг друга своими собственными электрическими полями. Пусть в растворе содержится по 
падение потенциала 1 в/см; катод находится слева, анод — справа. Подвижности анионов и катионов обозначим, как в вышеприведенной таблице, через 





Рассуждая аналогично, для катионов мы найдем, что количество положительного электричества, ежесекундно переносимого ими через ту же площадку, но в противоположном направлении, составляет
Согласно определению удельная электропроводность раствора (как и всякого проводника) есть количество электричества, переносимое через 
В этой формуле 




Если в растворе не два вида ионов, а больше, то вообще
т. е. доля участия каждого вида ионов в электропроводности пропорциональна их концентрации, с одной стороны, и подвижности, —
с другой. Например, электропроводность 
Здесь мы воспользовались правом считать сильные электролиты (какова азотная кислота) в разбавленных растворах ( 
Формула (6) показывает, что удельная электропроводность 
У достаточно разбавленных растворов такая пропорциональность между удельной электропроводностью и концентрацией действительно имеется. Примером могут служить числа, приведенные в таблице.
Электропроводность растворов хлористого калия при 18° С
В более концентрированных растворах пропорциональность между концентрацией и удельной электропроводностью, требуемая найденным выше соотношением, нарушается. Наблюденная электропроводность у обычно оказывается менее вычисленной т. е. 1. Это имеет две причины. Прежде всего в случае мало разбавленных растворов нет полной диссоциации электролита; в каждый данный момент часть ионов связана в молекулы и не участвует в проведении электрического тока. Поэтому отношение — должно быть равно степени диссоциации а электролита в данном растворе. В связи с этим измерение электропроводности растворов является весьма простым, удобным и широко применяемым способом определения степени диссоциации; полученные таким способом значения а согласуются со значениями а, вычисленными для тех же растворов на основании закона Оствальда (т. I, § 121). Однако согласование с законом Оствальда имеет место только для слабых электролитов.
Изменение электропроводности сильных электролитов с концентрацией происходит не так, как можно было бы ожидать на основании закона действующих масс. Здесь при высоких концентрациях уменьшается не число ионов, фактически участвующих в проведении тока, а уменьшаются 
Рис. 136 показывает, какая сложная зависимость существует между удельной электропроводностью растворов сильных электролитов и концентрацией, выраженной в единицах нормального раствора. Аналогичный вид имеют кривые, характеризующие зависимость электропроводности от концентрации» выраженной в процентах по весу. Эти графики показывают, что удельная электропроводность электролитов возрастает до определенной концентрации раствора и потом убывает. Например, среди растворов соляной кислоты наибольшую электропроводность имеет примерно пятинормальный раствор (около 20% 
Рис. 136. Зависимость удельной электропроводности сильных электролитов от концентрации, выраженной в грамм-эквивалентах на литр.
По формуле (6), которая, впрочем, справедлива только для слабых электролитов и при достаточно больших разбавлениях, отношение удельной электропроводности к грамм-эквивалентной концентрации раствора должно быть одинаковым для растворов всех концентраций. Указанное отношение, увеличенное в 1000 раз, называют эквивалентной электропроводностью:
По формуле (6) эквивалентная электропроводность должна выражаться как произведение суммы подвижностей ионов на заряд Фарадея:
Для удобства сопоставления различных электролитов и для выявления того, в какой мере свойства какого-либо электролита отличаются от свойств слабого, разбавленного, полностью диссоциированного электролита, в электрохимии результаты измерения электропроводности растворов почти всегда выражают в виде значений эквивалентной электропроводности.
Из определения эквивалентной электропроводности 

Удельное сопротивление и электропроводность некоторых электролитов (водных растворов) при 18° С
раствора 

Удельная электропроводность — это электропроводность неизменного количества раствора 
Эквивалентная электропроводность как сильных, так и слабых электролитов возрастает с уменьшением концентрации. На рис. 137 показан характерный для большинства электролитов вид кривых, определяющих зависимость эквивалентной электропроводности от концентрации. В таблице приведены значения эквивалентной электропроводности для некоторых электролитов.
Эквивалентная электропроводность некоторых электролитов в водных растворах при 18° С
Обратимся к вопросу о пределах применимости закона Ома к электролитам. Из теории движения тел в вязкой среде известно, что скорость установившегося (стационарного) движения в вязкой среде пропорциональна действующей на тело силе. Движущийся к электроду ион удовлетворяет тем условиям, для которых выведено это соотношение; поэтому скорость движения иона должна быть пропорциональна действующей на ион силе, т. е. произведению напряженности поля на заряд иона. Если напряжение тока а следовательно, и напряженность поля увеличатся в 
Рис. 137. Изменение эквивалентной электропроводности с изменением концентрации.
Таким образом, в случае элек тролитов закон Ома должен быть справедлив в тех пределах, в которых сохраняется пропорциональность между скоростью движения ионов и действующей на них электрической силой. Эти пределы очень широки, В недавнее время доказано, что отклонения от закона Ома становятся заметными лишь при напряжениях порядка 106 в/см. При этих напряжениям скорости движения ионов становятся сравнимы со скоростью движения пас сажирских поездов.
Что такое подвижность ионов
Проводники, обладающие ионной проводимостью, носят название электролитов. К ним относятся растворы солей, кислот и щелочей.
Молекулы электролита и растворителя представляют собой электрические диполи, состоящие из ионов противоположного знака, удерживаемых на определенном расстоянии силами кулоновского взаимодействия.
В растворе каждую молекулу электролита окружает группа молекул растворителя, которая своим электрическим полем ослабляет связи между ионами молекулы электролита, вследствие чего они могут оказаться разорванными за счет теплового хаотического движения.
Процесс распада молекул называется электролитической диссоциацией. Степенью диссоциации называется отношение числа диссоциированных молекул электролита к общему числу его молекул :
Наибольшей диссоциирующей способностью обладает вода, имеющая большое значение диэлектрической проницаемости ( ).
Электрический ток в электролитах обусловлен движением ионов и носит название тока ионной проводимости.
Плотность этого тока равна:
Плотность тока через подвижность ионов выражается формулой
Приравнивая электрическую силу силе внутреннего трения, получим для подвижности иона следующее выражение:
С повышением температуры подвижность иона возрастает за счет уменьшения вязкости среды и размеров сольватной оболочки. С повышением температуры несколько увеличивается и степень диссоциации молекулы электролита. Таким образом, электропроводность электролитов возрастает с повышением температуры, а сопротивление уменьшается по закону
Линейная зависимость сопротивления от температуры для электролитов носит приближенный характер, так как не является постоянной величиной. Однако в узком интервале температур зависимость от линейная.