Что такое патогенный вирус
Что такое «вирусы»?
Что представляют собой вирусы?
Вирусы — это мельчайшие частицы (от 15 до 3500 нм), своеобразные формы жизни, имеющие неклеточное строение, которые содержат собственный геном и способны размножаться только в клетках других организмов. Увидеть их можно в электронный микроскоп.
Впервые вирусные частицы были описаны Д. Ивановским (1892 г.) и М. Бейеринком (1898 г.). С тех пор их изучает отдельный раздел биологии – вирусология.
На настоящий момент считается, что вирусы — самая распространенная биологическая форма на Земле, насчитывающая около 100 млн. видов.
Обычно находятся они либо вне клеток (в покое), либо внутри их (вегетативная или репродуцирующая форма).
Ученые-биологи до сих пор спорят о том, что же такое вирусы, живые они или нет, разумные или не совсем.
Так как жить эти частицы могут только в чужих организмах, они являются паразитами. Встраивая свой генетический материал в клеточную структуру, они заставляют клетку воспроизводить себе подобных, разрушая её саму.
Вирион представляет собой комплекс нуклеиновой кислоты и белка (простые). В сложных есть еще и гликопротеиды. Снаружи находится оболочка – капсид, который защищает частицу от внешних воздействий и обеспечивает адсорбцию на нужных клетках-донорах. Он бывает спиральной, продолговатой, икосаэдрической и смешанной формы.
В зависимости от вида нуклеиновой кислоты, вирусы бывают РНК- и ДНК-содержащие.
Примеры первых: ротавирусы, ВИЧ, возбудители гепатита С, А и Е, гриппа, полиомиелита, бешенства, кори, лихорадки Эбола, ТОРС, коронавирусы (в частности, COVID-19) и др.
Ко вторым относятся: возбудители оспы, гепатита В, герпеса, папиллом и др.
Борьба с вирусами
Само название «вирус» в переводе с латыни обозначает «яд». И действительно, паразитируя в клетках других организмов, вирусы наносят им вред, заставляя работать на себя и, в конечном итоге, разрушая.
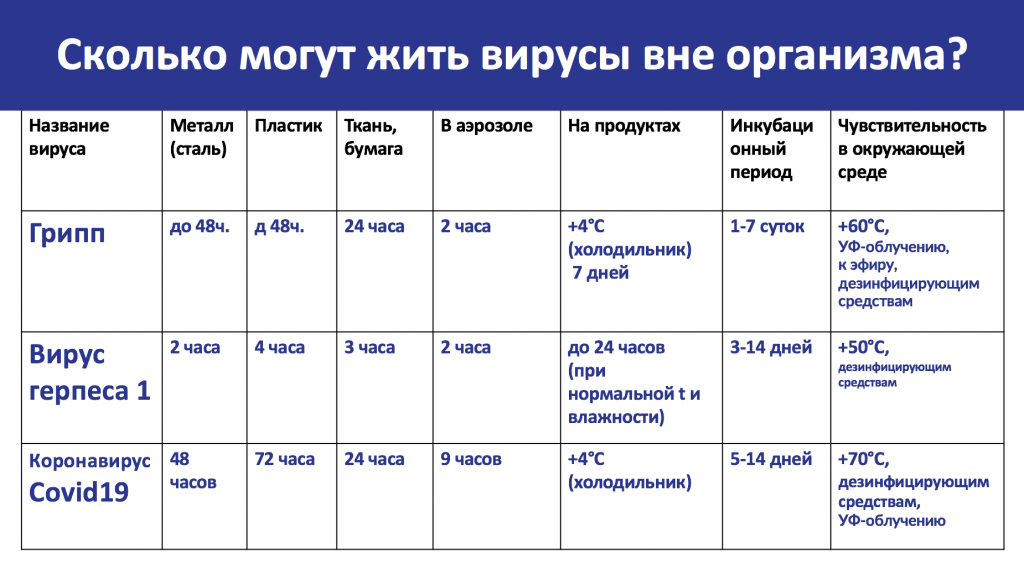
Находясь во внешней среде, эти зловредные сущности быстро погибают от сторонних воздействий: высокой температуры, солнечного света, дезсредств. Устойчивость к внешним факторам зависит от вида вируса. Например, при комнатной температуре возбудитель гепатита В живет до 3 месяцев, гепатита А — несколько недель.
При замораживании вирусы сохраняются месяцы, иногда даже годы.
Попадая в организм человека, животных или растений различными путями (воздушно-капельный, контактный, половой, алиментарный, через кровь), они поражают органы и ткани, вызывая различные заболевания.
Ученые научились использовать некоторые виды вирусов во благо человеку. Например, бактериофаги паразитируют в патогенных бактериях и ведут к их гибели, что помогает победить болезнь.
Вирусы обладают большой изменчивостью, что значительно затрудняет борьбу с ними.
Инфицированный организм обычно сам мобилизует свою иммунную систему для уничтожения вредных захватчиков.
Разрабатываются профилактические и лечебные меры для предотвращения распространения вирусных заболеваний.
Средства борьбы с вирусами:
Дезинфицирующие средства от вирусов
В настоящее время к дезинфектантам предъявляются повышенные требования.
Они должны обладать:
Например, препараты Септолит, которые производит компания Сателлит — это профессиональные дезинфектанты, отвечающие всем современным нормам и разрешенные Роспотребнадзором для дезинфекции как в различных учреждениях, так и в быту.
Рабочие растворы хлорсодержащих таблеток «Септолит ДХЦ» и жидкого концентрата «Септолит Плюс» идеально подходят для обеззараживания пола и других водостойких поверхностей при ежедневной и генеральной уборке любых помещений по противовирусному режиму.
Благодаря сочетанию дезинфицирующих и моющих свойств «Септолит Тетра» удается избавиться от бактерий, грибков и вирусов (в том числе, ВИЧ, гепатитов, полиомиелита, COVID-19) при обработке медицинских и маникюрных инструментов, оборудования, мебели, игрушек, посуды.
Природа патогенности вирусов
Об авторе
Вадим Израилевич Агол — член-корреспондент РАН и РАМН, доктор биологических наук, главный научный сотрудник Института полиомиелита и вирусных энцефалитов им. М. П. Чумакова, заведующий отделом Научно-исследовательского института физико-химической биологии им. А. Н. Белозерского МГУ. Область научных интересов — молекулярная биология и генетика вирусов.
Считается, что вирусы (от лат. virus — яд) — нечто противное, приносящее одни неприятности. Но это грубая ошибка. Вирусы — ключевые созидатели живой природы и двигатели ее эволюции.
Что возникло раньше — вирус или клетка? Долгое время преобладала очень логичная точка зрения: поскольку вирусы — облигатные паразиты и без клетки размножаться не могут, то они должны были возникнуть позже. И вообще считалось, что вирусы — нечто вроде «сбежавших», «сумасшедших» генов. Однако сейчас широко распространен противоположный взгляд — клетки произошли от вирусов.
Один из главных доводов против гипотезы о том, что вирусы «сбежали» из клеток, — тот факт, что вирусные генетические системы существенно разнообразнее клеточных. Как известно, клеточные организмы имеют только двунитевые — линейные или кольцевые — ДНК-геномы. А геном вируса может быть представлен как одно-, так и двунитевыми молекулами РНК или ДНК, линейными или кольцевыми. Также существуют системы, использующие обратную транскрипцию. Так, у ретровирусов (например, некоторых онковирусов, ВИЧ) и параретровирусов (вирусов гепатита В, мозаики цветной капусты и др.) одна из цепей геномной ДНК синтезируется на матрице РНК. У вирусов, в отличие от клеточных организмов, реализуются все теоретически возможные способы хранения и выражения генетической информации [1].
Второй важный довод против того, чтобы считать вирусы произошедшими из клеток, заключается в том, что существует множество вирусных генов, которых в клеточных организмах нет. Клеточные организмы не только произошли от вирусов, но и унаследовали от них (и продолжают наследовать) значительную часть своего генетического материала. Особый интерес в этом отношении представляют эндогенные вирусы (части генома РНК- или ДНК-вирусов, встроенные в геном клетки), среди которых преобладают гены, происходящие от ретровирусов. Полагают, что млекопитающие унаследовали свыше половины генома от вирусов и их ближайших родственников — «эгоистических» генетических элементов, например, плазмид и транспозонов. Таким образом, вирусы — сородители человека. Часто последовательности генов эндогенных вирусов, которые в большом количестве имеются в человеческом геноме, изменены и уже не кодируют белки. Есть серьезные основания полагать, что такие последовательности участвуют в регуляции работы клеточных генов, хотя часто их конкретные биологические функции неизвестны. Однако кое-что важное мы знаем: например, белок синцитин, который кодируется геном оболочки одного эндогенного ретровируса, необходим для слияния клеток при образовании плаценты [2]. Значит, ни человек, ни плацентарные животные не могли бы родиться без этого эндогенного вируса. Есть и другой важный пример. Выяснилось, что компонент генома одного из эндогенных вирусов контролирует экспрессию пролиндегидрогеназы в некоторых районах центральной нервной системы [3]. Возможно, этот фермент принимал важное участие в эволюции мозга человека. Если в результате мутаций экспрессия этого фермента нарушена, возникают психические болезни, в том числе шизофрения. Также важную роль вирусы и их родственники играют в горизонтальном переносе клеточных генов — от одного организма другому.
Механизмы защиты и противозащиты
В ответ на клеточную защиту эволюция вирусов вырабатывает противозащитные средства, и между вирусом и клеткой идет гонка вооружений. Эти средства направлены прежде всего против общих метаболических процессов, лежащих в основе защитных реакций клетки. Это опять угнетение синтеза клеточных РНК и белков, нарушение внутриклеточной инфраструктуры и транспорта клетки, подавление или, наоборот, запуск апоптоза и других механизмов, вызывающих программируемую клеточную гибель. Таким образом, противозащитная стратегия вируса во многом похожа на защитное поведение клетки. Образно говоря, борцы применяют одни и те же приемы, бьют в одни и те же ворота. Например, клетка, подавляя синтез вирусных белков, использует интерферон, а, чтобы затормозить его образование, вирус, в свою очередь, угнетает белковый синтез в клетке. В зависимости от обстоятельств выгоду получает та или другая сторона. Оказывается, главный вклад в патологию вносит не размножение вируса как таковое, а противоборство клеточной защиты и вирусной противозащиты. В фитопатологии давно существует понятие «толерантность»: патогенный вирус может активно размножаться в зараженном растении, не вызывая болезненных симптомов.
Далее речь пойдет в основном о РНК-содержащих вирусах (это более простой пример). Как РНК-вирус, проникнув в клетку, выдает свое присутствие? И как клетка узнает, что в нее попал вирус? Главный признак, благодаря которому клетка это «понимает», — вирусная двуцепочечная РНК, которая в принципе может образовываться и в незараженной клетке, но не в таких количествах и местах. Клетка в некоторых случаях узнает также вирусную одноцепочечную РНК, а иногда (значительно реже) — и вирусные белки. Важно, что узнавание вирусной РНК неспецифично: «почувствовав» двуцепочечную РНК, клетка может «подумать», что в нее попал вирус, но какой — она не знает. РНК улавливаются сенсорами двух типов: толл-подобными (от англ. toll-like и от нем. toll — замечательный) рецепторами и специализированными РНК-хеликазами. Они включают ряд защитных механизмов на транскрипционном уровне, в том числе образование интерферона. Кроме того, вирусные РНК узнаются уже «исполнителями» — зависимой от двуцепочечной РНК протеинкиназой PKR, которая фосфорилирует некоторые факторы инициации трансляции, угнетая тем самым синтез белков; олигоаденилатсинтетазой (OAS), которая активирует РНКазу L, расщепляющую РНК; системой РНК-интерференции, приводящей к деградации РНК и нарушению ее трансляции.
Поскольку вирус узнается как нечто неспецифическое, клетка не может знать его «намерений». И вообще на любой возможный вирус индивидуальную врожденную систему защиты было бы невозможно придумать. Значит, клетка может бороться с вирусом только стандартными приемами. И поэтому ее оборонительные действия часто несоразмерны имеющейся угрозе. Однако, если защитные реакции клетки столь неспецифичны, почему разные вирусы вызывают все-таки различные болезни? Во-первых, каждый вирус может заражать только определенный вид клеток конкретных организмов. Это связано с тем, что для проникновения в клетку он должен провзаимодействовать с клеточными рецепторами, которые ему «подходят». Кроме того, для размножения вирусов требуется определенная внутриклеточная среда (нередко нужны специфические клеточные белки). Во-вторых, в то время как защитные реакции клетки стандартны, противозащитные средства вируса в большой степени индивидуальны, хотя и направлены против стандартных клеточных механизмов.
У растений в качестве противовирусного механизма очень важную роль играет РНК-интерференция. Из вирусной РНК образуется двуцепочечная (важный фактор, по которому клетка узнает о наличии вируса). При участии компонентов системы РНК-интерференции — фермента Dicer, который разрезает эту двуцепочечную РНК на фрагменты длиной 21–25 пар нуклеотидов, а затем РНК-белкового комплекса RISC — в конце концов образуются одноцепочечные короткие фрагменты РНК. Гибридизуясь с вирусной РНК, они вызывают либо ее деградацию, либо угнетение ее трансляции. Такой защитный механизм эффективен, но может повреждать саму клетку, что хорошо видно на примере вироидов. Это патогены растений, короткие (несколько сотен нуклеотидов) молекулы кольцевой одноцепочечной РНК, не покрытые белковой оболочкой. Вироиды не кодируют белки, но могут вызывать тяжелые симптомы в зараженном растении. Это происходит потому, что клетка защищается. Образующаяся вироидная двуцепочечная РНК подвергается действию всех компонентов системы РНК-интерференции, в результате образуются фрагменты одноцепочечной РНК, которые гибридизуются уже не с вирусной РНК, а с клеточной. Это приводит к ее деградации и развитию симптомов заболевания. Однако многие вирусы растений кодируют разнообразные белки, препятствующие РНК-интерференции (viral suppressors of RNA silencing — VSR). Они либо угнетают распознавание и расщепление вирусных РНК, либо подавляют формирование и функционирование комплекса RISC. Поэтому эти VSR-белки могут нарушать механизмы физиологически важной (не связанной с вирусами) РНК-интерференции, вызывая патологические симптомы.
«Секьюрити»-белки
От работы таких белков в значительной степени зависит противозащита вирусов, в частности пикорнавирусов — мелких РНК-содержащих патогенов. В эту большую группу входят, в частности, возбудители полиомиелита, гепатита А, ящура и др. Особенность этих вирусов в том, что за редким исключением их белки синтезируются в виде единого полипротеина, из которого затем образуются отдельные зрелые белки. Среди них можно выделить три группы. Первая состоит из ключевых белков — жизненно важных, с фиксированными функциями, непосредственно обеспечивающих размножение вируса: РНК-зависимые РНК-полимеразы, необходимые для репликации вирусного генома; капсидные белки, образующие белковую оболочку вируса; протеазы, принимающие участие в процессе превращения полипротеина в зрелые белки; белок VPg (viral protein genome linked — вирусный белок, соединенный с геномом), служащий затравкой для синтеза молекул РНК; хеликаза — очень ценный фермент, который есть у всех пикорнавирусов, но играет не очень понятную роль. Вторая группа включает также жизненно необходимые белки, но выполняющие «подсобные» работы — гидрофобные белки-«гиды» 2В и 3А. Они направляют ключевые белки в места назначения и способствуют созданию оптимальной внутриклеточной среды для репродукции вируса. В третью группу включаются лидерный белок L, открытый в нашей лаборатории 30 лет назад [4], и белок 2А; мы назвали их «секьюрити»-белками (security — охрана) [5]. Это специализированное противозащитное «вооружение» пикорнавирусов. Вообще, все эти три класса белков могут бороться с защитными механизмами клетки. Но ключевые белки и белки-«гиды» занимаются этой работой «по совместительству», так как у них есть другие важные обязанности, которым должны соответствовать их структура и функции. Следовательно, их оборонительные возможности ограничены необходимостью выполнять основную работу. А вот «секьюрити»-белки трудятся по специальности «на полную ставку» — эволюция «наняла» их именно для «охраны» (потом некоторые из них «научились» делать и что-то еще). Для исполнения своих обязанностей они могут иметь любую необходимую структуру [6].

Схема полипротеина (белка-предшественника) пикорнавирусов
Одна из важнейших функций «секьюрити»-белков состоит в том, что они принимают участие в определении судьбы зараженной клетки. Существует много разных вариантов ее гибели, но два главных, наиболее известных механизма — некроз и апоптоз, которые различаются по морфологическим и биохимическим признакам. При некрозе клетка лизируется, а ее содержимое изливается наружу, в межклеточное пространство. При апоптозе на ее поверхности образуются хорошо различимые выпячивания, ее ДНК деградирует до нуклеосомных фрагментов, и в конечном счете клетка фрагментируется на отдельные апоптотические тельца, ограниченные плазматической мембраной. Очень важно, как именно клетка умрет. При некрозе развивается защитное воспаление, но при этом вирус выходит из клетки и распространяется. При апоптозе же распространение вируса ограничено и обычно нет воспалительной реакции. Гибель зараженной клетки, как правило, — это акт самопожертвования, ограничивающий репродукцию вируса.
Модель вируса полиомиелита. Фото: virology.wisc.edu
Другой противозащитный механизм «секьюрити»-белков пикорнавирусов — нарушение ядерно-цитоплазматического транспорта [10–12]. Мы показали, что при заражении этими вирусами повышается проницаемость ядерной оболочки и нарушается активный обмен макромолекулами между цитоплазмой и ядром. А если структура клетки повреждена, то она не может включать свои регуляторные механизмы для борьбы с вирусом. У полиовируса «секьюрити»-белок 2А нарушает ядерно-цитоплазматический транспорт, гидролизуя нуклеопорины — компоненты ядерных пор [11]. А у вируса энцефаломиокардита работает лидерный белок — он влияет на клеточный каскад фосфорилирования нуклеопоринов [12, 13].
Противозащитная функция «секьюрити»-белков может проявляться и по-другому. Так, L-белки кардиовирусов (в том числе вируса энцефаломиокардита) и 2А-белки энтеровирусов (включая полиовирус) угнетают образование интерферона. А его действие тормозят L-белок вируса ящура и 2А-белок полиовируса. Тем не менее «секьюрити»-белки пикорнавирусов — не жизненно важные. Обоих стражей можно удалить либо вызвать в них значительные делеции (как в случае L-белка кардиовирусов, 2A-белков вируса гепатита А и кардиовирусов) — и при этом вирус не лишается жизнеспособности.
Обоюдное разоружение
Модель менговируса (штамма вируса энцефаломиокардита). Фото: virology.wisc.edu
Каковы будут последствия инактивации вирусных «секьюрити»-белков для клетки? С одной стороны, повысится чувствительность вирусов к защитным механизмам врожденного клеточного иммунитета. Но, с другой стороны, возрастет и его самоповреждающая, самоубийственная активность. А что произойдет, если одновременно выключить оборонительные механизмы клетки и вируса? Мы изучали такую ситуацию на примере взаимодействия менговируса (штамма вируса энцефаломиокардита) и клеток HeLa [14]. Зараженные вирусом дикого типа, они достаточно быстро гибнут от некроза. А если вирус частично разоружен (инактивирован лидерный белок), клетки HeLa живут чуть дольше и гибнут не от некроза, а от апоптоза. Когда же снижена обоюдная оборона (в клетке выключен апоптоз химическим соединением, которое угнетает каспазы, а у вируса инактивирован его лидерный белок), даже через вдвое больший промежуток времени клетки чувствуют себя значительно лучше, чем те, которые не были разоружены. А размножение вируса (и динамика, и урожай) шло совершенно одинаково, независимо от того, была ли выключена только его противозащита или одновременно снята и клеточная оборона. Получается, что в клетках, в которых еще нет серьезных патологических повреждений (так называемого цитопатического эффекта), может образоваться уже очень много вирусных частиц. Таким образом, для размножения вируса повреждение клетки необязательно. Следовательно, эффективной стратегией антивирусной терапии, направленной на облегчение симптомов заболевания, может служить одновременное подавление как вирусной противозащиты, так и клеточной защиты.

Эффект одновременного выключения клеточных защитных и вирусных противозащитных механизмов. Зараженные менговирусом дикого типа, клетки HeLa (а, незараженные) быстро гибнут от некроза (б, 4 ч после заражения). Клетки, зараженные частично разоруженным вирусом, у которого инактивирован лидерный белок, живут чуть дольше и гибнут уже от апоптоза (в, 8 ч после заражения). Когда же частично разоружены и вирус (инактивирован его лидерный белок), и клетки (у них выключен апоптоз добавлением химического соединения, которое угнетает каспазы), даже через вдвое больший промежуток времени клетки чувствуют себя значительно лучше, чем те, которые не были разоружены (г, д, 8 и 16 ч после заражения). Большинство клеток на панелях г и д морфологически больше похожи на клетки на панели а, чем на б и в. Сканирующая электронная микроскопия. Фото С. И. Галкиной
Программируемая гибель
Таким образом, самопожертвование клетки при вирусной инфекции может проявляться в виде некроптоза или апоптоза. Некроптоз может быть защитной реакцией клетки на вирусную инфекцию, и не только в случае пикорнавирусов. Какой механизм выгоднее для вируса — зависит от условий. Мы видим, что его противозащитное действие может проявляться в виде «перемаршрутирования» механизмов, закодированных в геноме клетки. Это важный (хотя и не единственный) способ противозащиты и один из основных механизмов патогенности вирусов. Индуцированные вирусом программы апоптоза и некроза конкурируют друг с другом [15]. Мы показали, что при заражении клеток HeLa полиовирусом сначала включается апоптоз, а затем происходит его подавление и запускается некротический путь. Таким образом, заражение клетки вирусом активирует в ней ряд защитных действий, среди которых есть два самоубийственных механизма программируемой гибели — апоптозный и некротический. А дальше происходит конкуренция между этими путями: угнетение одного из них активирует другой, и наоборот [16]. И все это регулируется клеточными белками, вирусными (в первую очередь «секьюрити»-белками), а также внешними факторами.
Гонка вооружений
Однако длительная коэволюция хозяина и вируса должна приводить к снижению патогенности последнего (взаимовыгодному обоюдному разоружению). Классический пример — вирус миксомы / фибромы. В середине XIX в. в Австралию завезли европейских кроликов, которые быстро размножились и стали серьезной угрозой для сельского хозяйства. Через 100 лет для контроля их популяции стали использовать патогенный вирус фибромы / миксомы (из семейства поксвирусов, к которому относится и вирус оспы). Разные кролики по-разному реагируют на этот вирус. У бразильских кроликов через три недели после заражения он вызывает доброкачественную опухоль — фиброму (локализованный узелок на коже). Но у европейских кроликов, чувствительных к этому вирусу, уже через 10 дней после заражения развивается генерализованное смертельное заболевание.
Завезенный в Австралию, этот вирус вызывал переносимые комарами летние эпизоотии, когда более 99% инфицированных кроликов гибли меньше чем за две недели. Перезимовать больше шансов имели менее вирулентные варианты вируса, и это приводило к отбору ослабленных (аттенуированных) штаммов. И примерно через 10 лет смертность европейских кроликов от эволюционировавшего вируса снизилась вдвое. Одновременно шел отбор резистентных кроликов: их смертность от исходного вируса снизилась примерно в четыре раза. Всего за десятилетие (ничтожно малый срок в рамках эволюции) примерно в 10 раз улучшились взаимоотношения между патогеном и хозяином. Это, безусловно, несколько упрощенная схема, поскольку гонка вооружений не прекращается: в ответ на повышение резистентности кроликов может возрастать и вирулентность вируса. Однако это яркий пример роли взаимодействия вирусов и клеточных организмов в эволюции и тех и других. Вирусы и клетки «учат» друг друга, и полученные «знания» наследуются. В 2013 г. году два выпускника кафедры вирусологии МГУ Евгений Кунин и Валерьян Доля опубликовали статью о «вироцентрическом» взгляде на эволюцию, согласно которому противодействие и кооперация вирусов и клеточных организмов — главный фактор их эволюции [17].
Мой рассказ далеко не исчерпывает тему: о природе патогенности вирусов известно значительно больше. Многое из того, что мы сейчас знаем, удалось изучить в самые последние годы, и есть все основания ожидать новых сюрпризов. Можно и нужно винить вирусы за тяжелые болезни и необходимо бороться с ними, но мы должны быть благодарны вирусам за существование и разнообразие живой природы, и в том числе — за существование человека.
Автор благодарен коллегам по научной кооперации — сотрудникам Института полиомиелита и вирусных энцефалитов им. М. П. Чумакова РАМН, Московского государственного университета им. М. В. Ломоносова, Института белка РАН (Пущино Московской области), Университета Базеля (Швейцария), Университета штата Висконсин (США), Университета Неймегена им. Радбода (Нидерланды).
Статья основана на лекции, прочитанной на школе «Современная биология и биотехнологии будущего» (Звенигород, 26 января — 1 февраля 2014 г.).
Что мы знаем о вирусах и методах защиты от них?
Что такое вирус?
Как устроен вирус?
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
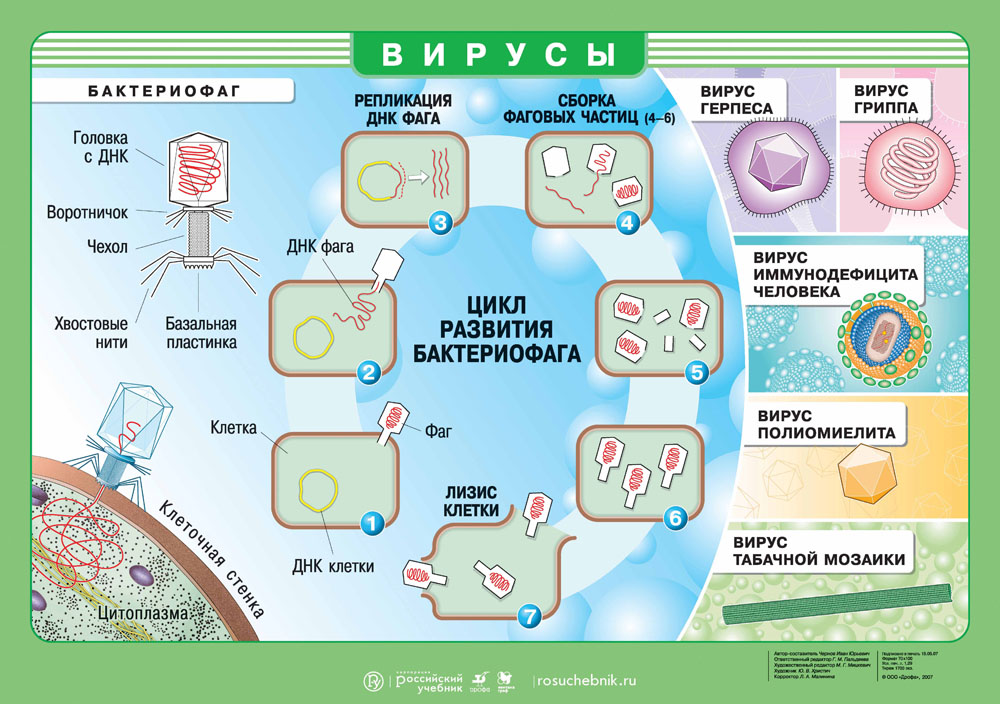
Вирусы. Цикл развития бактериофага. Скачать наглядное пособие в большом разрешении можно здесь.
Как вирус попадает в организм?
Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
«Для проникновения в клетку белки поверхности вируса связываются со специфическими поверхностными белками клетки. Прикрепление, или адсорбция, происходит между вирусной частицей и клеточной мембраной. В мембране образуется дырка, и вирусная частица или только генетический материал попадают внутрь клетки, где будет происходить размножение вируса. Сегодня ученые всего мира сделали важное открытие о том, что заражение коронавирусом людей преклонного возраста объясняется тем, что у пожилых людей накапливается специфический белок, который помогает COVID-19 проникать внутрь клетки эпителия».
Выход вируса
Скорость распространения вирусной инфекции
Вирусная латентность
Как вирус распространяется?
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
«Мы пытались рассказать Вам не только о существующих научных фактах о вирусах, но и показать, что определенные знания помогают нам в нынешней практической ситуации сохранить свое здоровье и здоровье своих близких. Мы понимаем, что сегодня коронавирус может находиться практически везде: на поверхностях любых предметов, в окружающей среде и т.д. Поэтому самоизоляция – это один из важнейших способов защиты от инфекции. Находясь дома, вы защищаете не только свое здоровье, но и помогаете медикам и ученым, которые сражаются с этим вирусов и день и ночь. Ведь, чем меньше шансов у нас с вами заболеть, тем больше шансов появляется у них, чтобы победить коронавирус. Пожалуйста, оставайтесь дома и соблюдайте режим самоизоляции и нормы гигиены».