Опыт применения эхографии при остром панкреатите и его осложнениях
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Материалы и методы
Результаты
На основе наших наблюдений выявлены следующие сонографические особенности острого панкреатита:
Изменения непосредственно в поджелудочной железе:
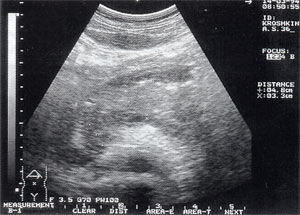
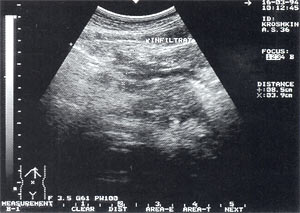
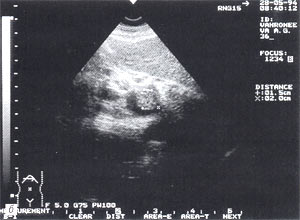
Рис. 1. Острый панкреатит, деструктивная форма. Увеличение размеров поджелудочной железы, нечеткость контуров, увеличение расстояния между задней стенкой желудка и поджелудочной железы.
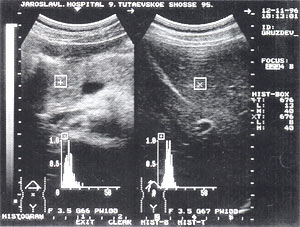
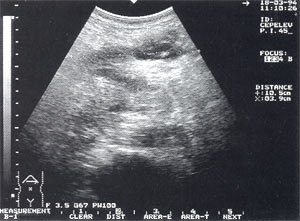
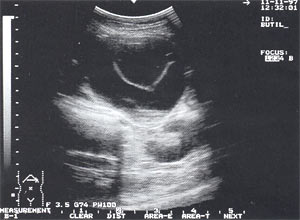
Рис. 2. Острый панкреатит, повышение эхогенности поджелудочной железы (по сравнению с эхогенностью печени).
Изменения в брюшной полости, являющиеся косвенными признаками острого панкреатита и относящиеся к его осложнениям:
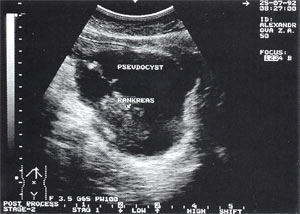
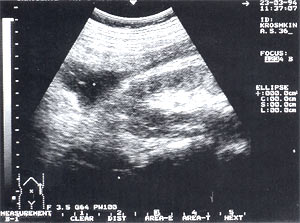
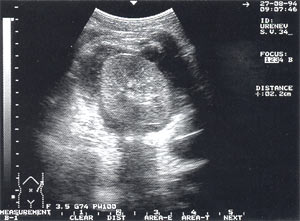
Рис. 3. Псевдокиста поджелудочной железы при остром панкреатите в виде анэхогенного образования с четкими контурами, однородной структурой, с наличием гиперэхогенных включений (детрит поджелудочной железы).
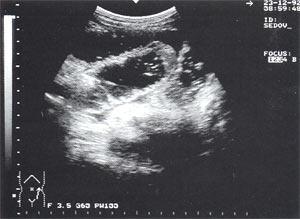
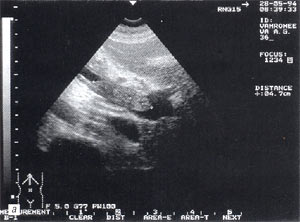
Рис. 4. Расширенные петли тонкого кишечника до 3,5 см, заполненные жидким содержимым на фоне свободной жидкости в брюшной полости.
Рис. 6. Инфильтрат в проекции большого сальника с анэхогенным включением до 4 см (абсцедирование).
Восходящий медиастенит, отмечаемый другими авторами, нами не наблюдался.
Разрывы псевдокист поджелудочной железы при ультразвуковой диагностике наблюдались у 2 больных (0,7%).
Кровоизлияние в псевдокисту поджелудочной железы с формированием организованной гематомы (рис. 9) отмечено у 1 пациента (0,35%).
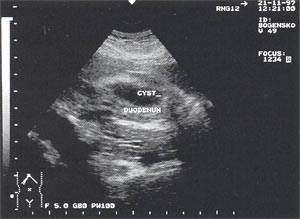
Рис. 10. Атипично расположенная псевдокиста поджелудочной железы (парадуоденально) в виде анэхогенного образования округлой формы с четкими контурами, однородной структурой, размером до 4,5 см, расположенного рядом с двенадцатиперстной кишкой.
Разрывы селезенки вследствие портальной гипертензии (нами не наблюдались).
Рис. 11. Левосторонний панкреатогенный паранефрит, визуализирующийся в виде жидкостного образования, окружающего почку со всех сторон. Поперечный срез.
Заключение
Проведенное исследование показывает, что ультразвуковая диагностика должна быть обязательным элементом диагностического алгоритма у больных острым панкреатитом. Для повышения диагностической ценности эхографии необходима определенная последовательность в выполнении ультразвукового исследования: детальный осмотр парапанкреатических тканей и самой железы; осмотр всех отделов брюшной полости на предмет свободной жидкости и инфильтратов; осмотр плевральных полостей и полости перикарда на наличие выпота; детальный осмотр внутри- и внепеченочных желчных протоков; прицельный осмотр сосудов системы воротной вены; исследование забрюшинного пространства; динамическое наблюдение (частота повторного УЗИ определяется степенью тяжести заболевания и вероятностью развития осложнений).
Для улучшения получаемых результатов УЗИ могут быть рекомендованы следующие технические приемы:
Литература
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Оментобурсит что это такое
Основной причиной летальных исходов при остром деструктивном панкреатите в настоящее время являются гнойно-септические осложнения. Будучи инфицирован гнойно – гнилостными микроорганизмами, некротический процесс склонен распространятся на отдаленные от своего источника отделы. Этому могут способствовать агрессивные свойства гноя, содержащего большое количество панкреатических ферментов и анатомические особенности забрюшинного пространства, допускающие сообщения между теми или иными его отделами. Развитие осложнений происходит, как правило, per continuitatem, путем расплавления брюшинного листка, отделяющего забрюшинно располагающуюся поджелудочную железу от свободной брюшной полости [1,2,5]. Исследование по лечению и применению хирургического вмешательства при гнойном оментобурсите является актуальной задачей.
Целью работы является рассмотрение проблемы диагностики и хирургической тактики при наиболее часто встречающемся гнойном осложнении деструктивного панкреатита – оментобурсите.
К сожалению, до сих пор не выработано четких единых рекомендаций относительно способов хирургического лечения гнойного оментобурсита (за исключением нескольких региональных стандартов)[6,7,8]. Практически ежегодно проблемы лечения осложнений деструктивного панкреатита обсуждаются на многочисленных конференциях и съездах, однако на настоящий момент летальность при инфицированном панкреонекрозе составляет до 70%[4,5,7]. Открытыми остаются вопросы относительно места малоинвазивных методик (пункционные методы и дренирование) в арсенале лечащего врача, сроки выполнения, показания и противопоказания к оперативным вмешательствам[4]. Проблема усугубляется тем, что рекомендуемые в литературных источниках современные методы инструментальной (МРТ, спиральная КТ, тонкоигольная пункция-аспирация под УЗ-контролем) и лабораторной (прокальцитониновый тест) диагностики практически недоступны на уровне хирургических отделений районных и небольших городских больниц.
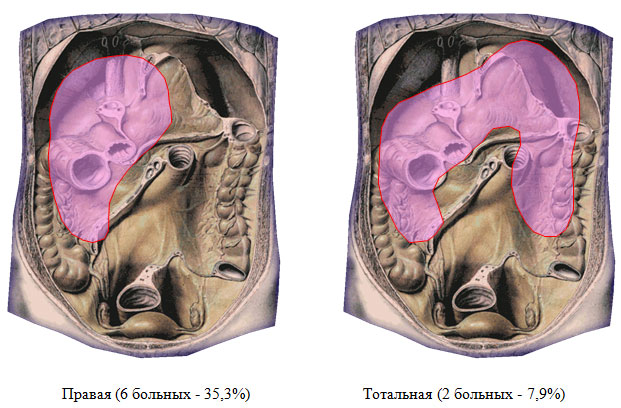
За период 2007-2011 гг. в хирургическом отделении ФГУЗ МСЧ №98 проведено лечение 37 больных деструктивным панкреатитом, в течение заболевания которых зарегистрированы гнойно-септические осложнения. При разборе хирургической анатомии присоединившихся осложнений выявлено следующее. Разрушение заднего листка брюшины над поджелудочной железой и проникновение гноя в сальниковую сумку вызывает гнойный оментобурсит (центральная локализация – 27 больных, 72,9%). Прорыв гноя через винслово отверстие приводит к образованию подпеченочного или правостороннего гнойника (6 пациентов – 16,3%), разрушение левых отделов mesocolon и желудочно-ободочной связки – к образованию левостороннего поддиафрагмального абсцесса (у 2 больных – 5,4%). Под тотальной локализацией имелось в виду абсцедирование обширных участков некроза парапанкреатической и параколярной клетчатки как по ходу восходящей, так и по ходу нисходящей ободочной кишки (2 человека – 5,4%). Области локализации панкреатогенных абсцессов приведены на рисунке 1. Проведен анализ историй болезни 27 пациентов, у которых течение деструктивного панкреатита осложнилось присоединением гнойного оментобурсита (в качестве единственного первичного гнойного очага).
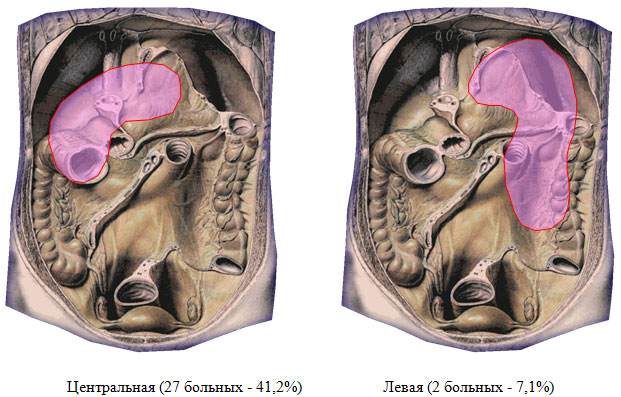
Рисунок 1. Локализация панкреатогенных абсцессов
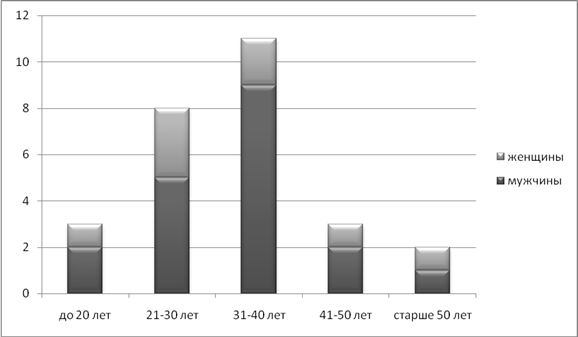
Возраст больных составил 17- 55 лет. Мужчин было 19 человек (70,4%), женщин – 8 (29,6%). Состав больных разделённых по возрастам приведён на рисунке 2.
Рисунок 2. Состав больных по полу и возрасту
Установление наличия гнойного осложнения базировалось на характерной клинической картине, данных инструментального исследования (УЗИ, КТ) и лабораторных тестах (определение активности панкреатических ферментов, прокальцитониновый тест) и являлось безусловным показанием к активной хирургической тактике.
Часть исследованных больных (26 человек) подверглись оперативному лечению, выполненному на 10-15 сутки от момента начала заболевания, 3 пациентам после предварительно выполненной компьютерной томографии было произведено эхоконтролируемое дренирование сальниковой сумки. Из числа больных последней группы у 2 человек манипуляция не дала положительного результата и они были оперированы традиционным способом через 3 суток после первичного дренирования. У всех больных операция выполнялась полуоткрытым способом, предусматривающим установку трубчатых дренажей вместе с тампоном Penrose. В послеоперационном периоде больным проводилась интенсивная инфузионно-трансфузионная, антибактериальная, антисекреторная, симптоматическая терапия.
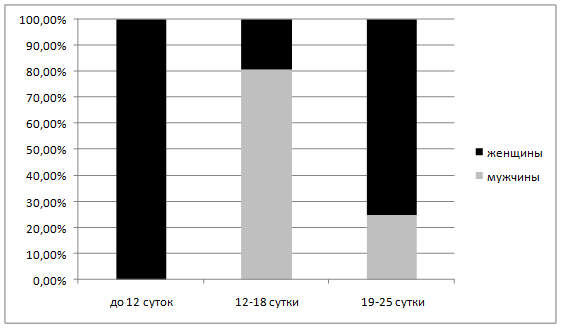
Присоединение при деструктивном панкреатите гнойно-септических осложнений является абсолютным показанием к оперативному вмешательству. Этот факт в настоящее время не вызывает сомнений, т.к. дальнейшее консервативное ведение больных с несанированными гнойными очагами бесперспективно и ведет к неблагоприятному исходу [4,9].
Рисунок 3. Сроки оперативных вмешательств у больных с гнойным оментобурситом.
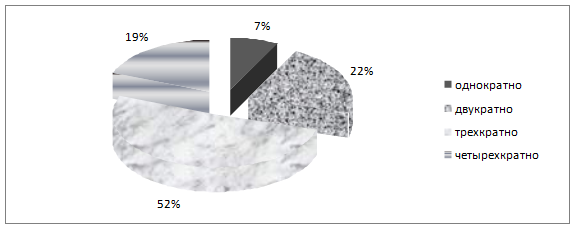
Полуоткрытый тип операций у больных с гнойным оментобурситом, завершающийся формированием оментобурсостомы предусматривает возможность многократных некр- и секвестрэктомий без риска подвергать больного повторной (пусть даже запрограммированной) лапаротомии, на что указывает большое количество авторов [3,4,5,7,9]. Однократная некрозосеквестрэктомия, как правило, не несет радикального характера и возникает необходимость в повторных санациях сальниковой сумки. В исследуемой группе однократная санация проведена у 2 (7%) человек, двухкратно – у 6 (22%), трехкратно – у 14(52%), четырехкратно – у 5 (19%) пациентов (рисунок 4).
Рисунок 4. Кратность некрсеквестрэктомий у больных с гнойным оментобурситом
Отдельно следует выделить группу из 3 больных, у которых была предпринята попытка дренирования жидкостного образования под УЗ-контролем. Во всех трех случаях попытка увенчалась успехом и сальниковая сумка была санирована через установленные дренажи. Однако в последующем течение заболевания у 2 пациентов, сопровождающееся длительным выделением гнойного экссудата (более 7-10 дней) и его объемом (более 100 мл/сут), несмотря на ежедневные санации растворами антисептиков и консервативную терапию, заставило заподозрить наличие секвестрированных очагов некроза, поддерживающих воспалительный процесс. Это было установлено при повторной КТ и больные были оперированы стандартным полуоткрытым способом.
В ходе проведённых исследований получены следующие результаты:
Работа выполнена в рамках Федеральной целевой программы ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009-2013 годы.
Рецензенты:
Сарвилина Ирина Владиславовна, д.м.н., ген. директор медицинского центра «Новомедицина», ведущий научный сотрудник ЗАО НПО «Европа-Биофарм», г. Ростов-на-Дону.
Масляков Юрий Степанович, д.м.н., профессор, зав. кафедрой «Фармокология и клиническая формакология» ГБОУ ВПО «РостГМУ» Минздрава России, г. Ростов-на-Дону.
Протокол лечения пациентов с острым панкреатитом
Протокол разработан на основе рекомендаций Российского общества хирургов и приказа Департамента здравоохранения города Москвы № 320 (2011г.)
Классификация острого панкреатита, формулировка диагноза.
1. Острый алкогольно-алиментарный панкреатит.
2. Острый билиарный панкреатит (холелитиаз, парафатериальный дивертикул дивертикул, папиллит, описторхоз ).
3. Острый травматический панкреатит (вследствие травмы поджелудочной железы, в том числе операционной или после ЭРХПГ).
4. Другие этиологические формы (аутоиммунные процессы, сосудистая недостаточность, васкулиты, лекарственные, инфекционные заболевания), аллергические, дисгормональные процессы при беременности и менопаузе, заболевания близлежащих органов.
1. Острый панкреатит лёгкой степени. Панкреонекроз при данной форме острого панкреатита не образуется (отёчный панкреатит) и органная недостаточность не развивается.
2. Острый панкреатит тяжёлой степени. Характеризуется наличием органной и полиорганной недостаточности, перипанкреатического инфильтрата, формированием псевдокист, развитием инфицированного панкреонекроза (гнойно-некротического парапанкреатита).
Диагностика острого панкреатита.
Диагностическая программа включает в себя: клиническую, лабораторную и инструментальную верификацию диагноза острого панкреатита; стратификацию пациентов на группы в зависимости от тяжести заболевания; построение развернутого клинического диагноза.
Верификация диагноза острого панкреатита включает в себя: физикальное исследование – оценка клинико-анамнестической картины острого панкреатита; лабораторные исследования – общеклинический анализ крови, биохимический анализ крови (в т.ч. а-амилаза, липаза, билирубин, АлАТ, АсАТ, ЩФ, мочевина, креатинин, электролиты, глюкоза), общеклинический анализ мочи, коагулограмма, группа крови, резус-фактор; обзорная рентгенограмма брюшной полости (увеличение диаметра петель тонкой кишки, уровни жидкости), рентгенография грудной клетки (гидроторакс, дисковидные ателектазы, высокое стояние купола диафрагмы, гипергидратация паренхимы, картина ОРДС), ЭКГ; УЗИ брюшной полости – оценка наличия свободной жидкости, оценка состояния поджелудочной железы (размеры, структура, секвестры, жидкостные включения), оценка состояния билиарного тракта (гипертензия, конкременты), оценка перистальтики кишечника.
Пациентам с предположительным клиническим диагнозом острого панкреатита показано выполнение ЭГДС (дифференциальный диагноз с язвенным поражением гастродуоденальной зоны, осмотр БДС).
Стратификация пациентов по степени тяжести острого панкреатита по следующим критериям:
1. Тяжелый панкреатит (более одного из критериев):
Пациенты с тяжелым панкреатитом госпитализируются в отделение хирургической реанимации.
Пациенты с панкреатитом легкого течения госпитализируются в хирургическое отделение.
Лечение пациентов с острым панкреатитом легкого течения.
Базисный лечебный комплекс:
В динамике ежедневно оцениваются: критерии ССВР, а-амилаза. Требования к результатам лечения: купирование болевого синдрома, клинико-лабораторное подтверждение разрешения активного воспалительного процесса.
Отсутствие эффекта от проводимой анальгетической и спазмолитической терапии в течение 12-48 часов, быстро прогрессирующая желтуха, отсутствие желчи в ДПК при ЭГДС, признаки билиарной гипертензии по данным УЗИ свидетельствуют о стеноза терминального отдела холедоха (вклиненный конкремент БДС, папиллит). В этом случае показано проведение ЭПСТ. При остром панкреатите ЭПСТ производится без ЭРХПГ!
Мониторинг общесоматического и локального статуса пациентов с тяжелым острым панкреатитом:
Лечебная тактика у пациентов с острым панкреатитом тяжелого течения в фазу панкреатогенной токсемии.
Основным видом лечения острого панкреатита в фазе токсемии является комплексная интенсивная консервативная терапия.
Базисная терапия острого панкреатита дополняется следующими компонентами:
— интенсивное ингибирование секреции поджелудочной железы (октреотид 300 мкг x 3 раза в сутки подкожно или 1000 мкг в сутки непрерывной инфузией) до нормализации показателей а-амилазы и липазы;
— продленная эпидуральная анестезия;
— доза инфузионных растворов должна быть не менее 40-60 мл/кг массы тела больного в сутки; высокообъемная инфузионная терапия включает в себя сбалансированные кристаллоидные растворы и коллоидные растворы (в сочетании кристаллоидов и коллоидов 2:1);
— реологически активная терапия: коллоиды в сочетании с антиагрегантами, НФГ (15-20 тыс. ед. в сутки) или НМГ; введение антиоксидантов;
— экстракорпоральная детоксикация: продленная вено-венозная гемодиафильтрация и серийный плазмаферез;
— установка ниппельного зонда энтерального питания за дуодено-еюнальный переход с одновременной установкой назо-гастрального зонда для желудочной декомпрессии; введение в первые 24-48 часов в тонкую кишку электролитных растворов (1 – 2 литра/сут); последующее энтеральное питание олигомерными и полимерными питательными смесями;
— обеспечение смешанной парентерально-энтеральной нутритивной поддержки с калоражем не менее 2000 ккал в сутки.
Хирургическая тактика:
Оперативные вмешательства лапаротомным доступом в фазу ферментной токсемии противопоказаны. По показаниям применяются малоинвазивные вмешательства – чрезкожные пункции и дренирования, лапароскопия, ЭПСТ.
Чрескожная пункция и дренирование острых жидкостных скоплений под контролем УЗИ позволяет снизить уровень эндогенной интоксикации.
Пункции подлежат очаги острых жидкостных скоплений, располагающиеся в сальниковой сумке, забрюшинной клетчатке, и в случаях, когда лапароскопическое дренирование острых жидкостных скоплений в брюшной полости невозможно (тяжесть состояния больного, больной перенес раннее несколько операций на брюшной полости, гигантская вентральная грыжа).
Экстренная декомпрессия желчевыводящих путей у больных острым билиарным панкреатитом показана при: отсутствии эффекта от проводимой консервативной терапии в течение 6-12 часов; вклиненном конкременте БДС; нарастании явлений механической желтухи; прогрессировании явлений острого холецистита и/или холангита.
При диагностированном резидуальном или рецидивном холедохолитиазе, холедохолитиазе на фоне хронического калькулезного холецистита, остром обтурационном холангите, папиллите или папиллостенозе показано проведение ЭПСТ без ЭРХПГ! При невозможности проведения ЭПСТ показана чрескожная чреспеченочная микрохолецистостомия под контролем УЗИ. При невозможности добиться адекватной декомпрессии из вышеописанных доступов показана чрескожная чреспеченочная холангиостомия. В случае вклинения конкремента в области большого дуоденального сосочка предпочтение отдается эндоскопической папиллогомии.
Показания к лапароскопии:
— клиническая картина перитонита с наличием УЗ-признаков свободной жидкости в брюшной полости;
— необходимость проведения дифференциальной диагностики с другими острыми заболеваниями органов брюшной полости.
Лечебная тактика у пациентов с тяжелым панкреатитом в фазу асептической секвестрации.
Клинико-морфологической формой острого панкреатита в фазе асептической секвестрации является постнекротическая псевдокиста поджелудочной железы, срок формирования которой составляет от 4 недель и в среднем до 6 месяцев.
Исходы острого панкреатита в фазу асептической секвестрации:
4) Инфицирование зон панкреатогенной деструкции (развитие гнойных осложнений).
Диагностические критерии фазы асептической секвестрации:
— уменьшение степени выраженности ССВР, отсутствие признаков инфекционного процесса;
— УЗ-признаки и КТ-признаки асептической деструкции в очаге поражения (сохраняющееся увеличение размеров поджелудочной железы, нечеткость ее контуров и появление жидкости в парапанкреатической и забрюшинной клетчатке c последующим формированием псевдокист, визуализация секвестров в ткани поджелудочной железы и в парапанкреатической клетчатке).
Лечение в фазу асептической секвестрации.
Хирургическая тактика у пациентов с острым панкреатитом в период асептических деструктивных осложнений.
Показание к оперативным вмешательствам – наличие отграниченных парапанкреатических жидкостных скоплений (с секвестрами или без таковых).
Приоритетным является выполнение малоинвазывных чрезкожных вмешательств под УЗ-контролем или КТ-контролем.
Чрезкожные пунции под УЗ-контролем показаны при наличии жидкостных образований объемом не более 100 мл. Систематические пункции могут послужить окончательным методом хирургической помощи или позволить отложить выполнение радикальной операции.
Чрезкожное дренирование под УЗ-контролем проводится при наличии жидкостных скоплений объемом более 100 мл. Дренирование кисты предусматривает аспирационно-промывную санацию полости кисты и оценку адекватности дренирования с помощью динамической фистулографии.
Оперативные вмешательства лапаротомическим и (или) люмботомическим доступом проводятся при наличии технических ограничений к безопасному выполнению пункционных вмешательств (расположение на предполагаемой траектории вмешательства ободочной кишки, селезенки, крупных сосудов, плеврального синуса); при преобладании в жидкостном скоплении или острой псевдокисте тканевого компонента (секвестров).
При очаговом процессе следует использовать мини-лапаротомию (параректальную, трансректальную, косую в подреберье) или мини-люмботомию. При распространенном процессе следует использовать широкую срединную лапаротомию, широкую люмботомию или их сочетание.
В условиях завершенной секвестрации и полной некросеквестрэктомии операция должна завершатся «закрытым» дренированием образовавшейся полости 2-х просветными дренажами, по числу отрогов полости, которые выводятся на брюшную стенку вне операционной раны. Рана ушивается наглухо. В послеоперационном периоде проводится аспирационно-промывное лечение до облитерации полости.
При незавершенной секвестрации и неполной некрсеквестрэктомии операция должна завершатся «открытым» дренированием 2-х просветными дренажами по числу отрогов полости, выводимыми вне раны через контрапертуры и введением тампонов в образовавшуюся полость через операционную рану. Рана частично ушивается и формируется бурсооментостома или люмбостома для доступа к очагу деструкции при последующих программных санациях. По дренажам проводится аспирационно-промывное лечение, перевязки с дополнительной некрсеквестрэктомией и сменой тампонов до очищения полости с последующим наложением вторичных швов на рану и переходом на закрытое дренирование.
Лечебная тактика у пациентов с тяжелым панкреатитом в фазу гнойно-септических осложнений.
Клинико-морфологическими проявлениями острого панкреатита в фазу гнойно-септических осложнений являются:
Диагностические критерии фазы гнойно-септических осложнений:
1. Клинико-лабораторные проявления инфекционного процесса: прогрессирование клинико-лабораторных показателей ССВР на 3 неделе заболевания; высокие показатели маркеров острого воспаления (С-реактивного белка – более 120 г/л и прокальцитонина – более 2 нг/мл); лимфопения, увеличение СОЭ, повышение концентрации фибриногена; ухудшение состояния больного по интегральным оценочным системам.
2. Инструментальные критерии нагноения: КТ-признаки (нарастание в процессе наблюдения жидкостных образований, в очаге панкреатогенной деструкции и/или наличие пузырьков газа) и/или положительные результаты бактериоскопии, полученные при тонкоигольной пункции.
Хирургическая тактика у пациентов с острым панкреатитом в фазу гнойно-септических осложнений.
При развитии гнойных осложнений показано срочное хирургическое вмешательство.
Малоинвазивные пункционные вмешательства (пункция и дренирование) показаны при наличии четко отграниченных гнойных скоплений (жидкостные скопления, панкреатический абсцесс, инфицированная псевдокиста) без выраженного тканевого компонента (секвестров). Оптимальным следует считать установку в полость гнойника двух дренажей с последующей установкой промывной системы.
Оперативные вмешательства лапаротомным и люмботомическим доступом показаны в случаях значительной распространенности процесса в забрюшинной клетчатке или при отграниченном процессе с наличием в полости гнойника крупных некротических фрагментов. Основным методом санации гнойно-некротических очагов является некрсеквестрэктомия, которая может быть как одномоментной, так и многоэтапной.
Оптимальным доступом является внебрюшинный, в виде люмботомии с продлением разреза на брюшную стенку по направлению к прямой мышце живота, что позволяет при необходимости, дополнить этот доступ лапаротомией.
Способ завершения операции зависит от адекватности некрсеквестрэктомии. При полном удалении некротических тканей возможно «закрытое» дренирование двухпросветными дренажами по числу отрогов полости с выведением дренажей через контрапертуры на брюшной стенке. Через дренажи в послеоперационном периоде проводится аспирационно-промывная санация.
При неполном удалении некротических тканей следует применять «открытое» дренирование двухпросветными дренажами по числу отрогов полости, в сочетании с тампонированием полости через операционную рану и оставлением доступа для последующих программных ревизий и некрэктомий в виде оментобурсостомы и (или) люмбостомы. Через дренажи в послеоперационном периоде проводится аспирационно-промывная санация.
Контроль за адекватностью дренирования и состоянием (размерами) дренированных полостей должен проводиться с помощью фистулографии, УЗИ и КТ каждые 7 суток. Неэффективность дренирования (по клинико-инструменальным данным) или появление новых гнойных очагов служит показанием к повторной операции с дополнительной некрэктомией и дренированием.
При развитии аррозивного кровотечения в очаге гнойной деструкции следует произвести ревизию зоны кровотечения, удалить секвестры, прошить место кровотечения (временный гемостаз) и выполнить перевязку сосудов на протяжении вне гнойного очага (окончательный гемостаз). Накладывать швы на стенку сосуда в зоне дефекта в гнойной запрещено. При невозможности лигирования сосудов вне гнойного очага показана дистальная резекция поджелудочной железы и спленэктомия.
Антибактериальная терапия при остром панкреатите.
• Антибиотикопрофилактика не показана у пациентов с тяжелым острым панкреатитом в фазе ферментной токсемии.
• У пациентов в фазе гнойно-септических осложнений эмпирической терапией считается:
Пиперациллин-тазобактам 4.5 г в/в каждые 6 часов
Цефепим 1 г в/в каждые 8 часов ПЛЮС метронидазол 500 мг в/в каждые 8 часов
Ципрофлоксацин 400 мг в/в каждые 12 часов ПЛЮС метронидазол 500 мг в/в каждые 8 часов
Проникновение селективных антибиотиков в поджелудочную железу.
Хорошее (>40%): фторхинолоны, карбапенемы, цефтазидим, цефепим, метронидазол, пиперациллин-тазобактам