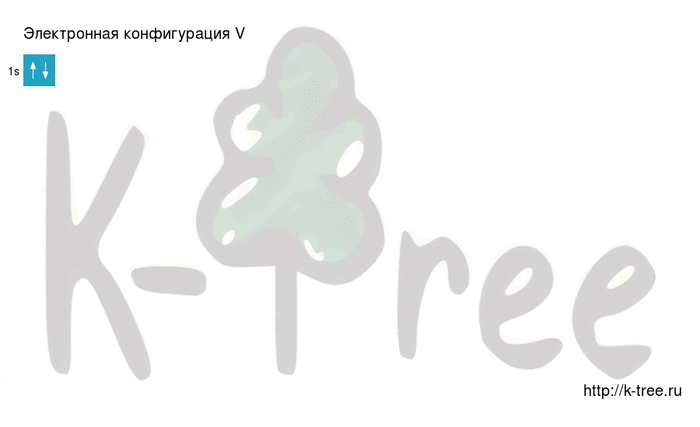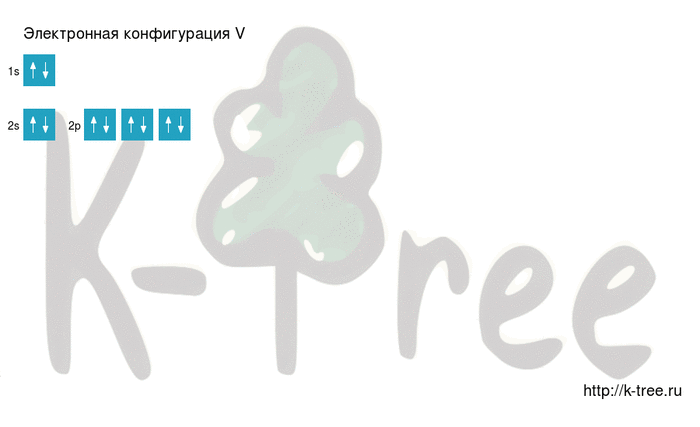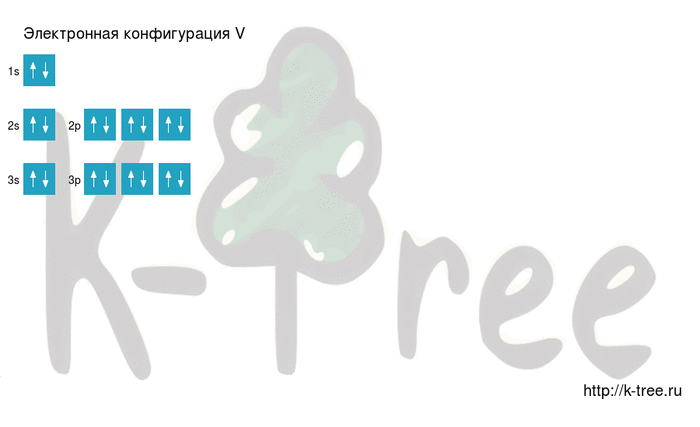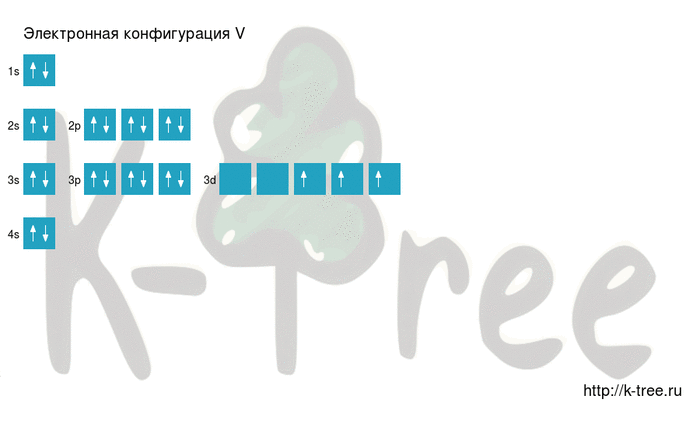Валентность ванадия
Валентность ванадия.
Валентность ванадия:
Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
| Валентность ванадия в соединениях | |
| II | VO |
| III | V2O3, VF3, VCl3 |
| IV | VO2, VCl4 |
| V | V2O5, VF5 |
Таблица валентности.
В таблице валентности приведены значения валентности элементов периодической таблицы Менделеева. Что такое валентность?
Точками здесь обозначаются неподеленные пары электронов, однако в структурных формулах их отмечают не каждый раз.
В химии принято, что валентность химических элементов можно узнать по группе (колонке) в таблице Менделеева. В действительности не всегда валентность элемента соответствует номеру группы, но в большинстве случаев определенная валентность по такому методу даст правильный результат часто элементы, в зависимости от разных факторов, имеют не одну валентность. Чтобы проще было понимать и не путаться, ниже приведена таблица валентностей всех элементов периодической таблицы.
Цифра положительной валентности элемента соответствует количеству отданных атомом электронов, а отрицательной валентности – количеству электронов, которые атом должен забрать себе для завершения внешнего энергетического уровня.
Значение, приведенное в скобках таблицы валентности, перечисляет менее распространенные валентности. Если у элемента указана только одна цифра, значит он может иметь только одну валентность.
Таблица валентности химических элементов.
Порядковый номер химического элемента, он же: атомный номер, он же: зарядовое число атомного ядра, он же: атомное число
Русское / Английское наименование
Валентность ванадия
Общие сведения о валентности ванадия
Валентность ванадия в соединениях
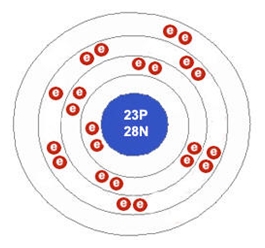
Ванадий находится в четвертом периоде в VB группе Периодической таблицы Д.И. Менделеева. Порядковый номер равен 23. В ядре атома ванадия содержится 23 протона и 27 нейтронов (массовое число равно 50). В атоме ванадия есть четыре энергетических уровня, на которых находятся 23 электрона (рис. 1).
Рис. 1. Строения атома ванадия.
Электронная формула атома ванадия в основном состоянии имеет следующий вид:
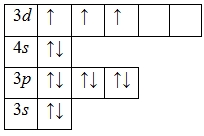
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие трех неспаренных электронов свидетельствует о том, что ванадий в своих соединениях может проявлять валентность III (V III 2O3, V III F3, V III Cl3).
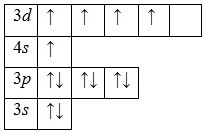
Атом ванадия способен переходить в возбужденное состояние: электроны 4s-подуровня распариваются и один из них занимает вакантную орбиталь 3d-подуровня:
Наличие пяти неспаренных электронов свидетельствует о том, что ванадий также проявляет валентность V в своих соединениях (V V 2O5, V V F5).
Известно, что у ванадия есть валентности II(V II O) и IV (V IV O2, V IV Cl4).
Примеры решения задач
| Задание | Подберите коэффициенты в схемах следующих окислительно-восстановительных реакций. Укажите, как изменяется степень окисления ванадия. |
В первой реакции степень окисления ванадия изменяется с 0 до +5.Во втором – с +5 до +4.
| Задание | Напишите формулы всех известных оксидов ванадия. Покажите, как изменяются кислотно-основные свойства этих оксидов с ростом степени окисления ванадия. |
| Ответ | Известны оксиды ванадия (II) (VO), III (V2O3), IV (VO2) и V (V2O5). |
Для оксида ванадия (II) характерно проявление сильных основных свойств, в реакции он выступает в роли сильного восстановителя:
Оксид ванадия (III) проявляет основные свойства и также является восстановителем:
Оксид ванадия (IV) проявляет амфотерные свойства в ОВР практически не участвует.
Оксид ванадия (V) проявляет амфотерные свойства с преобладанием кислотных, в реакциях является сильным окислителем:
Ванадий V
Ванадий в таблице менделеева занимает 23 место, в 4 периоде.
| Символ | V |
| Номер | 23 |
| Атомный вес | 50.9415000 |
| Латинское название | Vanadium |
| Русское название | Ванадий |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема ванадия
V: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 3
Порядок заполнения оболочек атома ванадия (V) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Ванадий имеет 23 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
3 электрона на 3d-подуровне
Степень окисления ванадия
Ионы ванадия
Валентность V
Атомы ванадия в соединениях проявляют валентность V, IV, III, II, I.
Валентность ванадия характеризует способность атома V к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа V
Квантовые числа определяются последним электроном в конфигурации, для атома V эти числа имеют значение N = 3, L = 2, Ml = 0, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Металлы V группы побочной подгруппы (V, Nb, Ta)
Много ли известно химических элементов, которые были открыты дважды? И уж совсем удивительно, что все три элемента подгруппы — ванадий, ниобий и тантал — носят имена мифологических персонажей.
В 1801 г. мексиканский геолог и минералог Андрес Мануэль дель Рио ( 1765— 1849) нашел в свинцовой руде примесь неизвестного элемента. Он назвал его эритронием (от греч. «эритрос» — «красный»). Вскоре учёный пришёл к ошибочному выводу, что обнаруженное им вещество не содержит новый элемент, а является смесью железа и хрома, и отказался от своего открытия.

В 1830 г. шведский химик Нильс Габриэль Сефстрём (1787—1845) из отходов производства железа выделил соединения нового элемента, соли которого обладали красивой окраской. В честь древнескандинавской богини красоты Ванадис учёный назвал элемент ванадием. И только в 1869 г. английский химик Генри Энфилд Роско взаимодействием хлорида ванадия(III) с водородом получил металл, исследовал его свойства и убедился в том, что ванадий идентичен эритронию дель Рио.
Похожая история произошла с ниобием. В начале ХIХ в. почти одновременно были открыты и описаны два новых элемента: англичанином Чарльзом Хатчетом (1765—1847) — колумбий, а шведом Андерсом Экебергом (1767— 1813) — тантал. Свойства этих элементов оказались столь схожи, что их приняли за один и стали называть танталом. А в 1844 г. немецкий химик Генрих Розе (1795— 1864), исследуя минералы, найденные в Баварии, доказал, что существуют два разных элемента с очень похожими свойствами. Чтобы подчеркнуть их «родство», он назвал второй элемент ниобием в честь Ниобы — дочери героя греческой мифологии Тантала. Интересно, что в США ниобий долгое время продолжали называть колумбием Cb.
Ванадий (Vanadium)
Ванадий — твердый и тугоплавкий металл (tпл = 1915 о С), химически довольно инертный. Его можно растворить лишь в горячей концентрированной серной или азотной кислоте, царской водке. Именно инертность обеспечила этому металлу широкое применение. Сплав ванадия и никеля, обладающий механическими свойствами стали, многократно превосходит её по химической стойкости. Поэтому его используют для изготовления деталей механизмов, работающих в агрессивных средах.
Еще большее применение находит феррованадий – сплав ванадия с железом, содержащий до 30% ванадия. Он сравнительно дешевый и может легко заменять сталь при создании коррозионно-стойких изделий даже небольшое (до 1 %) содержание ванадия в стали повышает её упругость примерно в два раза!
Химически чистый ванадий получают при восстановлении оксида кальцием:
Ванадий проявляет большое разнообразие степеней окисления: от +2 до +5. Высший оксид ванадия V2O5 — вещество жёлто-оранжевого цвета. Соответствующая ему кислота существует только в растворах. Он реагирует с горячими щелочами: V2О5 + 2KOH = 2KVO3 + H2O, при этом образуются соли ванадиевой кислоты ванадаты. Восстановлением V2О5 получают низшие оксиды ванадия:
Оксид VО2 проявляет и кислотные, и основные свойства. При реакции с кислотами образуются соли катиона ванадила VО 2+ :VO2 + H2SO4 = VOSO4 + H2O. Их окраска напоминает цвет медного купороса.
Ниобий(Niobium) и тантал(Tantalum)
Ниобий и тантал отличаются редкостной химической инертностью: для растворения этих металлов требуется смесь плавиковой и концентрированной азотной кислот. Любопытно, что подобный процесс аналогичен растворению циркония или гафния: азотная кислота окисляет металл, а плавиковая способствует образованию устойчивых фторидных комплексов:
Устойчивость ниобия и тантала по отношению к щелочным средам не имеет аналогов среди других металлов. Температура плавления тантала около 3000 o C; танталовые тигли легко выдерживают даже металлотермические реакции, в которых выделяется столько теплоты, что плавятся оксиды металлов!
Химически чистые металлы используют в качестве добавок к специальным сортам сталей. В частности, ниобий, добавленный в сталь, предотвращает интеркристаллическую коррозию, которая в первую очередь поражает сварочные швы. Ниобиевые нити используют в медицине для сшивания повреждённых сухожилий и кровеносных сосудов.

Для ниобия и тантала наиболее характерна степень окисления +5. Высшие оксиды Nb2О5 и Та2О5 — жаропрочные и химически инертные вещества, однако при высоких температурах (до 1000 о С) они реагируют с расплавленными щелочами, образуя соли – ниобаты (например, KNbO3) и танталаты (KTaO3).
Среди соединений ниобия низших степеней окисления наибольший интерес представляют германид ниобия Nb3Ge – вещество, сохраняющее сверхпроводимость вплоть до 24,5 K, и карбид ниобия NbC – термостойкое и пластичное вещество золотистого цвета, применяемое для создания прочных и в то же время красивых защитных покрытий.
*на изображении записи фотография минерала ванадита