Валентность бора
Общие сведения о валентности бора
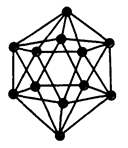
Бор имеет более 10 аллотропных модификаций (видоизменений) (явление аллотропии связано с существованием одного химического элемента в виде нескольких простых веществ – аллотропных модификаций). Атомы бора объединены в группировки B12, имеющие форму икосаэдра – двадцатигранника (рис. 1).
Рис. 1. Икосаэдрическая группировка атомов бора B12.
Расположение икосаэдров B12 относительно друг друга в кристалле показано ниже:
Кристаллы бора темно-серого цвета, тугоплавки (температура плавления 2075 o С, температура кипения 3700 o С), диамагнитны, обладают полупроводниковыми свойствами (рис. 2).
Рис. 2. Бор. Внешний вид.
Валентность бора в соединениях
Бор — пятый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится во втором периоде во IIIA группе. В ядре атома бора содержится 5 протонов и 5 нейтронов (массовое число равно 10). В атоме бора есть два энергетических уровня, на которых находятся 5 электронов.
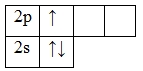
Электронная формула атома борав основном состоянии имеет следующий вид:
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
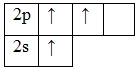
В основном состоянии в атоме бора есть 2 спаренных и 1 неспаренный электрон, а также 2 вакантные орбитали 2p-подуровня. За счет их наличия электроны 2s-подуровня могут распариваться и один из них совершает переход и занимает одну из свободных 2p орбиталей, т.е. для бора характерно возбужденное состояние.
Наличие трех неспаренных электронов свидетельствует о том, что бор в своих соединениях (B III F3, B III 2O3, KB III F4, B III Br3и др.) проявляет валентность равную III.Этот факт также можно подтвердить тем, что высшая валентность элементов определяется по номеру группы, в которой он находится в Периодической таблице. Т.к. бор – элемент III группы, то его высшая валентность равна III. Валентность бериллия постоянна.
Примеры решения задач
| Задание | Определите валентность элементов в следующих соединениях: а) Mg3P2; б) Al2S3; в) Na2O; г) AgCl; д) FeCl3. |
| Решение | Определение валентностей элементов в химическом соединении стоит начинать с указания валентности известного элемента. В варианте «а» — это магний, поскольку элементы IIA группы имеют постоянное значение валентности, равное номеру группы, т.е. II. Запишем формулу вещества и укажем римскими цифрами валентность известного элемента: |
Находим наименьшее кратное чисел единиц валентностей. Для этого умножаем значение валентности магния на количество атомов данного элемента в соединении (3):
Чтобы определить валентность фосфора поделим наименьшее кратное чисел единиц валентностей на количество атомов фосфора в соединении (2):
Это означает, что валентность фосфора равна III:
Аналогичным образом определяем валентности элементов в других соединениях: б) Al III 2S II 3; в) Na I 2O II ; г) Ag I Cl I ; д) Fe III Cl I 3.
| Задание | Определите валентность элементов в следующих соединениях: а) Al4C3; б) Cl2O5; в) HBr; г) WO3; д) BaH2. |
| Решение | Определение валентностей элементов в химическом соединении стоит начинать с указания валентности известного элемента. В варианте «а» — это алюминий, поскольку для него постоянное значение валентности, равное номеру группы, в которой он расположен, т.е. III. Запишем формулу вещества и укажем римскими цифрами валентность известного элемента: |
Находим наименьшее кратное чисел единиц валентностей. Для этого умножаем значение валентности алюминия на количество атомов данного элемента в соединении (4):
Чтобы определить валентность углерода поделим наименьшее кратное чисел единиц валентностей на количество атомов углерода в соединении (3):
Это означает, что валентность углерода равна IV:
Аналогичным образом определяем валентности элементов в других соединениях: б) Cl V 2O II 5; в) H I Br I ; г) W VI O II 3; д) Ba II H I 2.
Бор B
Бор в таблице менделеева занимает 5 место, в 2 периоде.
| Символ | B |
| Номер | 5 |
| Атомный вес | 10.8060000 |
| Латинское название | Borum |
| Русское название | Бор |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема бора
Порядок заполнения оболочек атома бора (B) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Бор имеет 5 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
1 электрон на 2p-подуровне
Степень окисления бора
Атомы бора в соединениях имеют степени окисления 3, 2, 1.
Ионы бора
Валентность B
Атомы бора в соединениях проявляют валентность III, II, I.
Валентность бора характеризует способность атома B к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа B
Видео заполнения электронной конфигурации (gif):
Результат:
Соединения бора
| Тип | Формула | Название |
|---|---|---|
| Кислота | H3BO3 | Борная кислота |
| Оксид | B2O3 | Оксид бора |
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Какая валентность у бора
Среди элементов IIIa группы один лишь бор относится к неметаллам. Представляет собой аморфное кристаллическое вещество красного или темного цвета, может быть бесцветным.
Общая характеристика элементов IIIa группы
От B к Tl (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Природные соединения
Получение
Бор получают путем пиролиза бороводородов, методом металлотермии (вытеснением активным металлом) и термическим разложением бромида бора в присутствии катализатора
BBr3 + H2 → (вольфрам, t = 1000-1200 С°) B + HBr
Химические свойства
Необходимо заметить, что бор довольно инертный неметалл. При комнатной температуре без нагревания он реагирует только со фтором:
При нагревании бор реагирует с другими галогенами, азотом, фосфором, углеродом и кислородом.
При сильном нагревании бор способен восстановить кремний из его оксида:
Ионы бора окрашивают пламя в оттенки зеленого цвета.
Оксид и гидроксид бора
Оксид и гидроксид бора (борная кислота) проявляют кислотные свойства.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Таблица валентности химических элементов
Таблица валентности химических элементов.
Таблица валентности химических элементов:
Ниже приводится таблица валентности химических элементов с примерами соединений.
Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Таблица валентности химических элементов:
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
Словари
Нахождение в природе
В промышленности из природных боратов сплавлением с содой получают буру. При обработке природных минералов бора серной кислотой образуется борная кислота. Из борной кислоты H3BO3 прокаливанием получают оксид B2O3, а затем его или буру восстанавливают активными металлами (магнием или натрием) до свободного бора:
При этом в виде серого порошка образуется аморфный бор. Кристаллический бор высокой чистоты можно получить перекристаллизацией, но в промышленности его чаще получают электролизом расплавленных фтороборатов или термическим разложением паров бромида бора BBr3 на раскаленной до 1000-1500 °C танталовой проволоке в присутствии водорода:
Возможно также использование крекинга бороводородов:
Физические и химические свойства
По многим физическим и химическим свойствам неметалл бор напоминает элемент группы IVA неметалл кремний. (см. КРЕМНИЙ)
Химический бор довольно инертен и при комнатной температуре взаимодействует только со фтором:
С водородом бор напрямую не взаимодействует, хотя известно довольно большое число бороводородов (боранов) (см. БОРОВОДОРОДЫ) различного состава, получаемых при обработке боридов щелочных или щелочноземельных металлов с кислотой:
При сильном нагревании бор проявляет восстановительные свойства. Он способен, например, восстановить кремний или фосфор из их оксидов:
Данное свойство бора можно объяснить очень высокой прочностью химических связей в оксиде бора B2O3.
При отсутствии окислителей бор устойчив к действию растворов щелочей. В горячей азотной, серной кислотах и в царской водке бор растворяется с образованием борной кислоты H3BO3.
Важно, что при этой ядерной реакции возникают только стабильные ядра. Поэтому чистый бор и особенно его сплавы применяют в виде поглощающих нейтроны материалов при изготовлении для ядерных реакторов регулирующих стержней, замедляющих или прекращающих реакции деления.
В медицине как антисептические средства находят применение бура и борная кислота (в виде водно-спиртовых растворов). В быту буру или борную кислоту используют для уничтожения бытовых насекомых, в частности, тараканов (бура, попадая в органы пищеварения таракана, кристаллизуется, и образовавшиеся острые игольчатые кристаллы разрушают ткани этих органов).