Биосинтез пуриновых нуклеотидов
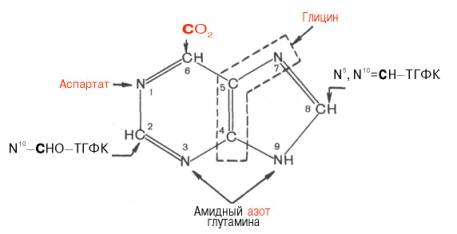
Пуриновые основания, образующиеся в процессе переваривания нуклеиновых кислот в кишечнике, в дальнейшем практически не используются, поэтому их синтез осуществляется из низкомолекулярных предшественников, продуктов обмена углеводов и белков. Впервые работами Дж. Бьюкенена, Дж. Гринберга экспериментально доказано включение ряда меченых атомов, в частности 15 N- и 14 С-глицина, 15 N-аспартата, 15 N-глутамина и др., в пуриновое кольцо мочевой кислоты. Скармливая птицам эти и другие меченые соединения, Дж. Бьюкенен анализировал места включения метки в пуриновое кольцо; полученные данные были в дальнейшем уточнены и подтверждены рядом других исследователей. Результаты этих исследований можно представить в виде схемы:
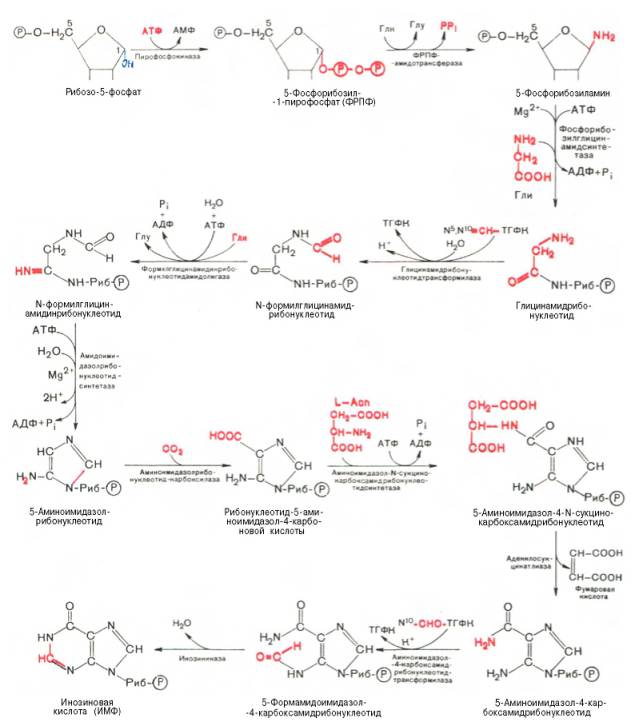
В настоящее время благодаря исследованиям Дж. Бьюкенена, Дж. Гринберга, А. Корнберга и сотр. полностью расшифрована последовательность включения перечисленных веществ в пуриновое кольцо, установлена природа всех промежуточных соединений и ферментных систем, катализирующих химические реакции синтеза. Интересным оказался факт почти полного совпадения путей синтеза пуриновых оснований в печени животных и у микроорганизмов, в частности у Е. coli и Neurospora crassa. Следует, однако, отметить, что конечным результатом синтеза оказалось не свободное пуриновое основание, а рибонуклеотид – инозиновая кислота (ИМФ), из которой далее синтезируются АМФ и ГМФ. На схеме представлена последовательность всех 11 химических реакций этого синтеза с указанием ферментных систем, коферментов, источников энергии и других известных к настоящему времени кофакторов (см. с. 472).
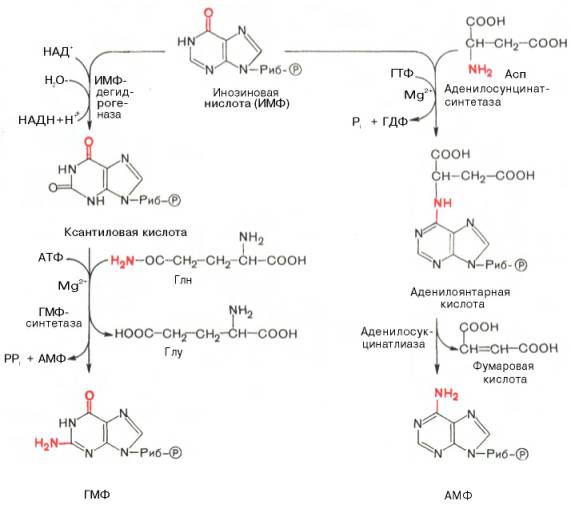
АМФ и ГМФ образуются из ИМФ, причем в синтезе обоих моно-нуклеотидов участвуют по два фермента, различных по своему механизму действия. Образование ГМФ из ИМФ катализируют ИМФ-дегидрогеназа и ГМФ-синтетаза, а образование АМФ из того же предшественника катализируется последовательным действием аденилосукцинатсинтетазы и аденилосукцинат-лиазы. Механизм двухэтапного синтеза АМФ и ГМФ можно представить в виде химических реакций.
В ферментативном синтезе АМФ из ИМФ специфическое участие принимает аспарагиновая кислота, являющаяся донором NH2-группы, и ГТФ в качестве источника энергии; промежуточным продуктом реакции является аденилоянтарная кислота. Биосинтез ГМФ, напротив, начинается с де-гидрогеназной реакции ИМФ с образованием ксантозиловой кислоты; в аминировании последней используется только амидный азот глутамина.
Превращение АМФ и ГМФ в соответствующие нуклеозидди- и нуклео-зидтрифосфаты также протекает в 2 стадии при участии специфических нуклеозидмонофосфат- и нуклеозиддифосфаткиназ :
ГМФ + АТФ ГДФ + АДФ; ГДФ + АТФ ГТФ + АДФ.
Следует указать на существование в клетках весьма тонкого механизма регуляции синтеза пуриновых нуклеотидов. Синтез их тормозится конечными продуктами по принципу обратной связи, т.е. ингибированием первой стадии переноса аминогруппы глутамина на ФРПФ. Фермент, катализирующий эту стадию, оказался аллостерическим регуляторным ферментом. Вторая особенность механизма регуляции заключается в том, что избыток ГМФ в клетках оказывает аллостерическое торможение только на свой собственный синтез, не влияя на синтез АМФ, и, наоборот, накопление АМФ подавляет свой синтез, не ингибируя синтеза ГМФ.