Оксид хрома(III)
| Оксид хрома(III) | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид хрома (III) |
| Традиционные названия | сесквиоксид хрома, хромовая зелень |
| Химическая формула | Cr2O3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдый тугоплавкий порошок зелёного цвета |
| Молярная масса | 152 г/моль |
| Плотность | 5,21 г/см³ |
| Термические свойства | |
| Температура плавления | 2435 °C |
| Температура кипения | 4000 °C |
| Удельная теплоёмкость (ст. усл.) | 781 Дж/(кг·К) |
| Энтальпия образования (ст. усл.) | −1128 кДж/моль |
| Удельная теплота плавления | 822000 Дж/кг |
| Классификация | |
| Рег. номер CAS | 1308-38-9 |
| SMILES | O=[Cr]O[Cr]=O |
| RTECS | GB6475000 |
Окси́д хро́ма (III) Cr2O3 (сесквиоксид хрома, хромовая зелень) — очень твёрдый тугоплавкий порошок зелёного цвета. Температура плавления 2435 °C, кипения ок. 4000 °C. Плотность 5,21 г/см³. Нерастворим в воде. По твердости близок к корунду, поэтому его вводят в состав полирующих средств.
Содержание
Способы получения
1. Дихромата аммония:
(NH4)2Cr2O7 → Cr2O3 + N2↑ + 4H2O
при этом ощущается слабый запах аммиака, так как при разложении бихромата аммония также идет параллельная реакция с выделением аммиака. Полученная окись хрома (III) имеет в своем составе примесь хрома (II) и хрома (VI), вероятно в виде хроми-хроматов (в частности Cr5O10). Внешний вид: зелёный, с вкраплениями серого и чёрного цвета, плотность 4,6 г/см³.
3. Гидроксида хрома(III):
Химические свойства
Относится к группе амфотерных оксидов. В высокодисперсном состоянии растворяется в сильных кислотах с образованием солей хрома(III):
При сплавлении со щелочами и содой даёт растворимые соли Cr 3+ (в отсутствие окислителей):
Cr2O3 + Na2CO3 → 2степени окисления, в присутствии сильного окислителя в щелочной среде он окисляется до хромата:
а сильные восстановители его восстанавливают:
Применение
См. также
Полезное
Смотреть что такое «Оксид хрома(III)» в других словарях:
Оксид хрома(VI) — Общие … Википедия
Оксид хрома(II) — Общие … Википедия
Оксид хрома(IV) — Оксид хрома(IV) … Википедия
Оксид хрома (VI) — Оксид хрома(VI) Общие Систематическое наименование Оксид хрома (VI) Химическая формула CrO3 Отн. молек. масса 100 а. е. м … Википедия
хрома(III) оксид — chromo(III) oksidas statusas T sritis chemija formulė Cr₂O₃ atitikmenys: angl. chrome green; chromic oxide; chromium(III) oxide rus. хрома сесквиоксид; хрома(III) оксид; хромовой зеленый ryšiai: sinonimas – dichromo trioksidas sinonimas – chromo… … Chemijos terminų aiškinamasis žodynas
Фторид хрома(III) — Фторид хрома(III) … Википедия
Сульфат хрома(III) — Эта статья или раздел нуждается в переработке. Пожалуйста, улучшите статью в соответствии с правилами написания статей. Сульфат хро … Википедия
Бромид хрома(III) — Общие Систематическое наименование Бромид хрома(III) Традиционные названия Бромистый хром Химическая формула CrBr3 Физические свойства … Википедия
Сульфид хрома(III) — Общие Систематическое наименование Сульфид хрома(III) Традиционные названия Сернистый хром Химическая формула Cr2S3 Физические свойства … Википедия
Хлорид хрома(III) — Хлорид хрома(III) … Википедия
Оксид хрома(VI)
| Оксид хрома(VI) | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид хрома (VI) |
| Химическая формула | CrO3 |
| Физические свойства | |
| Отн. молек. масса | 100 а. е. м. |
| Молярная масса | 99,99 г/моль |
| Плотность | 2,8 г/см³ |
| Термические свойства | |
| Температура плавления | 197 °C |
| Температура разложения | 250 °C |
| Классификация | |
| Рег. номер CAS | 1333-82-0 |
Окси́д хро́ма(VI) (трёхокись хрома, хромовый ангидрид), CrO3 — соединение хрома с кислородом, тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.
Содержание
Свойства
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
или дихромовая кислота (при избытке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет йод, серу, фосфор, уголь, например:
Получение
Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность
Оксид хрома(VI) очень ядовит, как и многие другие соединения шестивалентного хрома. Летальная доза для человека при попадании внутрь 0,1 г.
Техника безопасности
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или пластиковая герметичная посуда, и исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
См. также
Полезное
Смотреть что такое «Оксид хрома(VI)» в других словарях:
Оксид хрома(II) — Общие … Википедия
Оксид хрома(IV) — Оксид хрома(IV) … Википедия
Оксид хрома (VI) — Оксид хрома(VI) Общие Систематическое наименование Оксид хрома (VI) Химическая формула CrO3 Отн. молек. масса 100 а. е. м … Википедия
оксид хрома — (Cr2O3) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN chromic oxidechrome oxide … Справочник технического переводчика
Оксид хрома — – Cr2O3 с небольшим количеством примесей водорастворимых солей – пигмент темно зеленого цвета. Устойчив к воздействию щелочей, кислот и повышенных температур. Получают путем нагревания смеси хромпика с каким либо восстановителем, например… … Энциклопедия терминов, определений и пояснений строительных материалов
Оксид хрома(III) — Оксид хрома(III) … Википедия
Хрома оксиды — Существуют следующие хлориды хрома: Название Формула Температура плавления Температура кипения Цвет Оксид хрома(II) CrO черный Оксид хрома(III) Cr2O3 2440 °C 3000 °C зеленый Оксид хрома(IV) CrO2 … Википедия
ХРОМА СЕМЕЙСТВО — ПОДГРУППА VIB. СЕМЕЙСТВО ХРОМА ХРОМ, МОЛИБДЕН, ВОЛЬФРАМ Все три элемента VIB подгруппы хром Cr, молибден Mo, вольфрам W играют большую роль в промышленности, особенно в металлургии и электротехнике. Каждый из этих элементов занимает среднее… … Энциклопедия Кольера
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
Оксид калия — Общие … Википедия
Оксид хрома(II)
| Оксид хрома(II) | |
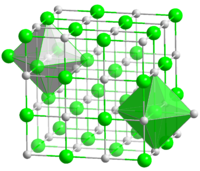 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид хрома (II) |
| Традиционные названия | закись хрома |
| Химическая формула | CrO |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое вещество черного или красного цвета |
| Молярная масса | 68 г/моль |
| Термические свойства | |
| Температура плавления | 1550 °C |
| Классификация | |
| Рег. номер CAS | 12018-00-7 |
| Безопасность | |
| Токсичность | Нетоксичен |
Оксид хрома (II) (закись хрома) — это черные или красные кристаллы. Основный оксид.
Содержание
Получения
Получают окислением амальгамы хрома CrHg3 или CrHg азотной кислотой или кислородом.
2CrHg3 + O2 = 2CrO + 6Hg 2CrHg + O2 = 2CrO + 2Hg
Так же можно получить термическим разложением карбонила Сr(СО)6
Химические свойства
При 100°С превращается в Cr2O3 :
Восстанавливается водородом до металлического хрома при 1000°С:
Также можно восстановить коксом:
Растворяется в соляной кислоте с выделением водорода и хлорида хрома(III). Не растворим в разбавленных серной и азотной кислотах.
Физические свойства
Может быть красным (не пирофорен) и чёрным пирофорным порошком (самовоспламенения на воздухе), поэтому чёрный сохраняют под слоем в воды (с водой не взаимодейсвует). Образует гексагональные пластинчатые кристаллы. Как и все оксиды хрома тугоплавок, температура плавления 1550°С.
См. также
Источники
Примечания
Полезное
Смотреть что такое «Оксид хрома(II)» в других словарях:
Оксид хрома(VI) — Общие … Википедия
Оксид хрома(IV) — Оксид хрома(IV) … Википедия
Оксид хрома (VI) — Оксид хрома(VI) Общие Систематическое наименование Оксид хрома (VI) Химическая формула CrO3 Отн. молек. масса 100 а. е. м … Википедия
оксид хрома — (Cr2O3) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN chromic oxidechrome oxide … Справочник технического переводчика
Оксид хрома — – Cr2O3 с небольшим количеством примесей водорастворимых солей – пигмент темно зеленого цвета. Устойчив к воздействию щелочей, кислот и повышенных температур. Получают путем нагревания смеси хромпика с каким либо восстановителем, например… … Энциклопедия терминов, определений и пояснений строительных материалов
Оксид хрома(III) — Оксид хрома(III) … Википедия
Хрома оксиды — Существуют следующие хлориды хрома: Название Формула Температура плавления Температура кипения Цвет Оксид хрома(II) CrO черный Оксид хрома(III) Cr2O3 2440 °C 3000 °C зеленый Оксид хрома(IV) CrO2 … Википедия
ХРОМА СЕМЕЙСТВО — ПОДГРУППА VIB. СЕМЕЙСТВО ХРОМА ХРОМ, МОЛИБДЕН, ВОЛЬФРАМ Все три элемента VIB подгруппы хром Cr, молибден Mo, вольфрам W играют большую роль в промышленности, особенно в металлургии и электротехнике. Каждый из этих элементов занимает среднее… … Энциклопедия Кольера
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
Оксид калия — Общие … Википедия
Оксид хрома (III)
| Оксид хрома (III) | |
|---|---|
 | |
 | |
| Систематическое наименование | Оксид хрома (III), эсколаит |
| Традиционные названия | сесквиоксид хрома, хромовая зелень |
| Хим. формула | Cr2O3 |
| Состояние | твёрдый тугоплавкий порошок зелёного цвета |
| Молярная масса | 152 г/моль |
| Плотность | 5,21 г/см³ |
| Температура | |
| • плавления | 2435 °C |
| • кипения | 4000 °C |
| Уд. теплоёмк. | 781 Дж/(кг·К) |
| Энтальпия | |
| • образования | −1128 кДж/моль |
| Удельная теплота плавления | 822000 Дж/кг |
| ГОСТ | ГОСТ 2912-79 |
| Рег. номер CAS | 1308-38-9 |
| PubChem | 517277 |
| Рег. номер EINECS | 215-160-9 |
| SMILES | |
| RTECS | GB6475000 |
| ChEBI | 48242 |
| ChemSpider | 451305 |
| Пиктограммы ECB |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Оксид хрома (III) Cr2O3 (сесквиоксид хрома, хромовая зелень, эсколаит) — очень твёрдый тугоплавкий порошок зелёного цвета. Температура плавления 2435 °C, кипения ок. 4000 °C. Плотность 5,21 г/см³ (из иностранных источников 5,22 г/см³). Нерастворим в воде. По твердости близок к корунду, поэтому его вводят в состав полирующих средств.
Содержание
Способы получения
При разложении дихромата аммония ощущается слабый запах аммиака (так как одна из параллельных реакций идет с образованием аммиака) и получается оксид хрома (III) с содержанием по основному продукту 95-97 %, нестехиометрического кислорода содержится 3 — 5 %. Прокалкой при 1000 °С в течение 3-4 часов получен оксид хрома (III) с содержанием по основному продукту до 99,5 %.
Химические свойства
Относится к группе амфотерных оксидов. В высокодисперсном состоянии растворяется в сильных кислотах с образованием солей хрома(III):
В сильнокислой среде может идти реакция:
При сплавлении со щелочами и содой даёт растворимые соли Cr 3+ (в отсутствие окислителей):
Поскольку Cr2O3 — соединение хрома в промежуточной степени окисления, в присутствии сильного окислителя в щелочной среде он окисляется до хромата:
а сильные восстановители его восстанавливают:
Cr2O3 + 2Al → Al2O3 + 2Cr 
Применение
Токсичность
Оксид хрома CrO(II)
Низший оксид для элементов 6-й группы состава MeO получен только для хрома.
Физические свойства CrO(II):
Химические свойства CrO(II):
Гидроксид хрома Cr(OH)2(II)
Физические свойства Cr(OH)2(II):
Химические свойства Cr(OH)2(II):
Соединения хрома со степенью окисления +2 являются неустойчивыми, легко окисляются кислородом воздуха в более устойчивые соединения хрома со степенью окисления +3:
4Cr(OH)2+O2+2H2O = 4Cr(OH)3
Cr2O3 в мелкоизмельченном состоянии применяют в качестве абразивного материала (паста ГОИ), зеленого пигмента, катализатора в органическом синтезе. Оксид хрома (III) является основной добавкой к корунду при выращивании искусственных рубинов, используемых в ювелирной промышленности и часовом деле, а также в качестве лазерного материала в оптоэлектронике.
Физические свойства Cr2O3(III):
Химические свойства Cr2O3(III):
Гидроксид хрома Cr(OH)3(III)
Физические свойства Cr(OH)3(III):
Химические свойства Cr(OH)3(III):
Оксид хрома CrO2(IV) (диоксид хрома)
Диоксид хрома применяется в производстве элементов памяти для компьютеров.
Оксид хрома CrO3(VI) (хромовый ангидрид)
Физические свойства CrO3(VI):
Химические свойства CrO3(VI):
Триоксид хрома получают действием концентрированной серной кислоты на концентрированные растворы хроматов/дихроматов калия/натрия:
K2Cr2O7+H2SO4 = 2CrO3↓+K2SO4+H2O
Гидроксиды хрома
Примечательно, что хромат-ионы и дихромат-ионы при изменении среды растворов без проблем переходят друг в друга, меняя при этом окраску раствора:
Хроматы получают сплавлением хромистого железняка или оксида хрома (III) с карбонатами в присутствии кислорода (t=1000°C):
4Fe(CrO2)2+8Na2CO3+7O2 = 8Na2CrO4+2Fe2O3+8CO2
Дихроматы получают из растворов хроматов, подкисляя их.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе




