Сероконверсия
Смотреть что такое «Сероконверсия» в других словарях:
сероконверсия — Появление в сыворотке крови больного специфических антител [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN seroconversion … Справочник технического переводчика
СЕРОКОНВЕРСИЯ — (seroconversion) выработка специфических антител в ответ на наличие какого либо антигена (например, вакцины или вируса) … Толковый словарь по медицине
Сероконверсия (Seroconversion) — выработка специфических антител в ответ на наличие какого либо антигена (например, вакцины или вируса). Источник: Медицинский словарь … Медицинские термины
бессимптомная сероконверсия — Изменение серологического статуса организма в отношении инфекционного агента без клинического проявления заболевания [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN asymptomatic seroconversion … Справочник технического переводчика
Беременность — I Беременность Беременность (graviditas) физиологический процесс развития в женском организме оплодотворенной яйцеклетки, в результате которого формируется плод, способный к внеутробному существованию. Возможно одновременное развитие двух и более … Медицинская энциклопедия
Специфичный (Specific) — 1. Лекарственное вещество, обладающее особыми свойствами, которые используются для лечения различных заболеваний. 2. По отношению к заболеванию болезнь, вызванная специфическим микроорганизмом (который приводит к развитию только данной болезни и… … Медицинские термины
Зеффикс — Действующее вещество ›› Ламивудин* (Lamivudine*) Латинское название Zeffix АТХ: ›› J05AF05 Ламивудин Фармакологическая группа: Противовирусные средства Нозологическая классификация (МКБ 10) ›› B18.0 Хронический вирусный гепатит B с дельта агентом … Словарь медицинских препаратов
Имовакс Полио — Латинское название Imovax Polio АТХ: ›› J07BF03 Вирус полиомиелита — трехвалентный инактивированный Фармакологическая группа: Вакцины, сыворотки, фаги Нозологическая классификация (МКБ 10) ›› B91 Последствия полиомиелита Состав и форма… … Словарь медицинских препаратов
Пегасис — Действующее вещество ›› Пэгинтерферон альфа 2а (40 кДа)* (Peginterferon alfa 2a (40 KD)*) Латинское название Pegasys АТХ: ›› L03AB11 Пэгинтерферон альфа 2a Фармакологическая группа: Иммуномодуляторы Состав и форма выпуска Раствор для подкожного… … Словарь медицинских препаратов
Полио Сэбин Веро — Латинское название Polio Sabin Vero Фармакологическая группа: Вакцины, сыворотки, фаги Нозологическая классификация (МКБ 10) ›› B91 Последствия полиомиелита Состав и форма выпуска Раствор для приема внутрь. 1 доза вакцины (2 капли или 0,5 мл) в… … Словарь медицинских препаратов
Иммуногенность новой гриппозной вакцины
Грипп и гриппоподобные заболевания занимают первое место по частоте и количеству случаев в мире. Эпидемия гриппа ежегодно приходит с наступлением осенне-зимнего сезона, и каждый раз иммунная система не готова к встрече с
Грипп и гриппоподобные заболевания занимают первое место по частоте и количеству случаев в мире. Эпидемия гриппа ежегодно приходит с наступлением осенне-зимнего сезона, и каждый раз иммунная система не готова к встрече с ним. Почему? Грипп является чемпионом среди вирусов по способности к генетической изменчивости, которая позволяет ему уходить от иммунного надзора. Вирус с изменившимися поверхностными белками уже не распознается специфическими противогриппозными антителами к штаммам-предшественникам.
Наиболее эффективным, безопасным и экономически оправданным средством профилактики гриппа является вакцинация. Чтобы вакцина защищала от гриппа, должно быть четкое соответствие вакцинных штаммов эпидемическим. В отличие от большинства других вакцинных препаратов, существует необходимость ежегодного обновления штаммового состава противогриппозных вакцин и, следовательно, необходимость ежегодной иммунизации. Проблема гриппа давно вышла за пределы одной страны. Центрами по гриппу ВОЗ, организованными по всему миру, проводится регулярный мониторинг и сбор информации по сезонным циркулирующим штаммам вируса гриппа и вспышкам заболеваемости. На основании анализа присланного материала эксперты делают прогнозы относительно разновидностей гриппа, которые будут циркулировать в следующем эпидсезоне, а также предлагают вирусы-кандидаты в вакцинные штаммы для производителей.
С учетом того, что дифференциальная диагностика гриппа от других ОРВИ затруднена, показатели иммуногенности вакцин принято оценивать по уровню специфических антител к гемагглютинину (ГА). Защитный эффект ГА-специфических антител неоднократно был продемонстрирован как у животных, так и у людей. Антитела нейтрализуют вирус гриппа, предотвращая его связывание с рецепторами, при этом уровень антител к гемагглютинину напрямую коррелирует с уровнем защищенности. При оценке потенциальной эффективности вакцины титр антител не менее чем 1:40 считают защитным. Антитела к другому изменчивому поверхностному белку вируса гриппа — нейраминидазе — не могут предотвратить инфекцию, однако играют важную роль в защите от тяжелых форм гриппа, препятствуя выходу вирусных частиц из инфицированных клеток и дальнейшему распространению вируса в организме. Гемагглютинин и нейраминидаза названы протективными белками, а вакцины, содержащие только эти очищенные белки, — субъединичными.
Современные достижения вирусологии, развитие технологий фармацевтической индустрии, интеграция исследователей разных стран в сфере контроля и борьбы с гриппом позволили вывести на новый уровень разработку и производство гриппозных вакцин. Вакцина Гриппол® Нео — результат международного сотрудничества двух компаний («Солвей Биолоджикалз Б. В.» и ФК «ПЕТРОВАКС»). Эта субъединичная вакцина содержит иммуноадъювант Полиоксидоний® и антигены (гемагглютинин и нейраминидазу) европейского качества, полученные из вируса, выращенного на культуре клеток. Рост вируса для вакцины осуществляется по современной технологии с использованием клеточной линии MDCK (Madine-Darbin Canine Kidney) в бессывороточной среде и является стандартизированным закрытым процессом, исключающим возможность контаминации любыми, в том числе неизвестными агентами. Применение культур клеток для наработки вирусного материала стало уже традиционным для целого ряда вакцинных препаратов. Но только благодаря разработкам специалистов компании «Солвей Биолоджикалз» технология стала доступной и для гриппозных вакцин. В 2001 году была зарегистрирована вакцина Инфлювак ТС (Нидерланды), в 2009 году в России — Гриппол ® Нео.
Снижение антигенной нагрузки в вакцинирующей дозе обеспечивает максимальный профиль безопасности препарата. Антигены с адъювантом образуют комплекс, который стимулирует гуморальное и клеточное звенья иммунитета. Это приводит к образованию специфических к протективным белкам антител, отвечающих за защиту от гриппа, и повышает общую резистентность организма к инфекции.
Клинические исследования безопасности и иммуногенности Гриппол ® Нео проводились с участием добровольцев в высокоспециализированных исследовательских центрах по изучению вакцинных препаратов и поствакцинальных реакций.
Материалы и методы
Вакцины
В клиническом испытании были использованы три инактивированные субъединичные вакцины, содержащие иммуноадъювант Полиоксидоний® и антигены (гемагглютинин и нейраминидазу) актуальных для эпидемического сезона 2008/2009 штаммов вируса гриппа: H1N1 A/Brisbane/59/2007; H3 N2 A/Uruguay/716/2007; B/Florida/4/2006. Два тестируемых препарата представляли собой две серии вакцины Гриппол® Нео производства ООО «ФК «ПЕТРОВАКС», содержащие по 5 либо по 10 мкг гемагглютинина каждого из трех штаммов и 500 мкг Полиоксидония®. В качестве препарата сравнения использовали коммерческую вакцину Гриппол® производства ФГУП «НПО «Микроген», содержащую по 5 мкг ГА штаммов вирусов гриппа типа А (H1N1 и H3N2), 11 мкг гемагглютинина вируса гриппа типа В, 500 мкг Полиоксидония®. Препараты, используемые в исследовании, были контролированы в ГИСК им. Л. А. Тарасевича на соответствие нормативной документации; испытуемые серии Гриппол® Нео и препарат сравнения зашифрованы специалистами ГИСКа, не принимающими участия в данном исследовании. Дешифровка была проведена после завершения клинического исследования и представления всех результатов в ГИСК.
Дизайн исследования
Исследования проведены в соответствии с утвержденными протоколами и согласно разрешению МЗ РФ на клинических базах ФГУ НИИ ДИ Росздрава и ГОУ ВПО СПбГМУ им. ак. И. П. Павлова в соответствии с требованиями Надлежащей клинической практики (GCP).
Дизайн исследования: рандомизированное, двойное слепое, контролируемое сравнительное в параллельных группах. Вакцинация добровольцев проведена после подписания информированного согласия.
Участники были отобраны в соответствии с критериями включения/исключения, определенными протоколом клинического испытания. Всего было вакцинировано 300 здоровых добровольцев в возрасте 18–55 лет (средний возраст — 24,5 ± 0,5 года). Перед прививкой все добровольцы были осмотрены врачом, было проведено измерение температуры тела, артериального давления, женщинам — тест на беременность.
Методом случайного выборочного распределения было сформировано три группы по 100 человек. Вакцинацию проводили однократно в дельтовидную мышцу в объеме 0,5 мл.
Постановка реакции и учет результатов
Парные сыворотки добровольцев, взятые до и через 21 день после вакцинации, исследовали с помощью стандартной методики в реакции торможения гемагглютинации (РТГА), как описано в МУ 3.3.2 1758–03. Постановка РТГА включала следующие этапы: подготовка сывороток, определение гемагглютинирующего титра в РГА и рабочей дозы вируса, постановка самой реакции. Для удаления неспецифических ингибиторов сыворотку обрабатывали RDE по методу, описанному в инструкции к препарату. В качестве рабочей дозы антигена использовалась доза 4АЕ, приготовленная из диагностикумов «Диагностикумы гриппозные для реакции торможения гемагглютинации сухие» (ФСП 42–0321–4042–03) трех штаммов, соответствующих вакцинным. Сыворотки титровали начиная с разведения 1:10. При учете результатов титр 1:1280 — равным 1:1280.
Иммуногенность оценивали в соответствии с требованиями Европейского комитета к противогриппозным вакцинам (СPMP/BWP/214/96), согласно которым должен выполняться по крайней мере один из трех критериев:
Статистика
Результаты исследований статистически обработаны с использованием t-критерия Стьюдента. Вариационный анализ полученных результатов проводили с применением пакета прикладных программ Statistica 6.0.
Результаты и обсуждение
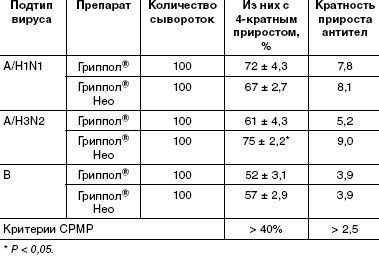
Серологическое обследование с целью оценки иммунологической эффективности вакцинации проводили, сравнивая уровень антител в парных сыворотках, взятых до прививки и на 21-й день после вакцинации. Во всех экспериментальных группах в сыворотках привитых регистрировали статистически достоверное нарастание титров антител. По всем анализируемым критериям не наблюдалось статистически достоверной разницы в иммунном ответе на серии вакцины Гриппол® Нео с различными дозировками антигенов. В таблицах приведены данные, относящиеся к серии, содержащей по 5 мкг гемагглютинина каждого штамма.
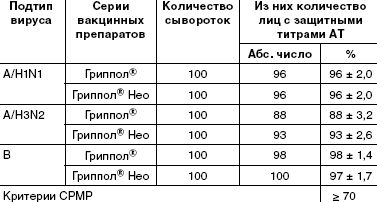
Подсчеты числа лиц с серопротекциями (защитными титрами антител (≥ 1:40)) показали, что в каждой группе уровень этих антител соответствует критерию CPMP (табл. 1).
Известно, что человеческая популяция неоднородна по наличию антител к различным штаммам и подтипам вируса гриппа вследствие гриппозных эпидемий и предыдущих вакцинаций. Среди вакцинированных добровольцев выявлены как серонегативные, так и серопозитивные участники (исходно имевшие защитный титр). Представлялось интересным оценить эффективность иммунизации в общей популяции людей (табл. 3).
Выводы и заключение
В настоящее время вакцина Гриппол ® Нео зарегистрирована (РУ № ЛСР-006029/09 от 23.07.2009 г.). Таким образом, семейство вакцин Гриппол ® пополнилось новым полноправным членом, а профилактическая медицина обрела новый инструмент для контроля такого заболевания, как грипп. Гриппол ® Нео стал первой в мире субъединичной адъювантной вакциной с клеточной технологией получения антигенов. При этом впервые вакцинация против гриппа разрешена людям с аллергией на белок куриного яйца. Исследования по расширению показаний к применению вакцины продолжаются.
Е. М. Войцеховская *
В. С. Вакин *, кандидат медицинских наук
А. А. Васильева *
Е. В. Кузнецова *, кандидат биологических наук
Н. И. Лонская **, кандидат медицинских наук
Г. А. Ельшина **, кандидат медицинских наук
М. А. Горбунов **, доктор медицинских наук
А. А. Соминина *, доктор медицинских наук
Ю. А. Зайцева ***
* ГУ НИИ гриппа РАМН, Санкт-Петербург
** ФГУН ГИСК им. Л. А. Тарасевича Роспотребнадзора, Москва
*** ООО ФК «ПЕТРОВАКС», Москва
Ключевые слова: вакцина, грипп, Гриппол ® Нео, клеточная культура
Варилрикс цена
| Услуга | Цена | Примечание |
|---|---|---|
| Варилрикс, Бельгия | 2100 | с 12 месяцев |

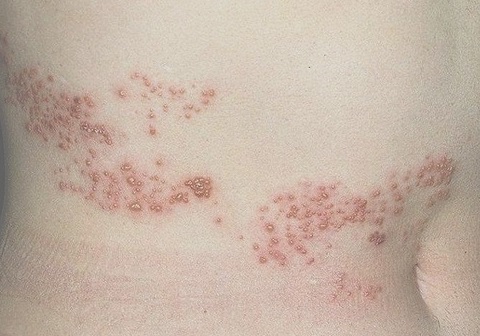
В детском возрасте заболевание протекает чаще благоприятно, во взрослом же состоянии переноситься гораздо тяжелее, чаще отмечаются бактериальные осложнения. Особую опасность вирус ветряной оспы представляет для беременных и плода.
О писание препарата
писание препарата
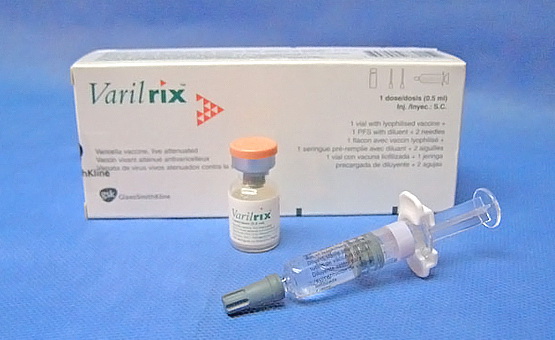
Варилрикс® (GlaxoSmithKline Biologicals, Бельгия) – это живая аттенуированная (ослабленная) вакцина, предназначенная д ля профилактики ветряной оспы.
В своем составе вакцина Варилрикс® содержит живой аттенуированный вирус Varicella zoster (штамм Oka), полученный размножением в культуре диплоидных клеток человека MRC-5, со специфической активностью.
Показания к применению
Режим дозирования
Разовая доза составляет 0,5 мл. Вакцина поставляется в двух компонентах: флакон с лиофилизированной вакциной (специально высушенной) и шприцем с растворителем. Данный шприц снабжен специальной тонкой иглой, минимизирующей болевые ощущения от инъекции. Применение подобного шприца исключает передозировку и его повторное использование.
Вакцина соответствует требованиям ВОЗ по производству биологических препаратов, требованиям к вакцинам против ветряной оспы.
Способ применения
В асептически упакованном блистере находится шприц с жидким растворителем и флакон с лиофилизатом ветряночной вакцины. Непосредственно перед введением сухая вакцина во флаконе растворятеся жидким растворителем из шприца и вводится из того же шприца.
Вакцина Варилрикс® вводится подкожно. Введение осуществляется в область дельтовидной мышцы (плечо). Внутривенное введение категорически противопоказано.
Схема вакцинации
Курс первичной вакцинации состоит из 1 дозы вакцины и ревакцинации. Схема иммунизации: первое введение и ревакцинация через 6-8 недель. Применение вакцины не имеет четкой привязки к возрасту. Важно соблюдать сроки вакцинации.
Экстренная профилактика
Вакцинацию проводят однократно 1 дозой вакцины (0.5 мл) в течение первых 96 ч после контакта (предпочтительно в течение первых 72 ч). Если заболевание не развивается, то проводится повторная вакцинация через 6-8 недель.
Клинические исследования показали высокую эффективность вакцины Варилрикс®. Уровень сероконверсии (выработка иммунитета) у здоровых детей в возрасте от 12 месяцев до 12 лет включительно, определенный через 6 недель после вакцинации, превышал 98% и сохранялся, по крайней мере, в течение 7 лет после вакцинации.
Уровень сероконверсии, определяемый у детей в возрасте 13 лет, после двукратной вакцинации, составлял 100% и сохранялся в течение как минимум 1 года.
В клинических исследованиях было показано, что большинство вакцинированных, находившихся впоследствии в контакте с заболевшими, либо не подвержены инфекции, либо переносят заболевание в значительно более легкой форме (меньшее количество высыпаний, отсутствие лихорадки).
Для того, чтобы уровень сероконверсии был как можно выше с конца 2012 года вакцина Варилрикс® применяется с ревакцинацией у всех возрастов, что предотвращает возникновение так называемых «ветрянок прорыва» (вспышки ветряной оспы у привитых детей).
Плановые прививки
Вакцина против ветряной оспы не входит в Национальный календарь прививок, но входит в некоторые региональные календари, например Москвы.
Применение препарата Варилрикс совместно с другими вакцинами
Вакцину Варилрикс® можно вводить одновременно со всеми препаратами из национального календаря профилактических прививок в один день, в разные участки тела, за исключением вакцины БЦЖ и антирабической вакцины (вакцинация против бешенства).
Применение вакцины Варилрикс® совместно с другими прививками не влияет на их иммуногенность (способность выработки иммунитета). Переносимость вакцин не ухудшается, количество побочных реакций не возрастает.
Введение нескольких вакцин в один день не является избыточной нагрузкой на иммунитет.
Введение вакцины Варилрикс® возможно не ранее, чем через 3 месяца после введения иммуноглобулинов или после гемотрансфузии.
Побочные реакции
Реакции на вакцину Варилрикс® редки и чаше всего переносятся легко. Делятся на местные и общие.
Местные реакции: боль и покраснение в месте инъекции.
Общие реакции: повышение температуры тела до субфебрильных цифр, лимфоаденопатия (припухание лимфатических узлов), слабость, недомогание. Возможно появление сыпи сходной с ветряночной. Сыпь необильная, редко развивается до пузырьков.
Чаще всего подобные реакции специального лечения не требуют, проводится симптоматическая терапия.
В среднем реактогенность вакцины при введении второй дозы (ревакцинации) не превышает реактогенность первой дозы. Также не отмечалось различий в профиле безопасности вакцины у людей, имеющих иммунитет к ветряной оспе и у людей не имеющих такового.
Противопоказания к применению
Вакцина противопоказана к применению при беременности или планируемой беременности (в течение 3 мес) и в период грудного вскармливания.
Дополнительные сведения
Для экстренной профилактики вакцина может применяться в первые 96 часов. Время отсчитывается не от момента установления диагноза больному, а от момента последнего контакта с больным ветряной оспой.
Вакцина Варилрикс® защищает только от ветряной оспы и не защищает от других заболеваний, сопровождающихся поражением кожи и от других заболеваний, вызванных вирусами семейства герпес.
Женщинам детородного возраста рекомендуется предохраняться от беременности в течение 1 месяца перед вакцинацией и 2 месяцев после вакцинации.
Как проходит вакцинация?

Без напоминаний, в обязательном порядке перед прививкой медицинский работник показывает препарат, срок годности вакцины.
Используется только стерильный и одноразовый инструментарий. Обязательно прививка проводится в одноразовых медицинских перчатках.
В день вакцинации ребенка осматривает врач-педиатр, измеряется температура. При отсутствии противопоказаний проводится прививка. Данные о проведенной прививке заносятся в карту, прививочный сертификат, а также даются подробные рекомендации по уходу за ребенком в поствакцинальном периоде.
Перед прививкой доктор ответит на все волнующие Вас вопросы. Обязательно возьмите на прием данные о предыдущих вакцинациях!
Сероконверсия
Сероконверсия (Seroconversion) – выработка организмом специфических антител или повышение их титров в ответ на присутствие какого-либо антигена, который попадает в организм, как правило, в результате инфекции или вакцинации. Понятие «сероконверсия» часто используется в диагностике как признак инфекции или критерий эффективности вакцинации. В обоих случаях для доказательства наличия сероконверсии требуется исследование парных образцов сыворотки, первый из которых был взят до начала или в самом начале антигенного воздействия (до болезни или вакцинации), а последующие — в период ожидаемого иммунного ответа. Сероконверсия устанавливается путем одновременного титрования парных образцов сыворотки с помощью соответствующих серологических реакций, причем достоверным признается увеличение титра, равное или превышающее два шага разведения. Если при постановке серологической реакции сыворотки разводятся 1:2; 1:4; 1:8, то сероконверсией можно считать четырехкратное и большее увеличение титра антител.
Таким образом, сероконверсия используется для оценки эффективности вакцинации и серологической диагностики заболеваний.
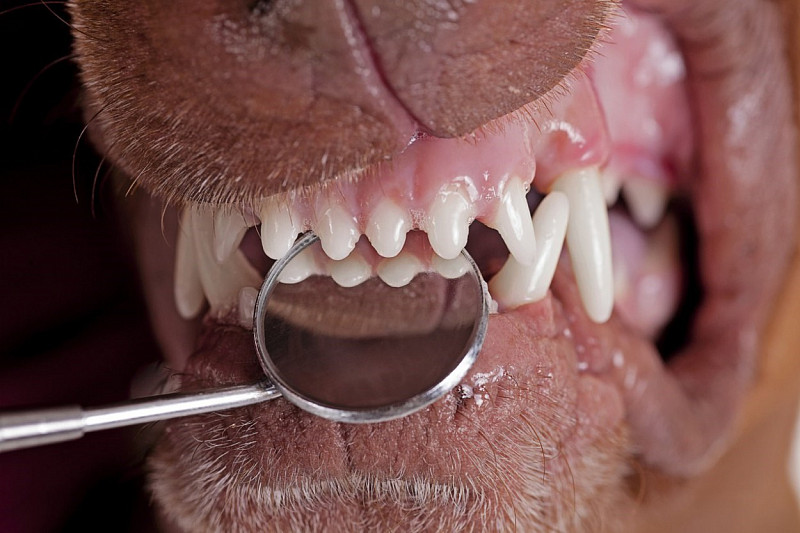
Наиболее распространёнными стоматологическими заболеваниями у собак является пародонтит и гингивит. Реже наблюдаются пародонтозы, периодонтиты и стоматиты.
Пародонтит – это воспалительное заболевание пародонта, сопровождающееся разрушением структур удерживающих зуб с образованием патологических зубодесневых карманов, а затем пародонтальных.
• Microsporum canis (поражает кошек, собак и, в меньшей степени, крупных животных)
• Trichophyton mentagrophytes, T. verrucosum и T. erinacei (поражает ежей)
• M. gypseum.
Бессимптомная сероконверсия иммуноглобулинов при SARS-CoV-2-инфекции и как она может уберечь медперсонал от COVID-19.
Ранее сообщалось, что отделения гемодиализа госпиталей подвержены высокому риску распространения инфекционных заболеваний. Причинами называют невозможность соблюдать социальное дистанцирование в открытых отсеках, большое числа сменяющих друг друга пациентов, а также значительное число процедур как при подготовке к гемодиализу, так и во время его проведения.
Целью исследования, проведённого на базе отдельно стоящего амбулаторного педиатрического отделения для гемодиализа с пятью койками и тремя изолированными помещениями в Riley Hospital for Children, Indianapolis, USA и опубликованного в JAMA, было измерить уровни серийных антител против SARS-CoV-2 у пациентов, медсестер, врачей и обслуживающего персонала, присутствовавших при проведении гемодиализа у пациента с симптомами вирусной инфекции.
Начать проведение данного исследования было решено после того как стало известно, что 7 дней назад (день 0) у одного из пациентов наблюдались лихорадка и общие симптомы вирусного заболевания. Результат ПЦР теста на SARS-CoV-2 в мазке из носоглотки оказался положительным, и оставался положительным при повторных тестах на 7, 14 и 19 день. Сеансы гемодиализа ему проводились в изолированной комнате, начиная со дня 0. При этом весь персонал отделения и пациенты, которым производился гемодиализ, всегда были в масках.
Измерения уровня сывороточного IgM и IgG в сыворотке из образцов цельной крови были произведены у 13 пациентов, проходивших гемодиализ в отделении, у 11 медсестер и 10 врачей отделения, а также у 4 человек из обслуживающего персонала на 7, 14 и 21 дни от начала исследования. Сероконверсией считались положительные анализы на IgM или IgG.
Между 0-м и 7-м днем у 2 человек из медицинского персонала отмечались симптомы вирусного заболевания верхних дыхательных путей и лихорадка при отрицательных результатах ПЦР теста. В дальнейшем один из них сероконвертировал на 21-й день, несмотря на 3 отрицательных результата ПЦР. У остальных участников исследования не проводилось назофарингеальное тестирование на SARS-CoV-2 и не было симптомов COVID-19 до 7-го дня.
К 21 дню у 11 из 25 сотрудников отделения (44%) и у 3 из 13 пациентов (23%) были обнаружены положительные антитела к SARS-CoV-2. При том, что ни у одного из участников исследования между 7 и 21 днями не наблюдалось симптомов заболевания. У одного человека из медицинского персонала, который непосредственно опекал ПЦР-положительного пациента и у двух из 11 медицинских работников, которые ухаживали за 2 двумя пациентами с субклинической сероконверсией, в дальнейшем были обнаружены антитела против SARS-CoV-2. Все они оставались бессимптомными, несмотря на то, что у одного из них всё же был положительным результат теста на ПЦР в мазке из носоглотки.
Данное исследование продемонстрировало высокую распространенность субклинической сероконверсии у лиц, находящихся в контакте с возможными носителями SARS-CoV-2. Это дает надежду, что большее число работников здравоохранения может быть антитело положительными, чем можно было бы ожидать. Информация о серопревалентности медсестер и врачей позволит стратегически правильно укомплектовать персонал по уходу за SARS-CoV-2-позитивными больными и пациентами с подозрением на положительную реакцию, и тем самым уменьшить риск заражения, которому подвергаются медицинские работники в период пандемии COVID-19.
Поскольку это исследование имеет небольшой размер выборки и короткое последующее наблюдение, необходимы более масштабные исследования данной проблемы.
 писание препарата
писание препарата