Тромбоз портальной вены (I81)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
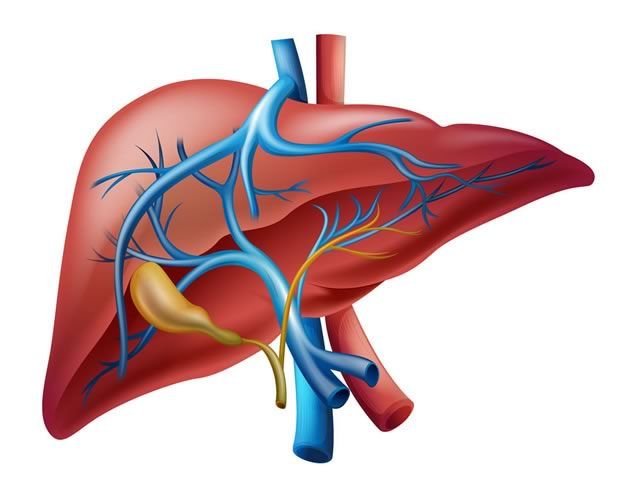
Обструкция портальной вены приводит к нарушению портального кровотока. Она может быть внепеченочной (вследствие тромбоза или врожденной атрезии портальной вены) или внутрипеченочной (микроваскулярная обструкция портальной вены при шистосоматозе).
Тромбоз портальной вены (обструкция портальной вены тромбом или опухолью) может локализоваться в различных ее отделах, в том числе и в селезеночных ветвях.
При циррозе печени наблюдается хроническое течение тромбоза портальной вены. Он развивается длительно (от нескольких месяцев до нескольких лет).
Тромбоз портальной вены приводит к портальной гипертензии и желудочно-кишечным кровотечениям.
Диагноз основан на результатах допплеровского ультразвукового исследования, КТ и МРТ органов брюшной полости, ангиографии.
Лечение заключается в предупреждении возникновения желудочно-кишечных кровотечений, назначении антикоагулянтов и тромболитических препаратов.
Этиология и патогенез
Закрытие просвета (обструкция) портальной вены приводит к нарушению портального кровотока. Такое закрытие может быть вызвано закупоркой портальной вены тромбом. Обструкция и тромбоз портальной вены могут располагаться в различных ее отделах, но выше уровня слияния селезеночной и верхней брыжеечной вен.
У 50% пациентов причины возникновения тромбоза портальной вены установить не удается.
Причины врожденного характера.
Причины приобретенного характера.
У 21-24% больных с обструкцией портальной вены обнаруживаются злокачественные опухоли (в большинстве случаев гепатоцеллюлярная карцинома и карцинома поджелудочной железы). Они оказывают компрессионное или прямое воздействие на портальную вену и приводят к формированию гиперкоагуляционного статуса.
Инфекционные заболевания брюшной полости также могут вызывать обструкцию и тромбоз портальной вены у взрослых пациентов, особенно при бактериемии возбудителем Bacteroides fragilis.
Миелопролиферативные заболевания, а также врожденные и приобретенные коагулопатии приводят к обструкции и тромбозу портальной вены в 10-12% случаев.
Венозный застой, вызванный резистентностью печеночной ткани, которая наблюдается при циррозе печени, также может провоцировать возникновение тромбоза портальной вены.
Портальная вена образуется слиянием селезеночной и верхней брыжеечной вен. Места обструкции и тромбоза локализуются выше уровня этого слияния.
При циррозе печени и злокачественных опухолях процесс тромбирования портальной вены начинается в ее внутрипеченочном отделе и распространяется на внепеченочную часть.
При тромбозе, вызванном другими причинами, патологический процесс возникает в месте начала портальной вены.
Обструкция портальной вены не нарушает функцию печени до тех пор, пока у пациента не возникнет заболевание печени (например, цирроз). Это происходит за счет компенсаторного усиления кровотока в системе печеночных артерий.
Кавернозная мальформация портальной вены (т.е. развитие перипортальных коллатералей) возникает при длительном течении тромбоза портальной вены в результате разрастания мелких сосудов вокруг места тромбоза. Скорость кровотока по этим сосудам составляет 2-7 см/сек. На снимках, выполненных в ходе эндоскопической ретроградной холангиогепатографии, у пациентов с портальной гипертензией кавернозная трансформация портальной вены выглядит как губкоподобная масса, расположенная под печенью. Аналогичные данные можно получить и у пациентов с гемангиосаркомой поджелудочной железы, и у больных псевдохолангиосаркомой. После выполнения трансюгулярного внутрипеченочного портосистемного шунтирования и устранения явлений портальной гипертензии кавернозная мальформация портальной вены на снимках не визуализируется.
Эпидемиология
Смерть при обструкции портальной вены обусловлена возникновением кровотечений из варикозно-расширенных вен желудка, пищевода и кишечника.
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Течение тромбоза портальной вены может быть острым и хроническим.
В некоторых случаях острая фаза заболевания может протекать бессимптомно. Для хронического течения тромбоза портальной вены характерно длительное развитие клинической симптоматики (от нескольких месяцев до нескольких лет).
Диагностика
С помощью этого исследования можно выявить гепатоспленомегалию, варикозно-расширенные непарную, паравертебральные вены и варикозно-расширенные вены пищевода.
Кавернозная мальформация портальной вены (т.е. развитие перипортальных коллатералей) возникает при длительном течении тромбоза портальной вены в результате разрастания мелких сосудов вокруг места тромбоза. Скорость кровотока по этим сосудам составляет 2-7 см/сек. На снимках, выполненных в ходе эндоскопической ретроградной холангиогепатографии, у пациентов с портальной гипертензией кавернозная мальформация портальной вены выглядит как губкоподобная масса, расположенная под печенью. Аналогичные данные можно получить и у пациентов с гемангиосаркомой поджелудочной железы, и у больных псевдохолангиосаркомой. После выполнения трансюгулярного внутрипеченочного портосистемного шунтирования и устранения явлений портальной гипертензии кавернозная трансформация портальной вены на снимках не визуализируется.
В 38% случаев у пациентов с тромбозом портальной вены диаметр сосуда более 15 мм. При развитии портального флебита стенки сосуда утолщены, а просвет сужен. Можно выявить кальцифицированные тромбы.
Чувствительность метода составляет 65-85%.
С помощью этого исследования можно выявить тромб в просвете портальной вены, нарушения структуры печени, варикозно-расширенные вены пищевода и желудка.
При комбинировании этого метода с допплеровским ультразвуковым исследованием можно обнаружить обструкцию портальной вены.
Проводится также КТ-портография. На снимках тромбоз портальной вены визуализируется как участок пониженной плотности в просвете портальной вены, периферия которого определяется как зона повышенной плотности. Кроме того, у пациентов с портальной гипертензией можно обнаружить сеть коллатералей, варикозно-расширенные вены.
Чувствительность, специфичность и точность метода составляет 100, 98 и 99% соответственно. С помощью этого исследования можно изучать состояние паренхимы печени (с целью выявления злокачественных опухолей); выявлять нарушения кровотока в системе портальной и печеночной вен (с целью решения вопроса о целесообразности хирургического лечения и для выбора необходимого метода). Кроме того, можно обнаружить коллатеральное кровообращение. Можно отдифференцировать причины тромбоза: кровяной тромб дает более интенсивное окрашивание при введении гадолиния, чем обструкция сосуда опухолью.
Остро возникший тромб (давностью менее 5-недельной) визуализируется как участок повышенной плотности в просвете портальной вены.
Ангиография.
Биопсия печени.
При наличии цирроза и злокачественных новообразований у пациента гистологическая картина биоптатов печени характерна для этих заболеваний.
У пациентов с тромбозом или обструкцией портальной вены, не страдающих циррозом и онкозаболеваниями, в биоптатах печени может не быть специфических изменений.
Лабораторная диагностика
У пациентов без цирроза печени и злокачественных новообразований может отмечаться незначительное увеличение показателей функции печени.
Дифференциальный диагноз
Дифференциальный диагноз тромбоза портальной вены проводится со следующими заболеваниями:
Воротная вена
Поражения воротной вены
Выделяют следующие виды патологий.
Портальная гипертензия. Данное заболевание характеризуется увеличением внутреннего давления в воротной вене. Причинами развития данной патологии могут быть вирусные гепатиты, печеночный цирроз, нарушения обменных процессов, тяжелые сердечные заболевания, тромбы печеночных, селезеночных вен и другие. Симптоматика выражена диспепсией, снижением веса, тяжестью в правом подреберье, общей слабостью.
Тромбоз. Данная тяжелая патология развивается при формировании кровяных сгустков в просвете воротной вены, препятствующих оттоку крови. Основными причинами развития тромбоза являются следующие: воспаление и злокачественные образования органов пищеварения, травмы печени, желчного пузыря, селезенки, аномалии свертываемости крови, цирроз, различные инфекции и другие. Патология проявляется болевыми ощущениями в области живота, тошнотой с последующей рвотой, повышением температуры, диспепсическим синдромом и другими симптомами.
Кавернозная трансформация. Заболевание характеризуется образованием сосудистых полостей (каверном), заполненных кровью, и развивается вследствие генетического порока формирования вен, заключающегося в их значительном сужении, частичном или полном отсутствии. Кавернозная трансформация является врожденной аномалией. Если она не была выявлена в детстве, то обнаруженная в зрелом возрасте указывает на прогрессирующую портальную гипертензию, вызванную гепатитом или циррозом.
Пилефлебит. Эта патология характеризуется гнойным воспалением воротной вены, спровоцированным перитонитом, возникшим после перенесенного острого аппендицита. Симптомами пилефлебита являются: сильный жар, боли в животе с признаками отравления, желтуха, внутреннее кровоизлияние в венозной области пищевода, желудка и другие.
Диагностика и лечение
Диагностические мероприятия включают в себя следующие этапы и методы: осмотр, сбор анамнеза, ультразвуковое обследование, компьютерную и магнитно-резонансную томографию, портографию. Полученные инструментальными обследованиями данные дополняются показателями анализов крови. Лечение зависит от вида и тяжести поражения, сопутствующих симптоматических патологий и других факторов.
Тромбоз воротной вены ( Пилетромбоз )
Тромбоз воротной вены – это полная или частичная окклюзия ствола воротной вены и ее ветвей тромботическими массами. Патология проявляется абдоминальным синдромом, рвотой, диареей, признаками портальной гипертензии (асцит, спленомегалия, расширение венозных коллатералей), осложняется кровотечением из верхних отделов пищеварительного тракта, инфарктом кишечника и другими состояниями. Основу диагностики составляют методы визуализации – УЗДС, МР- и КТ-ангиография, венография пораженных участков. Лечебная тактика предполагает антикоагулянтную терапию, тромболизис, хирургическую коррекцию.
МКБ-10
Общие сведения
Тромбоз воротной вены (пилетромбоз) считается достаточно редким явлением, риск возникновения которого не превышает 1% в общей популяции. Его распространенность среди пациентов с циррозом печени варьируется от 0,6 до 26%, что, по-видимому, связано с различием в критериях выборки и диагностических методах. Заболевание называют причиной 5–10% случаев портальной гипертензии у жителей развитых стран и до 40% – в азиатском регионе (из-за более высокой частоты инфекционной патологии). Распространенность первичного тромбоза у взрослых и детей одинакова. Гендерных отличий в развитии болезни не выявлено, кроме цирротической обструкции, чаще диагностируемой у мужчин.
Причины
Заболевание имеет мультифакторную природу. Тромбоз развивается под влиянием системных и локальных нарушений, участвующих в повреждении сосудистой стенки, усилении коагуляции, замедлении венозного кровотока. Среди наиболее значимых причин отмечают следующие:
К другим факторам риска тромбоза воротной вены относят беременность, прием пероральных контрацептивов, гиперхолестеринемию. Отмечена роль внутрибрюшной аденопатии, синдрома системного воспалительного ответа. В детском возрасте окклюзия возникает при врожденных аномалиях сосудистой системы (дефектах межжелудочковой и межпредсердной перегородок, деформации полой вены) и желчевыводящих путей. Причина 10–30% тромботических стенозов остается невыясненной.
Патогенез
Исходя из современных представлений, пилетромбоз является результатом системных коагулопатий (наследственных, приобретенных) и действия локальных факторов. Повреждение стенки сосуда опухолью, инвазивными процедурами или травмами характеризуется выработкой цитокинов, активацией тромбоксана A2 и тромбина, усилением адгезии и агрегации тромбоцитов. Венозный застой при наружной компрессии сопровождается гипоксией эндотелия, накоплением активированных факторов свертывания. Все это запускает формирование пристеночного кровяного сгустка с дальнейшим его увеличением.
Сосудистая окклюзия сопровождается портальной гипертензией, что ведет к изменению системной и внутриорганной гемодинамики. Печень теряет около 2/3 своего кровоснабжения, но это компенсируется дилатацией печеночной артерии и быстрым развитием сети коллатералей. Вокруг тромбированной вены формируется кавернома, а сама она превращается в фиброзный тяж. Новообразованные сосуды расположены в пределах желчных протоков и пузыря, поджелудочной железы, антрального отдела желудка, двенадцатиперстной кишки.
Патогенез тромбоза при печеночном циррозе до конца не ясен. Важное значение отводят портальной гипертензии с замедлением кровотока по воротной вене, периферическому лимфангииту, перипортальному фиброзу. Системное шунтирование крови провоцирует гемосидероз, гепатоциты в зонах гипоперфузии подвергаются апоптозу. В тонком и толстом кишечнике выше уровня окклюзии определяются застойные явления, в желудке – гастропатия. Брыжеечная ишемия может привести к переходу тромботического процесса на мезентериальные сегменты.
Классификация
Формальной классификации тромбоза воротной вены не существует. Согласно клиническим рекомендациям по портальной гипертензии, при постановке диагноза учитывают участок тромбоза и его проявления, наличие и характер основного заболевания, степень окклюзии (частичную, полную), вовлеченность внепеченочных сегментов. В зависимости от локализации тромба различают несколько форм патологии:
Представленная классификация позволяет оценить последствия тромботической обструкции и трудоспособность пациента. При поражении сначала интерстициальных сосудов, а затем крупных стволов констатируют восходящий (первичный) процесс. Мезентериальный тромбоз, возникающий из-за обструкции воротной или селезеночной вен, называют нисходящим (вторичным). В клинической флебологии также различают острую, подострую и хроническую стадии, последовательно сменяющие друг друга.
Симптомы
Клиническая картина тромбоза воротной вены определяется происхождением, степенью, протяженностью, локализацией, темпами нарастания окклюзии, выраженностью коллатералей. Частичное тромбирование протекает бессимптомно, выявляясь лишь при инструментальной диагностике, полной обструкции (90–100% просвета) присуще бурное развитие за несколько суток. Подострая форма прогрессирует на протяжении 4–6 недель, а хронический процесс характеризуется медленным нарастанием симптоматики (от нескольких месяцев до года).
Стволовой тромбоз
Острый стволовой пилетромбоз проявляется резкими болями в правом подреберье и эпигастрии, сочетающимися с метеоризмом, частой рвотой, диареей (нередко с примесью крови). Быстро нарастают признаки портальной гипертензии – расширение подкожных, пищеводных, геморроидальных вен, асцит. Зачастую выявляют желтуху, недостаточность печеночной функции. Общее состояние пациентов быстро становится тяжелым, что в основном обусловлено рецидивирующими кровотечениями из желудочно-кишечного тракта.
Радикулярный тромбоз
Радикулярный тромбоз на уровне селезеночного сегмента начинается остро, с боли в левом подреберье, кровавой рвоты и дегтеобразного стула. Увеличение селезенки и субфебрильная лихорадка сочетаются с обычными размерами печени. В подостром периоде постепенно нарастают спленомегалия, асцит, расширяется венозная сеть на животе. Терминальная форма патологии выявляется только при распространенном поражении – у таких пациентов обычно определяют увеличенную селезенку, широкие подкожные коллатерали.
Хронический тромбоз
Хронический пилетромбоз не имеет специфических проявлений. Отсутствие аппетита и общая слабость – иногда единственные симптомы болезни. У большинства пациентов выявляют подкожные анастомозы, умеренный асцит. В 20–40% случаев патология манифестирует кровотечением из варикозных расширений пищевода. Вялотекущие варианты тромбоза воротной вены характеризуются нерезким болевым синдромом, субфебрилитетом, чувствительностью печении при пальпации. Отмечаются спленомегалия с признаками гиперспленизма, тяжестью в подреберье, исхуданием.
Осложнения
Наиболее опасное следствие острой окклюзии мезентериальных сосудов – инфаркт кишечника с развитием перитонита и полиорганной недостаточности (характерно для 5% случаев). Большинство осложнений длительного пилетромбоза обусловлено портальной гипертензией. Расширение пищеводных вен у многих пациентов сопровождается кровотечением, риск которого в 100 раз выше при циррозе печени. Выраженное портосистемное шунтирование приводит к печеночной энцефалопатии, вторичным изменениям в желчевыводящих путях (портальной билиопатии, холангиопатии). При сохраняющихся факторах риска тромбозы могут рецидивировать, осложняться эмболизацией.
Диагностика
Отсутствие специфических признаков тромбоза, необходимость определения предпосылок, уровня, степени и последствий поражения создают потребность в комплексном обследовании пациента. Основой диагностической программы выступают методы инструментальной визуализации:
Проводя диагностику пилетромбоза, врачи-флебологи обращают внимание на показатели коагулограммы (увеличение фибриногена, протромбинового индекса, замедление времени свертывания крови), низкий уровень антитромбина. Выявить варикозно-расширенные вены пищевода позволяет ФГДС, исключить цирроз удается благодаря эластографии и биопсии печени. Дифференциальная диагностика осуществляется с печеночным шистосомозом, тромбозом нижней полой вены, сдавливающим перикардитом, рестриктивной кардиомиопатией.
Лечение тромбоза воротной вены
Задачами лечебной коррекции являются восстановление проходимости сосуда, предотвращение прогрессирования патологии, устранение осложнений венозной гипертензии. Исходя из остроты процесса, возраста пациента, этиологических и прочих факторов, применяют комбинацию консервативных и радикальных методов:
Варикозные расширения пищевода лечат с помощью лигирования, эндоскопической склеротерапии. В ургентных ситуациях при кровотечении могут производить операции азигопортального разобщения (гастротомию с прошиванием нижней трети пищевода, деваскуляризацию желудка). Тяжелый гиперспленизм требует спленэктомии.
Прогноз и профилактика
В целом прогноз при заболевании относительно благоприятный. Сгустки могут подвергаться асептическому аутолизу, организации, васкуляризации. Десятилетняя выживаемость для взрослых достигает 60%, а общий уровень смертности составляет менее 10%. При наличии цирроза и злокачественных новообразований прогноз ухудшается. Иногда тромбы превращаются в эмболы, становятся источником сепсиса. Но своевременное и интенсивное лечение приводит к реканализации сосуда, что сопровождается полным клиническим выздоровлением. Профилактика рецидивов проводится путем назначения антикоагулянтов.
Что такое тромбоз воротной вены
Тромбоз воротной вены: этиология, диагностика и особенности лечения
Российский научный центр хирургии им. академика Б.В.Петровского РАМН Гематологический научный центр, г. Москва
Ключевые слова: тромбоз воротной вены, этиология, диагностика, лечение
Key words: portal vein thrombosis, etiology, diagnosis, treatment
Тромбоз воротной вены: этиология, диагностика и особенности лечения
Portal vein thrombosis: etiology, diagnosis, and treatment characteristics
А.ГШЕРЦИНГЕР, Е.А.КИЦЕНКО, Е.Д.ЛЮБИВЫЙ, Е.Е.ФАНДЕЕВ, Е.П.СЫСОЕВА
A.G.SHERTSINGER, E.A.KITSENKO, E.D.LYUBIVY, E.E.FANDEYEV, E.P.SYSOEVA
Этиология

состояний этиологический спектр для данного заболе-вания с годами заметно увеличился. В таблице 1 пере-числены основные этиологические факторы развития ТВВ. Все эти состояния у конкретного пациента могут встречаться как поодиночке, так и в различных комби-нациях; при этом большинство системных факторов не имеют никаких клинических проявлений даже на момент обнаружения ТВВ и развития его осложнений [6, 7, 15, 21, 23, 25, 30, 36]. Несмотря на внушительный перечень этиологических факторов, значительные со-временные диагностические возможности, причина 10-30% наблюдений ТВВ остаётся неизвестной [1, 5, 6, 7, 9, 17, 20, 21, 23, 28].
Среди приобретённых системных тромбофилий первое место занимают хронические миелопролифера- тивные заболевания (ХМПЗ), составляя в этой группе от 35 до 55% [10-12, 20, 23, 28, 30-34, 39]. Критериями постановки такого диагноза служат трепанобиопсия красного костного мозга, а также анализ крови на му-тацию V617F в гене фермента Янус-киназы 2 (JAK 2) [36, 72, 73]. Эта группа болезней системы крови дли-тельное время протекает бессимптомно и осложнения ТВВ нередко являются первым проявлением указанной патологии. В исследовании Valla et al. (1988) пока-зано, что латентная форма ХМПЗ была обнаружена у 58% больных ТВВ, при этом 51% из них диагноз ХМПЗ был поставлен в отдалённый период наблюдения [34].
Другими, менее частыми приобретёнными при-чинами портального тромбоза выступают пароксиз-мальная ночная гемоглобинурия, антифосфолипидный синдром и др. [20, 22, 24, 35].
Врождённые системные факторы ТВВ, такие как дефицит естественных антикоагулянтов (антитромбин, протеины C и S), мутации генов II и V факторов свертывания, метилентетрагидрофолатредуктызы (МТГФР) также выступают инициаторами тромбоза у данной категории больных с различной частотой [6, 7, 8, 20-23, 25, 30-33, 36-39, 74]. Сравнительно недавно обнаружена ещё одна мутация в гене активируемого тромбином ингибитора фибринолиза (TAFI) [24, 41, 42].
Необходимо также сказать, что ЦП, синдром Бад- да-Киари, гепатоцеллюлярная карцинома и онкологи-ческие заболевания других органов, трансплантация печени, несомненно, являются факторами риска тром-боза портальной системы, но заслуживают отдельного внимания и, как уже было сказано, не являются темой данной статьи.
Клиническая картина и диагностика
В зависимости от срока возникновения ТВВ принято разделять на острый (ОТВВ) и хронический (ХТВВ). Отличие их заключается в том, что при остром тромбозе морфологические проявления синдрома пор-тальной гипертензии (ПГ) (развитие портопортальных, портосистемных коллатералей, спленомегалия и др.) незначительны или могут отсутствовать. ХТВВ характеризуется кавернозной трансформацией ворот-ной вены (формированием т. н. «портальной кавер-номы») [15]. Данный процесс, по некоторым данным, занимает от 3 до 5 недель [43, 44]. Проявляется ХТВВ уже развёрнутой картиной ПГ и её осложнениями, главным образом, кровотечением из ВРВ пищевода и желудка. Данный факт определяет уникальность таких больных: одновременная склонность к тромбозам и кровотечениям [1, 6, 7, 10, 12, 45].
Острый тромбоз воротной вены
ОТВВ характеризуется наличием болей в животе, появляющихся, как правило, внезапно; а также симптомами, характерными для ишемии кишечника. Однако, наиболее часто острый эпизод тромбоза, либо вообще протекает бессимптомно, либо сопровождается незначительными проявлениями и остаётся недиа-гностированным вплоть до развития осложнений ПГ [15, 17, 20, 22, 24, 35, 38]. Клинические проявления дан-ного варианта, возможно, связаны со скоростью раз-вития и протяжённостью самого тромбоза [46]. В слу-чае симптоматического течения основными жалобами больных являются боли в верхних отделах живота без чёткой локализации, субфебрильная лихорадка, сопровождаемые диспепсическими явлениями, такими как тошнота, рвота, диарея, чувство переполненности желудка, вздутие живота, общее недомогание и т. д. [20, 28, 40]. При поражении брыжеечных сосудов могут появляться симптомы мезентериальной ишемии, вплоть до развития инфаркта кишки и кишечной не-проходимости [22, 24, 35]. К счастью, такой сценарий наблюдается в небольшом количестве наблюдений (5%). Примерно у трети пациентов обнаруживается спленомегалия и незначительный асцит [28].
Клиническое обследование должно включать в себя, прежде всего, ультразвуковое допплерографиче-ское исследование (УЗДГ), по данным которого выяв-ляется наличие тромботических масс в просвете ВВ, её ветвей и/или притоков, отсутствие цветного доп-плеровского сигнала в просвете ВВ при отсутствии сформированной портальной каверномы [15, 20, 22, 24, 35, 40].
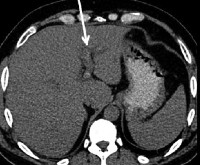
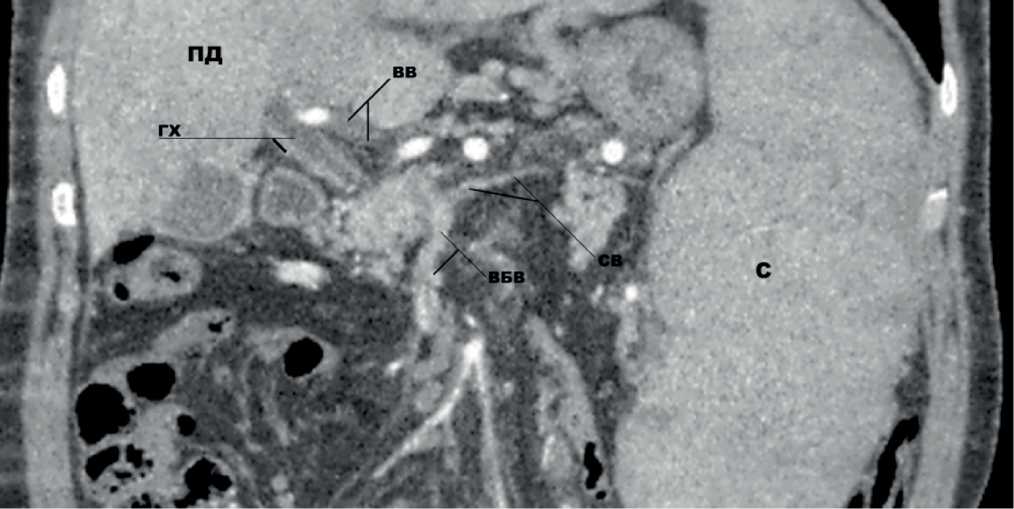
При выполнении компьютерной (КТ) или магнитнорезонансной ангиографии (МРТ) наблюдается дефект контрастирования в просвете ВВ (рис. 1), повышенное наполнение печени в артериальную фазу [15, 47, 57, 58]. Данные исследования, хотя и имеют второстепенное значение, но помогают, во-первых, определить протяжённость тромбоза, а во-вторых, верифицировать инфаркт кишечника, если таковой имеет место [20, 24, 47].
Роль инвазивных методов исследования порталь-ной системы, таких как спленопортография и др. в на-стоящее время отходит на второй план ввиду высокого разрешения получаемых при КТ и МР-ангиографии изображений, а также возможности последующего 3D-моделирования сосудов.
Всем пациентам с ОТВВ также необходимо вы-полнять эзофагогастродуоденоскопию (ЭГДС) [15, 20, 24]. Это позволяет провести дифференциальный диа-гноз с ХТВВ (отсутствие ВРВ пищевода и желудка); кроме того, существуют данные, что одновременное наличие у больного ОТВВ и портальной гастропатии более характерно для ЦП или онкологического про-цесса [17, 37, 40].
Хронический тромбоз воротной вены
Так как зачастую эпизод ТВВ протекает бессим-птомно, это заболевание диагностируется на поздних стадиях: либо когда развиваются осложнения, свя-занные с ПГ (пищеводно-желудочные кровотечения, спленомегалия, тромбоцитопения и, редко, желтуха), либо как случайная находка при обследовании боль-ного по другому поводу [15, 22, 24, 35].
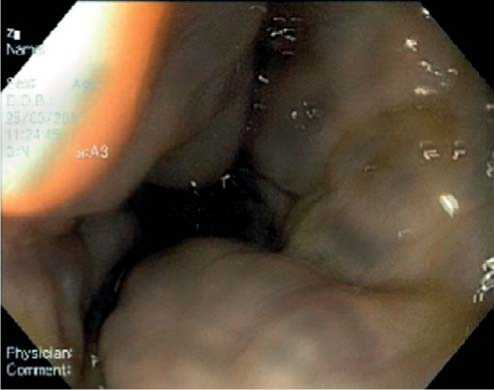
Рис. 2. Эндоскопическая картина ВРВ пищевода при тромбозе воротной вены
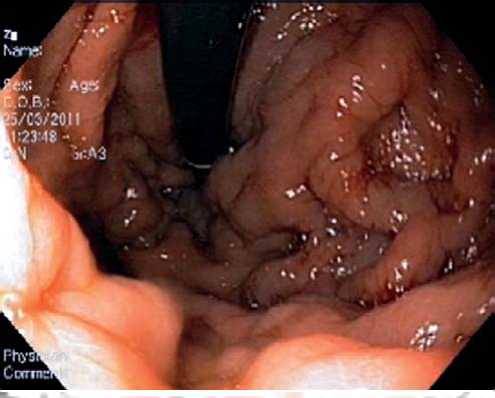
Рис. 3. Эндоскопическая картина ВРВ желудка при тромбозе воротной вены
Наряду с неспецифическими проявлениями, важ-ными клиническими симптомами являются спленоме- галия (нередко достигающая гигантских размеров), а также симптомы анемии и/или гипербилирубинемии (при их наличии) [20]. Набор инструментальных мето-дов исследования, так же как и в случае ОТВВ, вклю-чает в себя УЗДГ, КТ или МР-ангиографию, ЭГДС. Последняя обнаруживает ВРВ пищевода и желудка, при этом они часто имеют большой диаметр и распростра-няются на весь пищевод (рис. 2), начиная от его верх-ней трети; переходят на кардию, тело и дно желудка (рис. 3) [6, 7, 10, 13, 14, 25, 44, 50]. Наличие эктопиче-ских ВРВ (в двенадцатиперстной кишке, аноректаль-ной зоне, ложе желчного пузыря) более характерно для данной группы пациентов, чем для больных ЦП [53, 54].
Также немаловажным является обнаружение признаков так называемой «портальной билиопатии (ПБ)»: деформация, стриктуры, стенозы, формирование конкрементов билиарного дерева, ВРВ стенки желчного пузыря, его ложа, стенок холедоха и т. д., вы-званной ишемией желчевыводящих путей, а также их деформацией портальными коллатералями. ПБ обычно протекает бессимптомно, но иногда проявляется признаками билиарной гипертензии [48, 51, 55].
Умеренный асцит, если и возникает у таких боль-ных, то, как правило, после действия триггерного фак-тора, такого как кровотечение из ВРВ или инфекция. При этом он, либо ликвидируется спонтанно, либо легко поддаётся диуретической терапии [17, 20, 40, 56].
Печёночная энцефалопатия, связанная с форми-рованием спонтанных портосистемных коллатералей или после шунтирующих операций развивается крайне редко, имеет субклинические проявления и практи-чески никогда не влияет на качество жизни больных [57].
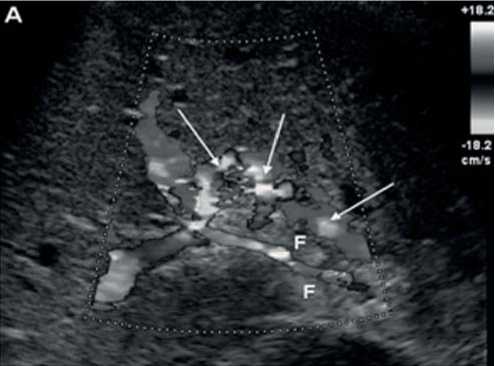
Рис. 4. Ультразвуковая допплерограмма больного с хроническим тромбозом воротной вены: представлены сеть коллатеральных сосудов (стрелки) и фиброз (F) в области воротной вены [35].
Биопсия печени позволяет исключить хрониче-ские паренхиматозные заболевания печени. При мор-фологическом исследовании печени при ТВВ никаких специфических изменений не наблюдается. Как прави-ло, они включают в себя комплекс атрофических из-менений и нодулярную регенераторную гиперплазию паренхимы [1, 2, 58].
Лечение и прогноз
Основные цели лечения направлены на ликви-дацию тромбоза (если это возможно) или предотвра-щение его рецидива и распространения, а также на
борьбу с осложнениями портальной гипертензии ( при ХТВВ) [15, 22, 24, 35].
В случае острого тромбоза наиболее эффектив-ным способом лечения является как можно более ран-нее назначение антикоагулянтной терапии (АКТ) [15, 17-22, 28, 29, 35, 39, 40, 46, 59, 60, 63]. Частота спонтанной полной реканализации при ТВВ ничтожно мала [22, 24, 28, 35], тогда как при раннем начале АКТ (в течение первого месяца после тромбоза) полная реканализация отмечена, по разным данным, в 35-45,4% наблюдений [28, 39, 59]. Согласно Международному консенсусу по портальной гипертензии Baveno V (2010 г.), длительность АКТ (низкомолекулярные гепарины с последующим переходом на оральные антикоагулянты) у таких больных должна составлять, по меньшей мере, 3 месяца (до 6 месяцев, т. к. в этот период наблюдается реканализация тромба); а у лиц, страдающих различными видами тромбофилий, может обсуждаться вопрос о пожизненной АКТ [15]. При присоединении инфекции в остром периоде следует назначать антибактериальную терапию [15, 17].
Кроме того, существуют несколько исследований небольших групп пациентов с применением локальной тромболитической терапии (препаратами урокиназы, стрептокиназы и рекомбинантного тканевого актива-тора плазминогена). И хотя процент той или иной сте-пени реканализации отмечен у 85% больных, тяжёлые осложнения, в том числе, массивные кровотечения, наблюдались у 60% пациентов[24, 59, 60]. Это застави-ло практически отказаться от данного вида лечения и отдать предпочтение более консервативным методам. Аналогично широкого распространения не получила и тромбэктомия. Положительный эффект этой мани-пуляции нивелируется, во-первых, частым развитием осложнений этого вмешательства, а во-вторых, данная процедура сама по себе может провоцировать рецидив ТВВ [61, 62].
Однозначного мнения по поводу АКТ у больных ХТВВ на данный момент не существует ввиду недо-статочного количества проведённых исследований [15, 63]. АКТ у данной категории больных направлена на профилактику рецидива и распространения тромбоза портальной системы. В исследовании Condat et al. было показано, что при должных мерах первичной и вторичной профилактики кровотечений из ВРВ пище-вода и желудка, АКТ не вызывает повышение риска и не усугубляет тяжесть варикозных кровотечений [46]. Вопрос длительности проведения АКТ у таких боль-ных должен решаться в индивидуальном порядке, но при выявлении тромбофилий у больных ХТВВ, реци-дивирующих тромбозах, семейном характере заболе-вания необходимо обсуждать вопрос пожизненной АКТ [6, 7, 15, 46, 63].
В настоящее время данные о проведенных иссле-дованиях в области первичной профилактики кровоте-чений из ВРВ недостаточно, поэтому тактика в данном случае идентична таковой при циррозе печени [15]. С этой целью используется фармакологическая терапия и эндоскопические методы лечения отдельно или в со-четании друг с другом [15, 20, 22, 24, 63].
Тактика при продолжающемся кровотечении сво-дится к использованию эндоскопического лечения и баллонной тампонады. Баллонная тампонада ВРВ зон-дом-обтуратором Блекмора способна лишь временно обеспечить гемостаз. Тем не менее, это позволяет ком-пенсировать геморрагический шок, даёт возможность подготовить больного к более радикальным манипу-ляциям: хирургическому вмешательству или эндоско-пическому лечению (эндоскопическое лигирование (ЭЛ) варикозных вен и эндоскопическая склеротерапия (ЭС)) [5-7, 10, 13, 64].
В дополнение, комплексное лечение кровотече-ния должно, помимо адекватного восполнения ОЦК с использованием, при необходимости, компонентов крови и кровезаменителей, включать в себя и про-филактическое назначение антибиотиков [15]. Эндо-скопическое лечение показало эффективность, как в острой ситуации, так и в качестве меры вторичной профилактики кровотечений из ВРВ пищевода и же-лудка [5, 9, 13, 14, 65-68]. Сравнительно недавно опу-бликованные данные 2-х исследований из Индии по-казали более высокую эффективность, меньшие число осложнений и интенсивность образовавшихся новых ВРВ в ходе наблюдения после ЭЛ, по сравнению с ЭС [69, 70]. Использование неселективных р-блокаторов отдельно или в сочетании с эндоскопическим лечением также снижает риск повторных кровотечений у таких больных [46, 65, 71].
Шунтирующие операции являются наиболее ра-дикальным способом лечения, фактически избавля-ющим человека от ПГ, проявлений гиперспленизма, портальной билиопатии [1-7, 10, 22, 24, 35, 72-74, 77-80]. Однако ограничивает использование данных операций тот факт, что тромбоз зачастую распространяется на селезёночную и верхнюю брыжеечную вены (37%) [74], поэтому у таких больных выполнить шунтирование технически не представляется возможным [1, 2, 4, 5, 7, 10, 20, 2, 24]. По данным зарубежных авторов, в настоящее время операции портокавального шунтирования, как правило, применяются при неэффективности консервативных и эндоскопических методов лечения [15, 20, 24, 63, 75, 76]. Наиболее целесообразным явля-ется селективное дистальное спленоренальное, мезен- терикокавальное шунтирование «бок в бок» или «Н»- типа с интерпозицией синтетического протеза [1-7, 10, 19, 22, 35, 77]. Мезентерикопортальное шунтирование является более физиологичным, но выполнимо (так называемый «Rex-шунт»), в основном, в педиатриче-ской практике [20, 22, 24, 35, 63, 75-81]. Применение данного пособия у взрослых (в т. ч. с использованием аутовенозной вставки), хотя и описано в ряде исследо-ваний [75, 76, 79], тем не менее, требует дальнейшего изучения [35, 63, 75-79, 80].
В исследовании Senzolo et al. (2006) была пока-зана эффективность трансъюгулярного внутрипече-ночного портосистемного шунтирования (TIPS) при лечении больных с тотальным ТВВ. Данная процедура выполнялась 23 пациентам. Успешность метода была отмечена в 73% наблюдений, включая 6 из 9 больных с кавернозной трансформацией ВВ [61].
Операции азигопортального разобщения, такие как деваскуляризация желудка, гастротомия с проши-ванием ВРВ нижней трети пищевода и желудка (опера-ция М. Д. Пациоры), по настоящее время не утратили своего значения, главным образом, в ургентных си-туациях, т. к. позволяют справиться с кровотечением при неэффективности других способов лечения. Хотя, несомненно стоит сказать, что подобные операции не избавляют пациента от ПГ и повторного образования ВРВ [1-7, 10, 80].
Ограничено в настоящее время и использование спленэктомии для коррекции ПГ. Применение оправдано лишь в случае тяжело протекающего ги- перспленизма [1, 74]. Наряду с паллиативностью этого вмешательства, данная операция лишает больного возможности выполнить ему в дальнейшем сплено-ренальное шунтирование; более того, при ХМПЗ па-ренхима селезёнки является очагом экстрамедулляр-ного кроветворения и её удаление может привести к фатальным последствиям [74]. Стоит добавить, что у больных с ХМПЗ как в до-, так и в послеоперационном периодах целесообразно проводить специфическую
Список литературы
1. Ерамишанцев А.К. Первичная внепеченочная портальная гипертензия и её хирургическое лечение. Дисс. докт. мед. наук. М. 1983; 325.
2. Ерамишанцев А.К., Лебезев В.М. Эволюция хирургии внепеченочной портальной гипертензии. Хирургия. 1998; 6: 29-32.
3. Ерамишанцев А.К., ЛебезевВ.М., Шерцингер А.Г., Цаца- ниди К.Н. Переоценка взглядов на сосудистые портока- вальные анастомозы в хирургии портальной гипертензии. Хирургия. 1991; 6: 78-82.
4. Пациора М.Д., Ерамишанцев А.К. Хирургия внепече-ночной портальной гипертензии. Хирургия. 1977; 6: 52-58.
5. Киценко Е.А. Прямые вмешательства на варикозно рас-ширенных венах пищевода и желудка у больных с вне-печеночной портальной гипертензией. Дисс. докт. мед. наук. М. 2004; 215.
6. Киценко Е.А., Любивый Е.Д., Лукина Е.А., Коршунов И.Б. Тромбофилия как причина внепеченочной портальной гипертензии. Анналы хирургической гепатологии. 2007; 12: 2: 26-30.
7. КиценкоЕ.А., Лукина Е.А., ДемьяновА.И., Любивый Е.Д., Сысоева Е.П., Дмитренко Е.В., Фандеев Е.Е. Результаты лечения кровотечений из варикозно расширенных вен пищевода и желудка у больных с внепеченочной портальной гипертензией и хроническими миелопро- лиферативными заболеваниями. Вестник хирургической гастроэнтерологии. 2011; 1: 33-42.
циторедуктивную терапию совместно со специалиста- ми-гематологами; это значительно улучшает результа-ты их лечения и дальнейший прогноз [6, 7, 10, 33, 34, 45].
Несмотря на тяжесть осложнений ПГ, прогноз у данной категории больных остаётся относительно благоприятным: 5- летняя выживаемость у них при адекватном лечении и профилактике достигает 8595% [10, 17, 18, 20-22, 24, 33, 40, 76, 81]. Летальность у таких больных, как правило, связана с сопутствую-щими заболеваниями, а не с осложнениями ПГ [16, 21, 24, 39, 76, 81].
ТВВ является относительно редким полиэтиоло-гическим заболеванием. Ввиду преобладания неспец-ифической симптоматики на момент своего возникно-вения, болезнь часто остается незамеченной вплоть до развития синдрома ПГ и её тяжелых, угрожающих жизни осложнений. Однако при должной насторо-женности клинициста, достаточном техническом ос-нащении лечебного учреждения, диагностика ТВВ не представляет больших сложностей. Вместе с тем, немедленное начало адекватного лечения при раннем обнаружении данной патологии дает шанс полностью исцелить больного или, по крайней мере, предотвра-тить прогрессирование заболевания и развитие серьез-ных осложнений, в частности, кровотечений из вари-козных вен пищевода и желудка.
8. Зубаиров Д.М. Врожденная тромбофилия. Соросовский образовательный журнал. 1997; 8: 33-37.
9. Сенько В.В., Калинин Е.Ю., Распереза Д.В. Внепеченочная портальная гипертензия: оптимизация подходов к лечению. Вестник Санкт-Петербургского университета. Серия 11. 2008. Прил. к вып. 1: 155-157.
10. Дмитренко Е.В. Лечение и профилактика кровотечений из варикозно расширенных вен пищевода и желудка у больных с внепеченочной портальной гипертензией и заболеваниями системы крови. Дисс. канд. мед. наук. М. 2009; 158.
11. Боровков Н.Н., Волкова С.А., Евдокимова Н.М., Лебедева А.И. Болезни системы крови: механизмы развития, диагностические критерии и принципы терапии. Ниж. Новгород. 2002; 141.
12. Воробьев А.И. Руководство по гематологии. 4-е изд. М.: Ньюдиамед. 2007; 1275.
13. Жигалова С.Б. Эндоскопические технологии в лечение и профилактике кровотечений из варикозно расширенных вен пищевода и желудка у больных с портальной гипертензией. Дисс. докт. мед. наук. М. 2011; 300.
14. Шерцингер А.Г., Киценко Е.А. Возможности прогнози-рования возникновения гастроэзофагальных кровоте-чений у больных портальной гипертензией. В кн.: Хи-рургия портальной гипертензии. М. 1984; 152-155.
15. De Franchis R. Revising consensus in portal hypertension: Report ofthe Baveno V consensus workshop on methodology of diagnosis and therapy in portal hypertension. J. Hepatol. 2010; 53: 762-768.
16. Ogren M, Bergqvist D., Bjorck M. et al. Portal vein thrombosis: prevalence, patient characteristics and lifetime risk: a population study based on 23,796 consecutive autopsies. World J Gastroenterol. 2006; 12: 2115-2119.
17. Sarin S.K., Sollano J.D., Chawla Y.K. et al. Members of the APASL Working Party on Portal Hypertension. Consensus on extra-hepatic portal vein obstruction. Liver Int. 2006; 26: 512-519.
18. Valla D.C., Condat B., Lebrec D. Spectrum of portal vein thrombosis in the West. J Gastroenterol Hepatol. 2002; 17: 3: 224-227.
19. Wang J.T., Zhao H.Y., Liu Y.L. Portal vein thrombosis. Hepatobiliary Pancreat Dis Int. 2005; 4: 515-518.
20. Ponziani F.R., Zocco M.A., Campanale C., Rinninella E. et al. Portal vein thrombosis: Insight into physiology, diagnosis, and treatment. World J Gastroenterol. 2010 14; 16: 2: 143-155.
21. Janssen H.L., Wijnhoud A., Haagsma E.B. et al. Extrahepatic portal vein thrombosis: aetiology and determinants of survival. Gut. 2001; 49: 720-724.
22. Chawla Y., Duseja A., Dhiman R.K. Review article: the modern management of portal vein thrombosis. Aliment Pharmacol Ther. 2009; 30: 881-894.
23. Garcia-Pagan J.C., Hernandes-Guerra M., Bosch J. Extrahepatic portal vein thrombosis. Semin Liver Dis. 2008; 28: 282-292.
24. Primignani M., Martinelli I., Bucciarelli P. et al. Risk factors for thrombophilia in extrahepatic portal vein obstruction. Hepatology. 2005; 41: 3: 603-608.
25. Rosendaal F.R. Venous thrombosis: a multicausal disease. Lancet. 1999; 353: 9159: 1167-1173.
26. Fujita F., Lyass S., Otsuka K. et al. Portal vein thrombosis following splenectomy: identification of risk factors. Am Surg. 2003; 69: 951-956.
27. Bick R.L. Coagulation abnormalities in malignancy: a review. Semin Thromb Hemost. 1992; 18: 4: 353-372.
28. Plessier A., Murad S.D., Hernandez-Guerra M. et al. A prospective multicentric follow-up study on 105 patients with acute portal vein thrombosis (PVT): results from the European Network for Vascular Disorders of the Liver (EN- VIE). Hepatology. 2007; 46: 1: 310.
29. Murad S.D., Valla D.C., de Groen P.C. et al. Pathogenesis and treatment of Budd-Chiari syndrome combined with portal vein thrombosis. Am J Gastroenterol 2006; 101: 1: 83-90.
30. Bombeli T., Basic A., Fehr J. Prevalence of hereditary thrombophilia in patients with thrombosis in different venous systems. Am J Hematol. 2002; 70: 126-132.
31. Bhattacharyya M., Makharia G., Kannan M. et al. Inherited prothrombotic defects in Budd-Chiari syndrome and portal vein thrombosis: a study from North India. Am J Clin Pathol. 2004; 121: 844-847.
32. Primignani M., Barosi G., Bergamaschi G. et al. Role of the JAK2 mutation in the diagnosis of chronic myeloproliferative disorders in splanchnic vein thrombosis. Hepatology. 2006; 44: 6: 1528-1534.
33. Amitrano L., Guardascione M.A., Scaglione M. et al. Prognostic factors in noncirrhotic patients with splanchnic vein thromboses. Am J Gastroenterol. 2007; 102: 11: 2464-2470.
34. Valla D, Casadevall N., Huisse M.G., Tulliez M, Grange J.D., Muller O., Binda T., VaretB., Rueff B., Benhamou L.P. Etiology of portal vein thrombosis in adults. A prospective evaluation of primary myeloproliferative disorders. Gastroenterology. 1988; 94: 1063-1069.
35. Hoekstra J., Janssen H.L. Vascular liver disorders (II): portal vein thrombosis. Neth J Med. 2009; 67: 46-53.
36. XavierS.G., Gadelha T., Pimenta G., Eugenio A.M., Ribeiro D.D., Gomez F.M., Bonamino M, Zalcberg I.R., Spector N. JAK2V617F Mutation in Patient with Splanchnic Vein Thrombosis. Dig Dis Sci. 2009; E-pub ahead of print.
37. Janssen H.L., Meinardi J.R., Vleggaar F.P. et al. Factor V Leiden mutation, prothrombin gene mutation, and deficiencies in coagulation inhibitors associated with Budd- Chiari syndrome and portal vein thrombosis: results of a case-control study. Blood. 2000; 96: 2364-2368.
38. Denninger M.H., Chait Y., Casadevall N. et al. Cause of portal or hepatic venous thrombosis in adults: the role of multiple concurrent factors. Hepatology. 2000; 31: 3: 587591.
39. Turnes J., Garcia-Pagan JC., Gonzalez M. et al. Portal hypertensive complications after acute portal vein thrombosis: impact of early anticoagulation. Clin Gastroenterol Hepatol. 2008; In press.
40. Sogaard K.K., Astrup L.B., Vilstrup H., GronbaekH. Portal vein thrombosis; risk factors, clinical presentation and treatment. BMC Gastroenterol. 2007; 7: 34.
41. De Bruijne E.L., Murad S.D., de Maat M.P. et al. Liver and Thrombosis Study Group. Genetic variation in thrombin- activatable fibrinolysis inhibitor (TAFI) is associated with the risk of splanchnic vein thrombosis. Thromb Haemost. 2007; 97: 181-185.
42. Martinelli I., Primignani M., Aghemo A. et al. High levels of factor VIII and risk of extra-hepatic portal vein obstruction. J Hepatol. 2009; 50: 916-922.
43. Henderson J.M., Gilmore G.T., Mackay G.J. et al. Hemodynamics during liver transplantation: the interactions between cardiac output and portal venous and hepatic arterial flows. Hepatology. 1992; 16: 715-718.
44. De Gaetano A.M., Lafortune M., Patriquin H. et al. Cavernous transformation of the portal vein: patterns of intrahepatic and splanchnic collateral circulation detected with Doppler sonography. A JR Am J Roentgenol. 1995; 165: 1151-1995.
45. Tefferi A., Thiele J., Orazi A. et al. Proposals and rationale for revision of the World Health Organization diagnostic criteria for polycythemia vera, essential thrombocythemia, and primary myelofibrosis: recommendations from an ad hoc international expert panel. Blood. 2007; 110: 1092-1097.
46. Condat B., Pessione F., Hillaire S. et al. Current outcome of portal vein thrombosis in adults: risk and benefit of anticoagulant therapy. Gastroenterology. 2001; 120: 2: 490-497.
47. Lee H.K., Park S.J., Yi B.H. et al. Portal vein thrombosis: CT features. Abdom Imaging. 2008; 33: 72-79.
48. Dhiman R.K., Puri D., Chawla Y. et al. Biliary changes in extrahepatic portal venous obstruction compression by collaterals or ischemia? Gastrointest Endosc. 1999; 50: 646-652.
49. Doria C., Marino I.R. Acute portal vein thrombosis secondary to donor / recipient portal vein diameter mismatch after orthotopic liver transplantation: a case report. Int Surg. 2003; 88: 184-187.
50. Ganguly S., Sarin S.K., Bhatia V., Lahoti D. The prevalence and spectrum of colonic lesions in patients with cirrhotic and noncirrhotic portal hypertension. Hepatology. 1995; 21: 5: 1226-1231.
51. Condat B., Vilgram V., Asselak T. et al. Portal carvernoma associated holangiopathy a clinical and MR cholangiography coupled with MR portography imaging study. Hepatology. 2003; 37: 1302-1308.
52. Malkhan G.H., Bhatia S.T., Bastin K. et al. Cholangiography associated with portal hypertension diagnostic evaluation and clinical implications. Gastroint Endos. 1999; 49: 344348.
53. Chawla Y., Dilawari J.B. Anorectal varices-their frequency in cirrhotic and non-cirrhotic portal hypertension. Gut. 1991; 32: 3: 309-311.
54. Chawla Y., Dilawari J.B., Katariya S. Gallbladder varices in portal vein thrombosis. AJR Am J Roentgenol. 1994; 162: 3: 643-645.
55. Sezgin O, Oguz D., Altintas E., Saritas U., Sahin B. Endoscopic management of biliary obstruction caused by cavernous transformation of the portal vein. Gastrointest Endosc. 2003; 58: 4: 602-608.
56. Rangari M, Gupta R., Jain M., Malhotra V., Sarin S.K. Hepatic dysfunction in patients with extrahepatic portal venous obstruction. Liver Int. 2003; 23: 6: 434-439. Minguez B, Garcia-Pagan JC., Bosch J. et al. Noncirrhotic portal vein thrombosis exhibits neuropsychological and MR changes consistent with minimal hepatic encephalopathy. Hepatology. 2006; 43: 4: 707-714.
57. Vilgrain V., Condat B., Bureau C. et al. Atrophy-hypertrophy complex in patients with cavernous transformation of the portal vein: CT evaluation. Radiology. 2006; 241: 1: 149155.
58. Condat B, Pessione F., Helcne D.M., Hillaire S., Valla D. Recent portal or mesenteric venous thrombosis: increased recognition and frequent recanalization on anticoagulant therapy. Hepatology. 2000; 32: 3: 466-470.
59. Cwikiel W., Keussen I., Larsson L., Solvig J., Kullendorff CM. Interventional treatment of children with portal hypertension secondary to portal vein occlusion. Eur J Pediatr Surg. 2003; 13: 5: 312-318.
60. Senzolo M, Patch D., Cholongitas E., Burroughs A.K. Transjugular intrahepatic portosystemic shunt for portal vein thrombosis with and without underlying cirrhosis. Cardiovasc Intervent Radiol. 2007; 30: 3: 545.
61. Thervet L., Faulques B., Pissas A. et al. Endoscopic management of obstructive jaundice due to portal cavernoma. Endoscopy. 1993; 25: 6: 423-425.
62. DeLeveLD., VallaD.C., Garcia-Tsao G. Vascular Disorders of the liver. Hepatology. 2009; 49: 1729-1764.
63. Pavini М.Т., Puyana J.C. Gastroesophageal Balloon Tamponade for Acute Variceal Hemorrhage, Irwin’s and Rippe’s Intensive Care Medicine, ed 6th, Ch. 15: 138-145, 2008.
64. Spaander C.W., Murad S.D., van Buuren H.R., Hansen B.E., Kuipers E.J., Janssen H.L. Endoscopic treatment of esophagogastric variceal bleeding in patients with noncirrhotic extrahepatic portal vein thrombosis: a longterm follow-up study. Gastrointest Endosc. 2008; 67: 6: 821-827.
65. Sarin S.K., Sachdev G., Nanda R. Follow-up of patients after variceal eradication. A comparison of patients with cirrhosis, noncirrhotic portal fibrosis, and extrahepatic obstruction. Ann Surg. 1986; 204: 1: 78-82.
67. Chawla Y.K., Dilawari J.B., Ramesh G.N., Kaur U., Mitra S.K., Walia B.N. Sclerotherapy in extrahepatic portal venous obstruction. Gut. 1990; 31: 2: 213-216.
68. Vleggaar F.P., van Buuren H.R., Schalm S.W. Endoscopic sclerotherapy for bleeding oesophagogastric varices secondary to extrahepatic portal vein obstruction in an adult Caucasian population. Eur J Gastroenterol Hepatol. 1998; 10: 1: 81-85.
69. Zargar S.A., Javid G., Khan B.A. et al. Endoscopic ligation compared with sclerotherapy for bleeding esophageal varices in children with extrahepatic portal venous obstruction. Hepatology. 2002; 36: 3: 666-672.
70. Zargar S.A., Javid G., Khan B.A. et al. Endoscopic ligation vs. sclerotherapy in adults with extrahepatic portal venous obstruction: a prospective randomized study. Gastrointest Endosc. 2005; 61: 1: 58-66.
71. Orr D. W., Harrison P.M., Devlin J. et al. Chronic mesenteric venous thrombosis: evaluation and determinants of survival during long-term follow-up. Clin Gastroenterol Hepatol. 2007; 5: l: 80-86.
72. Chait Y., Condat B., Cazals-Hatem D. et al. Relevance of the criteria commonly used to diagnose myeloproliferative disorder in patients with splanchnic vein thrombosis. Br J Haematol. 2005; 129: 553-560.
73. Kiladjian J.J., Cervantes F., Leebeek F.W. et al. The impact of JAK2 and MPL mutations on diagnosis and prognosis of splanchnic vein thrombosis: a report on 241 cases. Blood. 2008; 111: 4922-4929.
74. Wolff M, Hirner A. Current state of portosystemic shunt surgery. Langenbecks Arch Surg. 2003; 388: 141-149.
75. Warren W.D., Henderson J.M., Millikan W.J., Galambos J.T., BryanF.C. Management of variceal bleeding in patients with noncirrhotic portal vein thrombosis. Ann Surg. 1988; 207: 5: 623-634.
76. Orloff M.J., Orloff M.S., Girard B., Orloff S.L. Bleeding esophagogastric varices from extrahepatic portal hypertension: 40 years’ experience with portal-systemic shunt. J Am Coll Surg. 2002; 194: 6: 717-728.
77. Sharma B.C., Singh R.P., Chawla Y.K. et al. Effect of shunt surgery on spleen size, portal pressure and oesophageal varices in patients with non-cirrhotic portal hypertension. J Gastroenterol Hepatol. 1997; 12: 582-584.
78. Query J.A., Sandler A.D., Sharp W.J. Use of autogenous saphenous vein as a conduit for mesenterico-left portal vein bypass. J Pediatr Surg. 2007; 42: 1137-1140.
79. Krebs-Schmitt D., Briem-Richter A., Grabhorn E. et al. Effectiveness of Rex shunt in children with portal hypertension following liver transplantation or with primary portal hypertension. Pediatr Transplant. 2009; 13: 540-544.
80. Superina N., Shneider B., Emre S. et al. Surgical guidelines for the management of extra-hepatic portal vein obstruction. Pediatr Transplant. 2006; 10: 908-913.
81. Sarin S.K., Agarwal S.R. Extrahepatic portal vein obstruction. Semin Liver Dis. 2002; 22: 1: 43-58.
Информация об авторах