Что такое тмо пластика
При интраоперационном выявлении дефекта твердой мозговой оболочки (ТМО) или если консервативные и нехирургические мероприятия в лечении послеоперационно выявленных дефектов оказываются неэффективными, рекомендуется хирургическое лечение. Техники хирургического восстановления дефектов твердой мозговой оболочки (ТМО) варьируют в зависимости от величины дефекта, его сложности и доступности. Простой линейный дефект обычно восстанавливается путем наложения швов — непрерывного или узловых.
Для герметизации линии шва можно дополнительно использовать хирургический клей. Большие дефекты восстанавливают пластикой с использованием пластических материалов в комбинации со швами и/или клеем или без таковых. Сложные дефекты и дефекты, доступ к которым ограничен (например, со стороны передней или боковой поверхности дурального мешка), можно устранить путем наложения заплатки внахлест в сочетании с фибриновым клеем или без него.
а) Шовный материал. Для восстановления твердой мозговой оболочки (ТМО) обычно используется нерассасывающийся шовный материал маленького диаметра на круглой игле. Примерами такого материала являются:
— Нуролон (Ethicon), плетеный нейлон.
— Гор-Текс, монофиламентный материал из политетрафторэтилена (ПТФЭ).
— Пролен (Ethicon), монофиламентный материал из полипропилена.
— Шелк (Ethicon).
Некоторые хирурги отдают предпочтение Гор-Тексу, поскольку диаметр отверстия от иглы при работе с ним меньше диаметра самой нити, что уменьшает риск просачивания ликвора через отверстия от швов. Другие предпочитают шелк, поскольку шелковые нити способствуют формированию на своей поверхности фибринового сгустка, что помогает герметизировать линию шва.
В одном из ретроспективных исследований 338 дефектов твердой мозговой оболочки (ТМО) были эффективно восстановлены с использованием шелкового шовного материала и непрерывного блокированного шва, лишь у 1,8% пациентов после операции вновь отмечено истечение ликвора из дефекта, которое потребовало ревизионного вмешательства.
Перед ушиванием дефекта твердой мозговой оболочки (ТМО) необходимо защитить и погрузить в дефект нередко пролабирующие в него спинномозговые нервы. Для этого необходимо выпустить некоторое количество СМЖ, снизив тем самым интрадуральное давление. Некоторые хирурги считают необходимым перед ушиванием ТМО промыть интрадуральное пространство от возможных гематом, снизив тем самым вероятность ирритации спинномозговых нервов и, возможно, арахноидита.
Основным риском при восстановлении дефекта ТМО является повреждение корешков спинного мозга, поскольку зачастую бывает сложно отличить ткань корешков от ТМО. Для минимизации этого риска рекомендуется использовать операционный микроскоп. После наложения шва для дополнительной его герметизации поверх шва можно поместить гемостатический агент FloSeal (Baxte) или заплатку DuraGen (Integra LifeSciences, Cincinnati, ОН).
б) Материалы для пластики твердой мозговой оболочки (ТМО). Критериев, которым должен отвечать идеальный материал, который можно использовать для пластики твердой мозговой оболочки (ТМО), немало, однако основные из них следующие:
— Возможность герметичного восстановления дефекта твердой мозговой оболочки (ТМО).
— Отсутствие провоспалительных или иммуногенных свойств.
— Отсутствие стимуляции образования спаек со спинным и головным мозгом, оболочками мозга и корешками.
— Отсутствие усугубления риска инфекционных осложнений или кровотечения.
— Механические характеристики, близкие к таковым ТМО.
— Отсутствие значительного изменения объема материала.
— Простота в применении, оптимальное соотношение цены и качества, доступность на рынке
— Отсутствие токсичности и канцерогенности, инертность
В качестве таких пластических материалов применяются различные типы алломатериалов, аутогенные замещающие материалы, синтетические и химически модифицированные ткани. О некоторых из них мы поговорим ниже.
1. Аллотрансплантаты. Трупная ТМО и широкая фасция бедра в качестве материалов для пластики дефектов ТМО в настоящее время не используются ввиду риска переноса возбудителей инфекций, в т.ч. вызывающих болезнь Крейтцфельдта-Якоба. В результате этого был разработан материал AlloDerm (LifeCell, Bridgewater, NJ) — бесклеточная дерма человека, освобожденная от эпидермиса и всех клеточных элементов, которые могли бы стать причиной отторжения трансплантата. Следует, однако, отметить, что каждый донор предварительно обследуется на различные инфекции. Преимущества AlloDerm включают:
— Иммунологическую инертность
— Материал не приводит к формированию спаек и не отторгается
— Ввиду сохранения клеточной ультраструктуры сохраняется возможность врастания сосудов и клеточных элементов
— Простота в применении
— Использование AlloDerm возможно тогда, когда забор аутотрансплантата не представляется возможным.
В одном из исследований AlloDerm был использован при 200 краниотомиях с целью пластики дефектов ТМО, при этом материал фиксировался швами к ТМО или костям черепа. В течение последующего периода наблюдения за пациентами, который составил по меньшей мере один год, лишь в 3,5% случах понадобилось повторное вмешательство, у 1,5% пациентов после операции было отмечено истечение СМЖ, еще у 2% — поверхностные инфекции в области операционной раны.
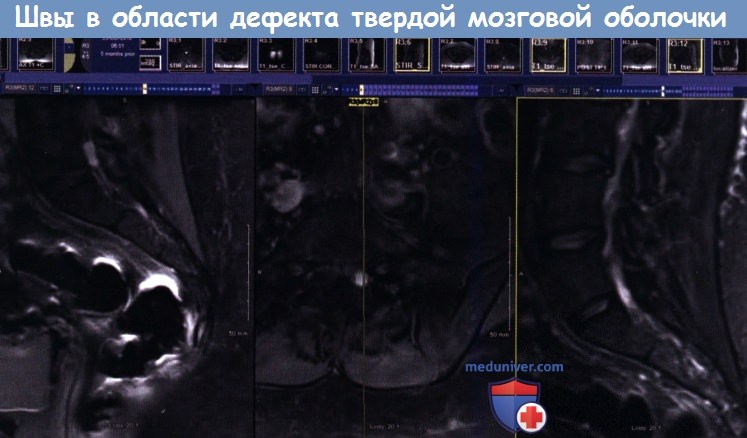
2. Аутогенные замещающие материалы. Эффективным материалом для пластики ТМО является жировая клетчатка — она непроницаема для воды и, как считается, вызывает лишь минимальные рубцовые изменения. Использование для пластики дефекта жировой клетчатки рекомендуется при дефектах, доступ к которым ограничен или невозможен, или при невозможности закрытия с использованием стандартных шовных техник. Аутогенные материалы являются хорошей альтернативой другим материалам, поскольку они 1) нетоксичны, 2) неиммуногенны, 3) не сопряжены с риском инфицирования пациента гемотрансмиссивными инфекциями.
Популярность их, однако, невелика в связи с тем, что приходится выполнять еще один доступ для забора материала. Кроме того, жировую клетчатку бывает сложно герметично фиксировать к дефекту ТМО. Группа исследователей применила эту методику у 27 пациентов, использовав в качестве пластического материала широкий жировой лоскут из подкожной клетчатки, укрыв им и область дефекта, и всю обнаженную в пределах операционного поля ТМО. «Лишними» частями лоскута тампонировались боковые завороты спинномозгового канала для закрытия возможных периферических дефектов ТМО, клетчатка фиксировалась к ТМО швами. Линия швов покрывалась фибриновым клеем, поверх укладывали губку Surgicel или Gelfoam. Операция оказалась эффективной у 96,3% пациентов.
Синтетические или химически модифицированные материалы. К этой группе материалов относят заплатки из растянутого политетрафторэтилена (рПТФЭ), коллагеновые матрицы и трансплантаты из дериватов полимолочной кислоты. Ввиду того, что синтетические пластические материалы довольно значительно отличаются друг от друга, их преимущества и недостатки также будут варьировать. Чаще всего хирурги отдают предпочтение именно синтетическим материалам, поскольку им легко можно придать нужную форму, они достаточно прочны, пластичны и удобны в использовании, они в меньшей степени подвержены деформации и/или некрозу.
В исследовании у 34 пациентов для восстановления дефектов твердой мозговой оболочки (ТМО) был использован рПТФЭ, заплатки из которого фиксировали непрерывными швами. У 14,7% пациентов после операции отмечено небольшое накопление СМЖ в зоне дефекта, а 17,6% в сроки 1-15 месяцев после первичной операции понадобились повторные вмешательства, не связанные с первичным, во время которых установлено, что прочность заплатки из рПТФЭ не изменилась. Между пластинкой рПТФЭ и головным мозгом образовался тонкий слой грануляционной ткани, однако формирования сращений между ним и мягкими тканями черепа, подкожной клетчаткой и тканью головного мозга не отмечено.
Еще в одном исследовании, где для пластики дефектов твердой мозговой оболочки (ТМО) также использовался рПТФЭ, применение которого ограничивалось вшиванием в дефект, частота ликвореи через линию шва составила 20%, и снизилась до 3% после герметизации линии шва фибриновым клеем.
Частота инфекционных осложнений, согласно данным одного из исследований, в которое включены 83 пациента, после пластики дефекта с использованием рПТФЭ, составила 9,6%. Несмотря на такие преимущества рПТФЭ, как его неиммуногенность и минимальное формирование спаек с окружающими тканями, герметичное закрытие дефекта с использованием этого материала достаточно затруднительно.
Примерами коллагеновых матриц и дериватов коллагена, используемых для пластики дефектов твердой мозговой оболочки (ТМО), являются DuraGen, DuraRepair (TEI Biosciences, Boston, MA) и Dura-Guard (Synovis Surgical Innovations, St. Paul, MN). Любой из них можно использовать как накладку или вшиваемый в дефект трансплантат и герметизировать с помощью того или иного хирургического герметика. Пористые коллагеновые трансплантаты, состоящие из коллагеновых волокон 1 типа, представляют собой матрицу, способствующую врастанию сюда кровеносных сосудов и фибробластов. Каждый образец коллагена отличается своими механическими характеристиками и, соответственно, качеством выполняемой с помощью него реконструкции, однако материалы на основе коллагена все же применяются достаточно широко, и этому есть четыре причины. Коллаген:
1) способствует врастанию в образованную им матрицу фибробластов;
2) хорошо покрывает зону дефекта;
3) может использоваться в виде заплатки «внахлест» и
4) обычно не приводит к образованию спаек и не обладает иммуногенностью.
Викрил Коллаген (Ethicon) представляет собой резорбируемую сетку из полиглактина 910 — сополимера гликолида и L-лактида, покрытую бычьим коллагеном. В исследовании, где Викрил Коллаген использовался для пластики дефектов ТМО у 78 пациентов, у 6,4% из них отмечено накопление жидкости в подкожной клетчатке. У четырех пациентов эта проблема разрешилась без дополнительного вмешательства, в одном случае потребовалось люмбоперитонеальное шунтирование.
Кроме того, у 5,1% пациентов развились инфекционные осложнения: у двух — контактный менингит, у одного поверхностная инфекция операционной раны, еще у одного — тяжелая экстрадуральная инфекция, потребовавшая удаления трансплантата.
Хирургам Викрил Коллаген в целом понравился благодаря своей герметичности и биосовместимости, минимальной способности приводить к образованию спаек и способности к резорбции в течение двух месяцев. Быстрая резорбция, однако, может не обеспечивать достаточного количества времени для прорастания собственной фиброзной ткани, особенно в условиях воспалительного процесса, который нарушает целостность формирующегося барьера.
Сомнения относительно спонгиформной энцефалопатии крупного рогатого скота, или «коровьего бешенства», привели к тому, что этот материал во многих странах перестал применятся.
В дополнение к описанным выше синтетическим пластическим материалам в качестве возможных замещающих материалов, которые могут использоваться для пластики ТМО, можно рассматривать и многие другие неаутологичные продукты: Duraform (коллагеновая матрица) и Ethisorb Dura Patch,— резорбируемый материал, состоящий из полиглактина 910 и полидиоксанона (Codman & Shurtleff, Raynham, МА), DuraMatrix (Stryker, Kalamazoo, MI) — коллагеновая матрица, Durasis (Cook Biotech, West Lafayette, IN) — подслизистая оболочка кишечника свиней.
в) Хирургические герметики. Хирургические герметики очень часто применяются при реконструкциях твердой мозговой оболочки (ТМО) для аугментации линии шва и/или замещающих материалов для создания герметичного соединения. Сами по себе они не могут служить альтернативой швам или замещающим материалам. Герметик может использоваться для «склеивания» краев ТМО, он совместим как с нативной ТМО, так и с различными пластическими материалами. Перед применением герметика операционное поле необходимо максимально осушить, истечение СМЖ должно быть устранено.
Наиболее часто используемые герметики имеют в своем составе активные формы фибрина и гидрогель на основе полиэтиленгликоля (ПЭГ).
Для аугментации линии швов ТМО могут применяться активные формы фибрина человеческого или коровьего происхождения. Смешивание раствора фибриногена и других факторов свертывания крови с хлоридом кальция и тромбином ускоряет конверсию фибриногена в фибрин, который адгезируется к тканям организма. Фибриновые герметики можно распылить над операционным полем, нанести в несколько слоев и сформировать с помощью канюли единый слой. Сравнение этих трех методик в гистологических исследованиях in vitro и с использованием теста на давление-сопротивление позволило установить, что наиболее оптимальным является метод распыления.
Фибриновые герметики обладают рядом преимуществ: они 1) обладают свойством адгезии к мягким тканям и помогают сформировать герметичное соединение между ТМО и замещающим ее материалом или швом, 2) запускают процесс коагуляции при минимальном высвобождении медиаторов воспаления, 3) пластичны и просты в применении и 4) доступны на рынке. Кроме того, испытание фибринового клея на животных моделях позволило установить, что он способствует уменьшению выраженности фиброза эпидурального пространства и катализирует запуск реакций коагуляционного каскада.
В исследовании на 20 пациентах, которым восстановление дефектов твердой мозговой оболочки (ТМО) выполнялось путем наложения шва с последующей герметизацией фибриновым клеем, установлено, что у 75% из них после операции истечение СМЖ прекратилось. Одному пациенту понадобилось повторное вмешательство ввиду несостоятельности шва, при этом каких-либо серьезных осложнений не зафиксировано. Еще в одном исследовании не отмечено статистически значимой разницы в отношении послеоперационных рецидивов сброса СМЖ при использовании для аугментации линии шва ТМО фибринового клея и, по усмотрению хирурга, фасциальной или мышечной заплатки (n = 278,50,8%) и реконструкциях, при которых фибриновый клей не использовался (n = 269 или 49,2%).
Сомнения, касающиеся применения фибриновых герметиков, включают временные затраты — на подготовку состава уходит порядка 20 минут, еще 3-5 минут необходимо для нанесения состава и оптимальной его адгезии с мягкими тканями, еще в течение последующих двух часов фибриновый клей должен приобрести «максимальную прочность». Фибриновые герметики могут ингибировать формирование костного блока. Но кроме этого, фибриновый клей, как и любой другой продукт, изготавливаемый из крови, может служить источником заражения гемотрансмиссивными заболеваниями.
Препарат DuraSeal (Covidien, Mansfield, МА) представляет собой резорбируемый ПЭГ-гидрогель, который путем распыления или нанесения используется для герметизации линии шва ТМО. Его преимуществами являются биосовместимость, небиологическая природа (отсутствие риска заражения вирусными инфекциями), резорбируемость, пластичность и способность адгезии к тканям.
Однако Управление по контролю за продуктами питания и медикаментами (FDA) при выдаче разрешения на медицинское применение препарата предупредило, что препарат нельзя использовать там, где рядом с костными образованиями располагаются нервы, поскольку гидрогель после своего применения увеличивается в объеме до 50% во всех доступных ему направлениях, что теоретически может стать причиной сдавления нервных образований. DuraSeal был использован после ушивания ТМО у 111 пациентов с повреждениями ТМО после вмешательств на черепе. Интраоперационная эффективность 1-2 нанесений геля на область шва в отношении его герметизации оказалась 100%.
Однако у 4,5% пациентов в послеоперационном периоде отмечено истечение ликвора (у одного пациента отмечена ликворея из операционной раны, у четырех диагностировано псевдоменингоцеле), еще у 7,2% зарегистрирована глубокая инфекция операционной раны. Еще в одной публикации описана компрессия шейного отдела спинного мозга после применения DuraSeal, в другом сообщении говорилось об усугублении тетрапареза у пациента вследствие увеличения объема использованного гидрогелевого герметика.
Препараты Gelfoam и Surgicel, хотя и не являются герметиками, но, обладая гемостатическими свойствами, нередко применяются в сочетании со швом или пластикой ТМО для повышения качества реконструкции. В исследовании на 88 пациентах с повреждениями ТМО показано, что эффективность применения Gelfoam в дополнение к блокированному шву ТМО с использованием шелкового шовного материала с последующим дренированием субфасциального пространства при первичных реконструктивных вмешательствах составляет 97,7%. Gelfoam также с успехом применялся в сочетании с пластикой жировой клетчаткой и фибриновым клеем.
г) Другие варианты хирургического лечения повреждений твердой мозговой оболочки (ТМО). Преимущества использования титановых непенетрирующих клипс включают:
1) простоту в применении, особенно в зонах, характеризующихся наличием анатомических препятствий,
2) непенетрирующий характер фиксации, что теоретически позволяет уменьшить вероятность рецидива ликвореи в послеоперационном периоде и
3) возможность выполнения МРТ.
В одном из исследований титановые непенетрирующие клипсы были использованы для закрытия дефекта твердой мозговой оболочки (ТМО) у 58 пациентов. Послеоперационная ликворея зафиксирована у 13,8% пациентов, инфекционные осложнения зарегистрированы у 10,3% (у пяти пациентов поверхностная инфекция, у одного — инфекция эпидурального пространства). Группа специалистов, проводивших исследование и впервые знакомившихся с этой системой, предположила, что такая высокая частота осложнений может быть связана с начальным этапом освоения данной методики.
В другое исследование были включены 26 пациентов, которым в течение 20-месячного промежутка времени было выполнено 27 вмешательств, только одному из этих пациентов через 13 месяцев после первичной операции понадобилось повторное вмешательство. В течение последующего периода наблюдения, который составил у разных пациентов от одного до 24 месяцев, каких-либо значимых осложнений не зафиксировано.
Также с целью восстановления целостности твердой мозговой оболочки (ТМО) в качестве как самостоятельного метода, так и как дополнение к традиционным шовным техниками предложена лазерная сварка. Проще говоря, это использование лазера для соединения тканей. Было проведено кадаверное исследование, в котором стандартная шовная техника (n = 25) сравнивалась с шовной техникой в сочетании с лазерной сваркой (n = 25) и с лазерной сваркой, использованной как самостоятельный метод (n = 25). Авторы исследования выявили статистически значимое увеличение давления сброса СМЖ и прочности на разрыв в отношении комбинированного применения швов в сочетании с лазерной сваркой.
Лазерная сварка как самостоятельный метод обеспечивала немедленную герметизацию дефекта ТМО, однако прочность на разрыв сформированного таким образом соединения оказалась очень низкой. Использование лазерной сварки как самостоятельного метода может быть полезно при наличии ограниченного пространства, в условиях которого применение традиционных методов реконструкции ТМО невозможно.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое тмо пластика
При отсутствии герметичности субдурального пространства существует реальная опасность возникновения ликвореи, инфекционных осложнений, развития спаечного процесса и как следствие последнего – эпилептических припадков [1]. Поэтому герметичное закрытие субдурального пространства является задачей первостепенной важности. Пластика твердой мозговой оболочки проводится с протезированием последней небиологическими материалами органической и неорганической природы и тканями биологического происхождения. Некоторые известные способы закрытия дефекта ТМО не всегда выполнимы. Так расщепление оболочки приемлемо при небольших дефектах и отсутствии пролабирования мозга. Апоневроз височной мышцы для пластики твердой мозговой оболочки не позволяет закрыть большие дефекты и нередко приводит к выраженному спаечному процессу. Использование фибриновой пленки для пластики дефектов твердой мозговой оболочки малопригодно из-за частого возникновения ликвореи, формирования ликворной подушки. Сочетанное применение фибриновой пленки и фасции обеспечивает достаточную герметичность субдурального пространства, но требует проведения дополнительной операции.
На сегодняшний день основные требования к любым пластическим материалам, подлежащим имплантации, сведены к тому, чтобы они в первую очередь не оказывали вредного влияния на ткани организма, а что касается их применения в нейрохирургии – на головной мозг и его оболочки. Кроме этого, пластический материал (эндопротез) должен легко моделироваться в зависимости от конкретной интраоперационной ситуации, хорошо приживляться в тканях, быстро и просто обрабатываться, удобно и совершенно стерилизоваться. Не на последнем месте стоит и экономическая составляющая, т.е. материал для пластики должен быть доступным и дешевым для использования широким кругом нейрохирургов [4].
ООО «Кардиоплант» (г. Пенза) разработана ксеноперикардиальная пластина для нужд реконструктивно-пластической хирургии, которая представляет собой неиммуногенный материал на основе коллагена. Сырьем для производства изделия служит перикард крупного рогатого скота, прошедшего ветеринарный контроль. Пластина имеет две поверхности: серозную гладкую, которая обладает биорезистентностью и в меньшей степени подвержена адгезии, и фиброзную ворсистую, обладающую высокой биоинтеграцией и активным сращением с тканями. Материал нашел применение в клинической практике и неплохо себя зарекомендовал в хирургии, стоматологии, а так же травматологии и ортопедии [2, 3].
Цель исследования. В процессе эксперимента нами была поставлена цель изучить возможности использования лиофилизированного ксеноперикарда быка как биопротеза твердой мозговой оболочки.
Материалы и методы исследования
Экспериментальное исследование проведено на базе центра доклинических исследований группы компаний «МедИнж». Для пластики ТМО использован перикард быка, в котором, в результате химико-ферментативной обработке обработки, сохранена коллагеново-эластическая структура. Данная обработка позволяет получить неиммуногенный материал являющимся биополимером. Материал сертифицирован и разрешен Роздравнадзором к продаже и применению на территории Российской Федерации.
Эксперимент проведен на 3-х животных (половозрелые свиньи весом 65-70 кг). Произведена имплантация ксеноперикардиальной пластины в сформированный дефект ТМО.
Ход операции следующий. В асептических условиях под комбинированным наркозом, в положении животного на левом боку, справа от срединной линии черепа производили дугообразный разрез, проходящий над правым ухом. Выделяли и отсепаровывали жевательную мышцу. В правой височной области накладывали фрезевое отверстие черепа с его последующим расширением до 2,5–3 см диаметром, что позволяло осуществить доступ к твердой мозговой оболочке. Твердую мозговую оболочку вскрывали линейно и формировали искусственный дефект диаметром около 2 см. Моделировали лоскут из ксеноперикардиальной пластины «Кардиоплант» неправильной формы, площадью до 7 см2 и укладывали в зону дефекта под твердую мозговую оболочку, обращая пластину гладкой поверхностью к мозговому веществу. Для предупреждения смещения протеза производили фиксацию последнего к краю дефекта твердой мозговой оболочки двумя-тремя швами. Костный дефект не ликвидировали, а лишь частично прикрывали его, возвращая назад жевательную мышцу. Рану ушивали послойно. В послеоперационном периоде назначали антибактериальную терапию (цефалоспорины) для профилактики возможных раневых осложнений. Отмечено благоприятное течение послеоперационного периода.
Выведение животных из эксперимента производили на 90-е сутки путем усыпления животного до полного обездвиживания и достижения анестезии с последующим обескровливанием или введением миорелаксантов. Для исследования изымали фрагмент черепной коробки с головным мозгом. Макроскопически, при наружном осмотре черепной коробки определить сторону, на которой производили операцию, было практически невозможно. Дефект костей черепа не определялся. В зоне, где выполняли трефинацию, отмечали лишь незначительное углубление костной пластинки. По вскрытии черепа был виден ксеноперикардиальный протез, плотно сросшийся с собственной твердой мозговой оболочкой при отсутствии адгезии к ткани головного мозга. В одном случае наблюдали сращение протеза с костями черепа в зоне фрезевого отверстия. Для проведения гистологического исследования забирали подготовленную часть черепа, включающую зону вмешательства с головным мозгом и его оболочками.
Из каждого фрагмента, взятого для гистологического исследования, после декальцинации в азотной кислоте и стандартной проводки, изготавливали парафиновый блок. С каждого блока получали по 5 микропрепаратов, которые окрашивали гематоксилином и эозином и по Ван-Гизону. Исследование микропрепаратов производили при помощи микроскопа Leica DM-1000, снабженного фотонасадкой Nikon с разрешением 7 мегапикселей.
Результаты исследования и их обсуждение
При микроскопическом исследовании вещество твердой мозговой оболочки было представлено компактно расположенными соединительнотканными волокнами. Кровеносные сосуды оболочки расширенные и полнокровные.
При исследовании области контакта ксеноперикардиальной пластины твердой мозговой оболочки и вещества мозга были выявлены следующие особенности. Не выявлено выраженной воспалительной реакции тканей в зоне имплантации. Отмечено прорастание собственной соединительной ткани твердой мозговой оболочки в ксеноперикардиальную пластину, неоангиогенез. Таким образом, в исследуемой области отмечались эффективные процессы биодеградации и биоинтеграции ксеноперикардиальной пластины. При этом не выявлено сращения ксеноперикардиальной пластины с поверхностью головного мозга.
В месте контакта ксеноперикардиальной пластины с внутренней пластинкой компактного вещества костей свода черепа отмечалось отсутствие воспалительной реакции. Более того, отмечались процессы неоостеогенеза. В ксеноперикардиальной пластине происходили процессы биодеградации, т.е. разрушение коллагеновых и эластических волокон и образование молодой костной ткани. Причем в полученных образцах встречались, только единичные островки хрящевой ткани, данный факт говорит о том, что образования костной ткани происходило по типу первичного остеогенеза. Данный тип остеогенеза отмечается в тканях только при создании наиболее благоприятных условий для образования костной ткани. Также в новообразованной ткани отмечалось образование костных балок, а между ними появлялись элементы красного костного мозга, и стромально-сосудистый компонент.
В результате проведенного эксперимента с последующим гистологическим исследованием нами выявлены новые свойства изучаемой ксеноперикардиальной пластины. Так в зоне контакта пластины с краями поврежденной твердой мозговой оболочки отмечены процессы биоинтеграции и, как следствие, закрытие дефекта ТМО. В то же время в зоне контакта ксеноперикардиальной пластины с краями дефекта костной ткани отмечены выраженные процессы остеогенеза и частичное закрытие дефекта костей черепа.
Исследуемый материал может рассматриваться как возможная альтернатива существующим материалам для пластики твердой мозговой оболочки. Безусловно, что эксперимент нуждается в продолжении и будет продолжен, поскольку требуется получение результатов в более поздние сроки после имплантации, изучение возможных вариантов размещения и фиксации ксеноперикардиальной пластины. Однако первые результаты расценены нами как вполне обнадеживающие, и мы считаем, что в перспективе, при положительных результатах экспериментального исследования, ксеноперикардиальная пластина может быть рекомендована для применения в клинике с целью укрытия дефектов твердой мозговой оболочки.