Тест поглощения тиреоидных гормонов (T-uptake)
Описание
Тест поглощения тиреоидных гормонов — оценка функции щитовидной железы. Назначается в сочетании с определением концентрации общего Т4.
Исследование проводится для оценки изменения концентрации белков, связывающих Т4 и Т3 . Только свободные (несвязанные) тиреоидные гормоны обладают биологической активностью.
Процент поглощения в первую очередь зависит от ТСГ, который связывает 80% Т3 и порядка 75% Т4, и уровня гормонального насыщения тироксинсвязывающего глобулина. Если активность щитовидной железы высока, то насыщение ТСГ тироксином увеличивается. Уменьшение уровня веществ приведет к увеличению процента в тесте поглощения тиреоидных гормонов.
Состояния гипертиреоза, гипотиреоза или эутиреоза подтверждаются, если % TU, соответственно, увеличен, снижен или находится в пределах референсных значений. Высокий уровень Т4 и низкий %TU наблюдаются при повышенной концентрации белков-переносчиков. Эта ситуация типична для беременных или принимающих оральные контрацептивы женщин, когда увеличение концентрации ТСГ обусловлено возрастанием уровня эстрогенов, а также при эстроген-зависимых опухолях, гиперпротеинемии.
Низкий уровень Т4 и высокий %TU свидетельствуют о снижении концентрации связывающих белков в крови ниже нормы. Подобные изменения бывают вызваны стрессовыми состояниями (хирургическое вмешательство, острая инфекция), гипопротеинемией (заболевания печени и почек, истощение), повышенным уровнем андрогенов.
Особые указания: при первичной проверке уровня тиреоидных гормонов следует отменить препараты, влияющие на функцию щитовидной железы за 2–4 недели до исследования (после согласования с лечащим врачом). При контроле лечения — исключить прием препаратов в день исследования и обязательно отметить это в направительном бланке (отметить также информацию о приеме других лекарств — аспирина, транквилизаторов, кортикостероидов, пероральных контрацептивов).
Интерпретация результатов
Норма: 24–35%.
Алгоритмы диагностики и лечения высокодифференцированого рака щитовидной железы
Гарбузов П.И.
Медицинский Радиологический Научный Центр РАМН, Обнинск
ЛЕЧЕНИЕ
Хирургия, ТТГ-супресивная терапия, радиойодтерапия, дистанционная лучевая терапия, химиотерапия и редифференцирующая терапия используются в настоящее время на различных этапах лечения. При этом в первую очередь при дифференцированном раке щитовидной железы проводится хирургическое удаление первичной опухоли и регионарных метастазов
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Стандартной операцией при ДРЩЖ является тотальная или околототальная тиреоидэктомия. Выполнение тотальной тиреоидэктомии на стороне опухоли и околототальной тиреоидэктомии на противоположной стороне позволяет сохранять кровоснабжение паращитовидных желез, что значительно снижает риск тяжелой послеоперационной гипокальциемии. Гемитиреоидэктомия на стороне первичной опухоли может быть адекватной только в случае обнаружения папиллярной микрокарциномы с диаметром опухоли Ј 1см, так как рак щитовидной железы довольно часто бывает многофокусным и с двухсторонним поражением.
ТТГ-СУПРЕССИВНАЯ ТЕРАПИЯ
Несмотря на то, что пока нет проспективных исследований эффективности ТТГ супрессивной терапии, но ретроспективные данные эпохи рутинной аблации йодом-131 показали значительное статистически значимое уменьшение 10 летних рецидивов с 20% у больных без медикаментозной терапии до 12% у больных, которые получали L-Т4 в дополнении к хирургии. Некоторые противоречия существуют относительно оптимального уровня ТТГ супрессии, так как супрессивная дозировка L-Т4 может вызывать такие неблагоприятные эффекты, как увеличения риска предсердной фибрибляции и деминерализации костей. При отсутствии такого риска супрессивная терапия рекомендуется ниже 0,1–0,2 МЕ/мл. Альтернативный, риск-ориентированный подход предлагает ТТГ-супрессию ниже 0,1 МЕ/мл у больных с высоким риском опухолевого роста или рецидива и ТТГ супрессия ниже нормального уровня у больных с низким уровнем
ЛУЧЕВОЕ ЛЕЧЕНИЕ
Повторное введение 131 I с интервалом 3 – 6 месяцев проводится при выявлении очагов гиперфиксации РФП до их полного исчезновения, отсутствия ультразвуковых и/или рентгенологических признаков рецидива опухоли и метастазов РЩЖ и снижении уровня ТГ в сыворотки крови
Что такое тест тиреоидной супрессии
31. ТЕСТЫ ОПРЕДЕЛЕНИЯ ФУНКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
1. Какой тест является наилучшим для проведения скрининга на нарушение функции щитовидной железы?
Определение в сыворотке крови уровня тиреотропного гормона (ТТГ) при использовании высокочувствительных методов исследования ТТГ является лучшим тестом для оценки тиреоидной функции. Это мнение основано на положениях, касающихся первичного поражения щитовидной железы, которое в действительности имеет место в подавляющем большинстве случаев. Однако, измерение ТТГ может ввести в заблуждение, когда тиреоидная дисфункция является вторичной, что связано с патологией гипоталамуса или гипофиза, которая вызывает нарушения секреции ТТГ.
3. Объясните, как определение ТТГ используется при контроле терапии и подборе доз тиреоидных гормонов для лечения пациентов с патологией щитовидной железы?
Гормоны щитовидной железы обычно назначаются по одной из двух причин: заместительная терапия при гипотиреозе или супрессивная терапия при доброкачественных узлах или раке щитовидной железы. При заместительной терапии тиреоидными препаратами дозы должны быть подобраны для поддержания уровня ТТГ в нормальных пределах. При назначении тиреоидных гормонов для супрессивной терапии уровень ТТГ необходимо поддерживать ниже нормальных значений при доброкачественных узлах и на неопределяемом уровне при раке щитовидной железы.
4. Обсудите преимущества определения свободных тиреоидных гормонов.
Исследование свободных T4 и T3 измеряет количество несвязанных, биоактивных гормонов в кровотоке. На эти показатели не влияют состояния, вызывающие нарушения связывания тиреоидных гормонов в плазме. Если уровни свободных гормонов выше или ниже пределов нормальных колебаний, у пациента имеет место патология щитовидной железы, и выраженность заболевания напрямую связана со степенью отклонения этих показателей от нормы. Таким образом, по возможности, определение этих показателей обычно предпочтительнее, чем оценка общих тиреоидных гормонов.
5. Как оценить результаты определения общих T3 и T4?
Эти исследования позволяют определить концентрации общих T3 и Т^ в кровотоке. Более 99% циркулирующего T4 и приблизительно 98% T3 связаны с такими белками, как тироксин-связывающий глобулин (ТСГ), тироксин-связывающий преальбумин и альбумин, в то время, как оставшиеся фракции остаются свободными в плазме. Соответственно, уровни общих T3 и T4 могут изменяться при патологии связывающих белков, симулируя заболевания щитовидной железы. Главными причинами, приводящими к увеличению связывания тиреоидных гормонов, являются беременность, прием эстрогенов и врожденный избыток ТСГ; с другой стороны, к снижению связывания приводят прием андрогенов и врожденный дефицит ТСГ.
Определение T3, абсорбированного на смоле (T3АС), помогает клиницистам отдиф-ференцировать эти состояния. T3АС обратно пропорционален содержанию связанного T4; T3АС снижается при увеличении связанного T4 и повышается при снижении связывания. T3АС следует определять для интерпретации уровней обших T3 и T4. Нижеследующая таблица показывает, как при помощи этих показателей поставить правильный диагноз.
| ОБЩИЙ T4 | ОБЩИЙ T3 | T3АС | |
| Гипертиреоз | ↑ | ↑ | ↑ |
| Увеличение связывания белками | ↑ | ↑ | I |
| Гипотиреоз | I | I | I |
| Уменьшение связывания белками | I | I | ↑ |
6. Имеет ли практическое значение определение содержания различных тиреоидных антител?
Повышенное содержание тиреоидных антител является важной клинической находкой, но не может быть доказательством аутоиммунного заболевания щитовидной железы, например, болезни Грейвса и тиреоидита Хашимото. Уровень тиреоид-связыва-ющих иммуноглобулинов [тиреоид-связывающие ингибирующие иммуноглобулины (ТСИИ) и тиреоидных стимулирующих иммуноглобулинов (ТСИ)] повышен у большинства больных с болезнью Грейвса и у некоторых больных тиреоидитом Хашимото. Антимикросомальные антитела и антитела к тиреоглобулину чаще всего обнаруживаются у больных тиреоидитом Хашимото. Действительно, повышенные титры анти-микросомальных антител (> 1:1600) у лиц с гипотиреозом являются основанием для клинического диагноза тиреоидита Хашимото.
7. В каких случаях целесообразно определять содержание в сыворотке тирео-глобулина?
Определение содержания тиреоглобулина может быть использовано как индикатор наличия функционирующей тиреоидной ткани. Таким образом, этот показатель является чувствительным и специфичным маркером рецидивирования опухоли у больных раком щитовидной железы в анамнезе. Однако, чтобы этот тест стал целесообразным, все функционирующие нормальные ткани щитовидной железы должны отсутствовать; иными словами, больные должны быть прежде всего подвергнуты ти-реоидэктомии с последующим введением радиоактивного йода. Такое лечение, безусловно, является традиционным у больных раком щитовидной железы.
8. В каких случаях целесообразно определять содержание кальцитонина?
Кальцитонин является продуктом С-клеток щитовидной железы. Медуллярный рак щитовидной железы (МРЩЖ) представляет собой неопластическое разрастание С-клеток. Таким образом, определение содержания кальцитонина необходимо производить при ведении больных с МРЩЖ, а также с целью выявления родственников больного, предрасположенных к МРЩЖ. Предварительные определения кальцитонина могут быть использованы в этом тесте в случаях, когда уровни его повышены. Однако самым чувствительным тестом является измерение уровня кальцитонина после стимуляции пентагастрином, изолированно или в сочетании с кальцием. В действительности, скрининг на наличие поражения С-клеток у больного МРЩЖ или у члена его семьи должен проводиться с использованием пентагастринового или каль-ций-пентагастринового теста, а также тестов на наличие феохромоцитомы и повышенного содержания кальция. Частота использования и продолжительность проведения таких тестов дискутируются, но, по-видимому, лучше взять за правило 1-годичный интервал в возрасте до 35-45 лет у ближайших родственников больного МРЩЖ. Конечно, даже в тех случаях, когда только у одного члена семьи имеется спорадическая МРЩЖ, должны быть проведены первоначальное и повторные обследования для выявления потенциальных больных. Однако, если МРЩЖ или синдром множественной эндокринной неоплазии 2 (МЭН-2) выявлены у двух или более членов семьи, то скрининг родственников приобретает еще большее значение.
9. Как влияет измерение распределения радиоактивного йода на оценку заболеваний щитовидной железы?
Измерение распределения радиоактивного йода (1311 или 1321) способствует дифференциации гипертиреоидных состояний, таких как болезнь Грейвса (поглощение йода обычно повышено), и различных форм тиреоидита, при которых гипертиреоз сочетается со снижением усвоения йода. Ниже в таблице перечислены состояния, при которых поглощение йода повышено или снижено. Измерение поглощения радиоактивного йода также используется для выбора необходимой дозы радиоактивного йода для лечения болезни Грейвса. В норме поглощение радиоактивного йода составляет 8-30% и зависит также от содержания йода в рационе.
| Поглощение повышено | Поглощение снижено |
| Болезнь Грейвса | Подострый тиреоидит |
| Токсический автономный узел | Безболезненный тиреоидит |
| ТМУЗ | Послеродовый тиреоидит |
| Тиреотоксикоз ятрогенный | |
| Гипертиреоз йод-индуцированный |
10. Какую роль играет сканирование с технецием при исследовании щитовидной железы?
Щитовидная железа захватывает, но не усваивает технеций. Исследование распределения технеция позволяет визуализировать железу, насыщенную контрастом, с выделением «горячих» и «холодных» зон. Это помогает в оценке функционального состояния узлов щитовидной железы, определяемых при пальпации. Такое разграничение помогает определить потенциал злокачественности узлов щитовидной железы, поскольку «холодный» узел скорее может оказаться злокачественным, чем «теплый» или «горячий». У лиц с гипертиреозом сканирование с технецием позволяет дифференцировать различные причины гиперфункции. Болезнь Грейвса, известная также как диффузный токсический зоб, характеризуется повышенной активностью щитовидной железы, причем распределение технеция происходит равномерно, в то время как токсический многоузловой зоб (ТМУЗ) сопровождается гетерогенным распределением технеция.
11. Супрессивные тесты с использованием цитомела (трийодтиронина) и тироксина.
Назначение супрафизиологических доз цитомела (T3) на 1 неделю или тироксина (T4) на 4-6 недель полностью подавляет секрецию ТТГ гипофизом. У людей с нормальной щитовидной железой этот тест снижает захват радиоактивного йода до нуля и при сканировании не позволяет получить изображения. Однако у пациентов с автономной секрецией тиреоидных гормонов щитовидной железой на фоне ее патологии (определяется как функционирование щитовидной железы, не зависимое от влияния ТТГ), захват и сканирование остаются неизменными после супрессии ТТГ. Следовательно, супрессивные тесты с применением цитомела и тироксина- тесты для определения тиреоидной автономии. Главными причинами автономной секреции тиреоидных гормонов являются стимулирующие иммуноглобулины при болезни Грэйвса и клеточная автономия, присущая токсическому многоузловому зобу и токсическим аденомам. Пациентам с тиреоидной автономией не стоит проводить суп-рессивную терапию тиреоидными гормонами по причине того, что ТТГ в таких случаях не поддается супрессии. Большинству необходима терапия тиреостатиками, радиоактивным йодом или резекция щитовидной железы.
12. Какова роль теста с ТРГ в диагностике заболеваний щитовидной железы?
Быстрое внутривенное введение тиреотропин-рилизинг гормона (ТРГ) в норме вызывает заметное увеличение в плазме ТТГ, которое может продолжаться до двух часов. Для пациентов с первичным гипотиреозом характерно резкое повышение уровня ТТГ (значительно большее, чем в норме), но наблюдается отсутствие подъема ТТГ у пациентов с первичным гипертиреозом. Слабое и/или позднее (по времени) увеличение ТТГ может отмечаться у пациентов с гипоталамо-гипофизарной патологией. В связи с наличием высоко чувствительных методов определения ТТГ и свободных тиреоидных гормонов, в настоящее время тест редко применяется для диагностики первичной патологии щитовидной железы и является недостаточно точным для диагностики вторичных заболеваний. Тем не менее, в некоторых случаях тест незаменим, когда прочие исследования недостаточны для постановки точного диагноза.
Диагноз: гестационный гипотиреоз
Поделиться:
Кажется, лет 10 тому назад академик, доктор медицинских наук, врач-эндокринолог Галина Афанасьевна Мельниченко, известная в том числе своей просветительской интернет-деятельностью, восхищенно воскликнула: «Наконец-то гинекологи оторвали головы от промежности и обнаружили еще одну железу внутренней секреции!».
Да, это так. Большинство российских гинекологов таки вспомнило о существовании щитовидной железы, освоило современные подходы к этой проблеме и выучило нормы для беременных и готовящихся.
О связи щитовидной железы и беременности знали еще древние египтяне. В день заключения брачного союза они завязывали специальную нить вокруг шеи женщины. Когда нить разрывалась из-за увеличения размеров щитовидной железы, врачи Древнего Египта подтверждали диагноз «беременность».
Сегодня мы не хуже древних египтян знаем, что во время беременности щитовидная железа матери обязана вырабатывать тироксин «за себя и за того парня», потому что свой собственный тироксин плод начинает вырабатывать только к 16–18-й недели беременности. Дефицит этого важнейшего гормона оказывает негативное влияние как на течение беременности, так и на здоровье плода.
Гипотиреоз — заболевание, связанное со снижением выработки гормонов щитовидной железой.

Признаки гипотиреоза столь многочисленны и неспецифичны, что пропустить это заболевание легче легкого. Кого во время беременности удивит утомляемость, сонливость и/или слабость, непереносимость холода, прибавка веса, ухудшение настроения, ослабление памяти, запоры, тонкие и ломкие волосы и ногти?
Если диагноз не поставили и/или не назначили правильное лечение, такая беременность может закончиться необъяснимым выкидышем, преэклампсией, отслойкой плаценты или послеродовым кровотечением. Часто роды происходят преждевременно, дети рождаются маловесными, с незрелой легочной тканью. У таких детишек достоверно чаще встречается аутизм, синдром дефицита внимания и гиперактивности, нарушение нейроинтеллектуального развития.
Самое неприятное в этой истории то, что гипотиреоз может протекать совершенно бессимптомно, обнаруживаться совершенно случайно, но риски и угрозы бессимптомный (или субклинический) гипотиреоз создает такие же, как махровый гипотиреозище.
Именно поэтому так важно проводить тиреоидный скрининг во время беременности.
Тиреоидный скрининг: кому проводить?
Абсолютно всем беременным, заинтересованным в сохранении беременности.
За рубежом этот вопрос активно обсуждается, эксперты приходят к выводу о нецелесообразности проведения тотального скрининга, однако важно понимать, что в нашей стране до сих пор не решена проблема дефицита йода: 95 % территории России — йоддефицитные регионы. Необходимость тиреоидного скрининга у женщин с осложненным анамнезом и на йоддефицитных территориях не подлежит ни малейшему сомнению.
Как проводят скрининг?
Необходимо сдать кровь на ТТГ и Т4 свободный утром, натощак, желательно исключив стрессовое воздействие.

Кто проводит скрининг?
Назначить обследование должен врач акушер-гинеколог. К сожалению, особенности программ ОМС позволяют лишь выборочно оплачивать это исследование, поэтому в ряде регионов обследование проводится за счет собственных средств пациенток.
Читайте также:
Полное обследование
Когда проводят скрининг?
Сегодня эндокринологи говорят о том, что это анализ «первой пробирки». В идеале женщина может проводить данное обследование вместе с определением уровня ХГЧ, задолго до изучения других маркеров. Не надо приравнивать скрининг 1-го триместра на хромосомные аномалии в сроке 11–13 недель к тиреоидному скринингу. Тиреоидный скрининг — это скрининг надежды. Тут легко поставить диагноз, легко устранить дефицит гормонов и легко предупредить негативные изменения.
Зачем проводят скрининг?
Ожидалось, исследование покажет, что тиреоидный скрининг с коррекцией дефицита йода и гипотериоза во время беременности позволит получить умненьких детей. Скрининг проводили в 12 недель беременности, лечение начинали в среднем в сроке 13–14 недель. Когда детям исполнилось 3 года, психологи провели замеры IQ, сравнивая результаты с контрольной группой. Увы — никакого улучшения когнитивных функций специалисты не обнаружили.
Эндокринологов это огорчило, но акушеры-гинекологи были весьма довольны — все беременности неплохо проходили, серьезных осложнений гестации не было, детки родились в срок и с хорошим весом. Оптимисты считают, что тиреоидный скрининг проводился слишком поздно, а при таком отсроченном начале терапии «защитить интеллект» уже не получится — вмешиваться надо раньше. Новое исследование затеяно, нам остается набраться терпения и ждать обнадеживающих результатов.
Кто ставит диагноз «гипотиреоз» во время беременности?
Тот, кто нашел. Если на обследование направил акушер-гинеколог, то он и поставит диагноз. Необходимо помнить, что нормальные значения ТТГ, указанные на бланке, сильно отличаются от целевых значений во время беременности.
В 1-м триместре уровень ТТГ должен быть менее 2,5 мЕд/л. Если получилось выше, акушер-гинеколог ставит диагноз «Первичный гипотиреоз, впервые выявленный в 1-м триместре», рекомендует немедленно бежать в аптеку за йодомарином и, как можно скорее, к эндокринологу.
Кто лечит гипотиреоз?
Уточнять диагноз и проводить лечение будет врач-эндокринолог. Если попасть к специалисту быстро не получается, не будет большой беды, если лечение L-тироксином начнет акушер-гинеколог, а эндокринолог скорректирует дозировку и будет контролировать процесс.
Если небольшое повышение ТТГ на ранних сроках беременности оказалось незамеченным, не стоит огорчаться. Вероятность развития серьезных последствий для интеллектуального и физического развития развития невысока. Уровень интеллекта ребенка зависит от многих факторов. И даже при идеальной работе щитовидной железы у матери во время беременности далеко не все дети становятся медалистами в школе и в будущем — нобелевскими лауреатами.
Товары по теме: [product strict=»йодомарин»](йодомарин), [product strict=»калия йодид»](калия йодид)
Заместительная и супрессивная терапия в практике эндокринолога
Е.А. Трошина, Н.В.Мазурина, Е.М.Скрынник
ФГУ Эндокринологический научный центр МЗСР РФ, Москва
Препараты тиреоидных гормонов относятся к числу наиболее часто используемых в клинической практике лекарственных средств. Их назначают с целью проведения заместительной или супрессивной терапии при ряде заболеваний щитовидной железы (ЩЖ).
Целью заместительной терапии является поддержание нормального обмена веществ у больных гипотиреозом любой этиологии.
Манифестный гипотиреоз
Левотироксин назначают из расчета 1,6–1,8 мкг на 1 кг массы тела (ориентировочная начальная доза для женщин 75–100 мкг/сут; мужчин – 100–150 мкг/сут).
Целевое значение тиреотропного гормона (ТТГ) при проведении заместительной терапии левотироксином первичного гипотиреоза составляет 0,5–1,5 мМЕ/л.
При проведении заместительной терапии центрального (вторичного) гипотиреоза необходимо добиться поддержания тироксина крови на уровне, соответствующем верхней трети нормальных значений для этого показателя.
Субклинический гипотиреоз
Тироксин назначают из расчета 1 мкг на 1 кг массы тела (ориентировочная начальная доза 50–75 мкг/сут).
Целью супрессивной терапии также является достижение концентрации ТТГ менее нижней границы нормы для предотвращения его возможного стимулирующего влияния на рост ткани ЩЖ (в том числе на рост резидуальной опухолевой ткани).
Целевое значение ТТГ составляет менее 0,1 мМЕ/л. Для этого используются дозы левотироксина от 2,2 до 2,5 мкг на 1 кг массы тела в сутки.
Принципы заместительной терапии левотироксином
Изменения секреции тиреоидных гормонов и снижение функции ЩЖ (гипотиреоз) могут происходить в результате поломки биосинтеза тиреоидных гормонов на разных его этапах: поступления йодида из крови, окисления его в элементарный йод, включения йода в состав тирозинов с образованием монойодтирозина и дийодтирозина, конденсации молекул йодтирозина с образованием Т4 и Т3. Независимо от того, на какой из стадий произошло нарушение метаболизма гормонов ЩЖ, будут изменяться те физиологические эффекты, за которые ответственны тиреоидные гормоны.
Основные физиологические эффекты тиреоидных гормонов:
• регуляция энергетического обмена
• регуляция роста и развития
• регуляция белкового, углеводного и жирового обмена
• влияние на сердечно-сосудистую систему
• влияние на костно-мышечную систему
• влияние на психику
Лечение всех форм гипотиреоза является заместительным и пожизненным. Исключение составляет только гипотиреоз, вызванный введением каких-либо медикаментов или веществ, блокирующих выработку тиреоидных гормонов.
Препараты левотироксина являются препаратами выбора для заместительной терапии гипотиреоза, и представляют собой синтетический тироксин (натриевая соль тироксина), который полностью идентичен тироксину, продуцируемому ЩЖ. Хорошо всасывается в желудочно-кишечного тракта (ЖКТ), причем при гипотиреозе его всасывание не нарушено.
Один из препаратов левотироксина – Эутирокс (фирма «Никомед»). Его отличием от других препаратов этой группы является возможность с легкостью подобрать нужную дозировку – 25, 50, 75, 100, 125 или 150 мкг, что существенно облегчает проведение как заместительной, так и супрессивной терапии.
На фоне заместительной терапии Эутироксом концентрация Т3 сохраняется постоянной. Режим дозирования препарата устанавливают индивидуально, с учетом тех возможных ситуаций, когда потребность в тироксине может изменяться (табл. 1).
Таблица 1. Ситуации, при которых может измениться потребность организма в тироксине
| Повышение потребности в тироксине | |
| • Снижение абсорбции в кишечнике (заболевания слизистой оболочки тонкой кишки и после операций на тонкой кишке) | |
| • Поносы при диабете | |
| • Цирроз печени | |
| • Беременность | |
| • Прием препаратов, снижающих абсорбцию | |
| Холестирамин Сукралфат Окись алюминия Сульфат железа | |
| • Препараты, увеличивающие выведение неметаболизированного Т4 | |
| Рифампицин Карбамазепин Возможно, фенитоин | |
| • Препараты, блокирующие конверсию Т4 в Т3 | |
| Амиодарон Дефицит селена | |
| Снижение потребности в тироксине | |
| • Пожилой возраст | |
| • Ожирение | |
Поскольку основной задачей лечения гипотиреоза является восстановление нормальных физиологических функций всех органов и систем, нарушенных вследствие гипотиреоза, то и при первичном, и при вторичном (третичном) гипотиреозе основа лечения – адекватная заместительная терапия препаратами тиреоидных гормонов. Критерием адекватности лечения служит исчезновение клинических и лабораторных проявлений гипотиреоза.
Компенсация манифестного гипотиреоза – 1,6–1,8 мкг левотироксина в сутки. Средняя суточная доза 75–150 мкг
Компенсация субклинического гипотиреоза – 1 мкг левотироксина на 1 кг массы тела. Средняя суточная доза 50–75 мкг
Терапию начинают с небольшой дозы Эутирокса, причем у пожилых она может составлять 12,5 мкг/сут. Препарат принимают утром, натощак. Дозу постепенно увеличивают до поддерживающей (у молодых больных за 4 нед, у пожилых за 2 мес, а иногда, при наличии сопутствующей кардиальной патологии, за 3–4 мес).
Оценивать уровень ТТГ на фоне лечения следует не раньше чем через 2 мес от начала терапии. Далее исследовать этот показатель нужно с интервалом 1 раз в 6 мес и корректировать дозу Эутирокса в зависимости от полученных результатов.
При лечении вторичного гипотиреоза схема назначения препарата аналогичная, однако контролировать, по понятным причинам, следует не ТТГ, а свободный Т4. В табл.2 представлен начальный этап лечения гипотиреоза.
Таблица 2. Начальный этап заместительной терапии у больных гипотиреозом
| Больные без кардиальной патологии моложе 65 лет |
| Левотироксин назначают из расчета 1,6–1,8 мкг на 1 кг массы тела |
| Ориентировочная начальная доза: |
| • женщины – 50–75 мкг/сут |
| • мужчины – 75–100 мкг/сут |
Больные с кардиальной патологией и/или старше 65 лет
Начальная доза 12,5 мкг левотироксина в день (увеличивать по 12,5 мкг с интервалом 2 мес до нормализации уровня ТТГ, при появлении или ухудшении кардиальных симптомов провести коррекцию терапии).
Тяжесть и длительность гипотиреоза являются основными критериями, определяющими тактику врача в момент начала лечения.
Чем тяжелее гипотиреоз и чем дольше он был некомпенсирован, тем выше будет общая восприимчивость организма к тиреоидным гормонам, особенно это относится к кардиомиоцитам. Поэтому процесс адаптации к препарату должен быть постепенным и плавным независимо от возраста пациента.
При назначении тироксина пациенту с гипотиреозом нужно выяснить, какие еще медикаменты он получает, поскольку многие препараты могут увеличивать потребность в тироксине. Если не учитывать этот эффект, компенсация гипотиреоза может быть затруднена.
Субклинический гипотиреоз характеризуется отсутствием четких клинических проявлений заболевания. Жалобы пациента, как правило, неспецифичны и часто сводятся к повышенной слабости и утомляемости. Лабораторные параметры включают в себя незначительное повышение ТТГ при нормальных уровнях Т3 и Т4. Нередко субклинический гипотиреоз является случайной находкой при общем обследовании больного. Данный синдром чаще обнаруживается у пожилых пациентов.
Для верификации диагноза нужно провести больному повторное определение уровня ТТГ через 6 мес. В том случае, если у пациента регистрируется стойкое повышение уровня ТТГ, вопрос о лечении следует решать в индивидуальном порядке. Однозначного мнения по поводу целесообразности специфической терапии субклинического гипотиреоза в настоящее время нет. Но если такая терапия проводится, то она должна сопровождаться адекватным и своевременным наблюдением за пациентом, включающим в себя определение уровня ТТГ. Как правило, заместительную терапию при субклиническом гипотиреозе начинают тогда, когда уровень ТТГ составляет 10 мЕ/л и выше, и Эутирокс назначают в дозе 1 мкг на 1 кг массы тела (суточная доза составляет 50–75 мкг).
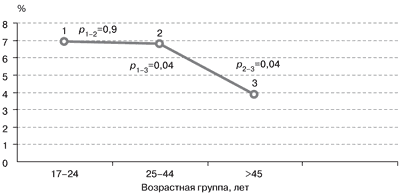
| Рис. 1. Распространенность ДЗ в различных возрастных группах. |
 |
Гипотиреоз и беременность
При некомпенсированном гипотиреозе наступление беременности крайне маловероятно. Если беременность все же наступила, то лечение гипотиреоза должно быть начато немедленно. Во время беременности потребность в левотироксине в среднем возрастает на 45% от расчетной исходной дозы. Если беременность наступила у женщины с компенсированным гипотиреозом, то доза препарата должна быть увеличена в соответствии с возросшей потребностью в нем.
Принципы супрессивной терапии левотироксином
Высокодифференцированный рак ЩЖ (ВДРЩЖ)
На протяжении многих лет основным способом терапии для больных, получивших радикальное лечение по поводу ВДРЩЖ, остается введение тиреоидных гормонов в дозах, превышающих физиологические (2,5 мкг на 1 кг массы тела в сутки), с целью снижения концентрации сывороточного ТТГ. Клетки рака ЩЖ, происходящие из фолликулярного эпителия, имеют рецепторы ТТГ, и в ответ на их стимуляцию происходит повышение активности аденилатциклазы. Предполагается, что эти опухоли ЩЖ могут расти под воздействием ТТГ. Многие исследователи отмечали уменьшение частоты рецидивов опухолевого роста благодаря подавлению секреции ТТГ под воздействием супрессивной терапии как при папиллярной, так и при фолликулярной тиреоидной карциноме.
Сегодня рекомендуется использовать методы анализа ТТГ III поколения, которые позволяют выявлять его присутствие в сыворотке в концентрациях порядка 0,01 мЕд/л.
До сих пор активно обсуждается вопрос о том, что более опасно для пациента: предотвращение рецидива рака при условии поддержания субклинического тиреотоксикоза или неблагоприятное влияние медикаментозного тиреотоксикоза на сердце и кости. Побочные эффекты супрессивных доз левотироксина включают нарушения контрактильности миокарда, увеличение частоты сердечных сокращений и предсердные аритмии, а также могут вызывать ускорение круговорота элементов костной ткани, остеопороз. По этой причине многие специалисты считают, что полное подавление секреции гипофизарного ТТГ на протяжении длительного периода (до 0,01–0,1 мЕд/л или ниже) целесообразно лишь у больных, входящих в группу высокого риска – в первую очередь при повышенной вероятности рецидивов или смерти у пациентов с ВДРЩЖ. В то же время большинство клиницистов полагают, что у подавляющего числа больных с папиллярной тиреоидной карциномой, относимых к группе низкого риска на основании результатов прогностической балльной оценки, хороший эффект дает относительно слабое подавление секреции ТТГ. У таких больных концентрацию сывороточного ТТГ следует поддерживать на уровне 0,1–0,4 мЕд/л. В целом при лечении ВДРЩЖ, по имеющимся на сегодняшний день данным контролируемых исследований, назначение высоких доз левотироксина с целью подавления уровня ТТГ имеет преимущества по сравнению с обычной заместительной терапией, при которой поддерживается эутиреоз, т.е. нормальный уровень ТТГ. Исключение могут составлять пожилые больные или больные с тяжелым заболеванием сердца и выраженным остеопорозом.
Узловой коллоидный зоб
В настоящее время в соответствии с Консенсусом РАЭ решение вопроса о целесообразности супрессивной терапии левотироксином при узловом коллоидном зобе определяется в индивидуальном порядке. Лечение препаратами тироксина наиболее эффективно при солитарных коллоидных узлах паренхиматозного типа строения, сочетающихся с увеличением ЩЖ и/или наличием в ткани железы зобных изменений, определяемых при ультразвуковом исследовании(УЗИ).
Левотироксин в лечении диффузного нетоксического зоба
Диффузный нетоксический зоб
Диффузный нетоксический зоб – общее диффузное увеличение щитовидной железы без нарушения ее функции. Основной причиной диффузного зоба является недостаточное содержание йода в окружающей среде и как следствие сниженное его потребление населением с привычными продуктами питания. В зависимости от распространенности диффузного зоба (ДЗ) в популяции различают спорадический и эндемический зоб. Зоб считается эндемическим, если в обследуемом регионе частота встречаемости зоба у детей младшего и среднего школьного возраста составляет более 5%. Хотя в подавляющем большинстве случаев причиной ДЗ является недостаточное поступление в организм человека йода, ряд закономерностей позволяет предположить о влияние генетических факторов на его формирование. Обращает на себя внимание тот факт, что в одном и том же регионе при одном и том же йодном обеспечении зоб определяется не у всего населения, а лишь у части. Важность генетических факторов подтверждена многими популяционными, семейными и близнецовыми исследованиями. Кроме того, при ДЗ выявлены некоторые мутации в таких генах, как ТРО, NIS, TG, TSHR.
Известно, что распространенность любых форм зоба в популяции существенно различается в зависимости от возраста. Считается, что ДЗ как первая стадия йододефицитного заболевания чаще встречается у молодых людей. Этот факт нашел свое подтверждение и на территории Москвы – зоны легкого йодного дефицита, при сравнении частоты встречаемости ДЗ в различных возрастных группах взрослого населения (рис. 1).
ДЗ достоверно чаще встречался у лиц моложе 45 лет.
Хотя пациенты с ДЗ, как правило, не предъявляют жалоб, функция ЩЖ у них не нарушена, они все же нуждаются в лечении данного заболевания, поскольку оно является первой фазой(обратимой при правильном лечении) формирования узлового и многоузлового йододефицитного зоба, в том числе и с развитием синдрома тиреотоксикоза на поздних стадиях процесса.
На сегодняшний день существует три варианта консервативной терапии ДЗ:
Как было сказано, назначение левотироксина широко применялось для лечения эутиреоидного ДЗ в прошлом. При этом на начальном этапе достигались отличные результаты. Во многих клинических исследованиях было показано, что уже через 3–4 мес от начала терапии происходило значительное (не менее 20%) уменьшение объема железы. Чаще же всего в клинической практике использовались дозы 150 мкг у взрослых и 100 мкг у подростков. Однако в многочисленных работах однозначно продемонстрирован «феномен отмены» – увеличение размеров ЩЖ почти до исходного уровня через короткое время после прекращения лечения. Данный феномен объясняется прежде всего тем, что при подавлении ТТГ снижается активность Na-I симпортера, а следовательно, уменьшается активный захват йода ЩЖ. На фоне резкого падения интратиреоидного содержания йода при отмене лекарственного препарата происходит новый рост железы. Также к нежелательным побочным явлениям терапии гормонами ЩЖ относят возможное возникновение лекарственного тиреотоксикоза, тахиаритмии, остеопороза, что ограничивает использование этой группы препаратов при длительном лечении ДЗ. Однако иногда для быстрого достижения терапевтического эффекта прибегают к кратковременному курсу лечения ДЗ Эутироксом с дальнейшим переходом на поддерживающую терапию Йодбалансом.
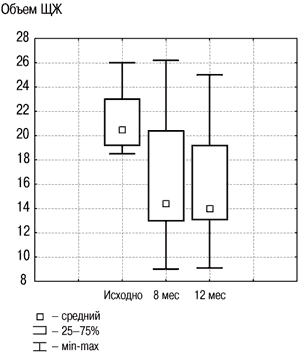
Рис. 2. Динамика объема ЩЖ в группе «Монотерапия препаратом йода» исходно, на 8 и 12-м месяце.
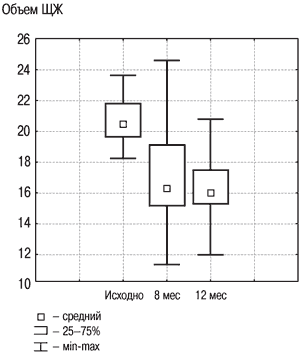
Рис. 3. Динамика объема ЩЖ в группе «Комбинированная терапия» исходно, на 8 и 12 месяце.
Таблица 3. Сравнение основных показателей между группами «Монотерапия» и «Комбинированная терапия» через 12 мес
| Показатель | Монотерапия | Комбинированная терапия | р (критерий) |
| Объем ЩЖ | 16,1 (13,1; 19,2) | 16,1 (15,2; 17,5) | 0,83 (Рм-у=0,21) |
| ТТГ | 0,9 (0,8; 1,1) | 1,2 (1; 1,48) | 0,07 (Рм-у=0,92) |
| АТ к ТПО*, % | 3 | 0 | 1 |
* – антитела к тиреоидной пероксидазе
Монотерапия препаратом йода и комбинированная терапия
Наиболее предпочтителен метод лечения ДЗ, являющийся этиологическим. Препараты йода назначают в физиологических дозировках (200 мкг в сутки) на 6 мес с последующей оценкой динамики объема ЩЖ.
При отсутствии выраженного эффекта от приема йодидов через 6 мес может быть рекомендован переход на комбинированную терапию. При этом предпочтение должно отдаваться либо фиксированной комбинации 75 мкг левотироксина +150 мкг йодида, либо индивидуально подобранной дозе Эутирокса из расчета 1 мкг на 1 кг массы тела в сочетании с 150 мкг йодида в сутки.
В настоящее время клиницисты имеют возможность использовать в этих целях комбинированные препараты, в состав которых входит как левотироксин, так и йод. Так, препарат Йодтирокс («Никомед») оптимально сочетает левотироксина натрий – 100 мкг и калия йодид – 100 мкг. Суточную дозу Йодтирокса принимают 1 раз в день утром, натощак, за 30 мин до завтрака, запивая таблетку небольшим количеством жидкости и не разжевывая.
Комбинированная терапия препаратами йода и тироксина, как было неоднократно показано, имеет ряд преимуществ. Во-первых, воздействуя на несколько патогенетических механизмов образования зоба, подавляется и гипертрофия, и гиперплазия тиреоцитов. Это позволяет добиться результатов, по эффективности сопоставимых с монотерапией тироксином (при гораздо меньшем его содержании), что в свою очередь уменьшает количество побочных эффектов, связанных с приемом тиреоидных препаратов. Во-вторых, снижается также склонность к «эффекту отмены» при кратковременном перерыве в лечении. В-третьих, менее выражено подавление уровня ТТГ, например по сравнению с эффектом тироксина в дозе 150 мкг.
Результаты исследования динамики объема ЩЖ у лиц с ДЗ на фоне разных схем терапии, проведенного в ФГУ ЭНЦ, представлены на рис. 2, 3. В целом по группе объем ЩЖ уменьшился на 20% к моменту завершения лечения, что явилось статистически значимым (р1–2
Литература
 Читайте также:
Читайте также: