Химическое сродство элементов к кислороду



Химическое сродство – способность реагирующих веществ образовывать новые соединения. Причинами, вызывающими химическое сродство, являются межатомные взаимодействия.
Значение химического сродства одних элементов по отношению к другим позволяет оценить характер взаимодействия различных веществ при сварке. Особенно значимы данные о сродстве элементов к кислороду. Существуют три основных способа оценки сродства элементов к кислороду:
– по тепловому эффекту реакции окисления;
– изменению изобарно-изотермического потенциала образованию окислов;
– упругости диссоциации окислов.
Оценка степени сродства элементов к кислороду по тепловому эффекту реакции.Степень сродства различных элементов к кислороду по тепловому эффекту реакции окисления оценивается при взаимодействии газообразного кислорода и вещества с образованием продуктов реакции в конденсированном виде, т.е. в жидком или твёрдом состоянии.
В этом случае тепловой эффект относится к одной граммолекуле кислорода, принимавшего участие в реакции. Такие реакции и их тепловые эффекты можно сравнивать между собой, и при этом чем больше значение теплового эффекта реакции, тем больше сродство реагирующих веществ к кислороду. Так, реакции:
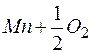
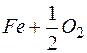
определяют следующий ряд элементов по увеличивающемуся сродству к кислороду: Fe, Mn, Si, Ti.
Оценка степени сродства к кислороду по изменению изобарно-изотермического потенциала. При наличии в системе газовой фазы кислорода направление протекания процессов определяется изменением изобарно-изотермического потенциала.
Если в реакции изобарно-изотермический потенциал уменьшается, процесс самопроизвольно развивается в направлении окисления; если этот потенциал увеличивается, значит самопроизвольное окисление невозможно, значение потенциала равно нулю, что отвечает состоянию равновесия. Чем меньше по своему значению изобарно-изотермический потенциал, тем больше сродство элемента к кислороду в этом окисле.
Оценка степени сродства элементов к кислороду по упругости диссоциации окислов. В сварочной металлургии наиболее распространена оценка степени сродства элементов к кислороду по упругости диссоциации окислов. В общем виде реакция окисления элемента с образованием конденсированного окисла определяется как:
Константа равновесия этой реакции
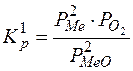
Так как значение парциального давления (упругость паров) не зависит от концентрации вещества, находящегося в конденсированном виде, и является величиной постоянной:
Величина Ро2 – давление свободного кислорода, необходимое для образования окисла данного элемента и отвечающее состоянию равновесия данной реакции называют упругостью диссоциации данного окисла MeO. Таким образом, упругость диссоциации химического соединения есть концентрация (давление) газообразного компонента (кислорода) в равновесной системе, выраженная в атмосферах.
Чем меньше значение упругости диссоциации химического соединения – окисла, тем прочнее этот окисел.
Поскольку давление свободного кислорода для образования окисла очень мало, то пользуются значением логарифма давления, т.е. lg Po2, который определяется как:
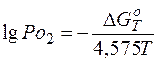
Чтобы определить, в каком направлении может протекать реакция образования окисла, следует сопоставить расчётное значение lg Po с логарифмом действительного парциального значения давления кислорода при протекании реакции (в нашем случае – атмосферное, т.е. Po2).
Возможны три соотношения этих величин:
а) lg Po2 = lg [Po2] – реакция находится в состоянии равновесия;
б) lg Po2 > lg [Po2] – наблюдается восстановление элемента из окисла;
При больших температурах значения упругости диссоциации окислов элементов выравниваются между собой по сравнению со значениями при низких температурах. Так, при Т = 2400 °С разница между значениями упругости диссоциации железа Si и Mn соответственно 3,62 и 3,82, а при Т = 1500 °С соответственно 7,18 и 5,98. Таким образом, наибольший эффект раскисления Si и Mn проявляется в низкотемпературной части сварочной ванны.
4. В отличие от Si, Mn и других раскислителей углерод с уменьшением температуры теряет раскисляющую способность, а при высоких температурах углерод является самым сильным раскислителем.
Химическое сродство элемента к кислороду тем больше, чем больше по абсолютной величине отрицательное значение DG 0 .
Из справочных данных следует, что у никеля, меди и молибдена химическое сродство к кислороду заметно ниже, чем у железа, поэтому эти элементы в присутствии жидкого железа (при продувке кислородом в конвертере) не окисляются.
Очень велико химическое сродство к кислороду у кальция, алюминия, магния, поэтому, если их ввести в конвертерную ванну, они окислились бы за несколько секунд.
Обычные составляющие жидкой конвертерной ванны: кремний, марганец и углерод имеют более высокое химическое сродство к кислороду, чем железо, поэтому при продувке окисляются эти элементы, а не железо.
При низких температурах (1450–1500°С и менее) химическое сродство к кислороду у кремния и марганца выше, а при более высоких температурах – ниже, чем у углерода.
По этой причине кремний и марганец всегда окисляются в начале продувки, когда температура в конвертере сравнительно невысока.
Иногда химическое сродство элементов к кислороду оценивают по давлению диссоциации оксида; чем ниже давление диссоциации, тем прочнее оксид и тем выше химическое сродство составляющих оксида.
Принцип смещения равновесия (принцип Ле-Шателье) заключается в том, что установившееся равновесие химического процесса смещается, если изменить внешние условия.
Использование этого принципа позволяет изменять ход реакций в необходимом направлении.
Этот принцип можно сформулировать следующим образом: если на систему, находящуюся в равновесии, оказано внешнее воздействие, то равновесие в ней смещается в направлении, уменьшающем оказанное воздействие.
1) если повысить температуру, то реакция пойдет в направлении, сопровождающемся поглощением тепла, и наоборот;
2) если в систему добавить компоненты, стоящие в уравнении реакции слева, например, компоненты А и В в реакции: A + B = C + D, то равновесие реакции сдвинется вправо, т.е. в сторону уменьшения количества веществ А и В и наоборот;
3) если в реакциях, идущих с участием газовой фазы, повысить давление, то реакция пойдет в направлении с уменьшением числа молей газообразных веществ, поскольку давление в системе тем меньше, чем в ней меньше молекул газа.
Чтобы распечатать файл, скачайте его (в формате Word).
Что такое сродство с кислородом
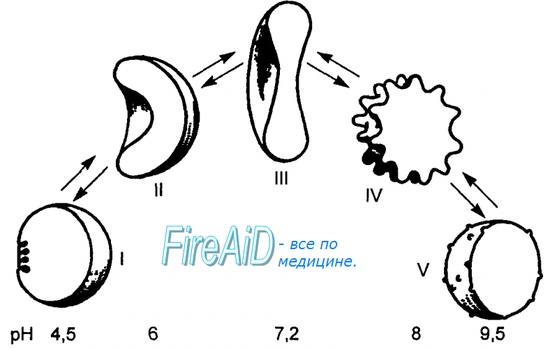
Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов.
Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц.
Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН.
Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани.
Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей.
Физико-химические процессы производства стали
Условия развития химических процессов, ведущих к изменению состава взаимодействующих фаз — металла, шлака и газа — в кислородном конвертере, характеризуется высоким начальным давлением дутья [до 1,013—1,217 Мн/м 2 (10—12 ат)], его высоким окислительным потенциалом, наличием ограниченной реакционной зоны с высокими температурами по границам контакта окислительного потока с расплавом и сильно развитым перемешиванием металла и шлака вследствие кинетической энергии дутья и газообразных продуктов обезуглероживания ванны.
Высокий окислительный потенциал газовой фазы создает условия одновременного развития реакций окисления элементов металлического расплава — кремния, марганца и углерода.
Соотношения скоростей процессов шлакообразования, реакций на границе шлак—металл и реакций в объеме металла тесно связаны с интенсивностью и организацией потока окислителя.
Управление дутьевым режимом конвертерной плавки путем изменения высоты кислородной фурмы и минутного расхода кислорода, а также применения фурм с соплами различной конструкции является мощным средством регулирования окислительных процессов во взаимодействующих фазах.
Химическое сродство характеризует способность веществ вступать в химическое взаимодействие. Если в системе имеется несколько веществ, то в первую очередь вступают в химическую реакцию те из них, которые обладают наибольшим химическим сродством друг к другу. Чем больше химическое сродство, тем прочнее получающееся химическое соединение. В конвертерной плавке прежде всего важны данные о химическом сродстве элементов к кислороду.
Мерой химического сродства двух вступающих в химическое взаимодействие (реакцию) элементов является изменение при этой реакции энергии Гиббса ∆G o (прежнее название энергии Гиббса — свободная энергия, т. е. это та часть выделяющейся при реакции энергии, которая высвобождается и может быть превращена в работу).
Рисунок 1. Химическое сродство элементов к кислороду при различных температурах
Из данных рис. 1 следует, что у никеля, меди и молибдена химическое сродство к кислороду заметно ниже, чем у железа, поэтому эти элементы в присутствии жидкого железа (при продувке кислородом в конвертере) не окисляются. Очень велико химическое сродство к кислороду у кальция, алюминия, магния, поэтому если их ввести в конвертерную ванну, они окислились бы за несколько секунд.
Обычные составляющие жидкой конвертерной ванны: кремний, марганец и углерод имеют более высокое химическое сродство к кислороду, чем железо, поэтому при продувке окисляются эти элементы, а не железо.
При низких температурах (1450—1500°С и менее) химическое сродство к кислороду у кремния и марганца выше, а при более высоких температурах — ниже, чем у углерода. По этой причине кремний и марганец всегда окисляются в начале продувки, когда температура в конвертере сравнительно невысока.
Иногда химическое сродство элементов к кислороду оценивают по давлению диссоциации оксида; чем ниже давление диссоциации, тем прочнее оксид и тем выше химическое сродство составляющих оксида.
Принцип смещения равновесия (принцип Ле-Шателье) заключается в том, что установившееся равновесие химического процесса смещается, если изменить внешние условия. Использование этого принципа позволяет изменять ход реакций в необходимом направлении. Этот принцип можно сформулировать следующим образом: если на систему, находящуюся в равновесии, оказано внешнее воздействие, то равновесие в ней смещается в направлении, уменьшающем оказанное воздействие. Так, если повысить температуру, то реакция пойдет в направлении, сопровождающемся поглощением тепла, и наоборот. Если в систему добавить компоненты, стоящие в уравнении реакции слева (например, компоненты А и Б в реакции: А+В = С + D), то равновесие реакции сдвинется вправо (в сторону уменьшения количества веществ А и В) и наоборот.
Изменение давления влияет на реакции, идущие с участием газовой фазы. Если, например, повысить давление, то реакция пойдет в направлении с уменьшением числа молей газообразных веществ (поскольку давление в системе тем меньше, чем в ней меньше молекул газа).
Знание принципа Ле-Шателье облегчает управление процессами конвертерной плавки.
Например, легко решить, каким должен быть шлак, чтобы более полно шла реакция десульфурации: [S] + F e+ (CaO) = (CaS) + (FeO). В соответствии с принципом Ле-Шателье реакция пойдет вправо, если увеличить концентрацию компонентов, стоящих в левой части уравнения, и уменьшить концентрацию компонентов, стоящих в правой части. Следовательно, для более полной десульфурации (ход реакции вправо) шлак должен содержать большое количество СаО и малое FeO.
Основные реакции конвертерных процессов
На рис. 2 показано изменение состава металлической и шла ковой фазы, а также температуры ванны по ходу кислородно-конвертерного процесса. Процесс характеризуется отсутствием четко выраженных периодов окисления отдельных элементов (кремний и марганец, углерод, фосфор), типичных для донной продувки воздушным дутьем. Это должно быть связано со значительным избытком кислорода в ограниченной реакционной зоне и наличием областей повышенных температур металла. Дополни тельным условием является высокая реакционная способность шлака, содержащего окислы железа и кальция.
Рис. 2. Изменение состава и температуры металла (а) и состава шлака (б) по ходу кислородно-конвертерного процесса в конвертере емкостью 100 т
Окисление кремния
Окисление кремния заканчивается за первые 3—5 мин процесса в зависимости от его концентрации в перерабатываемом чугуне.
Реакции, отражающие этот процесс: [Si] + O2 = (SiO2) и [Si] + (FеО) = (SiO2) + [Fе], показывают возможность непосредственного реагирования кремния с газообразным окислителем или с образующейся закисью железа шлака.
Одновременно с окислением кремния окисляется и марганец по аналогичным реакциям, однако этот процесс в условиях кислородного конвертера протекает с меньшей полнотой. Переход марганца в шлак обычно ограничивается остаточными содержаниями в металле 0,2—0,4%, которые по ходу дальнейшей продувки могут дополнительно повышаться вследствие восстановления марганца из шлака по реакциям: (МnО) + [Fе ] = [Мn] + (FеО), (МnО) + [С] = [Мn] + СО.
Заметное развитие восстановления марганца связано с высокотемпературным состоянием высокоосновного шлака, повышенной активностью в нем закиси марганца и пониженным содержанием и активностью FеО в условиях интенсивного обезуглероживания металла. При содержании марганца в чугуне 1,0—1,5% конечное его содержание в стали обычно составляет 0,3—0,6%, что позволяет экономить ферромарганец при доведении состава металла до заданной марки.
Окисление углерода.
Окисление углерода. Окисление избыточного углерода — одна из основных задач конвертерной плавки, поскольку чугун содержит от 2,8 до 4,6% С, а выплавляемая сталь — значительно меньше.
Углерод при температурах сталеплавильных процессов окисляется в основном до СО (до СО2 окисляется менее 10% углерода). Окисление углерода, растворенного в металле, может происходить по следующим реакциям:
[С]+ 1/2 О2 = СО+ 152470 Дж/моль;
[С] + [О] = СО + 22370 Дж/моль;
[С] + (FеО) =СО + Fе—98840 Дж/моль.
Третья реакция сопровождается поглощением тепла, о чем свидетельствует знак минус.
Окисление углерода сопровождается образованием газовой фазы — пузырей СО. Растворимость СО в железе ничтожно мала, поэтому при окислении углерода из ванны выделяются пузыри СО, вызывая эффект кипения ванны, ее перемешивание и вспенивание.
Реакция окисления углерода необратима, так как продукт реакции СО удаляется из ванны. Скорость реакции окисления углерода определяется скоростью подачи окислителя (кислорода) и условиями образования и выделения газообразного продукта реакции СО.
В любой точке конвертерной ванны пузырь СО может образоваться, если давление в нем (Рсо) превысит следующую величину:
Рсо ≥ Ратм + Рмет + Ршл + Р п.н.
То есть превысит суммарное давление, создаваемое:
С учетом этих величин установлено, что внутри жидкого металла образование пузырей СО невозможно, т. е. реакция окисления углерода может идти на поверхности раздела металла с уже имеющейся газовой фазой (вдуваемые струи кислорода, всплывающие из ванны пузыри СО). По сравнению с другими сталеплавильными агрегатами в кислородных конвертерах создаются благоприятные условия для окисления углерода (в объеме металла постоянно имеются газовые полости в результате внедрения кислородных струй в ванну).
Реакция окисления углерода занимает особое место среди других, поскольку при выделении газа СО обеспечивается перемешивание ванны; выравнивание состава и температуры; удаление из металла вредных газов водорода и азота; ускорение всех реакций между металлом и шлаком, так как при перемешивании возрастает поверхность контакта металл—шлак.
Продувка до низких содержаний углерода в металле
Продувка до низких содержаний углерода в металле представляет определенные трудности. Продувка сверху позволяет без затруднений получать содержание углерода в металле 0,05—0,06%; при дальнейшем вдувании кислорода для более полного окисления углерода существенно усиливается окисление железа, оксиды которого переходят в шлак, т. е. сильно возрастают потери железа со шлаком (в виде FеО и Fе2O3).
При донной и комбинированной продувке создаются более благоприятные условия для полного и быстрого окисления углерода, и без сильного переокисления шлака и металла можно получить содержание углерода в металле 0,02—0,03 % и менее. Причины этого заключаются в следующем:
Кроме того, после окончания кислородной продувки часто проводят перемешивающую продувку снизу аргоном; при этом также продолжается окисления углерода кислородом.
FеО, содержащегося в шлаке, что позволяет получать в металле содержание углерода
Важнейшей особенностью кислородно-конвертерного процесса является быстрое окисление фосфора.
Дефосфорация.
Удаление фосфора из металла в шлак протекает в две стадии, первая из которых — образование Р2О5 :
Если просуммировать эти две реакции, то получим итоговую реакцию удаления фосфора:
идущую с выделением значительного количества тепла (≈ 700 000 Дж/моль).
Реакция может протекать лишь до равновесного состояния, определяемого температурой и составом шлака. После достижения равновесия удаление в шлак фосфора происходить не будет. Полноту протекания реакции часто характеризуют коэффициентом распределения фосфора между шлаком и металлом (Р2О5)/[Р].
Более полному удалению фосфора в шлак (сдвигу равновесия реакции вправо) способствует увеличение основности шлака CaO/SiO2 (или содержания СаО), повышение окисленности шлака (или содержания FeO) и относительно низкая температура.
Наряду с этим достигаемая за время плавки степень удаления фосфора зависит от скорости протекания реакции дефосфорации, которая зависит от площади поверхности контакта металл—шлак и вязкости шлака. Поскольку реакция идет на границе металл—шлак, более быстрому ее протеканию способствует увеличение поверхности контакта металл—шлак, т. е. улучшение перемешивания металла со шлаком. Ускорению протекания реакции способствует также снижение вязкости шлака, поскольку в вязких шлаках затруднена диффузия компонентов, участвующих в реакции.
Вязкость шлака снижается при увеличении количества разжижающих компонентов (CaF2, FeO и др.) и повышении температуры.
С учетом изложенного необходимо отметить, что влияние температуры на дефосфорацию двояко; при снижении температуры равновесие реакции дефосфорации сдвигается в сторону более полного удаления фосфора, но скорость дефосфорации понижается вследствие увеличения вязкости шлака.
Большое значение имеет также количество шлака, поскольку при одном и том же коэффициенте распределения количество фосфора, перешедшего в шлак, тем больше, чем больше масса шлака.
В конвертерах с продувкой сверху реакция дефосфорации равновесного состояния не достигает; в большей степени она приближается к равновесию при донной и комбинированной продувке, где интенсивность перемешивания металла со шлаком значительно выше.
Десульфурация.
Сера при конвертерной плавке, как и при других сталеплавильных процессах, удаляется из металла в основной шлак по реакции: [S] + Fe + (CaO) = (CaS) + (FeO), тепловой эффект которой очень мал.
Эта реакция, как и реакция удаления фосфора, может идти до определенного равновесного состояния, после достижения которого удаления серы из металла происходить не будет. Полноту протекания реакции часто характеризуют коэффициентом распределения серы между шлаком и металлом (S )/[S ].
Более полному удалению серы (сдвигу равновесия реакции вправо) способствуют высокая основность шлака и низкое содержание в нем FеО. Поскольку тепловой эффект реакции близок к нулю, изменение температуры практически не вызывает смещения ее равновесия.
Полнота десульфурации так же, как и дефосфорации, зависит от скорости протекания реакции и возрастает при увеличении поверхности контакта металл—шлак (улучшении их перемешивания) и снижении вязкости шлака. Повышение температуры способствует удалению серы, поскольку вследствие снижения при этом вязкости шлака десульфурация происходит с большей скоростью. Увеличение количества шлака также обеспечивает получение более низкого содержания серы в металле.
Поскольку конвертерные шлаки содержат большое количество FеО, условия для протекания реакции десульфурации в кислородном конвертере неблагоприятные и десульфурация получает ограниченное развитие. При продувке сверху коэффициент распределения (S)/[S] составляет 2—12; степень десульфурации (доля удаленной серы, % от исходного содержания) не превышает 30—40%.
Отходящие газы практически состоят из окиси и двуокиси углерода.
Наличие в их составе СО2 свидетельствует о неполноте использования кислорода на окислительные реакции с металлическим расплавом, которая особенно проявляется в начале процесса при режиме незаглубленной струи. Соответствующие данные приведены на рис. 3. Из них видно, что содержание СО2 в этот период может достигать 20%, что свидетельствует о недоиспользовании окислителя на обезуглероживание. Однако в зоне струи, а также при ее реагировании с металлом, как показывают экспериментальные данные и расчеты, содержание СО2 должно быть более высоким. Наряду со свободным кислородом двуокись углерода в основном расходуется на окислительные реакции с расплавом: СО2 + [С] = 2СО; СО2 + [Fе] = (FеО) + СО.
Рисунок 3. – Изменение содержания СО2 в отходящих газах по ходу кислородно-конвертерной плавки
Раскисление стали.
В конце продувки металл в конвертере содержит 0,03—0,08 % растворенного кислорода, в твердом железе при комнатной температуре растворимость кислорода (количество, которое может удерживаться в растворе) не превышает 0,003 %. Если не удалить этот избыточный кислород, то он выделится в процессе затвердевания и из затвердевшего металла, что вызовет возникновение многих дефектов. К их числу относятся: красноломкость, вызываемая выделением оксидных пленок по границам зерен при кристаллизации; пузыри, обращующиеся в результате взаимодействия растворенного кислорода с углеродом; старение стали; большое количество оксидных неметаллических включений, вызывающих снижение ударной вязкости и ряда других механических свойств стали; снижение пластичности стали и др.
Для предотвращения возникновения этих дефектов производят раскисление стали. По степени раскисленности стали делят на спокойные (полностью раскисленные), кипящие и полуспокойные.
Раскисление спокойной стали.
Целью раскисления спокойной стали является снижение до минимума количества растворенного в жидкой стали кислорода и по возможности более полное его удаление из жидкого металла. Конвертерную сталь раскисляют осаждающим методом: в металл вводят раскислители — элементы, обладающие большим химическим сродством к кислороду, чем железо. Они взаимодействуют с растворенным кислородом, образуя оксиды, которые нерастворимы в жидкой стали и выделяются в объеме металла в виде мелких частиц самостоятельной фазы.
Спокойную сталь раскисляют марганцем, кремнием, алюминием, а в некоторых случаях кальцием, редкоземельными металлами (РЗМ) и др. Раскисление происходит по следующим реакциям:
Продукты раскисления (оксиды) должны быть удалены из металла. Поскольку оксиды легче металла, они всплывают, что обеспечивает удаление части продуктов раскисления; улучшение их удаления достигается при перемешивании металла, например, продувкой в ковше аргоном, порошкообразными материалами. Оставшиеся мелкие оксиды составляют основную часть обнаруживаемых в затвердевшей стали оксидных неметаллических включений; они ухудшают качество стали.
Элементы-раскислители имеют неодинаковую раскислительную способность; чем выше химическое сродство элемента к кислороду, тем выше его раскислительная способность, т. е. тем меньше останется в жидком металле растворенного кислорода после добавки данного раскислителя. По мере увеличения раскислительной способности элементы-раскислители располагаются в следующей последовательности: марганец, кремний, алюминий, титан, кальций, РЗМ. Обычно соблюдают следующий порядок раскисления — сначала вводят слабый раскислитель (марганец), затем более сильные (кремний, затем алюминий). Марганец и кремний вводят в виде ферросплавов, алюминий в чистом виде.
Раскисление кипящей и полуспокойной стали.
Целью раскисления кипящей и полуспокойной стали является снижение содержания растворенного кислорода до уровня, обеспечивающего требуемую интенсивность кипения металла в изложнице. Кипящую- сталь раскисляют только слабым раскислителем — марганцем; полуспокойную — марганцем и небольшим количеством кремния.
Сталеплавильные шлаки.
Конвертерный, как и все сталеплавильные процессы, сопровождается образованием шлаков. Шлак — это сплав оксидов с небольшим количеством СаS, МnS и иногда СаF2.
Основные и кислотные оксиды обладаю: высоким химическим сродством друг к другу.
Амфотерные ведут себя в основной среде как кислотные, а в кислотной среде как основные.
В результате химического взаимодействия оксидов в шлаках образуется большое количество различных соединений (2Ca0*SiО2; 2FeO • SiО2; CaO • Fe2О3; MnO • SiО2 и много других), часть из них диссоциирована.
Таким образом, шлаки состоят как из свободных оксидов, так и из связанных в различные химические соединения.
Различают основные и кислые шлаки. Основными называют шлаки, в которых преобладают основные оксиды (прежде всего СаО); кислыми называют шлаки, в которых преобладают кислотные оксиды (обычно S iО2). Конвертерные шлаки являются основными; их главные составляющие СаО (43—53%), SiO2 (14-22%), МnО (до 12%).
Шлак должен обладать определенными физико-химическими свойствами, наиболее существенно на технологию плавки влияют следующие свойства основных шлаков.
При слишком высокой вязкости (густые шлаки) замедляется удаление в шлак фосфора и серы и другие процессы обмена между металлом и шлаком; при низкой вязкости (жидкоподвижные шлаки) в шлаке быстро растворяется футеровка.
Вязкость основного шлака увеличивается при росте содержания в нем CaO, MgO, Сг2О 3 и снижается при увеличении содержания CaF2, А12О3, Si02, Fe2О3. Для снижения вязкости (разжижения) в шлак вводят вещества, содержащие CaF2, А12О3, Fe2О 3, Na2О и др.