Что такое гидроцеле (водянка яичка)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Лелявина Кирилла Борисовича, уролога со стажем в 28 лет.
Определение болезни. Причины заболевания
Как правило у новорожденных мальчиков гидроцеле проходит само в течении нескольких месяцев, при условии, что у ребенка нет сопутствующей паховой грыжи — патологического потенциально жизнеугрожающего состояние, при котором в грыжевой мешок через паховый канал выходят органы брюшной полости.
Причины возникновения гидроцеле у взрослых мужчин:
Симптомы гидроцеле
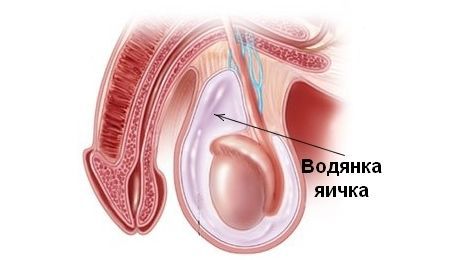
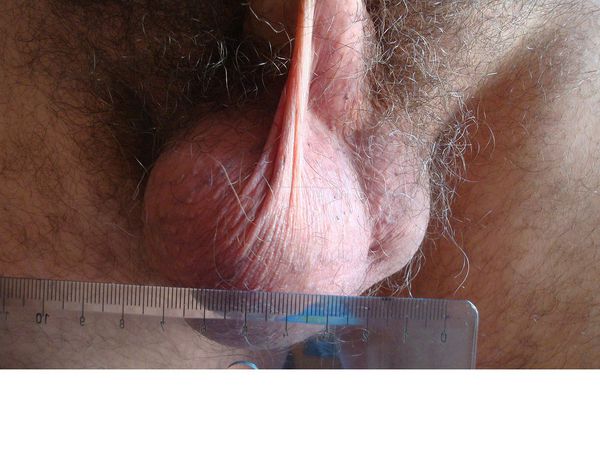
В большинстве случаев единственным признаком гидроцеле или водянки яичка является безболезненное увеличение размера мошонки за счёт отёка и скопления жидкости. Бессимптомное течение гидроцеле — самый распространенный вариант.
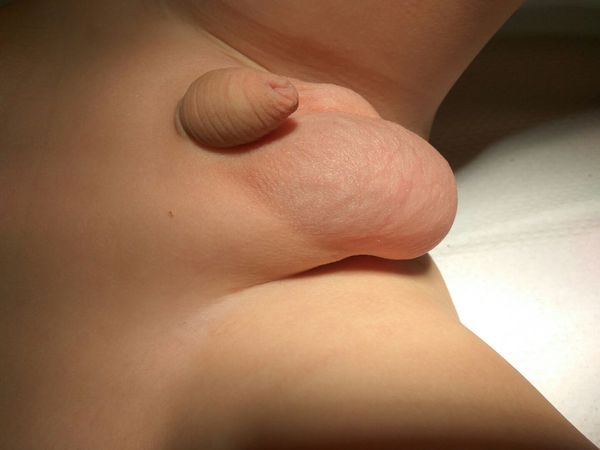
Родители новорожденных мальчиков могут обратить внимание на следующие признаки. Гидроцеле выглядит так, как будто у ребёнка одно яичко намного больше другого, или у мальчика просто большая мошонка.
Взрослые мужчины с гидроцеле могут испытывать некоторый дискомфорт в области мошонки в зависимости от степени развития отёка и количества накопившейся жидкости. У взрослого мужчины происходит постепенное, прогрессирующее увеличение мошонки без сопутствующей боли, появляется ощущение распирания. Чаще всего гидроцеле обнаруживается при самостоятельном осмотре, либо случайно на осмотре у врача.
В некоторых случаях у взрослых мужчин с гидроцеле может присоединиться болевой синдром, связанный с количеством накопившейся жидкости. Иногда пациент испытывает жгучую боль, отдающую в паховую область и половой член.
Хроническое гидроцеле возникает после острого гидроцеле, а также в результате травмы. В некоторых случаях хроническое гидроцеле может быть сопутствующим заболеванием, например при опухоли яичка у взрослых мужчин.
Патогенез гидроцеле
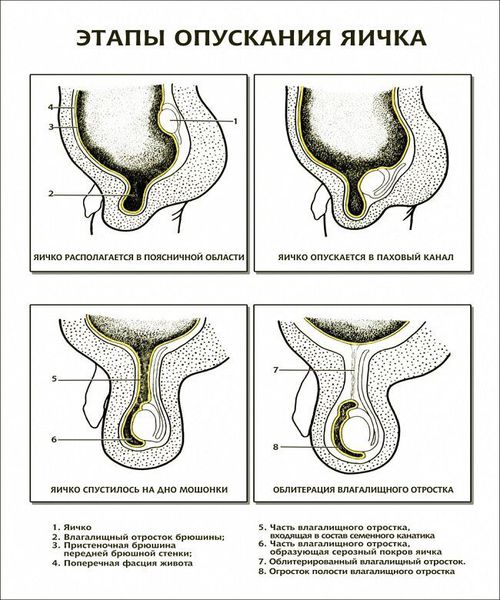
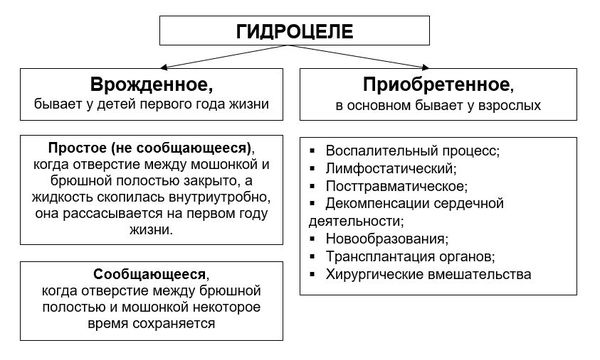
Происхождение гидроцеле объясняется тремя ведущими теориями: врожденного, травматического и инфекционного происхождения. К сожалению, не всегда удается установить истинную причину развития заболевания.
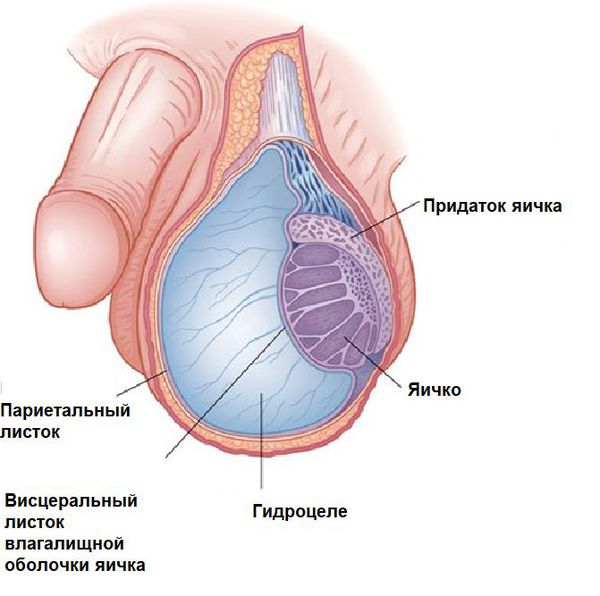
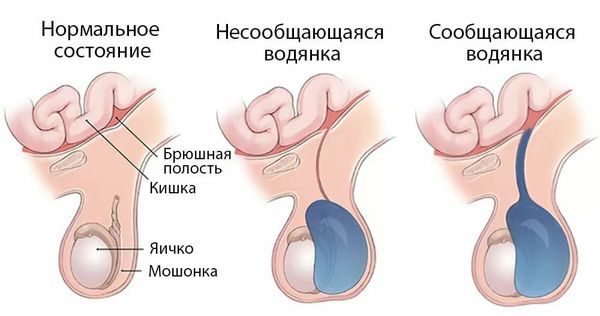
В дальнейшем при повышении внутрибрюшного давления (например когда ребёнок плачет или болеет) через отверстие в полость мошонки поступает серозная жидкость или кишечная петля (формируется грыжа). Формирование грыжи требует оперативного лечения. Что касается жидкости, то при патологии она попадает в мошонку и не успевает всасываться, приводя к формированию водянки. Со временем отверстие может закрыться, а остатки серозной жидкости в мошонке впитаются. Если этого не происходит в течение 2-х лет после рождения ребёнка, необходимо проведение операции.
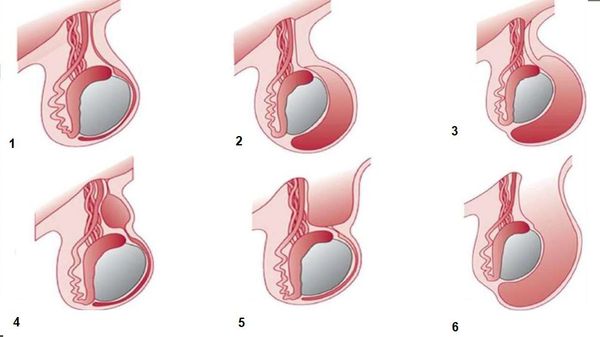
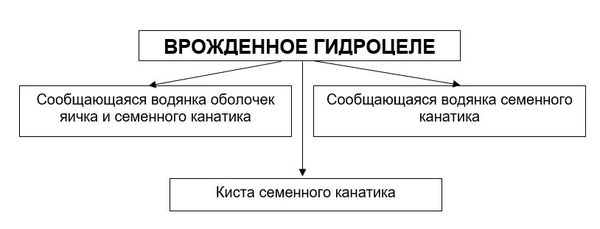
На рисунке ниже представлены виды водянки оболочек яичка:
Приобретенное гидроцеле формируется по ряду причин:
При травматическом повреждении органов мошонки может наступить обструкция (нарушение проходимости) лимфатического протока, что приводит к формированию гидроцеле.
Классификация и стадии развития гидроцеле
В МКБ-10 выделяют следующие формы водянки оболочек яичка и семенного канатика:
По клинической классификации гидроцеле подразделяют:
Осложнения гидроцеле
Если гидроцеле вызвано острой инфекцией или травмой, к нему могут присоединиться гематоцеле (скопление крови) и пиоцеле (скопление гноя), возникающие из-за инфекций. В таких случаях требуется интенсивное лечение.
Если своевременно не приступить к лечению или отсрочить проведение операции, имеющееся длительное время гидроцеле может способствовать:
Диагностика гидроцеле
Любое изменение в области мошонки требует обращения за помощью к урологу без промедления. Необходимо помнить, что злокачественные опухоли яичка имеют сходные симптомы, связанные с изменением размеров мошонки, поэтому пациент должен быть обязательно обследован.
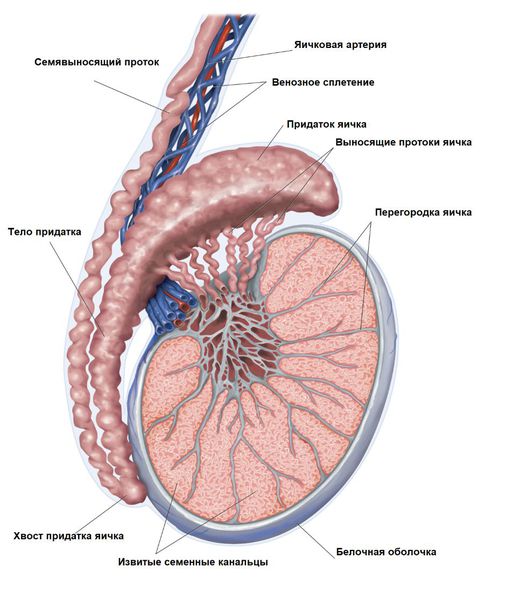
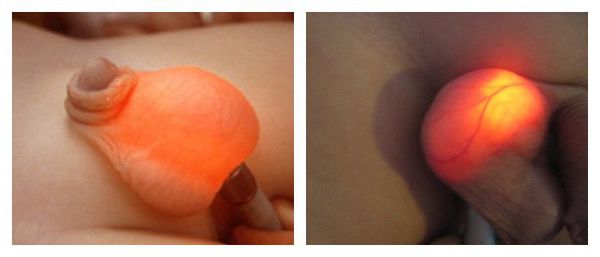
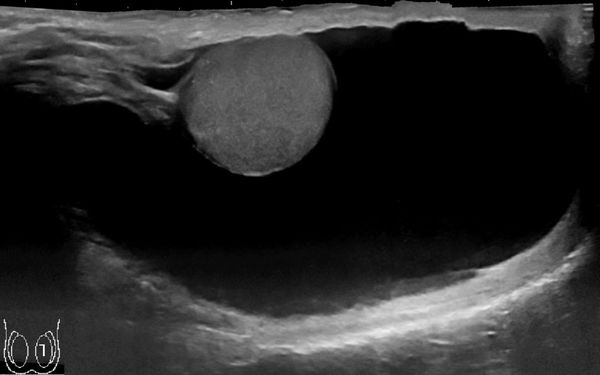
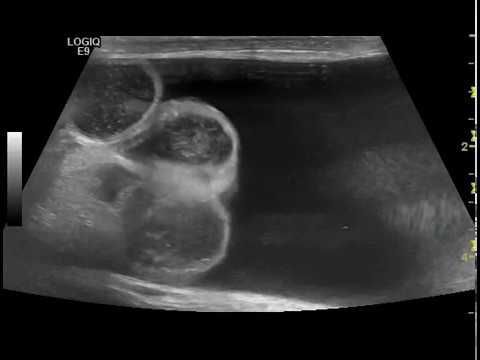
Постановка диагноза гидроцеле не вызывает затруднений и основана на данных характерного анамнеза (истории заболевания), осмотра и пальпации (ощупывания), проведения диафаноскопии и ультразвукового исследования органов мошонки.
При хроническом гидроцеле кожа мошонки может быть не изменена, размеры увеличения могут быть различными. Осмотр проводят в положении лежа и стоя, обращают внимание не только на размер мошонки, но и на её консистенцию: она может быть мягко-эластической, плотноэластической и напряжённой.
Помимо объективного исследования мошонки назначают лабораторные исследования. Однако они не специфичны: к ним относят общий анализ крови, анализ мочи, биохимию крови, коагулограмму, анализ мазка из мочеиспускательного канала на урогенитальную флору.
Отрицательный результат диафаноскопии при наличии патологии встречается в следующих случаях:
Гидроцеле является сопутствующей патологией у 5 % пациентов с паховыми грыжами. Диафаноскопия позволяет проводить дифференциальный диагноз с паховыми и пахово-мошоночными грыжами, в том числе и с ущемлёнными. У мальчиков подросткового возраста в первую очередь необходимо дифференцировать гидроцеле от опухоли яичка. В последние годы с появлением ультразвукового исследования мошонки значение диафаноскопии в диагностике заболевания утрачивается. УЗИ мошонки позволяет поставить диагноз со 100 % точностью и провести дифференциальную диагностику.
Лечение гидроцеле
Однако если гидроцеле не прошло в течение двух лет после рождения ребёнка, потребуется операция. Если в старшем возрасте гидроцеле не удалять хирургическим путем, оно способно продолжать рост. Проведение оперативного вмешательства рекомендуется для всех детей с гидроцеле в возрасте старше 2 лет в плановом порядке.
Наиболее радикальным и эффективным методом лечения гидроцеле считается хирургическое лечение. Прежде всего это открытые хирургические вмешательства:
Это миниинвазивные операции с видеоассистированием при иссечением оболочек яичка. Основная задача большинства перечисленных методов направлена на ликвидацию серозной полости между пластинками влагалищной оболочки яичка. Выполненная операция должна соответствовать определенным требованиям:
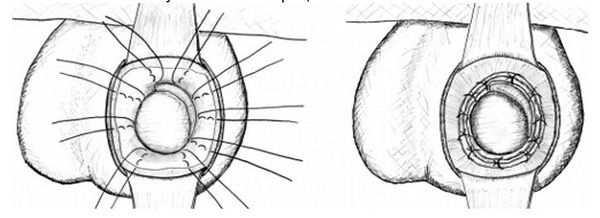
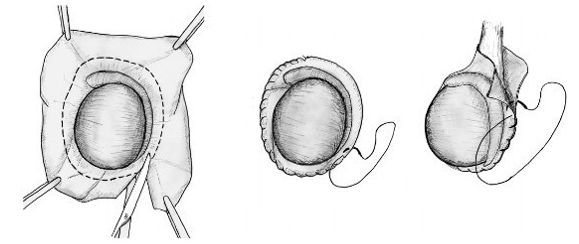
При водянке оболочек яичка в большинстве клиник России предпочтение отдается трём видам открытых оперативных вмешательств:
Операция Винкельмана. При этом оперативном вмешательстве один из листков собственной оболочки яичка рассекают по передней поверхности, выворачивают наизнанку и сшивают позади яичка. При этом накопления жидкости больше не происходит. Данная операция заключается в выполнении разреза длиной 4–5 см на передней
поверхности мошонки на стороне наличия гидроцеле. Выполняется рассечение всех оболочек вплоть до влагалищной. Яичко выводится в рану. Далее проводится пункция влагалищной оболочки и эвакуация жидкости. Затем эта оболочка также рассекается и яичко обнажается. Производится осмотр яичка и его придатка.
Далее выполняется пластика оболочек яичка по Винкельману: оболочки выворачиваются и сшиваются. Жидкость, продуцируемая эпителием влагалищной оболочки яичка, будет всасываться окружающими тканями. Далее яичко погружается в рану, производится послойный шов раны, с оставлением дренажной полутрубки, которая удаляется на следующие сутки после операции, накладывается тугая повязка. Швы снимаются на 10-е сутки после операции.
Операция Бергмана. Выполняют разрез кожи над водянкой. Водяночный мешок очищается от фасций и прокалывается троакаром, серозную жидкость собирают в подготовленную посуду. Оболочки’ яичка иссекаются, проводится тщательный гемостаз и яичко вновь помещается в своё ложе. Под яичко устанавливают дренаж. Кожа ушивается — антибактериальным, саморассасывающимся, косметическим материалом, который не оставляет рубцов. Накладывается асептическая повязка. Правильно проведенная операция Бергмана устраняет возможность появления осложнений. Повреждение семенного канатика при операции Бергмана также исключается. В послеоперационном периоде назначаются антибактериальные препараты. В течение некоторого времени необходимо ношение суспензория.
Операция Лорда. При этой операции проводится рассечение оболочек яичка, высвобождение водяночной жидкости и гофрирование влагалищной оболочки вокруг яичка. При этом само яичко от окружающих тканей не освобождается и в рану не вывихивается. Это позволяет снизить травматизацию прилежащих тканей и питающих сосудов яичка.
Прогноз. Профилактика
Для взрослых мужчин к основным факторам риска, способствующим формированию гидроцеле, относятся:
Чтобы избежать развития водянки яичка и сохранить репродуктивное здоровье, необходимо оберегать органы промежности от травматического повреждения, своевременно лечить инфекционные заболевания, не перенапрягаться, вести здоровый образ жизни и повышать свою медицинскую грамотность.
9 причин не игнорировать симптомы гастроэзофагеальной рефлюксной болезнь
Актуальная проблема
Для большинства людей, изжога – это просто случайно возникший дискомфорт. Примерно 20% населения высокоразвитых стран испытывают ее не реже одного раза в месяц.
Но для 6% людей, которые имеют хроническую форму изжоги, известную как гастроэзофагеальная рефлюксная болезнь (ГЭРБ), не купированные (не леченные) симптомы могут привести к различным осложнениям для здоровья. Люди с эрозиями на слизистой пищевода из-за кислого рефлюкса часто не осознают вреда от ГЭРБ, пока у них не разовьется запущенная стадия болезни.
Если вы испытываете частую или длительную изжогу (два раза в неделю на регулярной основе), обратитесь к врачу. Вот девять причин, почему Вы не должны игнорировать симптомы гастроэзофагеальной рефлюксной болезни.
1. Развитие воспаление в пищеводе (эзофагит)
При гастроэзофагеальной рефлюксной болезни пища, кислота и пищеварительные соки забрасываются в пищевод. Со временем это вызывает раздражение и отек слизистой, выстилающей пищевод изнутри. Это и есть эзофагит. Если кислотное воздействие в пищеводе наблюдается в течение всего лишь нескольких недель, то уже может развить воспаление слизистой. Это может вызывать дискомфорт и, даже боль, по срединной линии брюшной стенки, «под ложечкой», где сходятся правые и левые ребра у грудины. Это воспаление делает пищевод уязвимым для еще более опасных состояний – эрозий или рубцов.
2. Стриктура пищевода
Если эзофагит продолжается слишком долго, то возникающая рубцовая ткань, может сузить пищевод. Это стриктура может привести к трудностям прохождения и глотания пищи, которая может застревать на уровне образования рубцовой ткани, вызывая боль.
Большие куски пищи могут застрять и эта ситуация может потребовать эндоскопического вмешательства для их удаления. Стриктура может вызывать частые подавливания при приеме пищи. Из-за этого пациенты часто отказываются от еды и теряют много в весе.
Стриктура лечится расширением или растяжением пищевода (бужирование или дилятация). Эти лечебные процедуры могут быть неоднократными по воздействию на стрикутуру. Но прием блокаторов продукции кислоты в желудке (ингибиторы протонной помпы, ИПП или Н2-блокаторы) могут помешать возвращению рубцовых изменений в пищеводе в дальнейшем.
3. Проблемы с горлом и голосом
Основным симптомом гастроэзофагеальной рефлюксной болезни является изжога, но не все люди ее чувствуют и описывают. У них могут быть другие, более сложные для диагностики симптомы. Врачи называют эти случаи «немой рефлюкс», или бессимптомный рефлюкс. У пациента может не быть изжоги, как это классически описано в учебниках, но у них могут быть различные другие проблемы, которые происходят за пределами пищевода, такие как хрипота, изменения голоса, боль в горле или хронический кашель. У них такое ощущение, как будто в горле комок или волос, и им постоянно приходится очищать горло, покашливая и откашливаясь.
4. Проблемы с дыханием
Если кислота желудка случайно затечет в дыхательное горло после того, как она попадет при гастроэзофагеальной рефлюксной болезни в пищевод, то ГЭРБ может ухудшить течение бронхиальной астмы или пневмонии. Даже без проблем с легкими ГЭРБ может вызывать одышку и затруднение дыхания. А лечение в данной ситуации может быть обоюдоострым мечом. Так как, препараты ГЭРБ, такие как ингибиторы протонной помпы, могут фактически увеличить риск пневмонии. (Они могут способствовать росту бактерий и подавлять кашель, который призван на помощь для очищения легких).
Обращайте внимание Вашего лечащего врача на функцию Ваших легких при лечении рефлюкса.
5. Разрушение зубов
Когда желудочная кислота и пищеварительные соки попадают через пищевод в ротовую полость, это может вызвать кислый вкус и, если это происходит достаточно часто, то разрушается зубная эмаль, что способствуют кариесу.
6. Язвы пищевода
Желудочная кислота может разрушать слизистую пищевода, вызывая раны и язвы. Язвы пищевода отличаются от язв желудка, которые обычно вызваны бактериями. Люди с ранами и язвами могут сплевывать кровью, у них также может быть рвота кровью. Они могут увидеть кровь в своих испражнениях. Кровь может быть красной, вишневой, или как частицы кофе. В стуле обычно кровь из пищевода и желудка при прохождении через тонкий кишечник приобретает черный цвет, цвет и вид нефти — вязкой, скользкой, плохо смываемой.
Обратитесь к врачу немедленно, если у Вас имеются такие симптомы. При эндоскопии можно обнаружить язвы пищевода. Кислотно-блокирующие или кислотно-снижающие лекарства могут привести к их исчезновению.
7. Пищевод Барретта
Если не лечить в течение многих лет, постоянный кислотный рефлюкс могут образоваться изменения в клетках, известное как пищевод Барретта, считающееся предраковым состоянием. Это состояние не вызывает особых симптомов, кроме симптомов рефлюкса. Врач может диагностировать его, выполняя эндоскопию.
Если у вас есть изжога более двух раз в неделю в течение длительного времени, или если у вас есть симптомы гастроэзофагеальной рефлюксной болезни, которые ухудшаются или вы обнаружили новые, которых у вас не было раньше, это все причины, чтобы провериться и пройти эндоскопию.
8. Рак пищевода
В очень серьезных случаях не леченая гастроэзофагеальная рефлюксная болезнь (и последующий пищевод Барретта) может привести к раку пищевода. Основные факторы риска – это употребление алкоголя, курение, плохое питание, а также хронические заболевания пищевода с рефлюксом.
Симптомы включают потерю веса, проблемы с глотанием, или желудочно-кишечные кровотечения. Это то, что происходит в течение десятилетий не леченного рефлюкса (30-40 лет), поэтому у тех, кому 30 лет и в остальном здоровы, нет причин подозревать рак. Но если вам больше 50 лет, и у вас была изжога в течение многих лет, и вы внезапно теряете вес, например, это определенно то, что врач заподозрит в первую очередь.
9. Более низкое качество жизни
В дополнение к рискам для здоровья, симптомы гастроэзофагеальной рефлюксной болезни могут повлиять на здоровье и качество жизни, которые могут быть подорваны из-за проблем с питанием и сном, а также социальных и физических ограничений. У мужчин отчетливо снижалось либидо при длительном рефлюксе.
Особенности течения буллезного пемфигоида у лиц пожилого возраста
Рассмотрены патогенез и клиническая картина буллезного пемфигоида. Отмечено выраженное своеобразие течения этого дерматоза у пожилых пациентов. Приведены подходы к терапии данного заболевания.
Буллезный пемфигоид (БП), или неакантолитическая пузырчатка, парапемфигус, — заболевание, которое ранее описывалось как доброкачественный хронический пемфигус, старческий пемфигус, юношеский пемфигус, старческий герпетиформный дерматит.
БП (собственно неакантолитическая пузырчатка) представляет собой своеобразную форму пузырного заболевания, отличающегося от истинной пузырчатки клиническими, гистологическими и иммунологическими особенностями, но прежде всего отсутствием акантолиза.
Болеют чаще всего лица пожилого возраста (средний возраст составляет 65 ± 5 лет), хотя описаны случаи возникновения заболевания у молодых лиц.
Клиническая картина БП характеризуется появлением на неизмененной коже или эритематозном фоне пузырей с серозным или серозно-геморрагическим содержимым. «Излюбленной» локализацией сыпи являются конечности, туловище, пахово-бедренные складки. Высыпания чаще бывают генерализованными, иногда локализованными.
Термин «буллезный пемфигоид», предложенный W. F. Lever, в настоящее время принят большинством отечественных и зарубежных авторов [1].
Общепризнанной считается ассоциация БП и злокачественных новообразований внутренних органов [2]. Однако многие исследователи [3] не подтвердили закономерности этой связи.
Несомненным представляется аутоиммунный характер заболевания, что подтверждается дефицитом интерлейкина-2 в крови у этих больных, установленным A. A. Razzaque и соавт. в 1984 г., и о чем свидетельствуют течение БП и его клиническая симптоматика.
При аутоиммунных буллезных дерматозах иммунная система вырабатывает аутоантитела к структурным белкам кожи, обеспечивающим межклеточную адгезию кератиноцитов и сцепление эпидермиса с дермой.
Для гистологического подтверждения любого буллезного дерматоза требуется эксцизионная биопсия мелкого пузыря или инцизионная — более крупного. Биоптат должен включать достаточный фрагмент здоровой кожи, чтобы покрышка пузыря осталась целой. Для прямого иммунофлюоресцентного исследования берут биоптат внешне неизмененной кожи у края пузыря или элемента, предшествуюшего образованию пузыря (эритема, волдыря), так как в пузырях иммуноглобулины разрушаются вследствие воспалительного процесса, и иммунофлюоресцентное исследование дает отрицательный результат. Положительный результат прямого иммунофлюоресцентного исследования подтверждает диагноз аутоиммунного буллезного дерматоза даже при нетипичной гистологической картине. Отрицательный результат при характерной гистологической картине требует повторения прямого иммунофлюоресцентного исследования.
БП входит в группу хронических буллезных дерматозов с субэпидермальными пузырями и аутоантителами к структурным белкам гемидесмосом. Впервые аутоантитела к базальной мембране при БП были выделены R. E. Jordon и соавт. в 1967 г.
Связывание провоцирующих аутоантител, активация комплимента и, возможно, выброс интерлейкина-8 кератиноцитами вызывает миграцию лейкоцитов к базальной мембране. Активация лейкоцитов и выброс протеаз приводит к расщеплению светлой пластинки.
Лекарственная терапия как пусковой фактор для БП менее характерна, чем для обыкновенной пузырчатки.
Предполагают провоцирующую роль диуретиков и гипотензивных средств, но их пожилым людям назначают достаточно часто.
Более обоснована провоцирующая роль ультрафиолетового и ионизирующего излучения, а также ПУВА-терапии.
Клиническая картина БП разнообразна и зависит от типа заболевания. Почти всегда наблюдается зуд. В начальной фазе элементы высыпаний представляют собой волдыри, эритематозные папулы и экзематозные очаги. Они остаются такими от нескольких недель до нескольких месяцев, пока в какой-то момент не начинается образование пузырей. «Излюбленная» локализация: шея, подмышечные и паховые области, верхняя часть внутренней поверхности бедер, живот. Большие, напряженные, как правило, неровные пузыри развиваются на месте волдырей или на неизмененной коже. На ранней стадии они напоминают элементы многоформной эритемы. Пузыри достигают нескольких сантиметров в диаметре и имеют причудливую форму. Содержимое их серозное, иногда кровянистое. Покрышки пузырей очень прочные. При их разрыве образуются эрозии, которые покрываются кровянистыми корками. Заживление эрозий начинается с краев. Изредка пузыри локализуются на волосистой части головы. Прямой симптом Никольского отрицательный, непрямой (расширение пузыря при надавливании на него) положительный, но это для БП не специфично.
БП иногда прогрессирует как паранеопластический процесс. Однако БП встречается в основном в пожилом возрасте, когда заболеваемость злокачественными образованиями высока. Описано сочетание БП с другими заболеваниями, но они настолько редки, что обследование для их выявления не оправдано.
Течение БП легче, чем обыкновенной пузырчатки. Системная кортикостероидная терапия требует меньших доз. Общепринятой считается начальная доза преднизолона — 0,5 мг/кг в сутки. В отсутствии свежих высыпаний на протяжении недели и при заживлении 80% прежнюю дозу снижают на 20% каждые 14 дней, пока не появляются свежие высыпания.
Прогноз при БП зависит от состояния здоровья. До введения в практику кортикостероидов спонтанное выздоровление возникало в 30% случаев.
У пожилых больных прогностически неблагоприятны необходимость системной кортикостероидной терапии и гипоальбуминемия.
Диагностика БП основывается на клинических особенностях дерматоза, характеризуется развитием напряженных пузырей с плотной покрышкой (прежде всего у лиц пожилого возраста), быстрой эпителизацией эрозий без тенденции к периферическому росту, отрицательным симптомом Никольского и отсутствием акантолитических клеток в мазках-отпечатках. Диагностическое значение имеют также результаты гистологических исследований, позволяющие обнаружить подэпидермальное расположение пузырей. При биопсии кожи обнаруживают субэпидермальные пузыри, а при прямой реакции иммунофлюоресценции (РИФ) линейные отложения IgG (редко — IgA) и компоненты комплемента С3 в дермоэпидермальном соединении. Пемфигоидный антиген локализуется в пределах гемидесмосом, но нет доказательств, что антитела являются прямопатогенными, они могут играть роль в активации комплемента, что в дальнейшем вызывает местное воспаление [4]. Более чем у 75% пациентов имеются циркулирующие антитела к базальной мембране, но их титр не отражает активность заболевания [4].
Наше наблюдение за больными БП свидетельствует о выраженном своеобразии течения этого дерматоза у пожилых лиц в настоящее время.
Материалы и методы исследования
На протяжении года мы наблюдали 19 больных БП мужчин 64–79 лет. Все больные предъявляли жалобы на выраженный приступообразный зуд. У всех пациентов заболевание возникло недавно, за 2–3 месяца до поступления в стационар. Обращает на себя внимание, что у 15 из 19 больных высыпания «не строго» укладывались в обычную клиническую картину БП. Высыпания были распространенными, многочисленными, располагались повсюду, кроме кожи ладоней и подошв. Превалировали эритематозно-отечные пятнистые розовато-бурые очаги, формирующие причудливые гирляндовидные и дугообразные, кольцевидные фигуры с тенденцией к периферическому росту. У 5 больных на протяжении приблизительно недели иных высыпаний не было, но в последующем стали появляться единичные пузыри или мелкие пузырьки, линейно располагающиеся на отечно-эритематозном фоне. У 10 больных с самого начала постоянно возникали тонкостенные пузыри различной величины от вишни до грецкого ореха, с прозрачным содержимым, быстро вскрывающиеся. У 4 больных отмечалась типичная картина БП с крупными пузырями. Слизистая полости рта была интактна (рис. 1).
При обследовании у 10 из 19 больных (53%) БП в пузырной жидкости превалировали эозинофилы (от 32% до 58%), а у остальных — преобладали нейтрофилы. Одному больному с эритематозно-отечными фигурными образованиями была сделана биопсия с проведением прямой иммунофлюоресцентной реакции и был диагностирован БП (линейное расположение под базальной мембраной IgG с С3-компонентом комплемента).
Результаты и их обсуждение
.jpg)
У 11 наших пациентов (58%) в возрасте 71–79 лет генерализованные высыпания чрезвычайно напоминали буллезную форму многоформной экссудативной эритемы (МЭЭ) (рис. 1). При этом крупные напряженные пузыри одинаково часто формировались как на отечно-эритематозном основании, так и на неизмененной коже, в то время как при классическом БП пузыри чаще возникают на неизмененой коже, а при МЭЭ — на фоне отечной гиперемии.
Обращает на себя внимание разнообразие клинической симптоматики у 7 из 11 вышеописываемых больных БП (наличие волдырей, везикулезных элементов), создающее определенное сходство данного варианта БП с буллезной токсидермией.
.jpg)
У 2 больных БП (возраст 64–75 лет) имеющиеся высыпания были схожи с наблюдающимися при центробежной эритеме Дарье с формированием розово-отечных кольцевидных элементов с приподнимающимся плотноватым окаймлением и регулярным появлением в центре уртикарно-буллезных высыпаний (рис. 3).
У всех больных за время нахождения в стационаре был осуществлен расширенный онкопоиск, и онкопатология не была выявлена ни в одном случае.
Выводы
Таким образом, наши наблюдения свидетельствуют об увеличении числа больных БП, значительном разнообразии клинической симптоматики БП у лиц пожилого возраста, о чаще, чем раньше, встречающемся варианте БП по типу многоформной экссудативной эритемы или центробежной эритемы Дарье.
Наш опыт показывает, что причинные факторы БП у пожилых лиц не обязательно связаны с онкопатологией. Весьма вероятно, что своеобразие клинической картины, описанной выше, может быть связано с какими-либо токсическими факторами, вызванными неблагоприятной экологической обстановкой, употреблением в пищу недоброкачественных продуктов, пищевых добавок, самолечением по поводу различных терапевтических недугов.
Литература
И. Б. Трофимова*, доктор медицинских наук, профессор
М. М. Резникова**
З. А. Фаттяхетдинова**, кандидат медицинских наук
А. Ю. Путинцев**, 1
Е. В. Денисова**
Д. Р. Мильдзихова**
* ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ,
** ГБУЗ ГКБ № 14 им. В. Г. Короленко, Москва



.jpg)