Экстрапростатическая экстензия в перипростатическую клетчатку является более значимым предиктором рецидива рака простаты, чем инвазивный фенотип опухоли
Extraprostatic Extension into Periprostatic Fat is a More Important Determinant of Prostate Cancer Recurrence than an Invasive Phenotype
Jada Kapooremail address, Benjamin Namdarian, John Pedersen, Chris Hovens, Daniel Moon, Justin Peters, Anthony J. Costello, Paul Ruljancich, Niall M. Corcoran
Цель
Несмотря на то, что вероятность микрометастазирования для многих типов опухолей тесно коррелирует с глубиной инвазии, не ясно, является ли инвазия внутрь (но не сквозь простатическую псевдокапсулу) негативным прогностическим фактором, сходным по своему значению с экстрапростатической экстензией опухоли. Мы определили значение инвазии в псевдокапсулу в отношении риска биохимического рецидива опухоли после радикальной простатэктомии.
Материалы и методы
Пациенты с раком предстательной железы в стадии рТ2-3а были включены в проспективно собираемую базу данных. Пациенты со стадией заболевания рТ2 были разделены в соответствии с наличием или отсутствием инвазии в псевдокапсулу. Влияние инвазии в псевдокапсулу на вероятность биохимического рецидива было оценена при помощи одно- и многофакторного регрессионного анализа по Коксу.
Результаты
В когорте из 1338 пациентов мы идентифицировали 595 пациентов с раком предстательной железы, ограниченным органом, но с инвазией в псевдокапсулу. В сравнении с опухолями без признаков инвазии, инвазия в псевдокапсулу была положительным образом ассоциирована с суммой Глисона и объемом опухоли (1,2 против 1,9 мл, р
Рак предстательной железы: проблемы диагностики
 |
Рак предстательной железы (РПЖ) — наиболее частое онкологическое заболевание у мужчин, оно стоит на втором месте по уровню смертности, обусловленной раком. Рак предстательной железы редко встречается в возрасте до 50 лет, но его частота, так же как и смертность от этого заболевания, неуклонно увеличивается с возрастом и достигает максимума на девятом десятке лет жизни. Хотя это в основном болезнь пожилых людей, укорочение жизни от рака простаты составляет, по существующим оценкам, девять лет.
Внедрение в клиническую практику современных методов диагностики рака предстательной железы увеличивает вероятность выявления заболевания на ранних стадиях, когда еще возможно применение радикальных методов лечения.
Диагностика этого заболевания ставит две основные задачи: выявление заболевания и определение стадии и степени распространенности процесса, что имеет решающее значение для выбора лечебной тактики.
Рак предстательной железы выявляется в 4-7% случаев у мужчин в возрасте 50 лет и старше, не имеющих урологической симптоматики и заболеваний мочеполовой системы в анамнезе. Более того, РПЖ 1-2-й стадии, как правило, клинически ничем себя не проявляет, поэтому сбор анамнеза и выявление симптоматики не являются клинически значимыми факторами в диагностике ранних стадий. На более поздних стадиях заболевания больные предъявляют жалобы на затрудненное учащенное мочеиспускание “вялой” струей, ночную поллакиурию. При наличии таких жалоб обязательно более подробное обследование для исключения онкологического заболевания предстательной железы.
| Пальцевое ректальное исследование пока является стандартом для скрининговой диагностики первичной опухоли рака предстательной железы, хотя этот метод считается недостаточно чувствительным для диагностики опухолей, не выходящих за пределы простаты. Опухоль размером 1–1,2 см, как правило, остается незамеченной. Тем не менее пальцевое ректальное исследование можно считать базовым диагностическим методом, обязательным при первичном осмотре |
Пальцевое ректальное исследование (ПРИ) позволяет определить примерные размеры предстательной железы, ее конфигурацию и консистенцию. Его проводят также с целью выявления доброкачественной гиперплазии простаты, опухолей прямой кишки, хронического простатита, а также для оценки тонуса анального сфинктера. На характер тактильных ощущений может повлиять различное положение больного (на боку, коленно-локтевое и т. д.), а также степень наполненности мочевого пузыря. Специфичность пальцевого ректального исследования в отношении выявления рака простаты невелика: только у 26-34% мужчин с подозрительными результатами обнаруживается рак предстательной железы. Как правило, подозрение на рак простаты при ПРИ возникает лишь на поздних стадиях процесса. Доля ложно-отрицательных диагнозов при этом исследовании достигает 40-60%.
Диагностическими признаками РПЖ при проведении ПРИ являются увеличенный объем и асимметрия простаты, наличие затвердеваний.
Трансректальное ультразвуковое сканирование (ТРУЗ) является основным методом инструментального исследования простаты. Наиболее информативные для выявления первичной опухоли результаты удается получить при продольном трансректальном сканировании. Основной закономерностью является снижение эхогенности в пораженных опухолью участках, хотя патогномоничных ультразвуковых признаков аденокарциномы, по-видимому, не существует, а у 15-20% пациентов, у которых клиническая стадия аденокарциномы предстательной железы установлена другими методами, эхографические изменения отсутствуют. Эхографическими симптомами аденокарциномы простаты являются единичные, четко очерченные фокусы сниженной эхогенности, множественные гипоэхогенные участки с расплывчатыми границами, изо- и гиперэхогенные фокусы. При прорастании опухоли за пределы капсулы предстательной железы на эхограммах наблюдается прорыв капсулы и гиперэхогенной жировой полоски, окружающей ПЖ.
Менее эффективно сканирование в поперечной плоскости, позволяющее лишь изучить симметричность предстательной железы и семенных пузырьков. Возможности трансабдоминального сканирования ограничены из-за низкого разрешения; при этом определяются общие размеры предстательной железы, но дифференцировать ее внутренние структуры не удается.
В целом прогностичность положительного результата при использовании только ТРУЗ не превышает 40-43%, поэтому обязательным является сочетание его с другими методами.
Существует ТРУЗ с использованием цветового допплеровского картирования, позволяющего изучать сосудистую архитектонику простаты. В этом случае наиболее информативным является продольное ультразвуковое сканирование, а для изучения спектральных характеристик кровотока — поперечное сканирование. В участках злокачественного поражения наблюдается снижение индекса резистентности на 12-15% по сравнению с кровотоком неизмененной предстательной железы. Для диагностики и дифференциальной диагностики цветовое допплеровское картирование имеет вспомогательное значение.
| Почти все раковые опухоли, зарождающиеся в простате, являются аденокарциномами. Во многих западноевропейских странах и Америке аденокарцинома простаты — наиболее распространенный вид рака внутренних органов у мужчин; в США в 1991 году было зарегистрировано 122 тыс. заболевших, притом что раком легких в том же году заболели 101 тыс. мужчин. Ежегодная смертность от аденокарциномы простаты составляла в 1983 и 1984 годах 22,7 случая на 100 тыс. населения при заболеваемости 75,3 случаев на 100 тыс. населения. Заболеваемость и смертность от рака простаты имеют тенденцию к увеличению во всех странах. В России с 1985 по 1995 год заболеваемость РПЖ возросла с 6 до 12 случаев на 100 тыс. мужчин |
Важная цель исследований рака каждого органа — найти сывороточные маркеры, которые могут определять присутствие и степень злокачественности заболевания, обеспечивать контроль его развития во времени и подтверждать успех или неудачу лечения. Рак простаты — первое злокачественное заболевание, для которого такая биохимическая оценка стала возможной по уровню простат-специфического антигена (ПСА). При наличии рака предстательной железы в клетках опухоли не только повышается продукция ПСА, но и значительно возрастает синтез антихимотрипсина. В результате увеличивается количество связанной и снижается содержание свободной фракции ПСА при увеличении общей концентрации этого антигена.
Нормальным считается содержание общего ПСА менее 4 нг/л, повышение уровня ПСА более 10 нг/л уже является показанием для проведения детального обследования для исключения рака простаты даже при нормальных данных ПРИ. При высоких цифрах общего ПСА биопсию предстательной железы проводят в обязательном порядке. С целью более точной интерпретации повышенных значений общего ПСА необходимо исследование концентрации свободного ПСА и расчет соотношения свободного и общего ПСА. При значении этого показателя ниже 15% требуется биопсия предстательной железы. При значении более 15% необходимы наблюдение и повторное обследование больного через шесть месяцев. Показатель 15% является границей для дифференциальной диагностики рака предстательной железы и доброкачественной гиперплазии простаты.
В определенных случаях изолированный показатель общего ПСА может соответствовать различным размерам опухоли. Его значимость теряется при наличии низкодифференцированного рака простаты.
Уровень ПСА является наиболее точным маркером для скрининговой диагностики рака предстательной железы, однако его возможности ограничены при определении стадии процесса, так как уровень ПСА не зависит от объема опухоли.
При обнаружении в биоптате картины рака предстательной железы необходимо определение степени дифференцировки опухоли, от которой во многом зависит ее биологическое поведение и, следовательно, дальнейшая лечебная тактика. Общепринятая в России в настоящее время “Гистологическая классификация ВОЗ опухолей предстательной железы” (1980, № 22) основное внимание уделяет формально-гистологическому типу опухоли, который не является определяющим в плане установления ее биологического поведения и выбора наиболее эффективных методов лечения. В этом отношении более продуктивна система степеней гистологической дифференцировки рака предстательной железы по Глиссону (1977), используемая в национальной программе США по борьбе с раком.
Система Глиссона основана преимущественно на гистоархитектурных критериях. Процесс дедифференцировки определяется как потеря способности вновь образующихся опухолевых клеток формировать железы.
Согласно этой системе различают пять степеней дифференцировки опухоли. При изучении препаратов с наличием рака предстательной железы патолог должен выделить две основные картины: “первичную”, или преобладающую, занимающую наибольшую площадь образца, и “вторичную”, т. е. вторую по величине, а затем определить степень дифференцировки по Глиссону каждой из них. Дополнительные участки строения меньших площадей и участки, занимающие меньше 5% общей площади рака, игнорируются. Сумма степеней и определяет индекс Глиссона. В случае практически полной однородности структуры для получения индекса определяемая степень Глиссона удваивается. Чем ниже индекс Глиссона, тем эффективнее лечение и лучше прогноз для больного.
Первые три степени (степени 1, 2, 3), расцениваемые как наиболее хорошо дифференцированные, сходны по структуре с нормальной предстательной железой. Эпителиальные ткани хорошо отграничены от окружающей стромы, железы образованы одним слоем эпителиальных клеток, окружающих железистые просветы. Тем не менее выявляется менее упорядоченное ветвление желез по сравнению с доброкачественными простатическими протоками и ацинусами. Злокачественные железистые структуры имеют тенденцию к разнообразию размеров и формы желез, величины просветов.
Различия первых трех степеней незначительны. Если железы однородны, а признаки инвазии отсутствуют или выражены слабо, опухоль может быть отнесена к 1-й или 2-й степени дифференцировки. Эти степени могут быть также установлены, если клетки имеют светлую цитоплазму, которая более, чем темная, увеличивает сходство с нормальной тканью. В очень маленьких образцах отличие от нормальной ткани должно основываться не только на архитектонике, оно также должно быть подтверждено цитологическими критериями, например очень крупными ядрышками.
Важным исключением из этих правил определения хорошо дифференцированных опухолей является криброзный вариант, который также относится к 3-й степени дифференцировки по Глиссону. Отличие криброзного варианта от рака 4-й степени дифференцировки — небольшие размеры опухолевых комплексов, сопоставимые с размерами крупных протоков, округлая форма, четкие границы, хорошо выраженный стромальный компонент.
Опухоли 4-й степени дифференцировки по Глиссону характеризуются большим разнообразием гистологических проявлений и отсутствием сформированных желез, свойственных первым трем степеням.
Опухоли 5-й степени дифференцировки являются наиболее слабо дифференцированными, с едва различимыми или практически отсутствующими железистыми структурами, с крупными полями опухолевых клеток практически без каких-либо просветов. Опухолевые клетки обычно имеют скудную цитоплазму.
К 5-й степени дифференцировки обычно относят рак типа камедокарциномы. Под этим вариантом описывается интрадуктальный рак с наличием небольших криброзных участков по периферии и с тотальным некрозом клеток в центре опухолевых комплексов. Это единственный вариант рака предстательной железы, в котором отмечается некроз опухолевых клеток. Статистически доказано, что наличие подобных неинвазивных участков связано с крайне плохим прогнозом, сопоставимым с прогнозом при инвазивном раке 5-й степени дифференцировки.
Определение индекса Глиссона при обнаружении рака в биоптате предстательной железы совершенно необходимо. Однако и система Глиссона не лишена недостатков. Во-первых, по биоптату не всегда удается определить биологическое поведение опухоли для индивидуального больного: рак предстательной железы характеризуется большим разнообразием гистологических структур даже в пределах одной опухоли, а биопсийный образец имеет весьма небольшие размеры. Во-вторых, биологическое поведение опухоли может быть обусловлено потерей дифференцировки на небольших участках и не связано с доминирующими структурами.
Более точное предсказание о поведении опухоли можно сделать на основании ее объема, определяемого при радикальной простатэктомии. Объем опухоли, как правило, коррелирует со степенью ее дифференцировки и в равной степени с наличием метастазов в лимфатические узлы и отдаленных метастазов. Поэтому он является важным фактором в определении клинической стадии заболевания и в сочетании со степенью дифференцировки наиболее точно отражает биологическое поведение опухоли.
Компьютерная томография не является эффективным методом, она непригодна для дифференцирования рака предстательной железы и доброкачественной гиперплазии. Главная задача КТ состоит в оценке состояния тазовых и абдоминальных лимфатических узлов. В диагностике поражения лимфатических узлов решающее значение имеет изменение их формы и увеличение размеров более чем на 1–1,5 см.
Магниторезонансная томография (МРТ) позволяет оценить вовлечение в процесс уретры, различных отделов простаты, мочевого пузыря, клетчатки, мышцы, поднимающей наружный сфинктер прямой кишки, семенных пузырьков и лимфатических узлов. Преимущество МРТ по сравнению с КТ состоит в возможности выбора проекции: аксиальной, саггитальной и коронарной. Возможно получение объемного изображения, создаваемого посредством комбинирования коронарной и сагиттальной проекций. МРТ лучше отражает внутрипростатические изменения, чем КТ. Тем не менее распознавание ткани, пораженной доброкачественной или злокачественной опухолью, производится недостаточно надежно.
Скрининг рака простаты должен проводиться начиная с поликлинического отделения. Всем мужчинам старше 50 лет вне зависимости от наличия жалоб один раз в год необходимо выполнение пальцевого ректального исследования и определение уровня ПСА. При повышении ПСА выше 4 нг/мл показано определение соотношения свободного и общего ПСА и выполнение трансректального ультразвукового исследования.
Дальнейшее обследование пациентов предпочтительнее проводить в специализированных стационарах — урологических либо онкологических отделениях. Выполнение трансректальной мультифокальной биопсии простаты показано при повышении ПСА выше 10 нг/мл, в случае, когда соотношение свободного и общего ПСА больше 15%, при выявлении гипоэхогенных зон на трансректальном ульразвуковом сканировании и при наличии пальпируемого твердого образования в предстательной железе.
Всем больным с верифицированным диагнозом необходимо выполнение остеосцинтиграфии для выявления костных метастазов. Применение компьютерной или магниторезонансной томографии показано больным, в отношении которых планируется радикальное хирургическое или лучевое лечение для выяснения состояния тазовых лимфатических узлов.
В диагностике рака предстательной железы только один метод — биопсия — является инвазивным. При выполнении трансректальной биопсии возможно несколько осложнений: инфицирование простаты с последующим развитием острого простатита и уретроррагии. Всем больным, перенесшим биопсию простаты, необходимо назначение пероральных антибиотиков, предпочтительно группы цефалоспоринов, для профилактики воспалительных осложнений. Уретроррагия не бывает обильной и в большинстве случаев прекращается самостоятельно в течение первых суток после биопсии. Абсолютных противопоказаний к проведению диагностического поиска для выявления рака предстательной железы не существует, препятствием может служить только крайне тяжелое состояние больного.
Доброкачественная гиперплазия предстательной железы (ДГПЖ)
Что такое доброкачественная гиперплазия предстательной железы (ДГПЖ)?
Патогенез (особенности развития) ДГПЖ
В основе развития заболевания лежит высокая чувствительность специфических рецепторов клеток предстательной железы к дегидротестостерону. Концентрация тестостерона в крови с возрастом снижается, однако уровни одного из его изомеров остается прежней. Клетки простаты реагируют на активную форму тестостерона, синтезируя факторы роста. Это затормаживает процесс апоптоза (запрограммированной гибели старых клеток). В итоге изношенные клетки железы живут дольше, а новые быстро делятся.
Сначала в простате формируется один или несколько узелков, которые постепенно разрастаются. Железа увеличивается в объеме, меняет свою структуру, нарушается ее секреторная функция. Предстательная железа расположена в области верхнего отдела уретры, в близком контакте с пузырной шейкой. Ее увеличение провоцирует стеноз уретры и нарушения пассажа мочи.
На первых порах состояние компенсируется активной работой детрузора (мышечного слоя пузыря), который выталкивает урину за счет сильных сокращений. По мере прогрессирования заболевания мускулатура ослабевает, в стенках формируются фиброзные волокна. Оболочки пузыря постепенно растягиваются, затем теряют эластичность. Возможно формирование дивертикулов пузыря.
Хронический застой мочи является благоприятным условием для присоединения инфекции и развития цистита. Постоянное повышение внутрипузырного давления ведет к расширению мочеточников, рефлюксу урины и развитию пиелонефрита, гидронефроза, хронической почечной недостаточности.
Классификация: стадии ДГПЖ
Согласно классификации Гюйона, аденома простаты развивается в 3 стадии:
Объем предстательной железы в норме равен 2,5-3 см³. Аденому классифицируют, исходя из размеров патологически измененной простаты:
Симптомы доброкачественной гиперплазии предстательной железы (ДГПЖ)
Признаки доброкачественной гиперплазии предстательной железы (ДГПЖ) зависят от степени увеличения органа, потому что от этого зависит величина просвета мочеиспускательного канала. На ранних этапах симптомы выражены слабо. Мужчина замечает, что при утреннем мочеиспускании ему приходится напрягать пресс, струя мочи становится слабой. Происходит учащение позывов в туалет днем, больной встает по нужде 1–2 раза ночью.
Прогрессирование заболевания ведет к неполноценному опорожнению пузыря. Позывы становятся еще более частыми, принимают императивный (повелительный) характер. Возможно выделение мочи небольшими порциями сразу после позыва. Нарушается ночной сон. У пациента возникает ощущение неполного опорожнения пузыря. На протяжении всей микции (процесса мочеиспускания) ему приходится напрягать пресс. Моча выделяется прерывисто, струя становится вертикальной. При присоединении инфекции появляются симптомы уретрита и цистита (болезненные позывы, рези во время мочеиспускания).
На поздних стадиях развития заболевания возникает «парадоксальная задержка мочи», когда пациент не может самостоятельно опорожнить пузырь, несмотря на сильнейшие позывы. При этом урина выделяется по каплям самопроизвольно. Из-за расширения мочеточников и повышения пузырного давления, происходит ретроградный заброс мочи, развивается почечная недостаточность.
Осложнения ДГПЖ
В основе развития большинства осложнений ДГПЖ лежит нарушение оттока мочи. При отсутствии лечения мужчина может столкнуться со следующими проблемами:
Реже заболевание провоцирует развитие недержания мочи, склероза шейки мочевого пузыря и других проблем. Не исключен риск перерождения доброкачественной гиперплазии в рак.
Причины ДГПЖ
Основным провоцирующим фактором развития аденомы простаты признано влияние гормонов на стареющий организм мужчины. Риск повышается, если у мужчины имеются проблемы с обменом веществ:
Важную роль играет генетическая предрасположенность. Доказано, что склонность к аденоме может передаваться из поколения в поколение.
Рак предстательной железы
Вам поставили диагноз: рак предстательной железы?
Данная брошюра содержит информацию о диагностике и лечении рака предстательной железы. Здесь собраны основные методики лечения данного заболевания, в том числе, последние разработки отечественных и зарубежных ученых-онкологов.
Ежегодно в России выявляется более 38 тысяч новых случаев заболеваний рака предстательной железы, что особенно настораживает, болезнь всё чаще проявляется у молодых мужчин.
Мы хотим Вам помочь победить рак!
Филиалы и отделения, где лечат рак предстательной железы
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Урологическое отделение
Заведующий – к.м.н, ВОРОБЬЁВ Николай Владимирович
тел.: +7(495) 150-11-22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
Онкологическое-урологическое отделение
Заведующий отделением – к.м.н. КАЧМАЗОВ Александр Александрович
тел.: +7(499) 110 40 67
Введение. Анатомия органа
Предстательная железа (синоним: простата) — железа наружной секреции, есть только у мужчин. Предстательная железа расположена ниже мочевого пузыря, спереди от прямой кишки. Через неё проходит начальная часть мочеиспускательного канала. Выводные протоки предстательной железы открываются в мочеиспускательный канал (рис.1). Функции простаты контролируют гормоны, наибольшее влияние на рост клеток предстательной железы оказывает мужской половой гормон – тестостерон. Андрогены – общее названия для всех мужских половых гормонов. Жидкость, вырабатываемая предстательной железой является основной составляющей семенной жидкости. Эта жидкость является питательной средой для сперматозоидов. Также простата выполняет роль клапана — закрывает выход из мочевого пузыря во время эрекции.
Рис.1 Анатомия предстательной железы
Что представляет собой злокачественная опухоль предстательной железы?
Рак простаты – это злокачественная опухоль, развивающаяся из эпителиальных клеток желез простаты.
Опухоль может располагаться в одной или обеих долях железы, приобретать тотальное распространение с инвазией за пределы капсулы железы, вовлечением семенных пузырьков.
Рак простаты – сравнительно медленно прогрессирующее заболевание. Но при длительном существовании и отсутствии лечения, как и другие злокачественные опухоли, имеет способность прогрессивно увеличиваться и врастать в прилежащие органы и структуры, а также давать отсевы в ближайшие к органу лимфатические узлы (регионарные метастазы). Опухоль предстательной железы на поздних стадиях может врастать в шейку мочевого пузыря, прямую кишку или стенку таза. Опухолевые клетки могут переноситься с током крови в другие органы (кости, легкие, печень, и др) и давать рост новых очагов (отдаленные метастазы).
Статистика рака предстательной железы (эпидемиология)
На протяжении последнего десятилетия в структуре заболеваемости злокачественными новообразованиями мужского населения России рак предстательной железы занимает второе место после рака легких.
Показатель заболеваемости раком предстательной железы в России за последние 15 лет с 2001 по 2015 годы увеличился 3,0 раза с 19,01 до 57,22 случаев на 100 тысяч населения.
В России в 2016 г. отмечен 38371 новый случай данной патологии, а среднегодовой темп прироста заболеваемости составил 7,12 %
Морфологическая классификация рака предстательной железы
Наиболее часто встречающимся морфологическим вариантом злокачественной опухоли простаты является ацинарная аденокарцинома до 85-90% случаев. Степень дифференцировки и агрессивности опухоли простаты выражается в морфологических характеристиках, которые оцениваются по шкале Глисона.
Шкала / сумма баллов Глисона (Gleason score)
Шкала / сумма Глисона используется для описания злокачественности опухоли, обнаруженной при биопсии простаты. Чем выше сумма по шкале Глисона, тем более агрессивна / злокачественна опухолевая ткань. Сумму баллов по Глисону можно определить только при исследовании морфологического материала – материала толстоигольной биопсии или послеоперационного материала.
Шкала Глисона основана на степени отличия раковых клеток, найденных в ткани простаты, от нормальных клеток простаты. Если раковые клетки выглядят как обычные клетки простаты, то опухоль получает 1 балл. Если раковые клетки максимально отличаются от нормальных, то опухоль получает максимальное количество баллов — 5. Чаще всего в диагнозах встречаются оценки в 3 балла и выше.
Сумма Глисона включает оценки (баллы), данные по шкале Глисона (от 1 до 5 баллов) двум самым большим или злокачественным опухолям, найденным в тканях простаты (обычно рак простаты поражает несколько областей простаты). Например, сумма Глисона, равная 7 баллам, обозначает, что две самые большие или злокачественные опухоли получили 3 и 4 балла соответственно (3+4=7). Различают три вида злокачественности рака предстательной железы:
Стадии и симптоматика рака предстательной железы
Как все злокачественные новообразования, в развитии рака простаты выделяют 4 стадии:
Классификация рака предстательной железы
TNM-классификация (Tumour, Node, Metastasis – Опухоль, Лимфатический узел, Метастазы) – это международная классификация стадий развития злокачественных опухолей.
Т – первичная опухоль:
Т1-2 – опухоль не выходит за пределы капсулы предстательной железы
Т3-4 – опухоль прорастает за пределы капсулы предстательной железы, может врастать в соседние органы (мочевой пузырь, прямая кишка)
N – лимфатические узлы:
N0 – нет метастазов в лимфоузлах, N1 – наличие метастазов в одном или нескольких лимфоузлах
Клинические проявления рака предстательной железы
На начальных стадиях заболевания рак предстательной железы (РПЖ) не имеет самостоятельных клинических проявлений. Клиническая симптоматика при локализованном РПЖ чаще всего связана с сопутствующей доброкачественной гиперплазией ткани предстательной железы. Наиболее часто больные с локализованным РПЖ имеют симптомы инфравезикальной обструкции, связанной с доброкачественной гиперплазией предстательной железы такие как: учащенное, затрудненное мочеиспускание, вялая струя, императивные позывы на мочеиспускание, никтурия.
Для местно-распространенного рака предстательной железы характерно наличие симптомов обструкции мочевых путей, что обусловлено как сопутствующей доброкачественной гиперплазией предстательной железы, так и большим объемом опухоли. При прорастании опухоли в шейку мочевого пузыря, уретру возможно появление примеси крови в моче, недержание мочи.
Обширное опухолевое поражение шейки мочевого пузыря может привести к блоку устьев мочеточников, развитию почечной недостаточности. Распространение опухолевого процесса на сосудисто-нервные пучки приводит к развитию эректильной дисфункции. Симптомами опухолевого прорастания или сдавления стенки прямой кишки являются нарушение акта дефекации, примесь крови в моче. Распространение опухоли на мышцы тазового дна может вызывать чувство дискомфорта при сидении, боли в промежности. Массивное опухолевое поражение тазовых лимфатических узлов приводит к лимфостазу, отеку наружных половых органов, нижних конечностей.
Причины возникновения рака предстательной железы и факторы риска
Рак предстательной железы (РПЖ) является одним из наиболее распространенных онкологических заболеваний у мужчин. Во всем мире заболеваемость и смертность от данной патологии неуклонно возрастают. Вопрос о причине развития данной патологии остается открытым, поскольку причины возникновения РПЖ до конца не изучены. Тем не менее, сейчас уже выделены некоторые факторы риска развития данного заболевания. Основными, наиболее изученными факторами риска развития рака предстательной железы являются возраст, расовая принадлежность, а также наличие так называемого семейного рака предстательной железы. Кроме того ряд исследований показывает влияние на частоту возникновения рака предстательной железы и других факторов, таких как гормональный статус организма, диета, половое поведение, факторы внешней среды и генетические особенности. В настоящее время установлено огромное количество факторов, которые непосредственно или опосредовано могут способствовать возникновению рака предстательной железы. Тем не менее, воздействие многих из данных факторов не является стойким и постоянным, в то время как влияние других факторов не является достоверно доказанным для того, чтобы делать какие-нибудь четкие утверждения об их влиянии на заболеваемость данной патологией. Многие исследования фокусировались на изучении роли диеты, продуктов питания, гормональных воздействиях, а также инфекции в возникновении рака предстательной железы.
Диагностика рака предстательной железы
Пальцевое ректальное исследование
Пальцевое ректальное исследование является рутинным методом обследования больных с подозрением на рак предстательной железы, один из основных методов обследования на ряду с измерением уровня ПСА в сыворотке крови. Преимуществами пальцевого ректального исследования является доступность, безопасность и не требует экономических затрат. Данные метод позволяет выявить опухоли предстательной железы, локализующиеся в периферических отделах, если их объём превышает 0,2 мл.
Простат-специфический антиген (ПСА)
Впервые простат-специфический антиген был выделен из семенной жидкости в 1979 г. Тогда же установили его наличие в ткани предстательной железы. В 1980 году произведен серологический тест для определения ПСА в крови. Начиная с 1987 года ПСА широко используют в диагностике рака предстательной железы, установлении стадии процесса, оценке эффективности лечения. Широкое применение в клинической практике определения уровня ПСА кардинально изменило структуру заболеваемости рака предстательной железы во всем мире. В настоящее время измерение уровня ПСА является скрининговым методом выявления рака предстательной железы.
Механическое воздействие на паренхиму предстательной железы также приводит к повышению уровня ПСА в сыворотке крови. Такие вмешательства как, биопсия предстательной железы, трансуретральная резекция или наличие воспалительного процесса могут являться причиной значительного повышения уровня ПСА и требуют, как минимум, 4-6 недель для возврата ПСА к исходному уровню.
Таким образом, обладая органо-специфичностью, ПСА не является опухолево-специфическим маркером, а потому интерпретация данных по содержанию общего ПСА в сыворотке крови пациентов должна проводиться врачом с учетом вышеуказанных факторов. В течение длительного времени верхней границей нормы считали уровень ПСА = 4,0 нг/мл. Учитывая актуальность проблемы выявления РПЖ на ранних стадиях на основе оценки уровня ПСА, было проведено несколько крупных исследований, подтвердивших остающуюся значимость ПСА-диагностики в скрининге рака предстательной железы и определивших новые подходы к пороговым значениям ПСА.
| Возраст (годы) | Среднее значение (нг/мл) | Средний предел (нг/мл) | Рекомендуемый предел (нг/мл) |
|---|---|---|---|
| 40-49 | 0,7 | 0,5-1,1 | 0-2,5 |
| 50-59 | 1,0 | 0,6-1,4 | 0-3,0 |
| 60-69 | 1,4 | 0,9-3,0 | 0-4,0 |
| 70-79 | 2,0 | 0,9-3,2 | 0-5,5 |
Таблица1. Значение условной нормы общего ПСА с учетом возраста
Ультразвуковое исследование рака предстательной железы
В случае выявления повышенного уровня ПСА и нализия подозрения на наличие РПЖ при пальцевом ректальном исследовании выполняется ультразвуковое исследование (УЗИ) малого таза, а также трансрекатальное УЗИ (ТРУЗИ). ТРУЗИ представляет собой ультразвуковое исследование простаты, выполняемое с помощью специального высокочастотного ультразвукового датчика особой конструкции через прямую кишку пациента. При этом ультразвуковой датчик находится в непосредственной близости от простаты и отделен от нее лишь стенкой прямой кишки. Главным преимуществом ТРУЗИ является возможность получения полноценного и очень точного изображения простаты, различных ее отделов (зон), а, следовательно, и патологических процессов этого органа. ТРУЗИ позволяет также детально рассмотреть семенные пузырьки. ТРУЗИ является наиболее точным при определении объема простаты и при наличии соответствующего оборудования обладает высокой разрешающей способностью.
Биопсия простаты
Биопсия простаты выполняется с целью гистологической диагностики рака и постановки окончательного диагноза. Она также позволяет установить степень агрессивности опухоли и стадию заболевания (его распространенность). Результаты биопсии простаты являются важнейшим фактором, определяющим тактику лечения пациента, а также прогноз заболевания.
Биопсия предстательной железы и гистологическое исследование (исследование ткани простаты) – единственный способ постановки диагноза «рак предстательной железы».
Магнитно-резонансная томография рака предстательной железы
Магнитно-резонансная томография (МРТ) — метод исследования внутренних органов и тканей с использованием электромагнитных волн в постоянном магнитном поле высокой напряжённости. МРТ является уточняющим методом обследования. МРТ позволяет лучше выявлять распространение опухоли за капсулу предстательной железы и на соседние органы, увеличение лимфатических узлов (что может свидетельствовать о наличии метастазов, либо о наличии воспалительного процесса).
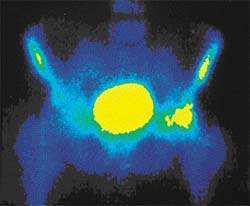
Радионуклидное исследование скелета
Лечение рака предстательной железы
Лечение больных раком предстательной железы во многом зависит от стадии и распространенности опухолевого процесса на момент постановки диагноза. Основными вариантами лечения локализованных форм опухоли без отдаленных метастазов являются хирургическое лечение и лучевая терапия в сочетании с гормональной терапии. В случае наличия отдаленных метастазов проводится лекарственная системная терапия. Ниже мы представляем информацию о различных видах лечения рака предстательной железы.
Хирургическим лечением является радикальная простатэктомия, которая заключается в удалении предстательной железы с семенными пузырьками и окружающей простату клетчаткой, чтобы гарантировать полное удаление опухоли. Часто эта операция сопровождается удалением тазовых лимфоузлов, так как лимфатические узлы являются первым барьером на пути распространения опухолевых клеток. Данная операция направлена на устранение злокачественного процесса с сохранением функции удержания мочи и по возможности потенции.
Радикальная простатэктомия выполнятся в классическом варианте открытым способом и малоинвазивными лапароскопическими методами. В настоящее время применяются также методы роботассистированного (роботизированного) хирургического лечения на роботе «да Винчи».
Лучевая терапия – это методы лечения с использованием ионизирующей радиацией. Лучевую терапию при лечении раке предстательной железы подразделяют на дистанционную и внутритканевую (брахитерапия).
Дистанционная лучевая терапия (ДЛТ) – источник излучения находится на некотором удалении от пациента, при дистанционном воздействии между очагом воздействия и источником излучения могут лежать здоровые ткани. Чем их больше, тем сложнее доставить необходимую дозу излучения к очагу, и тем больше побочных эффектов терапии. Внутритканевая лучевая терапия (брахиерапия) – источники излучения, так называемые «зерна» при помощи специальных инструментов внедряются непосредственно в ткань предстательной железы.
В некоторых случаях применяется комбинация брахитерапии с ДЛТ для улучшения эффективности противоопухолевого лечения. При раке предстательной железы лучевая терапия обеспечивает такую же продолжительность жизни, как и хирургическая операция. Качество жизни после лучевой терапии по меньшей мере не хуже, чем после хирургического метода лечения. В нашем Центре выбор тактики лечения принимается на консилиуме с участием хирурга-онколога и радиотерапевта и химиотерапевта. Обязательным условием является согласие пациента, основанное на полном информировании о диагнозе, методах лечения и возможных осложнениях.
Методы фокальной терапии
В настоящее время в качестве альтернативных экспериментальных методов лечения локализованного рака предстательной железы применяется криохирургическая деструкция предстательной железы, использование высокоинтенсивного сфокусированного ультразвука и фотодинамическая терапия (ФДТ). Необходимо помнить, что вышеуказанные методы применяются только в случае выявления рака на ранней стадии.
Гормональная терапия при раке предстательной железы
Что такое орхитэктомия?
Орхидэктомия (или хирургическая кастрация) представляет собой удаление яичек путём операции, целью которой является снижение уровня тестостерона в организме для устранения его воздействия на опухоль предстательной железы. Операция обычно выполняется под местной или внутривенной анестезией. При этом яички удаляются через один разрез длиной 3–4 см в области корня мошонки, или через два аналогичных разреза, расположенных по бокам мошонки. При визуальном осмотре мошонки через месяц после операции определить, что яички удалены, практически невозможно.
К преимуществам этого вида гормональной терапии относят достаточно быстрое и необратимое снижение уровня тестостерона, а недостатками являются возможные осложнения операции – гематома (кровоизлияние) мошонки и раневая инфекция. Кроме того, многие мужчины отказываются от удаления яичек по эмоциональным причинам.
Что такое гормональная терапия путем инъекций?
При проведении гормонотерапии путём инъекций (уколов) пациентам вводят препараты, называемые аналогами ЛГРГ (аналогами гормонов гипофиза – эндокринной железы, расположенной в головном мозге). Через 3–4 недели после введения препаратов этой группы содержание тестостерона в крови снижается до минимального уровня, аналогичного таковому после орхидэктомии, т.е. происходит так называемая «медикаментозная кастрация». В этом случае нет необходимости удалять яички, и операция остаётся резервным методом лечения, который может быть использован в будущем при появлении побочных эффектов гормонального лечения или отказе пациента от его продолжения. В России наиболее известными препаратами этой группы являются «Диферелин», «Люкрин», «Декапептил», «Супрефакт», «Простап», а также «Золадекс», который выпускается в готовом к применению шприце, и вводится под кожу живота ежемесячно или один раз в 3 месяца – в зависимости от дозы (3,6 мг или 10,8 мг).
Что такое максимальная андрогенная блокада?
Небольшое количество (около 5%) мужских половых гормонов (андрогенов) вырабатывается в надпочечниках – эндокринных железах, находящихся в области верхних полюсов обеих почек. Считается, что при проведении гормонотерапии помимо инъекций аналогов ЛГРГ (например, Золадекса) или удаления яичек, необходимо также принимать препараты – антиандрогены.
Антиандрогены блокируют способность опухолевых клеток взаимодействовать с половыми гормонами, вызывая совместно с инъекционными препаратами эффект, называемый максимальной андрогенной блокадой. По данным большого количества исследований эффективность максимальной андрогенной блокады выше, чем орхидэктомии или изолированной терапии путём инъекций.
Среди антиандрогенных препаратов в России наиболее часто используются «Флуцином», «Анандрон», «Андрокур» и «Касодекс» (бикалутамид), выпускаемый в виде таблеток по 50 мг для приёма один раз в сутки, что достаточно удобно для пациентов.
Каковы возможные побочные эффекты гормонального лечения?
К нежелательным эффектам гормонотерапии относят ощущения «приливов», снижение либидо и потенции, набухание и болезненность молочных желёз, диарею, изменения функции печени и др. Необходимо подчеркнуть, что большинство указанных побочных действий гормональных препаратов встречается сравнительно нечасто и редко требует отмены лечения.
Что такое монотерапия антиандрогенами?
Монотерапия антиандрогенами показана пациентам с местно-распространённым неметастатическим раком предстательной железы, как альтернатива медикаментозной или хирургической кастрации. Для этого вида лечения применяется Касодекс по 150 мг в день. Использование Касодекса в такой дозировке обеспечивает пациентам лучшее качество жизни по сравнению с орхидэктомией. У многих мужчин сохраняется половое влечение и способность к возникновению эрекции. Нежелательным эффектом данной терапии является увеличение в размерах (гинекомастия) и болезненность грудных желёз.
Что такое интермиттирующая гормональная терапия?
Под термином «интермиттирующая (прерывистая) терапия» понимают прекращение гормонального лечения, когда уровень ПСА снижается до минимального значения. Лечение возобновляют, когда отмечается рост уровня ПСА. Подобная схема лечения позволяет уменьшить его стоимость и минимизировать возможные побочные эффекты. Следует отметить, что в настоящее время нет достаточного количества сведений о том, насколько интермиттирующая терапия эффективна и, главное, безопасна с точки зрения прогрессирования рака предстательной железы. Именно поэтому данная методика считается пока экспериментальной.
Для чего назначается гормональное лечение перед операцией или лучевой терапией?
Приём гормональных препаратов в течение нескольких месяцев до оперативного лечения или облучения простаты (неоадъювантная терапия) позволяет уменьшить предстательную железу в объёме и, таким образом, облегчить ход операции или повысить эффективность лучевых методов лечения. Недостатком этого вида терапии считают риск негативных проявлений гормонального лечения – например, эректильной дисфункции или «приливов», которых можно было бы избежать при немедленном выполнении операции. Изучение данной методики также продолжается.
Химиотерапия при раке предстательной железы
Химиотерапия – это применение одного противоракового препарата или их сочетания. Ее назначают в случае рецидива или рака предстательной железы поздней стадии, который не отвечает на гормональное лечение, но она не используется в лечении ранних стадий заболевания. Химиотерапию назначают циклами лечения, за которыми следует период восстановления. Все лечение обычно продолжается 3 – 6 месяцев, в зависимости от вида применяемых химиотерапевтических препаратов.
Каковы побочные эффекты?
Химиотерапия убивает не только раковые клетки, она и здоровые клетки организма, такие как мембраны выстилки рта, выстилку желудочно-кишечного тракта, волосяные фолликулы и костный мозг. В результате, побочные эффекты химиотерапии зависят от количества поврежденных клеток. Специфические побочные эффекты, которые могут быть, зависят от вида и количества препаратов, от длительности приема. К наиболее распространенным временным побочным эффектам химиотерапии относятся:
К другим побочным эффектам, связанным с воздействием химиотерапии на костный мозг, относятся повышенный риск инфекции (из-за низкого уровня лейкоцитов), кровотечение или кровоподтеки от малейших повреждений (из-за низкого уровня тромбоцитов в крови) и утомляемость, вызванная анемией (из-за низкого уровня эритроцитов в крови). Побочные эффекты химиотерапии исчезнут, когда лечение прекратится.
Использование уникальных методик рака предстательной железы
В МНИОИ им. П.А.Герцена разработан протокол комбинированного лечения больных раком простаты с наличием единичных метастазов в лимфоузлах таза или костях. В случае выявления вышеуказанных метастатических очагов на момент постановки диагноза рака простаты, больному проводят на первом этапе гормональную терапию в комбинации с 6 курсами химиотерапии (препарат Доцетаксел). На втором этапе выполняют хирургическое удаление предстательной железы и лимфоузлов таза и забрюшинного пространства. При необходимости, в послеоперационном периоде проводят лучевую терапию на очаги в костях. Отмечено, что данный лечебный подход позволяет добиться увеличения времени безлекарственной терапии, увеличить сроки без рецидива, и, возможно, продолжительность жизни пациентов этой сложной для лечения группы.
Особенности реабилитации после лечения рака предстательной железы
Реабилитация после хирургического лечения проводится как правило в несколько этапов. В раннем послеоперацонном периоде пациент активизируется, садится, встает, начинает ходить уже через 12 часов после операции. Питание также начинается в первые сутки послеоперационного периода. Во время операции хирурги устанавливают 1 или 2 дренажа в полость малого таза, в полость мочевого пузыря устанавливают уретральный катетер для контроля диуреза и адекватного заживления анастомоза между мочевым пузырем и мочеиспускательным каналом. Уретральный катетер удаляют, как правило, на 7-8 сутки после операции. По истечении 7-10 дней после операции пациент выписывается в удовлетворительном состоянии.
В послеоперационном периоде необходимо применение бандажа, который требуется носить 1-1,5 месяца. В это время рекомендуется избегать чрезмерных физических нагрузок.
Прогноз заболевания
Прогноз заболевания в первую очередь зависит от своевременности диагностики заболевания, а также от характеристик опухоли и факторов прогноза (стадия опухолевого процесса, уровень ПСА, морфологические характеристики опухоли при биопсии). Рак простаты по количеству летальных исходов занимает третью позицию после рака легкого и рака желудка. Принципиально важное значение играет раннее выявление опухоли и правильное лечение. В случае установления диагноза на 1-2 стадиях, а также и при 3 стадии в случае верно подобранного лечения (хирургическое лечение или лучевая терапия в сочетании с гормонотерапией) возможно полное излечение от рака. В случае установления 4 стадии заболевания при помощи лекарственного лечения можно добиться стойкой ремиссии.
Филиалы и отделения, в которых лечат рак предстательной железы
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.


