Протокол лечения пациентов с острым аппендицитом
Протокол разработан на основе рекомендаций Российского общества хирургов и приказа Департамента здравоохранения города Москвы № 320 (2011г.)
Классификация:
Морфологическая форма: катаральный, флегмонозный, гангренозный.
Осложнения: аппендикулярный инфильтрат, перфорация, аппендикулярный абсцесс, перитонит (отграниченный, распространенный), забрюшинная флегмона, пилефлебит.
Диагностика.
В приемном отделении, после осмотра хирургом, в течение 1 часа со времени поступления, больному должны быть проведены следующие исследования: общий клинический анализ крови, биохимия крови, коагулограмма, общий анализ мочи, группа крови и резус-фактор, ЭКГ, рентгенография грудной клетки и брюшной полости, ультразвуковое исследование брюшной полости.
В случаях неясной клинической картины выполняется компьютерная томография органов брюшной полости и малого таза. Все пациенты женского пола подлежат осмотру гинекологом. При необходимости производятся консультации урологом и терапевтом.
При неясной клинической картине и отсутствии явных признаков другой острой хирургической патологии показано динамическое наблюдение в течение 12 часов с оценкой клинических, лабораторных инструментальных данных в динамике.
При сохраняющейся после 12-часовго наблюдения неясной клинической картине и невозможности исключить острый аппендицит, а также с целью дифференциальной диагностики с другими острыми заболеваниями органов брюшной полости и малого таза, в качестве заключительного этапа диагностики показано проведение диагностической лапароскопии, которая при необходимости может быть трансформирована в лапароскопическую аппендэктомию.
В любых сомнительных случаях, при невозможности исключить острый аппендицит, выбор лечения решается в пользу операции. При установленном диагнозе острого аппендицита оперативное лечение должно быть начато в течение 2 часов с момента установления диагноза.
Анестезия.
Приоритетным вариантом является комбинированный эндотрахеальный наркоз.
Хирургическая тактика.
Приоритетным является выполнение видеолапароскопической аппендэктомии.
Противопоказанием к видеолапароскопической аппендэктомии являются: тяжелая сердечно-сосудистая и дыхательная недостаточность, распространенный перитонит, выраженный спаечный процесс в брюшной полости, грубый рубцовый процесс на передней брюшной стенке вследствие ранее перенесенных операций. При наличии противопоказаний к видеолапароскопической аппендэктомии и отсутствии показаний к выполнению срединной лапаротомии (см. ниже) показано выполнение аппендэктомии из доступа по Волковичу-Дьяконову.
При лапароскопической аппендэктомии брыжейка червеобразного отростка по частям коагулируется с использованием биполярной электрокоагуляции Ligasure и пересекается. Основание отростка перевязывается тремя лигатурами с формированием узлов Редера. Между двумя дистальными лигатурами червеобразный отросток пересекается, культя обрабатывается йодом или спиртом, затем, в зависимости от диаметра, отросток извлекается из брюшной полости через троакар или в эндоконтейнере через троакарный разрез.
При наличии воспалительных изменений в области основания червеобразного отростка его культя, после предварительной перевязки лигатурой, погружается в кисетный и (или) «Z»-образный шов. В случае невозможности надежного укрытия культи червеобразного отростка кисетным и (или) «Z»-образным швом показано выполнение резекция купола слепой кишки с культей червеобразного отростка аппаратами Eshelon или EndoGia. Операция всегда завершается оставлением в полости малого таза как минимум одной дренажной трубки.
При визуальной картине катарального аппендицита и несоответствии клинической картины заболевания морфологическим изменениям, показана дополнительная ревизия подвздошной кишки (не менее 1 метра), придатков матки на предмет патологии этих органов.
При вторичном (поверхностном) аппендиците санируется основной (первичный) патологический процесс; аппендэктомия выполняется только при наличии деструктивной формы воспаления червеобразного отростка (флегмонозная, гангренозная).
Удаленный червеобразный отросток направляется на гистологическое исследование. Выпот и содержимое абсцессов направляется на бактериологическое исследование для идентификации микрофлоры и ее чувствительности к антибиотикам.
В случаях обнаружения во время операции распространенного фибринозного (гнойно-фибринозного) перитонита показано выполнение срединной лапаротомии, аппендэктомии (см. раздел «Перитонит»).
Применение антибиотиков при остром аппендиците.
Антибиотикопрофилактика показана во всех случаях операций по поводу острого аппендицита.
Антибиотикопрофилактика проводится цефалоспоринами генерации. Первая доза препарата (2 г) вводится внутривенно за 30 минут до начала операции.
При остром катаральном аппендиците повторно вводится 2г препарата через 12 часов.
При деструктивных формах аппендицита в послеоперационном периоде проводится антибактериальная терапия.
При остром флегмонозном аппендиците проводится терапия цефалоспоринами генерации в дозировке 2г х 2 раза в сутки – 5 суток.
При остром гангренозном аппендиците, при осложнениях в виде перфорации, абсцесса, перитонита показана комбинация из цефалоспаринов III поколения (4 г/сут), аминогликозидов (амикацин 7,5 мг/кг – 2 раза в сутки), метронидазола (2 г/сут).
Хирургическая тактика при аппендикулярном инфильтрате.
Статья добавлена 31 мая 2016 г.
Как проводится гистологическое исследование: виды, методы, особенности
Злокачественные новообразования — это группа заболеваний, насчитывающая несколько тысяч видов опухолей разных типов и разной степени злокачественности. Они подразделяются на большие группы в зависимости от того из каких тканей они развиваются: если из эпителиальных (барьерных) — то это раки, если из соединительных тканей (мягких тканей и костей) – саркомы, если из лимфоидных (иммунных) – лимфомы/лейкозы. От того насколько правильно верифицирована опухоль (определен ее тип, степень злокачественности и другие характеристики) зависит правильность и эффективность лечения. Важную роль в этом играют гистологические исследования.
О том, как проходят гистологические исследования, какие задачи кроме диагностических они позволяют решать, что влияет на сроки их выполнения рассказывает заведующая патологоанатомическим отделением с прозектурой НМИЦ онкологии им. Н.Н. Петрова, к.м.н. Анна Сергеевна Артемьева.
Что служит материалом для патоморфологических (гистологических) исследований?
Процесс получения фрагмента ткани (биоптата) — биопсия – это несколько разных способов забора материала для гистологического исследования.
Биопсию внутренних органов делают под УЗИ-навигацией, либо с помощью хирургического вмешательства.
Как обрабатывают эти материалы для проведения гистологического исследования?
1 Этап. Фиксация — «консервирование» биоптата в формалине — специальном химическом растворе, который предотвращает гниение, позволяет сохранить структуры ткани.
Фиксация биоптата может занимать от 6 до 24 часов – в зависимости от его вида и размера.
Операционный материал фиксируется дольше, в несколько этапов. Сначала предварительная фиксация, которая занимает примерно 12 часов. Затем вырезка нужных фрагментов и повторная фиксация еще 24 часа.
Соотношение объема материала к объему формалина должно быть 1:20.
2 Этап. Процессинг — процесс обезвоживания, обезжиривания и пропитки материала парафином. Автомат перемещает кусочек материала из раствора в раствор.
В качестве растворов применяются: абсолютированный изопропиловый спирт (6-8 смен), ксилол (2 смены), расплавленный парафин (2 смены).
Программа разнится для «жирного» материала (к которым относятся, например, ткани молочной железы) и «нежирного» – 36 и 24 часа соответственно.
Процесс получения парафиновых блоков.
3 Этап. Изготовление парафинового блока. Кусок материала помещается в форму с расплавленным парафином (уже другим нежели во время процессинга – с более высокой температурой плавления) и охлаждается. Выполняется вручную, сложно ускорить.
4 Этап. Изготовление срезов. Толщина образца — кусочка ткани, залитого в парафин – 1-3 мм. Толщина каждого среза 4-5 мкм (0,004-0,005 мм). Выполняет лаборант с использованием специального инструмента – микротома.
Срезы монтируются на стекла и должны высохнуть.
Несмотря на то, что часть материала теряется при выравнивании в микротоме, при должном профессионализме, из одного образца — материала от одной биопсии, операционного материала от одной опухоли, возможно изготовить около 100 стекол (микропрепаратов).
Для чего делаются срезы?
Срезы делаются для рутинной окраски гематоксилинном и эозином, иммуногистохимического исследования и других видов исследований.
Срезы для всех исследований используются одинаковые, различается окраска, могут отличаться стекла, на которые они монтируются, так для ИГХ и FISH нужны специальные адгезивные стекла или заряженные стекла.
Блоки и стекла способны храниться долгие годы и использоваться для проведения дополнительных гистологических исследований, пересмотров, а также в научных целях.
Архив гистологических материалов собирается в НМИЦ онкологии им. Н.Н. Петрова с 1927 года и содержит более 10 млн единиц хранения (микропрепараты — стекла, парафиновые блоки, архивные карточки, влажный архив).
Какие виды гистологических исследований наиболее информативны?
Что позволяют определить разные виды гистологических исследований
Гистологическое исследование – что это такое?
Позволяет верифицировать опухоль – то есть определить из каких клеток она состоит (из какой ткани она развивается), степень ее дифференцировки (зрелости).
Рутинная окраска, выполняющаяся при гистологическом исследовании, позволяет выявить патологический процесс в анализируемом материале (биоптате, операционном материале):
Также, в большинстве случаев, благодаря рутинной окраске, можно определить степень злокачественности опухоли и, если она достаточно зрелая, то какова ее природа.
Окрашенные срезы под микроскопом
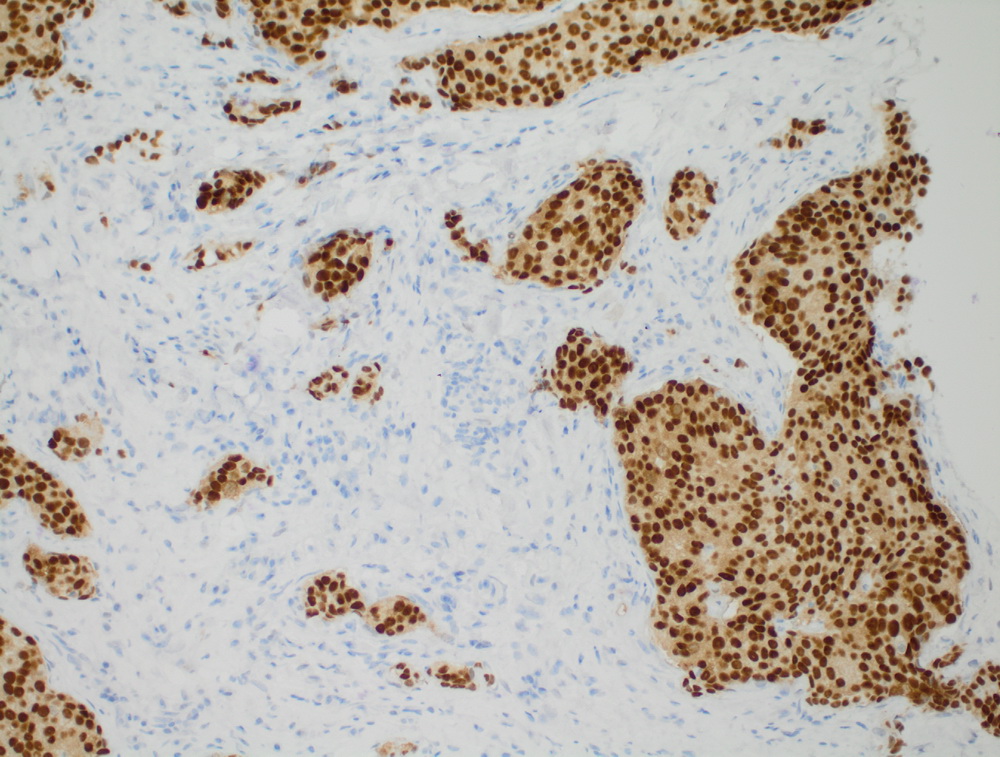 |
Инвазивный протоковый рак er 100%.
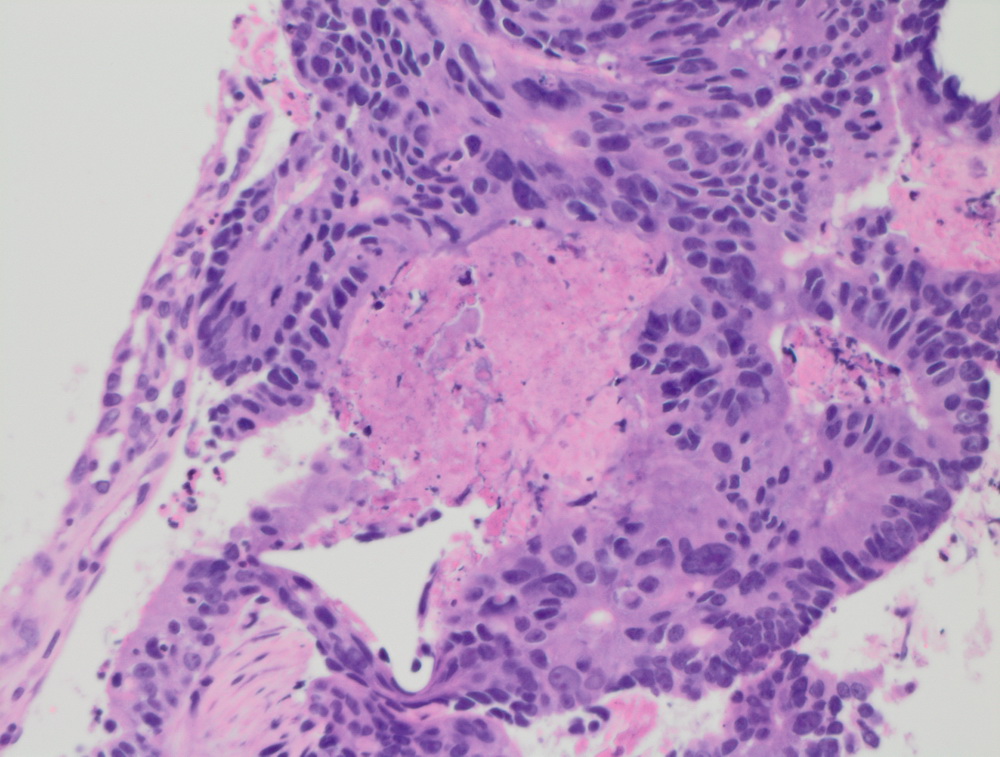
Карцинома сигмовидной кишки.
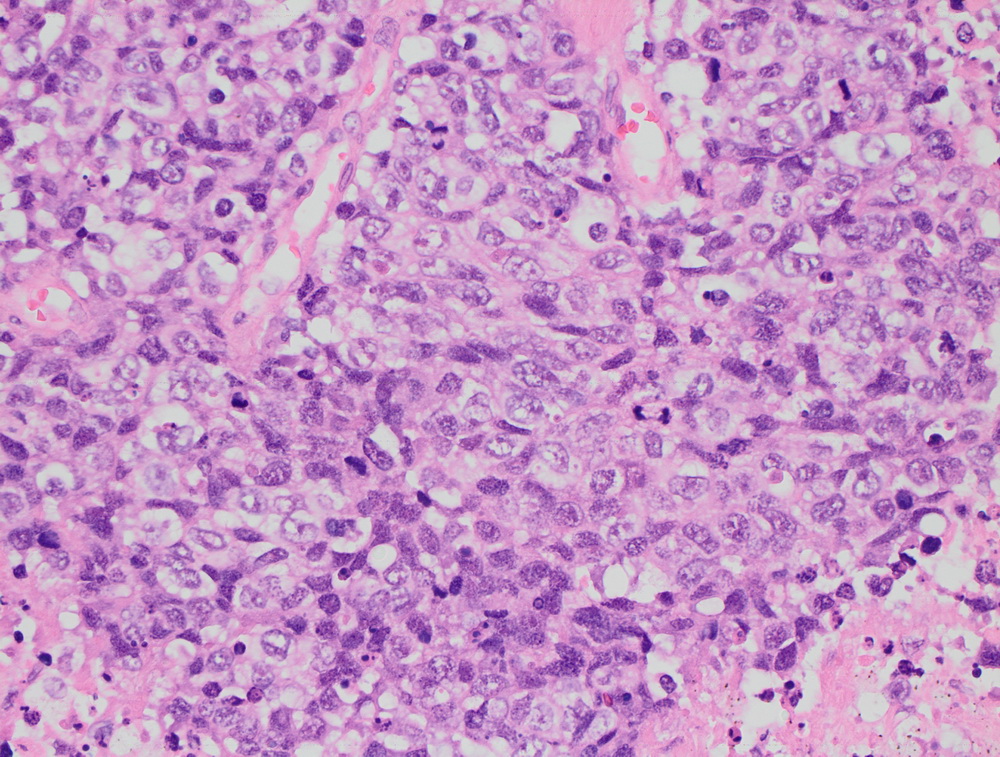
Крупноклеточная нейроэндокринная опухоль.
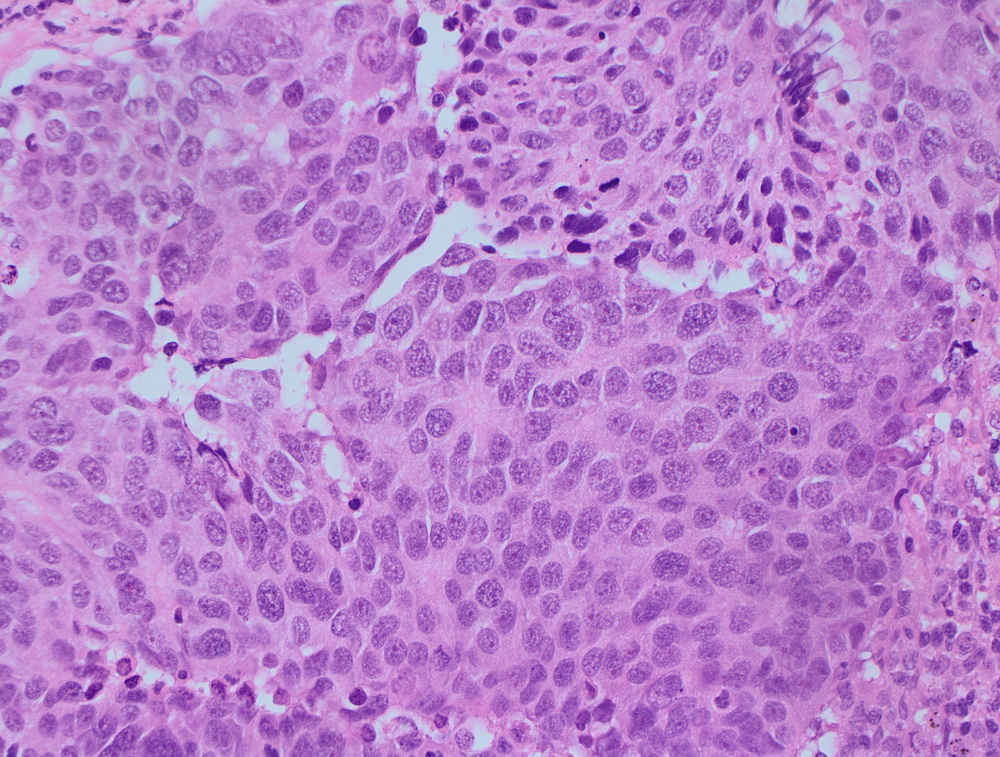
МТС крупноклеточной нейроэндокринной опухоли.
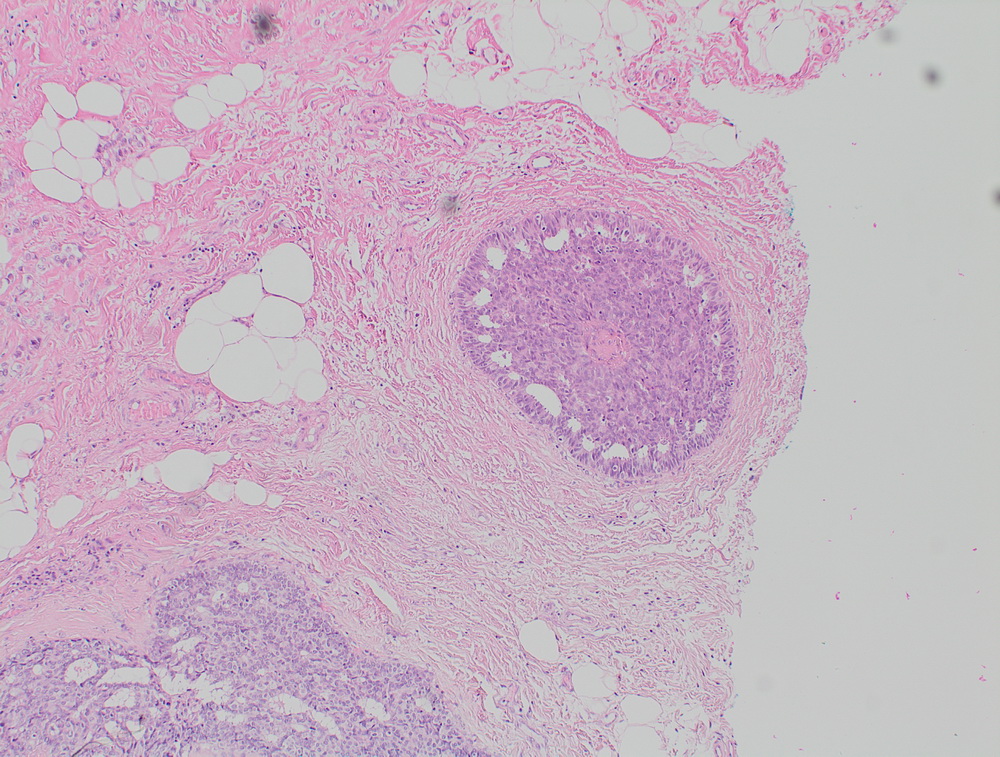
Неспецифический рак молочной железы. Участок in situ карциномы внутри протока, криброзного типа.
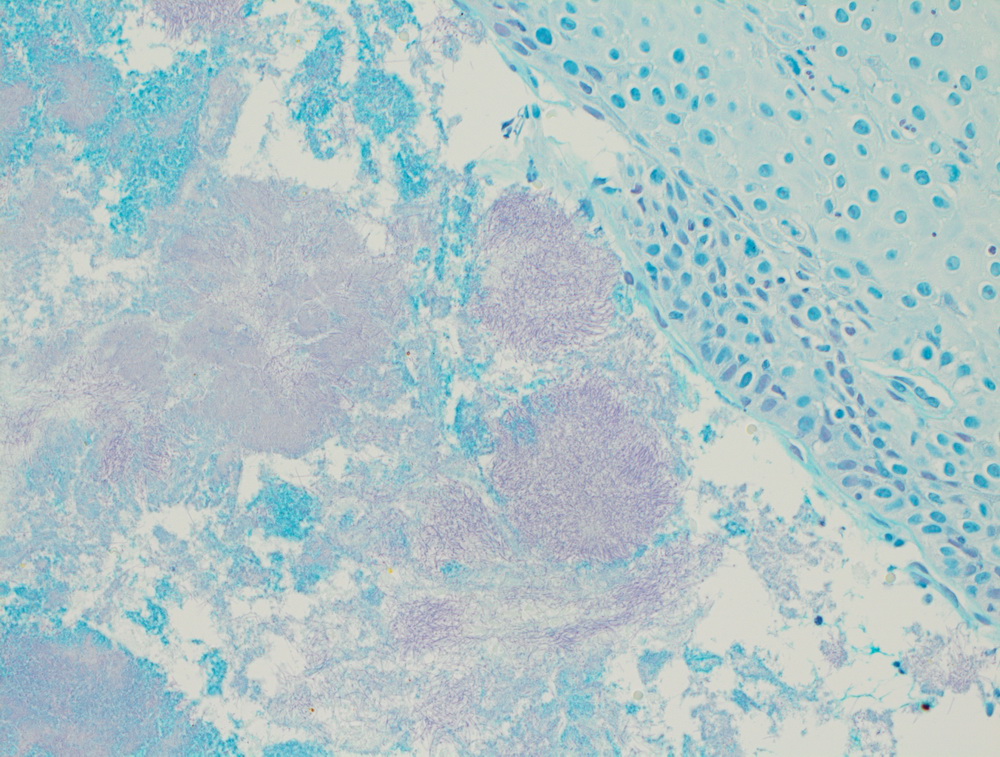
Низкодифферинцированный рак пищевода.
При гистологическом исследовании биоптата и операционного материала можно оценить распространенность: размер опухоли и прорастание в окружающие ткани, насколько затронуты лимфоузлы и есть ли метастазы в отдаленные органы (если эти все структуры присланы для гистологического исследования). При консультации готовых микропрепаратов – стекол, это, как правило, невозможно, если опухоль больше размеров гистологической кассеты или рассечена предыдущим исследователем и не предоставлены данные макроскопического исследования.
Во время гистологического исследования изучаются все стекла от одного образца – материала, полученного от одного вмешательства — одной операции или одной биопсии, вне зависимости от их количества, это считается одной консультацией.
Сроки выполнения гистологического исследования зависят от количества микропрепаратов и от категории сложности того процесса, который в них обнаруживается, сроки могут удлиняться, особенно при необходимости использования дополнительных методов исследования и анализа дополнительных сведений. На сроки выполнения гистологического исследования влияет полнота предоставленной пациентом клинической информации, в том числе данных уже проведенных исследований.
Иммуногистохимия (ИГХ)
Сложное многоэтапное исследование, выполняется после гистологического исследования на том же материале. Опухолевые срезы окрашиваются антителами, которые способны связываться антигенами (белками), которые несут опухолевые клетки. Разные опухолевые клетки несут разные антигены, к каждому из которых подобно ключа к замку подходит антитело.
Один из этапов ИГХ
ИГХ исследование — это комбинаторика. 100% специфичных и чувствительных к какой-то опухоли маркеров не существует, но есть набор антигенов, которые в определенном типе опухоль должны быть и набор тех, которых там быть не должно, таким образом ИГХ-панель строится так чтобы включать несколько антител, которые должны быть позитивны и несколько, которые должны быть негативны. Для разных опухолей различаются эти наборы позитивных/негативных маркеров.
При проведении прогностической ИГХ – выявлении маркеров чувствительности к терапии определяется набор таких маркеров для конкретных опухолей, например, рака молочной железы: рецепторы стероидных гормонов (эстроген, прогестерон), рецептор эпидермального фактора роста (HER2) и индекс пролиферативной активности Ki67 (скорости деления клеток).
Стекла окрашиваются последовательно — различными антителами красятся наборы маркеров в несколько этапов, процесс окраски стекол одним антителом занимает 48 часов.
Таким образом, каждое антитело наносится на отдельный срез ткани, монтированный на отдельное стекло, как правило с соответствующим внешним контролем, количество реакций (используемых антител) и этапов окраски может существенно варьировать в зависимости от конкретной диагностической ситуации, все зависит от индивидуальных особенностей опухоли. Проводится такое количество окрасок, которое необходимо для того, чтобы выявить наиболее характерный для определенной опухоли набор позитивных и негативных маркеров.
Кому-то для этого будет достаточно 5 антител, а кому-то необходимо сделать 20 окрасок и более. Максимальное количество окрасок, которое нам приходилось делать – 212.
Поэтому точные сроки и стоимость этого исследования невозможно определить заранее. Разные по течению и прогнозу опухоли могут быть очень похожи друг на друга, только минимальные различия в окрашивании, с учетом клинических данных и данных других методов обследования, могут позволить установить верный диагноз.
Есть целый ряд доброкачественных опухолей, симулирующих злокачественные, в том числе высокоагрессивные, а некоторые злокачественные высоко дифференцированные опухоли трудно отличить от воспалительных и реактивных процессов. В таких ситуациях только опыт и квалификация патоморфолога, анализ всего комплекса доступной информации (снимки КТ, МРТ, рентген, протокол операции, и др.) позволяют поставить диагноз.
В грамотной интерпретации результатов ИГХ очень важна роль эксперта, ведь те случаи, с которыми приходится работать, в большинстве своем, сложные. Практически не существует антител, которые могут выступать в качестве 100%-х маркеров той или иной опухоли, врачу всегда приходится взвешивать различные вероятности.
Что определяется с помощью ИГХ?
Иммуногистохимия позволяет оценить потенциальный темп роста опухоли, ответ на химио-, таргетную, гормональную терапию.
Флуоресцентная гибридизация in situ (FISH-тест)
Это метод молекулярно-генетической диагностики в ткани.
FISH проводится в срезе ткани и позволяет привязать генетическую перестройку к конкретной опухолевой клетке.
В этом тесте также используются специальные красители, которые связываются только с определенными участками хромосом. Их называют зондами, которые могут быть помечены флуоресцентным или хромогенным красителем, визуализирующимися при помощи флуоресцентного или светового микроскопа.
Технические операции по подготовке гистологических стекол к этому исследованию занимает 2 рабочих дня.
Анализ препарата с помощью многоголового микроскопа.
Полученные микропрепараты очень чувствительны к внешней среде – они могут выцвести со временем, чтобы избежать потерь информации все FISH-препараты сканируются, создается их цифровая копия, которая доступна для внешнего пересмотра. Специалисты просматривают флуоресцирующий материал в темном поле, в анализе препарата принимают участие как минимум 2 специалиста. При необходимости используется и цифровой анализ.
Что определяется с помощью FISH-теста?
FISH-тест позволят диагностировать некоторые виды опухолей, определяет целесообразность использования некоторых химиотерапевтических препаратов.
Проведение гистологического исследования, и в первую очередь FISH-теста — это экспертная работа, которая зависит от квалификации специалиста. Очень многие мутации, которые выявляются в опухолях, не всегда являются метками опухолей, они могут находиться и в доброкачественных образованиях или нормальных тканях.
За год патологоанатомическое отделение НМИЦ онкологии имени Н.Н. Петрова выполняет около 20000 гистологических исследований (пациентов), из них около 5000 консультативных случаев (пересмотров), более 30000 ИГХ исследований, а также участвует в программе внешнего контроля качества ИГХ исследований NordIQ.
Специалисты отделения обладают огромным опытом проведения гистологических исследований и экспертными компетенциями.
Скорость выполнения гистологических исследований и адекватность гистологического заключения зависят от ряда факторов:
После выполнения гистологического исследования пациент получает гистологическое заключение/протокол исследования гистологического материала.
Расшифровка гистологического исследования: на что обратить внимание?
Гистологическое заключение включает в себя несколько рубрик (полей):
Макроскопическое описание
Заполняется как для биоптатов — не обязательно, так и для операционного материала, для которого имеет крайне важное значение в ряде случаев.
Микроскопическое описание
Описание изменений на микроскопическом уровне, не обязательно к заполнению, так как вся необходимая информация может быть отражена в поле «заключение».
Результаты иммуногистохимического исследования
В этом поле описано какие антитела использовались в данном случае и каков результат окрашивания: наличие окрашивание или его отсутствие, локализация в клетке при необходимости, а также процент позитивных клеток и интенсивность реакции, когда это имеет значение.
Патологоанатомическое заключение
Содержит нозологическую/классификационную единицу, если ее возможно установить по исследованному материалу, то есть дает ответы на вопросы:
Также приводятся все необходимые прогностические данные: степень дифференцировки, параметры, влияющие на стадию, состояние краев резекции, если возможно их оценить и т.п.
Дополнительные замечания и рекомендации
Поле может содержать комментарии, относительно возможного направления дальнейшего обследования, вероятности того или иного диагноза, необходимости ознакомиться с теми или иными клиническими данными и др.
Мы не рекомендуем пациентам самостоятельно заниматься расшифровкой показателей гистологического исследования, используя информацию, полученную на различных Интернет-сайтах и форумах пациентов, так как на интерпретацию данных влияет большое количество факторов, в том числе, возраст пациента, данные других исследований и др.
Расшифровкой исследования может заниматься только специалист – врач онколог по профилю заболевания!
Авторская публикация:
АРТЕМЬЕВА АННА СЕРГЕЕВНА
заведующий патологоанатомического отделения с прозектурой ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, кандидат медицинских наук
Осложнения ран. Основные принципы лечения
Ранения могут сопровождаться разнообразными осложнениями, как сразу после нанесения ран, так и в отдаленные сроки. К осложнениям ран относятся:
· Развитие травматического или геморрагического шока – является наиболее ранним и грозным осложнением. В отсутствие немедленной помощи становится причиной неблагоприятного исхода.
· Серомы – скопления раневого экссудата в раневых полостях, опасные возможностью нагноения. При развитии серомы необходимо обеспечить эвакуацию жидкости из раны.
· Раневые гематомы – образуются вследствие неполной остановки кровотечения. Гематомы являются потенциальными очагами инфекции, кроме того, сдавливая окружающие ткани, приводят к их ишемии. Их необходимо удалять с помощью пункции или при ревизии раны.
· Некрозы окружающих тканей – развиваются при нарушении кровоснабжения в соответствующей области при травматизации тканей во время операции или неправильном наложении швов. Влажные некрозы кожи необходимо удалять из-за опасности появления глубоких скоплений гноя. Поверхностные сухие некрозы кожи не удаляют, так как они выполняют защитную функцию.
· Раневая инфекция – ее развитию способствуют высокий уровень контаминации и высокая вирулентность попавшей в рану микрофлоры, наличие в ране инородных тел, некрозов, скоплений жидкости или крови, повреждение при ранении костей, нервов, сосудов, хроническое нарушение местного кровоснабжения, а также поздняя хирургическая обработка и общие факторы, влияющие на течение раневого процесса. В экспериментальных и клинических исследованиях установлено, что в большинстве случаев для развития инфекционного процесса в ране необходимо, чтобы ее контаминация превысила критический уровень, составляющий 105-106 микроорганизмов на 1 грамм ткани. Среди общих факторов, способствующих развитию раневой инфекции, важную роль играет значительная кровопотеря, развитие травматического шока, предшествующее голодание, авитаминозы, переутомление, наличие сахарного диабета и некоторых других хронических заболеваний.
При попадании в рану с землей, пылью, инородными телами Cl. Tetani возможно развитие столбняка. В отсутствие специфической профилактики вероятность заболевания столбняком при наличии контаминированных ран достигает 0, 8%. Через укушенные раны в организм может проникать вирус бешенства.
· Осложнения рубцов – образование гипертрофированных рубцов и келоидов. Гипертрофированные рубцы развиваются при склонности к избыточному образованию рубцовой ткани и чаще всего при расположении раны перпендикулярно к линии Лангера. Келоиды в отличие от гипертрофированных рубцов имеют особую структуру и распространяются за пределы границ раны. Осложнения рубцов ведут не только к косметическим, но и к функциональным дефектам, таким как нарушение ходьбы или функций верхней конечности из-за ограничения объема движений в суставах. Хирургическая коррекция показана при гипертрофированных рубцах с нарушением функции, однако при келоидах она нередко приводит к ухудшению результата лечения.
· Длительно существующие хронические раны могут осложниться развитием малигнизации. Диагноз подтверждает биопсия тканей раны. Лечение оперативное – необходимо радикальное иссечение в пределах здоровых тканей.
Основные принципы лечения ран
Лечение при ранениях обычно проходит в два этапа – этап первой помощи и этап квалифицированной помощи.
¨ Этап первой помощи
При оказании первой помощи на месте ранения решаются две основные задачи: остановка кровотечения и предотвращение дальнейшей микробной контаминации. Первая помощь включает в себя применение доступных методов временной остановки кровотечений, обезболивание, наложение защитной повязки и транспортную иммобилизацию. На этом этапе не следует промывать рану и удалять из нее инородные тела.
¨ Этап квалифицированной помощи
На этапе госпитальной помощи решаются следующие задачи:
· профилактика и лечение раневых осложнений;
· ускорение процесса заживления;
· восстановление функций поврежденных органов и тканей.
Основные принципы лечения ран:
· строгое соблюдение асептики на всех этапах лечения;
· обязательная хирургическая обработка;
· активное дренирование;
· максимально раннее закрытие ран первичными или вторичными швами или с помощью аутодермопластики;
· целенаправленная антибактериальная и иммуннотерапия, коррекция системных нарушений.
Для выбора адекватной тактики лечения ран необходима тщательная оценка ее состояния, при этом оцениваются:
· Локализация, размер, глубина раны, повреждения нижележащих структур, таких как фасции, мышцы, сухожилия, кости.
· Состояние краев, стенок и дна раны, а также окружающих тканей, наличие и характеристика некротических тканей.
· Время, прошедшее с момента ранения.
¨ Лечение контаминированных ран
Риск развития раневых осложнений при наличии контаминированных ран гораздо выше, чем при асептических ранах. Лечение контаминированных ран состоит из следующих этапов:
В целях профилактики столбняка вакцинированным пациентам вводят 0, 5 мл столбнячного адсорбированного анатоксина, невакцинированным пациентам – 1 мл анатоксина и 3000 МЕ противостолбнячной сыворотки. Из-за опасности развития анафилактических реакций на белок введение противостолбнячной сыворотки производится по Безредко: сначала 0, 1 мл разбавленной сыворотки вводится внутрикожно, при величине папулы менее 10 мм через 20 минут вводится 0, 1 мл неразведенной сыворотки подкожно, и только при отсутствии реакции на подкожное введение через 30 минут вводится вся доза подкожно.
При укусах животных (собак, лис, волков и др. ), подозрительных на бешенство, или попадании их слюны на поврежденные ткани нельзя производить первичную хирургическую обработку раны. Рана только промывается и обрабатывается антисептиком. Швы не накладываются. Необходим курс подкожного введения антирабической вакцины, который выполняется в специализированных антирабических пунктах, и проведение профилактики столбняка. При наличии поверхностных повреждений (ссадины, царапины) любой локализации кроме области головы, шеи, кистей рук, пальцев ног и гениталий, нанесенных домашними животными, культуральная очищенная концентрированная антирабическая вакцина (КОКАВ) вводится по 1 мл немедленно, а также на 3, 7, 14, 30 и 90 дни. Но если при наблюдении за животным оно остается здоровым в течение 10 суток, то лечение прекращают после 3 инъекции.
При попадании слюны животных на слизистые оболочки, при локализации укусов в области головы, шеи, кистей рук, пальцев ног и гениталий, а также при глубоких и множественных укусах и любых укусах диких животных, кроме введения КОКАВ необходимо немедленное введение антирабического имунноглобулина (АИГ). Гетерологический АИГ назначается в дозе 40 МЕ на кг массы тела, гомологичный – в дозе 20 МЕ на кг массы тела. Большая часть дозы должна быть инфильтрирована в ткани, окружающие рану, остальная часть вводится внутримышечно. Если возможно наблюдение за животным, и оно в течение 10 суток остается здоровым, то введение КОКАВ прекращают после 3 инъекции.
· Во всех случаях контаминированных ран, кроме небольших поверхностных повреждений и случаев, когда имеются косметические и функциональные противопоказания, обязательно проведение первичной хирургической обработки (ПХО) с рассечением раны, ревизией раневого канала, иссечением краев, стенок и дна раны. Цель ПХО в полном удалении нежизнеспособных и контаминированных тканей. Чем позже производится ПХО, тем ниже вероятность предупреждения инфекционных раневых осложнений.
ПХО не проводится при локализации ран на лице, так как приводит к увеличению косметического дефекта, а хорошее кровоснабжение данной области обеспечивает низкий риск нагноений и активное заживление ран. При обширных ранах волосистой части головы выполнение ПХО в полном объеме может привести к невозможности сопоставления краев и закрытия раны. Не подлежат ПХО также колотые непроникающие раны без повреждения крупных сосудов и укушенные раны при подозрении на возможность проникновения вируса бешенства. ПХО может завершаться наложением первичных швов – с ушиванием наглухо либо, при наличии факторов риска нагноения раны, – с оставлением дренажей.
Предпочтительно проточно-промывное дренирование ушитых ран с последующим диализом эффективными антисептиками. Проточно-промывное дренирование осуществляется установкой встречных перфорированных дренажей, по одному из которых вводится лекарственное средство, по другому осуществляется отток. Введение препаратов может быть струйным и капельным, дробным или постоянным. Отток при этом может осуществляться пассивным и активным способом – с помощью вакуумирования.
Данный метод предохраняет раны от вторичного обсеменения, способствует более полному удалению отделяемого, создает условия управляемой абактериальной среды и благоприятные условия для заживления ран. При дренировании необходимо соблюдать несколько общих принципов. Дренаж устанавливают в отлогих местах раневой полости, где максимально скопление жидкости. Выведение дренажной трубки через контрапертуру предпочтительнее, чем через рану, так как дренаж, являясь инородным телом, мешает нормальному заживлению раны и способствует ее нагноению.
При высоком риске развития нагноения раны, например, при наличии резких изменений окружающих тканей, показано наложение первично-отсроченных швов, в том числе провизорных. Как и первичные, эти швы накладываются на рану до развития грануляционной ткани, обычно на 1-5 сутки после ПХО при стихании воспалительного процесса. Заживление таких ран протекает по типу первичного натяжения. Швы не накладываются только после обработки огнестрельных ран и при невозможности сопоставления краев раны без натяжения, в последних случаях показано максимально раннее закрытие раневого дефекта с помощью реконструктивной операции.
· Антибиотикопрофилактика проводится по той же схеме, что и при «грязных» оперативных вмешательствах. Требуется 5-7 дневный курс введения антибиотиков.
· Антисептикопрофилактика предполагает использование эффективных антисептиков на всех этапах операции и при уходе за раной. При обработке ран могут применяться хлоргексидин, гипохлорит натрия, диоксидин, лавасепт, перекись водорода, перманганат калия и другие антисептики. Такие препараты, как фурацилин, риванол, хлорамин, в настоящее время не рекомендуются для использования в хирургических отделениях, так как госпитальная микрофлора устойчива к ним практически повсеместно.
· Ведение раны после проведения ПХО при наложении швов аналогично ведению операционных ран. Выполняется регулярная смена асептических повязок и уход за дренажами. Лечение открытых ран после ПХО производится, как и лечение гнойных ран, в соответствии с фазами течения раневого процесса.
¨ Лечение гнойных ран
· Во всех случаях инфицированных ран, когда нет особых функциональных противопоказаний, производится вторичная хирургическая обработка (ВХО). Она заключается во вскрытии гнойного очага и затеков, эвакуации гноя, иссечении нежизнеспособных тканей и обязательном обеспечении адекватного дренирования раны. Если после проведения ВХО рана не ушивалась, в последующем возможно наложение вторичных швов. В отдельных случаях при радикальном иссечении гнойника при ВХО могут быть наложены первичные швы с обязательным дренированием раны. Предпочтительно проточно-промывное дренирование. При наличии противопоказаний к проведению ВХО ограничиваются мероприятиями по обеспечению адекватной эвакуации экссудата.
· Дальнейшее местное лечение гнойных ран зависит от фазы течения раневого процесса.
В фазе воспаления основные задачи лечения – борьба с инфекцией, адекватное дренирование, ускорение процесса очищения раны, снижение системных проявлений воспалительной реакции. Основой является лечение повязками. Для всех ран, заживающих вторичным натяжением, стандартным методом лечения считается влажная обработка. Сухая обработка с наложением на рану сухих стерильных салфеток используется только для временного покрытия ран и обработки ран, заживающих первичным натяжением.
Смена повязок должна происходить при адекватном обезболивании. Частота смены повязок зависит от состояния раны. Обычно требуется 1-2 смены повязок в день, гидроактивные повязки типа «Гидросорба» могут оставаться на ране несколько дней, необходимость немедленной смены повязки возникает в следующих случаях: пациент жалуется на боль, развилась лихорадка, повязка промокла или загрязнилась, нарушилась ее фиксация. На каждой перевязке рану очищают от гноя и секвестров, иссекают некрозы и промывают антисептиками. Для промывания раны могут использоваться хлоргексидин, гипохлорит натрия, диоксидин, лавасепт, перекись водорода, озонированные растворы. Для ускорения некролиза применяются протеолитические ферменты, УЗ-кавитация, вакуумная обработка раны, обработка пульсирующей струей. Из физиотерапевтических процедур показано УФО раны, электро- и фонофорез с антибактериальными и аналгезирующими веществами.
В фазе регенерации основные задачи лечения – продолжение борьбы с инфекцией, защита грануляционной ткани и стимуляция процессов репарации. Необходимость в дренировании уже отсутствует. Повязки, накладываемые в фазу регенерации, должны защищать рану от травматизации и инфекции, не склеиваться с раной и регулировать влажность среды в ране, препятствуя как высыханию, так и избыточной влажности. Применяют повязки с жирорастворимыми антибактериальными мазями, стимулирующими веществами, современные атравматичные повязки.
· Общее лечение гнойных ран включает антибактериальную терапию, дезинтоксикацию, иммуннотерапию, симптоматическое лечение.
Антибактериальная терапия применяется в 1-2 фазах раневого процесса. Препарат необходимо назначать с учетом чувствительности микрофлоры раны. Показано системное введение антибиотиков, топическое введение в настоящее время не рекомендуется. Первичный эмпирический выбор антибактериальной терапии до получения результатов чувствительности должен быть направлен против типичных возбудителей, которыми являются стафилококки, стрептококки и грамотрицательные аэробные бактерии.
Детоксикация применяется при наличии системных проявлений воспалительного процесса. Используются инфузии солевых растворов, детоксицирующих растворов, форсированный диурез, в тяжелых случаях – экстракорпоральная детоксикация.
Иммунокорригирующая терапия может быть специфическая (вакцинами, сыворотками, анатоксинами) и неспецифическая. Часто применяются столбнячный анатоксин, противостолбнячная и противогангренозная сыворотка, противостолбнячный и антистафилококковый гамма-глобулин. Из средств неспецифической иммунотерапии у больных с гнойными ранами используются только иммуномодуляторы, причем лишь при наличии иммунных нарушений и обязательно в комплексе с антимикробным препаратом, так как они обостряют течение инфекции. Синтетические иммуномодуляторы, такие как диоцефон, полиоксидоний, являются наиболее перспективными. Полиоксидоний имеет свойства не только восстанавливать нарушенный иммунный ответ, но и сорбировать токсины, а также является антиоксидантом и мембраностабилизатором. Обычно назначается по 6 мг 2 раза в неделю, полный курс 5-10 инъекций.
¨ Профилактика инфекционных осложнений операционных ран
Операционные раны наносятся в условиях, минимизирующих риск раневых осложнений. Кроме того, до нанесения раны имеется возможность проведения профилактики раневых осложнений. Профилактика осложнений операционных ран включает:
· Проведение подготовки к операции
Перед плановой операцией проводится тщательное обследование пациента, в ходе которого выявляются имеющиеся факторы риска раневых осложнений. При оценке степени риска учитывается возраст, состояние питания, иммунный статус пациента, сопутствующие заболевания, нарушения гомеостаза, предшествующее медикаментозное лечение, состояние тканей в зоне предполагаемого разреза, вид и длительность предстоящего оперативного вмешательства. Производится коррекция имеющихся нарушений и непосредственная подготовка больного к операции с учетом требований асептики.
При операциях на толстой кишке, а также при обширных оперативных вмешательствах у крайне тяжелых больных для профилактики инфекционных осложнений проводится селективная деконтаминация кишечника. Селективная деконтаминация кишечника снижает риск энтерогенного инфицирования, происходящего в результате транслокации кишечных микроорганизмов. Обычно используется сочетание аминогликозида или фторхинолона с полимиксином и амфотерицином В или флуконазолом.
С каждым днем пребывания в стационаре увеличивается обсемененность пациента возбудителями госпитальных инфекций, поэтому этап стационарной предоперационной подготовки не следует затягивать без необходимости.
· Тщательное соблюдение оперативной техники
При выполнении оперативного вмешательства необходимо аккуратное обращение с тканями, тщательный гемостаз, сохранение кровоснабжения тканей в области раны, облитерация образующегося «мертвого» пространства, сопоставление краев раны и их сшивание без натяжения. Швы не должны быть ишемизирующими, но должны обеспечивать полное смыкание краев раны. По возможности, шовный материал, оставляемый в ране, должен быть рассасывающимся и монофиламентным. Кроме того, большую роль играет длительность операции. С ее увеличением возрастает степень контаминации раны и восприимчивость тканей к возбудителям раневой инфекции за счет подсыхания тканей, нарушения кровоснабжения, реактивного отека.
· Антибиотикопрофилактика
Антибиотикопрофилактика инфекционных раневых осложнений зависит от вида оперативного пособия. При чистых операциях она показана только при наличии факторов, неблагоприятно влияющих на течение раневого процесса, таких как имуннодефицитные состояния, сахарный диабет, прием имуннодепрессантов. При большинстве чистых и условно-чистых операций, а также при загрязненных вмешательствах на верхних отделах ЖКТ для антибиотикоприфилактики могут использоваться цефалоспорины 1-2 поколения, такие как цефазолин или цефуроксим. При загрязненных операциях на толстой кишке, желчевыводящей системе и внутренних половых органах показано применение защищенных аминопенициллинов или цефалоспоринов 1-2 поколения в сочетании с метронидазолом.
При проведении периоперационной профилактики используются средние терапевтические дозы антибиотиков. Первую дозу препарата вводят внутривенно за 30-60 минут до кожного разреза, обычно во время вводной анестезии. При длительности операции более 2-3 часов требуется повторное введение антибиотика для поддержания его терапевтической концентрации в тканях в течение всего оперативного вмешательства. В большинстве случаев продолжительность введения антибиотиков не превышает 24 часов, однако наличие дополнительных факторов риска обуславливает необходимость продления профилактики до 3 суток. При «грязных» вмешательствах показан полноценный курс антибиотикотерапии, который следует начинать еще в предоперационном периоде.
· Антисептикопрофилактика
· Дренирование операционных ран
Дренирование операционных ран проводится по определенным показаниям. Оно необходимо при невозможности облитерации образующегося после операции «мертвого пространства», при большой площади раневой поверхности подкожно-жировой клетчатки, при использовании искусственных материалов для пластики апоневроза и в некоторых других случаях, создающих предпосылки для образования сером. Дренирование также обязательно при радикальном иссечении гнойников с ушиванием послеоперационной раны. Предпочтительно аспирационное или проточно-промывное дренирование, при этом обязателен правильный уход за дренажной системой в послеоперационном периоде.
· Правильное ведение раны в послеоперационном периоде
Назначается холод местно сразу после операции, адекватное обезболивание, производится регулярная смена асептических повязок и уход за дренажами, по показаниям – диализ и вакуумирование раны, физиотерапия и прочие мероприятия.
¨ Контроль лечения ран
Эффективность лечения ран оценивается по динамике общих и местных признаков воспаления. Ориентируются на стихание лихорадки, лейкоцитоза, болей в области раны, нормализацию общего самочувствия больного. Во время перевязок визуально оценивают состояние швов, наличие и распространенность гиперемии и отека в окружности раны, некрозов краев раны, вид раневого отделяемого и грануляций. Для контроля течения раневого процесса при лечении дренированных ран могут применяться инструментальные методы исследования.
Используется эндоскопический метод осмотра раны с одновременной биопсией подкожно-жировой клетчатки для бактериологического исследования. При этом во время перевязки через дренаж послеоперационной раны вводится оптическая трубка эндоскопа с торцевой оптикой диаметром 3-6 мм, оценивается наличие раневого экссудата, участков некроза, фибрина, затем берется биопсия. Степень обсемененности ткани раны определяется с использованием экспресс-методик, например, методом фазово-контрастной микроскопии. После взятия биопсии раневой канал заполняют физиологическим раствором для оценки правильности расположения дренажей и направления потока жидкости при ее струйном введении.
Благоприятными эндоскопическими признаками течения раневого процесса и показанием к прекращению дренирования являются: наличие ярко-розовых грануляций, отсутствие гноя, некрозов, значительного количества фибрина, обсемененность ткани ниже критической. Вялые грануляции, наличие в ране большого количества экссудата и фибрина, а также высокая бактериальная обсемененность требуют продолжения диализа раны растворами антисептиков.
После удаления дренажных систем для оценки состояния раневого канала и окружающих тканей показано ультразвуковое сканирование. Благоприятными ультразвуковыми признаками течения раневого процесса являются:
· сужение раневого канала на следующие сутки после удаления дренажных трубок, визуализация его в виде неоднородной эхонегативной полоски к 3-5 суткам, отсутствие дилятаций и исчезновение канала к 6-7 суткам;
· равномерная эхогенность окружающих тканей, отсутствие в них дополнительных образований.
Неблагоприятными ультразвуковыми признаками течения раневого процесса являются дилятация дренажного канала и повышение эхогенности окружающих тканей с появлением в них дополнительных образований. Данные симптомы указывают на развитие гнойно-воспалительных раневых осложнений еще до появления их клинических признаков.
При лечении гнойной раны необходим ежедневный контроль за течением раневого процесса. При продолжающейся экссудации и вялой грануляции требуется коррекция лечения. Кроме визуальной оценки состояния раны и оценки выраженности общих клинических и лабораторных симптомов применяются различные методы контроля за динамикой микробного пейзажа, уровня обсемененности и регенераторных процессов в тканях: бактериологические, цитологические, современные высокоточные – газожидкостная хроматография, тесты с использованием ферментных систем и прочие.






