Простагландины – универсальные биорегуляторы в организме человека (обзор литературы)
Авторы
Ключевые слова:
Аннотация
В последнее время учеными разных отраслей уделяется огромное внимание проблеме простагландинов.
Цель работы – на основе анализа данных отечественной и зарубежной литературы изучить и систематизировать основные вопросы структуры, биологического действия, метаболизма простагландинов в организме человека и применение их аналогов в фармации.
Простагландины – биологически активные вещества, близкие по своему действию к гормонам, но, в отличие от гормонов, они синтезируются не в эндокринных железах, а в клетках различных тканей организма. Простагландины как универсальные клеточные медиаторы широко распространены в организме, синтезируются в минимальных количествах практически во всех тканях, имеют как местное, так и системное воздействие. Для каждого простагландина существует свой орган-мишень. По химическому строению они небольшие молекулы, относящихся к эйкозаноидам – группе жироподобных веществ (липидов). В зависимости от химической структуры простагландины делятся на серии (A, B, C, D, E, F, G, H, I и J) и три группы (1–3); изомеры типа F обозначаются дополнительно буквами α и β.
Простагландины обладают чрезвычайно широким спектром физиологических эффектов, относятся к самым активным биогенных веществам, выполняют в организме три основные функции: поддерживающую, молекулярную, медиаторную. Большинство простагландинов взаимодействуют со специфическими рецепторами цитоплазматических мембран, однако некоторые простагландины (группа А) могут действовать нерецепторно. Запас простагландинов в организме отсутствует, жизненный цикл их короткий, они быстро образуются в ответ на воздействие биологических стимуляторов, проявляют свое действие в чрезвычайно скудных количествах и быстро инактивируются, попадая в кровь. В связи с чрезвычайно быстрым распадом в организме простагландины действуют в основном вблизи места их секреции. Препараты простагландинов и их производных используют в экспериментальной и клинической медицине для прерывания беременности и стимуляции родовой деятельности, терапии язвы желудка, бронхиальной астмы, некоторых сердечно-сосудистых заболеваний, врожденных пороков сердца у новорожденных, глаукомы, атеросклероза, ревматических, неврологических заболеваний, болезнях почек, сахарном диабете, коррекции гемостаза, как антикоагулянты при операциях с искусственным кровообращением, а также при гемодиализе.
Выводы. Простагландины – самые активные универсальные биогенные вещества в организме человека с чрезвычайно широким спектром физиологических эффектов. Они имеют как местное, так и системное воздействие, реализуют свое действие различными путями, их рецепторы содержатся практически во всех органах организма, для каждого простагландина существует свой орган-мишень. Указанные свойства простагландинов отражаются в их широком применении в медицине и фармации. Несмотря на активные исследования в данном направлении, у ученых остается много вопросов относительно механизмов действия, функций простагландинов и их аналогов в организме человека.
Библиографические ссылки
Bondarenko, O. A. (2012). Riven prostahlandyniv ta tsyklichnykh nukleotydiv u syrovattsi krovi khvorykh na khronichnyi pankreatyt, spoluchenyi z ozhyrinniam v dynamitsi zahalnopryiniatoho likuvannia [The level of prostaglandinums and cyclic nucleotides in serum blood of the patients with chronic pancreatitis, combined with obesity]. Ukrainskyi medychnyi almanakh, 15(2), 31–34 [in Ukrainian].
Victorov, О. P., Deyak, S. I., Bazyka, O. Y., Kashuba, O. V., & Matveyeva, О.V. (2011). Efektyvne ta bezpechne medychne zastosuvannia analhetykiv-antypiretykiv (pohliad na problemu) [Effective and safe analgetics-antipyretics use (problem view)]. Ukrainskyi medychnyi chasopys, 6(86), 90–93. [in Ukrainian].
Zharkova, T. S. (2015). Klinichne znachennia prostahlandyniv u formuvanni variantiv perebihu bakterialnykh kyshkovykh infektsii u ditei [Clinical significance of prostaglandins in the formation of courses of bacterial intestinal infections in children]. Zdorov’e rebenka, 62, 120–122. [in Ukrainian].
Zhuk, S. I., Khoroshaeva, N. E., & Salnikov, S. N. (2012). Dosvid dopolohovoi pidhotovky shyiky matky preparatamy, shcho mistiat promestryn [Experience of prenatal preparation of the cervix with drugs containing promestrin]. Reproduktivnaya e’ndokrinologiya, 4(6), 70–73 [in Ukrainian].
Ilkiv, I. I., Panasiuk, N. B., Biletska, L. P., & Skliarov, O. Ya. (2014). Zminy pokaznykiv systemy NO-syntaza/arhinaza za umov poiednanoi dii hostroho stresu ta blokuvannia tsyklooksyhenazy/lipooksyhenazy u tonkii kyshtsi [Changes indicators of NO-synthase/arginase under conditions combined effects of acute stress and blocking cyclooxygenase/lipooksyhenazе in the small intestine]. Eksperymentalna ta klinichna fiziolohiia i biokhimiia, 4, 19–25 [in Ukrainian].
Kuznietsov, S. V., & Zharkova, T. S. (2010). Rol prostahlandyniv u formuvanni klinichnoho variantu perebihu shyhelozu u ditei [The role of prostaglandins in the formation of the clinical alternative course of shigellosis in children]. Sovremennaya pediatriya, 3(31), 58–60 [in Ukrainian].
Pertseva, T. O., & Sanina, N. A. (2012). Rol systemnykh zapalnykh protsesiv u patohenezi khronichnoho obstruktyvnoho zakhvoriuvannia lehen [The role of systemic inflammation in the pathogenesis of chronic obstructive pulmonary disease]. Ukrainskyi pulmonolohichnyi zhurnal, 4, 48–50. [in Ukrainian].
Svintsitskyi, A. S., Kozak, N. P., & Antonenko, A. V. (2011). Adaptatsiia slyzovoi obolonky shlunka do dii nesteroidnykh protyzapalnykh preparativ [Adaptation of gastric mucosa to nonsteroidal anti-inflammatory drugs]. Ukrainskyi revmatolohichnyi zhurnal, 46(4), 1–3 [in Ukrainian].
Austin, S. C., Sanchez-Ramos, L., & Adair, C. D. (2010) Labor induction with intravaginal misoprostol compared with the dinoprostone vaginal insert: a systematic review and metaanalysis. Am J Obstet Gynecol, 202, 624.e1-9. doi: 10.1016/j.ajog.2010.03.014.
Brenneis, C., Coste, O., Altenrath, K., Angioni, C., Schmidt, H., Schuh, C. D., et al. (2011) Anti-inflammatory role of microsomal prostaglandin E synthase-1 in a model of neuroinflammation. J Biol Chem, 286(3), 2331–42. doi: 10.1074/jbc.M110.157362.
Brock, J. S., Hamberg, M., Balagunaseelan, N., Goodman, M., Morgenstern, R., Strandback, E., et al. (2016) A dynamic Asp-Arg interaction is essential for catalysis in microsomal prostaglandin E2 synthase. Proc Natl Acad Sci,113(4), 972–977. doi: 10.1073/pnas.1522891113.
Diakowska, D., Markocka-Mączka, K., Nienartowicz, M., Lewandowski, A., & Grabowski, K. (2014) Increased level of serum prostaglandin-2 in early stage of esophageal squamous cell carcinoma. Arch Med Sci., 10(5), 956–961. doi: 10.5114/aoms.2013.34985.
Facchinetti, F., Fontanesi, F., & Del Giovane, C. (2012) Pre-induction of labour: comparing dinoprostone vaginal insert to repeated prostaglandin administration: a systematic review and meta-analysis. J Matern Fetal Neonatal Med., 25, 1965–9. doi: 10.3109/14767058.2012.668584.
Hui, Y., Ricciotti, E., Crichton, I., Yu, Z., Wang, D., Stubbe, J., et al. (2010) Targeted deletions of cyclooxygenase-2 and atherogenesis in mice. Circulation, 121, 2654–2660. doi: 10.1161/CIRCULATIONAHA.109.910687.
Johansson, J. U., Woodling, N. S., Wang, Q., Panchal, M., Liang, X., Trueba-Saiz, A., et al. (2015) Prostaglandin signaling suppresses beneficial microglial function in Alzheimer’s disease models. J Clin Invest., 125(1), 350–364. doi: 10.1172/JCI77487.
Legler, D. F., Bruckne, M., Uetz-von Allmen, E., & Krause, P. (2010) Prostaglandin E2 at new glance: Novel insights in functional diversity offer therapeutic chances. Int J Biochem Cell Biol., 42, 198–201. doi: 10.1016/j.biocel.2009.09.015.
Rania, N., Ramzi, H., & Hébert, R. L. (2014) Chronic kidney disease: targeting prostaglandin E2 receptors. Am J Physiol Renal Physiol, 307, 243–250. doi: 10.1152/ajprenal.00224.2014.
Regner, K. R. (2012) Dual Role of Microsomal Prostaglandin E Synthase 1 in Chronic Kidney Disease. Hypertension, 59(1), 12–14. doi: 10.1161/HYPERTENSIONAHA.111.180034.
Ricciotti, E., & FitzGerald, G. A. (2011) Prostaglandins and Inflammation. Arterioscler Thromb Vasc Biol., 31(5), 986–1000. doi: 10.1161/ATVBAHA.110.207449.
Rooney Thompson, M., Towers, C. V., Howard, B. C., Hennessy, M. D., Wolfe, L., & Heitzman, C. (2015) The use of prostaglandin E1 in peripartum patients with asthma. Am J Obstet Gynecol, 212, 392.e1-3. doi: 10.1016/j.ajog.2014.11.042.
Samuelsson, B., Morgenstern, R., & Jakobsson, P. J. (2007) Membrane prostaglandin E synthase-1: a novel therapeutic target. Pharmacol Rev., 59, 207–24. doi: 10.1124/pr.59.3.1.
Satoh, H., Amagase, K., Ebara, S., Akiba, Y., & Takeuchi, K. (2013) Cyclooxygenase (COX)-1 and COX-2 both play an important role in the protection of the duodenal mucosa in cats. J. Pharmacol. Ther., 344(1), 189–195. doi: 10.1124/jpet.112.199182.
Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
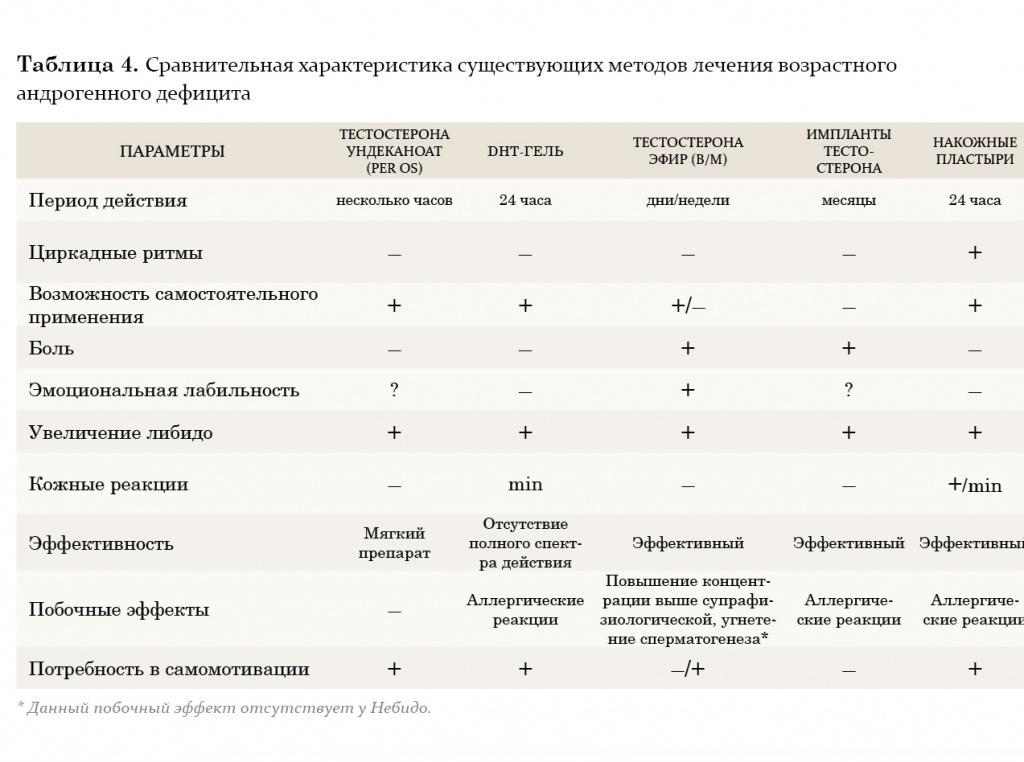
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
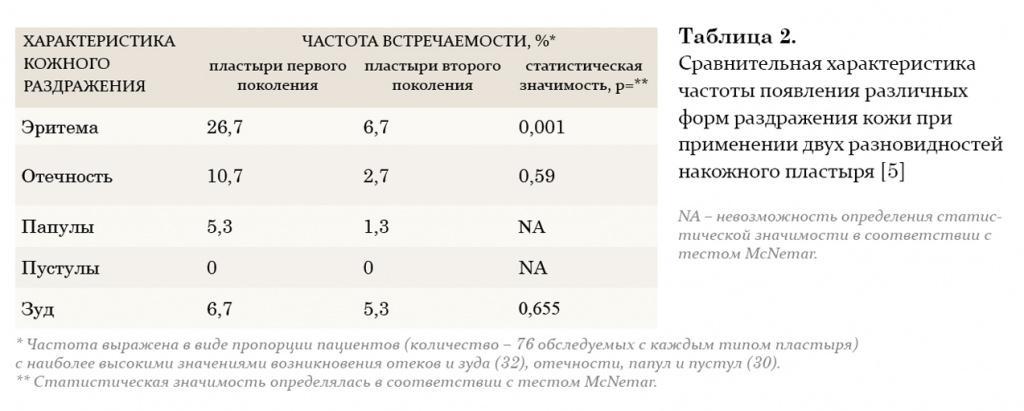
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
«Эрекция по заказу»
Что такое интракавернозная фармакотерапия (ИКФ) эректильной дисфункции (ЭД)?
ИКФ или «эрекция по заказу» — это метод лечения эректильной дисфункции, заключающийся во введении с помощью инъекции (укола) в пещеристые тела полового члена сосудорасширяющего вещества, значительно усиливающего приток крови к половому члену и вызывающего полноценную эрекцию. Главное в этом методе лечения то, что он позволяет мужчине, страдающему ЭД, иметь полноценную эрекцию в нужное время и дает возможность регулировать ее длительность. При этом эрекция возникает независимо от степени сексуальной привлекательности половой партнерши. Этим ИКФ выгодно отличается от других существующих сегодня медикаментозных методов лечения ЭД.
Кому показана ИКФ и кому она противопоказана?
ИКФ рекомендуется мужчинам, страдающим ЭД или мужской импотенцией. В особенности она показана тогда, когда прием таблетированных препаратов для лечения ЭД не дает должного эффекта. ИКФ с успехом применяется, если ЭД была вызвана сахарным диабетом, заболеваниями и травмами головного и спинного мозга, начальными стадиями заболеваний сосудов полового члена и пещеристых тел. ИКФ не рекомендуется пациентам перенесшим кавернит (воспаление пещеристых тел) или имеющим кавернозный фиброз, страдающим болезнью Пейрони и некоторыми врожденными аномалиями полового члена. В любом случае для определения показаний и противопоказаний к ИКФ необходимо обследование у врача уролога или андролога.
Какие препараты применяются для ИКФ?
ИКФ осуществляется с помощью сосудорасширяющих препаратов, значительно усиливающих приток крови в то место, куда они вводятся. Ранее для ИКФ применялся папаверин. Однако в последние годы наиболее эффективным и безопасным считается альпростадил или простагландин Е1. Одним из лучших препаратов альпростадила доступным в нашей стране является Каверджект (производство шведско-американской компании Фармация). Каверджект подтвердил свою эффективность и безопасность в многочисленных международных клинических испытаниях. В общеевропейских клинических испытаниях Каверджекта у больных сахарным диабетом участвовала и клиника «Андрос». В настоящее время для ИКФ применяются также смеси препаратов простагландина Е1, папаверина и фентоламина (бимикс, тримикс).
Насколько эффективна ИКФ? Существует ли курс лечения ИКФ, с помощью которого можно излечиться от ЭД?
ИКФ препаратом Каверджект эффективна в 72 — 80% случаев. Более 60% пациентов, применяющих Каверджект, и большинство их половых партнерш полностью удовлетворены качеством вызываемой Каверджектом эрекции. Вопреки рекламным обещаниям некоторых «специалистов», что «10 уколов избавят Вас от импотенции на 98%», ИКФ полностью не излечивает от ЭД. Инъекции необходимо делать перед каждым половым актом. Исключение составляют лишь пациенты с психогенной ЭД, которым чудодейственный укол помогает преодолеть страх сексуальной неудачи.
Как мне начать пользоваться ИКФ? Как часто можно вызывать «эрекцию по заказу»?
Для этого необходимо пройти тщательное врачебное обследование и с помощью специалиста подобрать индивидуальную дозу препарата. Затем врач научит Вас делать самому себе укол в половой член. Это кстати совершенно безболезненно. Однако если Вы не можете сами себя уколоть, на помощь придет автоматический самоинъектор. «Эрекцию по заказу» с помощью укола Каверджекта и его аналогов можно вызывать не более 3-х раз в неделю и не более 1 раза в день.
Есть ли привыкание к ИКФ, и какие бывает осложнения ИКФ?
Никакого привыкания препараты для ИКФ, в том числе и Каверджект не вызывают. Они, напротив, особенно у молодых людей при регулярном применении более 1 года способны вызвать улучшение качества собственных эрекций. У тех, кто выполняет инъекции слишком часто (см. предыдущий вопрос), а также у больных тяжелыми формами сахарного диабета возможно развитие рубцов в половом члене (фиброз). Некоторые пациенты (не более 15%) отмечают боли в половом члене после инъекции. В целом же ИКФ безопасна и необременительна.
Если у Вас остались вопросы, Вы можете получить консультацию ведущих специалистов клиники Андрос.
УРОЛОГИЯ В ОМСКЕ
ТЕЛЕФОН «ГОРЯЧЕЙ ЛИНИИ» +79095377482
ОПЕРАТИВНАЯ И КОНСЕРВАТИВНАЯ ПОМОЩЬ НА БЕРЕЗОВОЙ
Уровень тестостерона у мужчин. Гормональная регуляция предстательной железы.
Современные представления о биохимии и физиологии предстательной железы потверждают концепцию ее сложной нейроэндокринной регуляции, включающей влияние внутриклеточных гормонов (цАМФ, простагландины), действие стероидных половых гормонов яичек и коры надпочечников, гормонов аденогипофиза (гонадотропинов и пролактина), синтез и выделение которых находится под контролирующим влиянием гипоталамуса (рис. 1). Эти сведения имеют не только важное значение для понимания патогенеза дисгормональных опухолей предстательной железы (рака и аденомы), но и являются предпосылкой к развитию фундаментальных клинических исследований, используемых для диагностики и контроля за лечением этих заболеваний.
Андрогены. Уровень тестостерона у мужчин.
Им принадлежит важная роль в развитии и функции предстательной железы. В работах последних лет подчеркивается значение андроген-эстрогенного взаимодействия в осуществлении влияния на клеточные структуры предстательной железы (строму и эпителий). Основным андрогеном в мужском организме является тестостерон, который продуцируется в яичках и коре надпочечников. При физиологических условиях клетки Лейдига служат главным источником тестикулярных андрогенов. Морфологическое развитие клеток Лейдига и их гормональная активность регулируются Л Г. Андрогены по своему биологическому действию относятся к гормональным веществам, оказывающим влияние на так называемые органы-мишени, в которых происходит их избирательное накопление и где они осуществляют присущее им влияние. Они свободно проникают через клеточную мембрану в цитоплазму, где происходит связь андрогенов с высокомолекулярными белковыми рецепторами, специфическими для каждого гормона. Рецепторы андрогенов обнаружены в клетках семенных канальцев и придатках яичка, семенных пузырьках, предстательной железе, гипоталамусе. В мужском организме наиболее активным андрогеном является тестостерон, 95 % продукции которого тестикулярного происхождения. Другие естественные андрогены (андростендион, андростерон) обладают в 6—10 раз меньшей активностью, а дегидроэпиандростерон и эпитестостерон — в 25 — 30 раз менее активны, чем тестостерон. Основная физиологическая роль андрогенов в мужском организме в репродуктивном периоде состоит в стимуляции определенных этапов сперматогенеза и развитии вторичных половых признаков. Под влиянием тестостерона в периоде полового созревания происходит развитие предстательной железы и семенных пузырьков.
По химическому строению половые стероидные гормоны являются производными циклического углеводорода циклопентанпергидрофенантрена (стерана), состоящего из трех шестичленных и одного пятичленного кольца, которые носят название колец А, В, С и D. Главным источником андрогенов является холестерин, который образуется из ацетата. Эта реакция протекает как в яичках, так и в коре надпочечников; в процессе биосинтеза андрогенов может быть использован холестерин, приносимый на предстательную железу.
ЦНС
Рис. 1. Гормональная регуляция предстательной железы (по Griffiths, 1975).
Эстрогены.
Концентрация плазматических эстрогенов у мужчин более низкая, чем тестостерона. В настоящее время установлено, что 75 — 90% плазматических эстрогенов у молодых здоровых мужчин являются продуктами периферического метаболизма андростендиона и тестостерона в эстрон и эстрадиол. Из общего количества суточной продукции тестостерона (7 мг) непосредственное превращение в эстрадиол составляет 24 мкг/сут (0,35%), а из тотальной суточной продукции андростендиона (2,5 мг) превращение в эстрон соответствует 42 мкг/сут (1,7%). Несмотря на относительно небольшую степень метаболизма тестостерона в эстрадиол и андростендиона в эстрон, основная часть плазматических эстрогенов происходит в результате периферической ароматизации тестостерона и андростендиона. Значительная часть эстрогенов аккумулируется в жировой ткани. Суточная продукция эстрадиола у мужчин составляет 40 мкг. Помимо периферического синтеза эстрогенов из тестостерона и андростендиона, источником секреции эстрогенов в мужском организме являются яички. Это подтверждается признаками феминизации мужчин при опухолях клеток Сертоли, что указывает на их участие в синтезе эстрогенов. Взаимодействие двух гормонопродуцирующих клеток яичка — Лейдига и Сертоли — обеспечивает синтез эстрогенов, поскольку клетки Сертоли в противоположность клеткам Лейдига не утилизируют прегненолон как субстрат для ароматизации эстрогенов. В интерстициальных клетках яичка под влиянием Л Г происходит синтез тестостерона, который транспортируется к клеткам Сертоли. Это подтверждается высокой концентрацией тестостерона в тестикулярной лимфе, достигающей таких же уровней, как HBV. spermaticae, что создает благоприятные условия для проникновения тестостерона и других стероидов в канальцы яичка. Таким образом, в клетках Сертоли происходит достаточное накопление субстанций, необходимых для стероидогенеза и метаболизма тестостерона в эстрадиол-17р. Как показали наши исследования, у здоровых мужчин пожилого возраста и больных аденомой предстательной железы происходит усиление секреции эстрогенов и, параллельно с этим, морфофункциональные изменения в клетках Сертоли, гистохимическая характеристика которых отражала их повышенную секреторную активность, повышенное содержание суданофильных липидов, кетостерои- дов. Этот процесс осуществляется под контролем ФСГ, по отношению к которому клетки Сертоли являются мишенями, что подтверждается присутствием специфических ФСГ-рецепторов на мембранах клеток Сертоли. Предполагается, что ФСГ регулирует синтез спектра стероидов, находящихся в канальцах, и путем изменения концентрации андрогенсвязывающих протеинов оказывает влияние на превращение тестостерона в эстрадиол. В связи с этим возникла концепция единой тестостерон-эстрогенной секреторной системы яичек, морфофункциональной основой которой являются оба типа гормонпродуцирующих клеток яичка.
Связывание половых стероидных гормонов с плазматическими протеинами. Стероидные половые гормоны всех классов транспортируются плазмой крови в виде комплексов в связанной с белками форме. Существуют два вида связей стероидных гормонов с белками крови — связь с неспецифическими белками (альбумином), имеющими низкую константу ассоциации с белком и высокую связывающую емкость, и комплексы гормонов с бел-
ками, специфически связывающими только определенные стероидные гормоны. Они имеют высокую константу ассоциации и ограниченную связывающую емкость, насыщаемую в пределах физиологической концентрации гормонов. К ним относится а-глобулин, который способен связывать только кортикостерон и прогестерон. Транспорт андрогенов и эстрогенов осуществляется путем их ассоциации со специфическим глобулином, связывающим с высоким сродством половые стероиды. Альбумин также обладает свойством связывания стероидов, но степень сродства этого протеина к стероидному гормону низкая, в связи с чем комплексы половые гормоны — альбумин имеют небольшое физиологическое значение. В настоящее время является совершенно очевидным, что свободные, не связанные с белками половые гормоны отражают биологически активные компоненты, в связи с чем при оценке гормонального состояния в организме человека необходимо учитывать соотношение свободных и связанных форм. Так, лишь 2 % тотального тестостерона в плазме крови взрослого мужчины остаются в свободной форме, а остальные 98 % образуют связь со специфическим (3-глобулином, который является основным циркулирующим эстрофильным и андро- фильным протеином, хотя и отмечается более низкая способность эстрогенов по отношению к андрогенам образовывать комплексы с глобулином — ТСГ, ЭСГ. Величины свободного эстрадиола и тестостерона в плазме крови у мужчин почти одинаковы (1,79 и 1,71 %). Ассоциация тестостерона с белками плазмы предотвращает избыточную андрогенизацию организма и предохраняет гормон от преждевременного разрушения в результате катаболических процессов в печени и других органах. Специфический белок — ТСГ — имеет важное биологическое значение, поскольку его концентрация в плазме регулирует поступление тестостерона и его активных метаболитов в андрогенчувствительные клетки-мишени. Однако, несмотря на высокое сродство ТСГ к ДГТ, он не обладает способностью осуществить такую жизненно важную функцию, присущую андроген-рецепторным белкам, как перенос активного метаболита в хроматин [Mainwaring W., 1981].
Возрастные изменения секреции половых гормонов.
Несмотря на то, что концентрация в плазме тотального тестостерона в организме мужчины сохраняется на относительно постоянном уровне в возрастном периоде 20— 60 лет, это не является результатом продолжающейся андрогенпродуци- рующей активности яичек, а объясняется снижением метаболического клиренса тестостерона, изменением соотношения свободной и связанной с глобулином фракций тестостерона. Наиболее признанным является факт, что после достижения периода половозрелое™ уровни тотального тестостерона в плазме крови достигают плато с колебанием индивидуальных величин в пределах 2,8—10 мкг/л при продукции гормона 4—10 мг/сут [Vermeulen A. et al., 1981]. После 60 лет происходит постепенное снижение уровней плазматического тестостерона, и к 80 годам жизни средние величины концентрации тотального тестостерона составляют 2,5 мкг/л со значительной вариабельностью величин — от 0,5 до 6 мкг/л. Снижение уровней тотального тестостерона у мужчин в возрасте 60 лет в значительной степени отражает ослабление биосинтеза гормона в клетках Лейдига. Предположение об основной причине снижения числа клеток Лейдига при старении, обусловленной лишь артериосклеротическими изменениями в кровеносных сосудах яичек, недостаточно обоснованно. Общее число клеток Лейдига является относительно постоянной величиной у мужчин молодого и старшего возраста [Портной А. С., 1970]. Однако при этом происходят изменения в соотношении малых, средних и больших клеток Лейдига в сторону уменьшения больших и нарастания малых форм инволюционирующего типа со сниженным содержанием в них суданофильных липидов, ядрышковой РНК, т. е. того резервного материала, который необходим для синтеза стероидов. Важное значение в нарушении биосинтеза тестостерона имеют ферментные сдвиги в метаболизме его предшественников в связи с возрастным ослаблением их секреции в яичках и коре надпочечников. У мужчин пожилого и старого возраста отмечается значительное снижение в плазме крови предшественников тестостерона: прегненолона — на 60 %, дегидро- эпиандростерона — на 60 %, 17а-гидроксипрогестерона — на 47 %, андростен- диона — на 39%, андростендиола — на 53,8% [Pirke К. et al., 1980]. Эти данные свидетельствуют о том, что с возрастом происходит нарушение на всем пути метаболического синтеза тестостерона как в яичках, так и в коре надпочечников.
Концентрация тотального плазматического тестостерона не является надежным показателем биологически активного андрогена в плазме крови. В мужском организме с возрастом отмечается тенденция к нарастанию концентрации связанного с глобулином тестостерона, что определяет снижение средних величин свободной фракции тестостерона на 50%. Снижение в плазме крови уровней свободной фракции тестостерона в процессе старения взаимосвязано с нарастанием ТСГ, что, наряду с ослаблением скорости метаболического клиренса тестостерона, создает предпосылки для уменьшения снабжения гормоном органа-мишени — предстательной железы. В предстательной железе происходит метаболизм лишь свободной фракции тестостерона, в то время как тестостерон, связанный с глобулином, не обладает специфической транспортной функцией, обеспечивающей поступление гормона в ткань-мишень. Таким образом, при старении мужского организма происходят снижение уровней свободного тестостерона в плазме крови, нарастание способности связывания тестостерона глобулинами и снижение скорости метаболического клиренса тестостерона.
Если в процессе старения мужского организма уровни тотального плазматического тестостерона остаются относительно постоянной величиной, то концентрация эстрогенов в плазме крови нарастает, что объясняется более интенсивным превращением андростендиона в эстрон и возможным усилением продукции эстрогенов клетками Сертоли, что подтверждается накоплением в них липидов [Портной А. С., 1979]. В противоположность возрастному снижению свободного тестостерона отмечается повышение концентрации плазматических комплексов эстрадиол — глобулин при отсутствии изменений в содержании свободных эстрогенов. Таким образом, в процессе старения в мужском организме происходит сдвиг в балансе тестостерон/эстрадиол в сторону увеличения продукции эстрадиола. Эстрадиол по сравнению с тестостероном обладает меньшей способностью связывания с (3-глобулином,»-в результате чего снижение свободной фракции эстрогена в плазме крови у мужчин пожилого возраста происходит лишь на 7%. Взаимосвязь между концентрацией в плазме крови свободных и связанных с белком форм половых гормонов (андрогенов и эстрогенов) определяет биохимические процессы, лежащие в основе транспорта стероида в клетку-мишень. Хотя наиболее вероятной является простая диффузия свободных фракций тестостерона или эстрадиола в предстательную железу, но не исключается также возможность взаимодействия связанных с глобулином половых гормонов с плазматической мембраной, играющей определенную роль в проникновении гормонов в простатическую клетку. Нарастание в процессе старения связанных форм половых гормонов является проявлением защитно-приспособительного механизма, направленного на «сохранение» свободного тестостерона для его действия на андрогенчувствительный орган-мишень — предстательную железу, в которой с возрастом происходит снижение метаболизма тестостерона. Альтернативной гипотезой является
ограничение биологической активности тестостерона в его влиянии на предстательную железу на фоне нарастания периферического превращения тестостерона в эстрадиол и повышения в плазме крови комплексов половые гормоны — глобулин.
Стероидный метаболизм в предстательной железе.
Действие тестостерона на предстательную железу связано с его трансформацией в метаболиты 5ос-групп (5а-дигидротестостерон, 5а-андростан-За, 17(3-диол и 5а-андро- стан-Зр, 17р-диол-диолы). Наиболее выраженным биологическим действием на предстательную железу обладает ДГТ, который оказывает значительное влияние на развитие и дифференциацию этой железы и осуществляет функцию андрогенного стимула на клеточном уровне органа-мишени. ДГТ в мужском организме, в основном, является продуктом периферической трансформации тестостерона в предстательной железе, и лишь 20% непосредственно продуцируется яичками. Наряду с 5а-ДГТ диолы также обладают значительным потенциалом активности. Под влиянием диолов происходит стимуляция клеточного деления и индуцируются эпителиальная гиперплазия и секреторная активность в эксплантатах тканевой культуры предстательной железы. Концентрация диолов в плазме крови может явиться показателем активности метаболизма тестостерона в предстательной железе. За-диолы оказывают влияние на внутриклеточные процессы, связанные со стимуляцией ДНК-полимеразы, ДНК-зависимой РНК-полимеразы и синтеза РНК в простатической клетке. Предполагается, что За-диолы обладают способностью торможения секреции ФСГ и ЛГ. При инкубировании гомогенатов срезов АПЖ в среде, содержащей диолы, происходит значительное нарастание концентрации 5а-ДГТ в исследуемой ткани. Это свидетельствует о биотрансформации диолов, которые в конечном счете оказываются метаболи- зированными в 5а-ДГТ.
Таким образом, тестостерон и его метаболиты активно участвуют в контролировании роста и функции предстательной железы. Регуляторный механизм внутриклеточных процессов в простате обеспечивается взаимодействием 5а-ДГТ, За- и Зр-диолов, нарушение которого может явиться одним из факторов в развитии гиперпластических и метапластических процессов в предстательной железе. Предстательная железа весьма чувствительна к гормональным сдвигам, происходящим в процессе жизнедеятельности мужского организма. В процессе старения в предстательной железе происходит ослабление гормонального метаболизма и активности ферментов (снижение активности 5а-редуктазы, 17|3-гидроксистероидцегидрогеназы, фосфофруктокиназы и др.), что отражает возрастные сдвиги андрогенной чувствительности предстательной железы.
Циклические нуклеотиды и простагландины в гормональной регуляции предстательной железы.
Исследования последних лет значительно расширили знания о клеточно-молекулярных основах влияния половых гормонов на предстательную железу, включающих роль стероидно-рецепторных комплексов, циклических нуклеотидов и простагландинов в механизме регуляции действия половых гормонов на клеточном уровне предстательной железы и обеспечения энергетического обмена в простатической клетке. Образующийся в результате метаболизма тестостерона в простатической клетке ДГТ является сильным митозогенным гормоном, что подтверждается его стимулирующим влиянием на генетический аппарат клетки. Биологический эффект ДГТ проявляется повышением транскрипции специфических структуральных генов с появлением новых носителей рибонуклеиновой кислоты (тРНК) и, в конечном счете, синтезом протеинов в цитоплазме клетки. Определенную роль в реализации андрогензависимой реакции предстательной железы играют циклические нуклеотиды и простагландины.
Специфические белки клетки — нуклеотиды, оперирующие внутри клетки (цАМФ и цГМФ), имеют важное биологическое значение как внутриклеточные медиаторы в механизме влияния половых гормонов на предстательную железу. Стимуляция цАМФ под влиянием гормонов тесно связана с повышением активности аденилциклазы — фермента, локализующегося в плазматических мембранах всех клеток организма млекопитающих, за исключением эритроцитов. Биологическая ценность цАМФ первоначально определена на основании его участия в процессе гликогенолиза в печени, и затем показана ключевая роль циклического нуклеотида в регуляции ряда важных клеточных реакций, связанных с влиянием гормонов на ткань-мишень. Способность экзогенного цАМФ регулировать и поддерживать некоторые стероидозависимые реакции в ткани добавочных репродуктивных желез мужского организма дает основание предполагать существование двухсигнальной системы гормонального действия. Первым носителем сигнала к клетке-мишени — простатической ткани — является непосредственно гормон, который, будучи транспортированным в клетку, стимулирует образование в ней внутриклеточного вторичного сигнала путем изменения уровней цАМФ. В последующем вторичный сигнал реализует окончательный эффект гормона и «приказывает» эффекторной клетке осуществить необходимую в возникшей ситуации функцию. В настоящее время цАМФ является единственно признанным вторичным передатчиком гормонального стимула к клетке и предполагается, что гормональные рецепторы функционально связаны с системой аденилциклаза — цАМФ, которая действует как дискриминатор и генератор полученных первичных сигналов. С помощью этого механизма первоначальные экстраклеточные сигналы, осуществляемые гормонами, трансформируются во вторичные стимулы, реализуемые внутри клетки по заданной программе, что обеспечивает клеточный гомеостаз. Регуляция уровней цАМФ осуществляется, помимо аденилциклазы, другим ферментом — фосфодиэстеразой, которая катализирует гидролиз цАМФ до неактивного соединения 5′-АМФ. Активность простатической аденилциклазы повышается под влиянием ряда гормонов (АКТГ, пролактин, глюкагон, эпинефрин, ДГТ), простагландинов, солей магния. Активность фосфоди- эстеразы угнетается АТФ, пирофосфатом, метилксантином (теофиллином). Катехоламины стимулируют аккумуляцию цАМФ в предстательной железе путем повышения активности аденилциклазы, не оказывая при этом влияния на уровень тканевой фосфодиэстеразы; цАМФ и аденилциклаза выявлены в предстательной железе и ее секрете, в семенных пузырьках, яичках. Биохимические реакции, протекающие в предстательной железе под влиянием половых гормонов, могут быть опосредованы активацией системы аденилциклаза — цАМФ. Это относится к синтезу ключевых ферментов, участвующих в карбонгидратном метаболизме. Так, после кастрации крыс- самцов в ткани предстательной железы отмечается значительное снижение активности ряда ферментов (гексокиназы, фосфофруктазы, пируват- киназы, глюкозо-6-фосфатазы, 6-фосфатглюконатдегидрогеназы, ос-глице- ролфосфатдегидрогеназы), что указывает на нарушение энергетического обмена клетки — процесса, который восстанавливается введением тестостерона. Эти наблюдения свидетельствуют о гормональной зависимости метаболических процессов в предстательной железе, протекающих под контролем регулирования синтеза нуклеотидов и активности гликолитичес- ких и гексозомонофосфат-шунт-ферментов, что обеспечивает клетку основным энергетическим субстратом.
Наряду с цАМФ простагландины осуществляют регуляцию гормонального действия на простатическую клетку-мишень. Биологически активные простагландины являются продуктами ферментативного превращения кар
бонненасыщенных карбоксильных кислот с циклопентановым кольцом. Они происходят из клеточных фосфолипидов, холестеролэстеров, плазматических триглицеридов или неэстерифицированных жирных кислот. U. Euler (1934) выделил из экстракта предстательной железы человека и семенной жидкости активный липидорастворимый компонент, который при внутривенном введении собакам вызывал повышение артериального давления. Этот субстрат назван простагландином. Однако этот термин является не совсем точным, так как большинство тканей млекопитающих, включая репродуктивную систему мужского организма, способны синтезировать несколько типов простагландинов. Из семенной жидкости человека выделены простаглан- дины ПГЕ и ИГР. В зависимости от числа двойных связей в каждом из этих классов простагландинов применяются обозначения ПГЕь ПГЕ2, ПГЕз и, соответственно, ПГР> и nrF2, а стереоизомеры этих субстратов обозначаются символами а и 3. Фармакологические свойства класса простагландинов определяются различным характером взаимодействия биологически активных компонентов в клетках репродуктивной системы, которыми являются простагландины и цАМФ. Простагландины типа Е являются более сильными модуляторами биосинтеза цАМФ, чем простагландины типа F. Простагландины типа Е повышают аккумуляцию цАМФ в различных тканях, включая предстательную железу, легкие, сердце, аорту, матку, кишечник.
Источником простагландинов в семенной жидкости является их секреция предстательной железой и семенными пузырьками. Одним из важных аспектов влияния простагландинов на репродуктивную систему в мужском организме является их активная роль в процессе эякуляции. Выраженный эффект простагландинов на гладкомышечные элементы мочевыводящих путей и их присутствие в секрете предстательной железы и семенных пузырьков дало основание полагать, что подвижность сперматозоидов и продвижение семенной жидкости находятся под контролем этих активных липидов. ПГЕ2 играют важную роль в реакциях мочевого пузыря и мочеиспускательного канала на симпатические стимулы. Основные функции простагландинов включают их способность модулировать процесс передачи нервного стимула между окончаниями вегетативных волокон и эффекторного органа. С точки зрения регуляции уродинамики нижних мочевых путей представляет интерес, что активация симпатической нервной системы или введение норадреналина сопровождаются выделением простагландинов типа Е2. Значительное освобождение ПГЕ2 происходит при растяжении мочевого пузыря. В то время как ПГЕ2 вызывает снижение величины уретрального сопротивления, nrF2 его повышает. Поскольку простагландины серии Е2, F2 оказывают влияние на гладкую мускулатуру, то, возможно, механизм их действия на уретральное сопротивление опосредован влиянием на сократительную способность детрузора благодаря непрерывности его мышечных волокон с гладкой мускулатурой мочеиспускательного канала. Как известно, вариабельность внутрипузырного давления и степень растяжения стенки мочевого пузыря оказывают рефлекторное влияние на уретральное сопротивление. При значительном растяжении мочевого пузыря происходят более активное раскрытие шейки и уменьшение уретрального сопротивления. Падение уретрального сопротивления при таких условиях не блокируется атропином и полностью блокируется индометацином — препаратом, угнетающим синтез простагландинов. Сравнение содержания простагландинов серии Е2 В моче, полученной из мочевого пузыря (при надлобковой пункции) и мочеиспускательного канала у больных АПЖ, показало более высокую концентрацию ПГЕ2 в порции мочи из последнего [Rolland Р. et al., 1981]. Предполагается, что повышенный синтез простагландинов серии Е2 является результатом стимуляции ткани предстательной железы пролактином. Таким образом, степень продукции простагландинов при аденоме предстательной железы, возможно, отражает чувствительность аденоматозной ткани к про- лактину. В свете изложенных данных можно заключить, что патогенез нарушения уродинамики нижних мочевых путей при АПЖ включает изменение реактивности нервных рецепторов в стенке мочевого пузыря и мочеиспускательного канала (преимущественно 3-рецепторов) по отношению к автономным стимулам, модулирующим активность гладкой мускулатуры, одним из которых являются простагландины. В модифицировании эффекта простагландинов на 3-адренорецепторы в гладкомышечных структурах мочевого пузыря и мочеиспускательного канала большое значение имеет взаимосвязь между пролактином, рецепторами пролактина в предстательной железе и ПГЕ2. ПГЕ2 способен образовывать связь с клеточными рецепторами, которые активируют аденилциклазу и повышают внутриклеточные уровни цАМФ, что является пусковым механизмом биохимических процессов, играющих роль в сохранении физиологического состояния простатической клетки [Kaneti J. et al., 1981]. Взаимосвязь синтеза и метаболизма ПГЕ^ с андрогенами подтвердилась выявлением рецепторных мест на клеточных мембранах ткани аденомы предстательной железы [Cavanaugh A., Farnsworth W., 1977]. С помощью радиоиммунологических исследований выявлены специфические рецепторы для простагландина F,K в предстательной железе, связывающие ЗН-ПГЕ^ с высокой степенью сродства. Под влиянием тестостерона отмечалось значительное нарастание сродства рецепторов к простагландинам. Такое же повышение синтеза nTF^ имеет место при введении пролактина. Предполагается, что пролактин и nrFjc, оккупируют одни и те же рецепторные места на мембранах, в которых происходит замещение пролактина простагландинами. Следовательно, эффект пролактина на синтез nrF^ опосредован тестостероном, чувствительность к которому значительно повышается в ткани предстательной железы под влиянием стимуляции пролактином. Результаты этих исследований имеют не только теоретическое значение, расширяя представление о гуморальных и гормональных факторах андрогенной чувствительности предстательной железы, но и важное практическое значение, указывая на целесообразность использования препаратов, тормозящих секрецию пролактина, в лечении РПЖ и АПЖ.
Гипоталамо-гипофизарный комплекс и гонады в регуляции деятельности предстательной железы.
Ведущее значение в осуществлении влияния стероидных половых гормонов на предстательную железу принадлежит гипоталамусу и аденогипофизу. Продукция основного андрогена в мужском организме — тестостерона — клетками Лейдига яичек контролируется секрецией ЛГ. В свою очередь, тестостерон участвует в регуляции секреции ЛГ посредством механизма отрицательной обратной связи. В настоящее время является общепризнанным, что отрицательная обратная связь между тестостероном и активностью ЛГ осуществляется на гипоталамическом уровне с участием ЛГ-РГ (рис. 2). Представляет значительный интерес, что эстрадиол- 17(3 тормозит образование ЛГ-РГ с последующим ослаблением секреции ЛГ и падением концентрации тестостерона в плазме крови. Это представляет один из механизмов действия эстрогенотерапии при РПЖ. Исследования последних лет свидетельствуют о том, что регуляция плазматического тестостерона осуществляется механизмом отрицательной обратной связи с участием ДГТ или эстрадиола на уровне гипоталамуса. Высокая степень 5а-редуктазной активности обнаружена в гипоталамусе, особенно в лате- рально-преоптическом, латерально-гипоталамическом и медиально-преопти- ческом ядрах. Специфические ДГТ-рецепторы выявлены в гипоталамусе и аденогипофизе. В ЦНС происходит не только метаболизм тестостерона
17/3—эстрадиол
Рис. 2. Первичный (сплошная стрелка) и вторичный (пунктирная стрелка) механизмы регуляции секреции тестостерона (по Mawhinney, 1979).
в ДГТ, но и ароматизация тестостерона в эстрадиол. После введения радиоактивного тестостерона половозрелым крысам-самцам в ядрах клеток лимбической области обнаружена значительная концентрация 3Н-эстрадиола [Lieberburg J. et al., 1975]. Влияние тестостерона на секрецию ЛГ осуществляется по принципу механизма отрицательной обратной связи на уровне гипоталамуса с участием непосредственного метаболита тестостерона — ДГТ и эстрадиола, которые тормозят секрецию ЛГ-РГ. Введение ЛГ-РГ молодым мужчинам сопровождается повышением в плазме крови концентрации тестостерона и андростендиона. С возрастом отмечается снижение реактивности ЛГ к стимулирующему влиянию ЛГ-РГ. У мужчин пожилого возраста в связи со сдвигом баланса половых гормонов в сторону эстрадиола происходит блокирование секреции ЛГ-РГ. Данные возрастной динамики
гонадотропной активности в мужском организме указывают, что до половой зрелости отмечаются низкие концентрации ЛГ и ФСГ в плазме крови, которые нарастают к периоду пубертатности, достигая при этом значений, несколько превышающих величины, наблюдаемые у взрослых мужчин. Наши исследования показали, что гонадотропная активность повышается у мужчин пожилого возраста. В то же время значительная вариабельность гонадотропной активности дает основание полагать существование двух популяций — с нормальными и высокими концентрациями гонадотропинов. В ряде случаев отмечается повышение уровней ФСГ без значительных изменений в величинах ЛГ, хотя наиболее типичной является высокая степень корреляции между содержанием ФСГ и ЛГ. В то же время в пожилом возрасте, несмотря на усиление гонадотропной активности, имеет место вариабельность в реагировании яичек к ЛГ, что не дает возможности установить корреляцию между плазматическим содержанием ЛГ и концентрацией тестостерона. Это объясняется рядом сложных метаболических процессов в синтезе и секреции половых гормонов, связанных со старением, изменяющих процесс взаимодействия между гипофизом и яичками. Гормональная регуляция клеток Лейдига является сложным процессом, в котором участвует ряд факторов. Популяции клеток Лейдига в яичках функционально не синхронизированы и отражают значительное внутриклеточное различие по отношению к стимуляции ЛГ. Нарастание стероидо- генеза в клетках Лейдига под влиянием ЛГ происходит до определенного предела, после чего наступает значительное снижение андрогенной секреции в связи с изменением в числе ЛГ-рецепторов на мембранах клеток Лейдига и уровней цАМФ, т. е. сдвигами процесса рецепторной активации гормонального синтеза.
Таким образом, когда клетка Лейдига достигает максимальной функциональной активности, включается автономный механизм сохранения клеточного гомеостаза, защищающий клетку от дальнейшей стимуляции ЛГ. При такой ситуации в определенной клеточной популяции сохраняется секреторная активность, тогда как в другой наступает фаза покоя. В сохранении максимальной секреторной активности клетки Лейдига значительная роль принадлежит пролактину, который проявляет свое влияние лишь в присутствии ЛГ. Десенсибилизация отдельных клеток Лейдига внутри активно секретирующей клеточной популяции может быть осуществлена локально внутриклеточными гормонами (андрогенами, эстрогенами), которые оказывают влияние на число ЛГ-рецепторов, цАМФ. Следовательно, цикличность андрогенной секреции в клетках Лейдига обеспечивается сложным механизмом, включающим влияние ЛГ, пролактина, взаимодействием этих гормонов с рецепторами на мембранах клетки, ферментной активностью 5а-редуктазы и цАМФ, а также влиянием на внутриклеточный гомеостаз андрогенов и эстрогенов. Ослабление функции клеток Лейдига у мужчин в процессе старения находит свое биохимическое выражение в снижении концентрации свободного тестостерона. В процессе старения в мужском организме повышается константа периферического превращения тестостерона и андростендиона в эстрадиол и эстрон, что происходит на фоне андрогенной недостаточности и повышения гонадотропной активности. Возможный механизм «старения» яичек включает атрофию герминативного эпителия, изменения в кровоснабжении органа, сдвиг в соотношении гормонально-активных и неактивных типов клеток Лейдига и Сертоли [Портной А. С., 1969]. Степень выраженности этих изменений значительно варьирует у мужчин пожилого возраста, что объясняется состоянием центрального регуляторного механизма периферической эндокринной железы — яичек. Существует точка зрения, что возрастные изменения у мужчин первично проявляются на уровне гонад. Однако более убедительной явля
ется концепция возрастного снижения чувствительности гипоталамуса к воздействию половых гормонов по принципу отрицательной обратной связи, что приводит к повышению секреции гормонов, ускоряющих процесс старения. Это подтверждается усилением гонадотропной активности у мужчин пожилого возраста.
Роль гонадотропинов в регуляции деятельности предстательной железы изучалась в ряде исследований [Портной А. С., 1965; Asano М., 1965; Giuliani L. et al., 1981]. В экспериментах на крысах-самцах удалось показать, что инволюционные изменения в предстательной железе оказались более выраженными после гипофизэктомии, чем после кастрации. После гипофизэктомии наблюдалась значительная атрофия железистого эпителия предстательной железы с истощением в нем активности ферментов. Введение гормона роста и АКТГ гипофизэктомированным и кастрированным крысам оказывало стимулирующее действие на предстательную железу, в то время как подобный эффект ЛГ и ФСГ не проявлялся. Значительное повышение массы и секреторной активности предстательной железы у гипо- физэктомированных и кастрированных крыс происходило при одновременном введении им АКТГ и пролактина [Портной А. С., 1973].
За последние годы внимание ученых концентрируется на различных аспектах действия пролактина, включающих регуляцию его синтеза и секреции аденогипофизом, взаимосвязь с гонадотропинами и стероидными гормонами, биохимические механизмы его влияния на органы-мишени и возможную роль в канцерогенезе ряда органов — предстательной железы, молочной железы и др. В организме мужчины пролактин секретируется аденогипофизом и может быть обнаружен в плазме периферической крови. Секреция пролактина контролируется пролактинтормозящим фактором, который выделяется гипоталамусом, и, как полагают в настоящее время, является допамином. Несмотря на значительную концентрацию пролактина в передней доле гипофиза, физиологическая роль этого гормона в мужском организме недостаточно изучена. В ряде исследований на грызунах продемонстрировано, что уровни циркулирующего в крови пролактина повышаются в период развития репродуктивной системы у самцов. В связи с этим представляют интерес наблюдения, что введение пролактина гипофизэктомированным мышам повышает не только концентрацию холестеррла в яичках, но и процент эстерифицированного холестерола — основного продукта синтеза тестостерона, происходящего под влиянием ЛГ. В яичках мышей при введении пролактина также наблюдается повышение активности Зр-гидроксистероиддегидрогеназы — фермента, участвующего в тестикулярном стероидогенезе. На основании многочисленных экспериментальных исследований к настоящему времени накопилась достаточно точная информация о физиологическом действии пролактина, вероятно, синергичном с ЛГ в регулировании тестикулярной активности. Длительное введение крысам бромкриптина — препарата, ингибирующего секрецию пролактина, дает в результате снижение уровней плазматического тестостерона и «компенсаторное» повышение в плазме ЛГ. В противоположность этому под влиянием стимуляции синтеза пролактина допаминергическим антагонистом сульпи- ридом наблюдается повышение продукции тестостерона.
Механизм действия пролактина на предстательную железу включает, с одной стороны, опосредованное влияние, связанное со стимуляцией биосинтеза андрогенов в яичках, а с другой — непосредственную регуляцию гормональных процессов в предстательной железе.
Косвенное влияние пролактина на предстательную железу связано с активацией тестикулярного стероидогенеза, дающего в результате стимуляцию предстательной железы андрогенами. В этом процессе значительная роль принадлежит синергизму пролактина и ЛГ в регуляции синтеза тестостерона. В ряде экспериментальных исследований показано, что пролактин повышает реактивность ткани вентральной доли предстательной железы половозрелой крысы-самца к ЛГ. Под влиянием введения пролактина и ЛГ отмечается значительное повышение массы и способности поглощения радиоактивного цинка (65Zn) дорсолатеральной долей предстательной железы крысы, что является важным индикатором происходящих в железе ферментативных процессов, связанных с метаболизмом андрогенов. В то же время введение одного пролактина не изменяет массу и секреторную активность предстательной железы гипофизэктомированных крыс. В связи с этими наблюдениями возникает альтернатива, является ли стимуляторньш эффект ЛГ и пролактина на предстательную железу результатом синергизма этих гормонов на тестикулярном уровне или же обусловлен взаимодействием пролактина и андрогенов, секреция которых нарастает под влиянием ЛГ.
Непосредственное действие пролактина на предстательную железу подтверждено в экспериментах с гипофизэктомированными и кастрированными крысами, у которых пролактин усиливал стимулирующий эффект экзогенных андрогенов на предстательную железу [Портной А. С., 1970]. Пролактин усиливает реактивность предстательной железы к андрогенам, и индикаторами этого процесса являются повышение массы и секреторной активности предстательной железы с нарастанием содержания в ней тестостерона, фруктозы и лимонной кислоты.
Под влиянием пролактина в ткани предстательной железы нарастает превращение тестостерона в 5а-ДГТ, а при введении бромкриптина происходит снижение поглощения радиоактивного тестостерона и его превращения в 5а-ДГТ. Значительную роль в этом процессе играет влияние пролактина на аденилциклазную активность, стимулирующую цАМФ — регулятор действия пролактина на клеточном уровне; повышение активности аденил- циклазы может быть использовано как показатель физиологической активности гормона, оказывающего прямое влияние на андрогенный метаболизм на клеточном уровне предстательной железы. Увеличение массы предстательной железы под влиянием пролактина ассоциируется с нарастанием уровней ДНК и РНК. В экспериментах на животных установлено, что пролактин не способен оказывать прямое влияние на синтез нуклеиновой кислоты, но он значительно усиливает стимулирующий эффект тестостерона на синтез ДНК в ткани предстательной железы. Результаты этих исследований дают основание полагать, что пролактин оказывает влияние на один из важных аспектов андрогенного действия на предстательную железу, обеспечивающего развитие и секреторную активность эпителия. Прямое вмешательство пролактина в действие андрогенов на клеточном уровне органа-мишени — предстательной железы — включает несколько механизмов. Пролактин оказывает влияние на процесс связывания андрогенов предстательной железой, который определяется содержанием ДГТ в простате. Это подтверждается обнаружением снижения связывания ДГТ ядерными рецепторами клеток предстательной железы гипофизэктомированных крыс. Внутриклеточный механизм действия пролактина связан с наличием специфического рецепторного протеина на мембранах клеток предстательной железы, связывающего этот гормон. Предполагается, что возникновение пролактин-рецепторного комплекса служит инициатором серии внутриклеточных процессов, в результате которых повышается концентрация цитоплазматического рецепторного протеина для связывания ДГТ и дальнейшей его транслокации в ядро. Следовательно, пролактин участвует в стимуляции образования ядерно-рецепторных комплексов с ДГТ, диссоциация которых с освобождением ДГТ реализует андрогенный эффект на клеточном уровне. Можно предположить, что пролактин повышает специфичность цитоплазматических рецепторных протеинов к ДГТ. В любой из рассмотренных ситуаций пролактин повышает транслокацию ДГТ в ядро клетки и этим усиливает андрогенный эффект в предстательной железе. Не исключается также возможность, что пролактин изменяет ход событий в аппарате ядер, связанных с действием андрогенов.
Гормоны передней доли гипофиза активно участвуют в развитии и функции предстательной железы. Среди питуитарных гормонов пролактину принадлежит важная роль в осуществлении эндокринной регуляции предстательной железы, одним из механизмов которого является пролактин-опосредованное усиление влияния тестостерона на предстательную железу. Кроме того, пролактин участвует в регуляции внутриклеточных процессов, связанных с действием андрогенов на клеточно-молекулярном уровне железы.



