Карбонат калия: способы получения и химические свойства
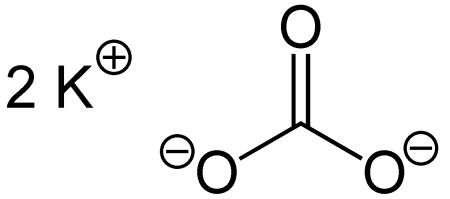
Карбонат калия K2CO3 — соль щелочного металла калия и угольной кислоты. Белое вещество, плавится без разложения, при дальнейшем нагревании разлагается. Очень хорошо растворяется в воде.
Относительная молекулярная масса Mr = 138,20; относительная плотность для тв. и ж. состояния d = 2,428; tпл = 891º C;
Способ получения
1. Карбонат калия можно получить путем взаимодействия при комнатной температуре пероксида калия и влажного углекислого газа. В результате реакции образуется карбонат калия и кислород:
2. В результате взаимодействия пероксида калия и угарного газа при 50º С образуется карбонат калия и кислород:
3. При взаимодействии концентрированного гидроксида калия и углекислого газа образуется карбонат калия и вода:
4. Взаимодействуя с углеродом (графитом) при 30º С надпероксид калия карбонат калия и углекислый газ:
5. Разлагаясь при температуре 100 — 400 ºС гидрокарбонат калия образует карбонат калия, углекислый газ и воду:
6. В результате реакции между гидрокарбонатом калия и гидроксидом калия образуется карбонат калия и вода:
Качественная реакция
Качественная реакция на карбонат калия — взаимодействие его с раствором сильных кислот. В результате реакции происходит бурное выделение углекислого газа, образование которого можно проверить, если пропустить его через известковую воду, которая мутнеет из-за образования осадка:
1. При взаимодействии с хлороводородной кислотой, карбонат калия образует хлорид калия, углекислый газ и воду:
2. Взаимодействуя с серной кислотой, карбонат калия образует углекислый газ и воду, а также сульфат калия:
Химические свойства
1. Карбонат калия может реагировать с простыми веществами :
С хлором, бромом и йодом концентрированный и горячий раствор карбоната калия реагирует с образованием хлорида, бромида или йодида калия, хлората, бромата или йодата калия и углекислого газа:
2. Карбонат калия вступает в реакцию со многими сложными веществами :
2.1. Насыщенный карбонат калия реагирует при 30–40º C с водой и углекислым газом, образуя осадок гидрокарбоната калия:
2.2. Карбонат калия может реагировать с насыщенным гидроксидом кальция с образованием гидроксида калия и осадка карбоната кальция:
2.3. Карбонат калия способен реагировать с кислотами :
2.3.1. При взаимодействии с разбавленной хлороводородной кислотой карбонат калия образует хлорид калия, углекислый газ и воду:
2.3.2. В результате реакции между насыщенным карбонатом калия и концентрированной и холодной хлорной кислотой образуется осадок хлорат калия, вода и газ углекислый газ:
2.3.3. Взаимодействуя с разбавленной фосфорной кислотой концентрированный раствор карбоната калия образует фосфат калия, воду и углекислый газ:
а если кислота концентрированная, то образуется гидрофторид калия, вода и углекислый газ:
Карбонат калия
| Карбонат калия | |
|---|---|
 | |
 | |
| Систематическое наименование | Карбонат калия |
| Традиционные названия | поташ |
| Хим. формула | CK₂O₃ |
| Состояние | кристаллическое |
| Молярная масса | 138,205 г/моль |
| Плотность | 2,44 г/см³ |
| Т. плав. | 891 °C |
| Растворимость в воде | 110,5 г/100мл (20 °C) |
| ГОСТ | ГОСТ 4221-76 ГОСТ 10690-73 |
| Рег. номер CAS | 584-08-7 |
| PubChem | 11430 |
| Рег. номер EINECS | 209-529-3 |
| SMILES | |
| Кодекс Алиментариус | E501(i) |
| RTECS | TS7750000 |
| ChEBI | 131526 |
| ChemSpider | 10949 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Карбонат калия, углекислый калий, арх. поташ K2CO3 — средняя соль калия и угольной кислоты. Это белое кристаллическое вещество, хорошо растворимое в воде. Малотоксичен, относится к III классу опасности.
Содержание
История
Поташ — одна из солей, известных людям ещё в древности. Обычно поташ загрязнён различными примесями, поэтому не имеет такого чисто-белого цвета, как измельчённый карбонат калия. До XX века в Европе поташ был одним из важнейших промышленных химических реагентов. Его получали путём водной экстракции из растительной золы, с дальнейшей очисткой до необходимого уровня. Производство было сосредоточено в местах, богатых лесом — кое-где в Европе, но, в основном, в России и Северной Америке, — то есть именно там, где за несколько тысяч лет до н. э. находились языки отходящих в сторону северного полюса вместе с глобальным потеплением ледников (как правило, в тех местностях, где вода предельно жёсткая).
На производство поташа ещё Петр I в 1721 году установил монополию: «Нигде никому отнюдь поташа не делать и никому не продавать под страхом ссылки в вечную каторжную работу». С целью сбережения леса, поскольку вводил технологию производства поташа из «худых бочек, сучьев и прочих обрезков» то есть вторичная переработка.
Физические и химические свойства
Образует несколько различных гидратов с 5, 1,5 и 0,5 молекулами воды, гидрат с 1,5·H2O образуется при кристаллизации из водных растворов и хранении безводной формы на воздухе. Все перечисленные гидраты полностью обезвоживаются при 150—160 °C.
Водные растворы карбоната калия присоединяют углекислый газ с образованием гидрокарбоната калия. С двуокисью серы водные растворы реагируют с образованием гидросульфита калия и двуокиси углерода.
Получение
Карбонат калия получают:
Для использования в качестве удобрения, поташ получают из щёлока при выщелачивании водой золы из злаков или водорослей, так как именно карбоната калия больше всего в растворимой части растительных остатков (белая «зола» от костра — в основном поташ). Принцип добычи: в глиняный обожжённый сосуд с небольшим отверстием на дне насыпали золу и слегка утрамбовывали. Потом его заливали определённым количеством воды. Воду, прошедшую через сосуд, тщательно собирали и ею заливали следующую партию. И так до тех пор, пока жидкость не приобретала сиропообразную консистенцию. После лишнюю жидкость выпаривали в металлической посуде и получали поташ.
Применение
Карбонат калия применяют:
Что такое поташ и где его применяют
Содержание статьи
Физические и химические свойства поташа
Поташ представляет собой одну из средних солей неустойчивой угольной кислоты. Очищенный поташ выглядит как мелкокристаллический порошок белого цвета без запаха с щелочным вкусом. В неочищенном виде он имеет несколько красноватый оттенок из-за наличия примесей. Отлично растворяется в воде, не способен растворяться в этаноле. Водный раствор поташа обладает ярко выраженным бактерицидным действием, причем чем выше его температура, тем сильнее противомикробное действие. Температура плавления карбоната калия составляет 891 градус.
Водные растворы поташа различных концентраций способны обезвоживаться при температуре около 160 градусов. Получаются бесцветные кристаллы моноклинной сингонии. Водный раствор может реагировать с двуокисью углерода и серы, образуя гидрокарбонаты и гидросульфаты соответственно.
Получение поташа
История способа получения поташа уходит корнями в глубокую древность. Этот способ заключался в следующем: древесную золу пересыпали в посуду и добавляли горячей воды. Золу получали из деревьев, богатых калием. Затем разжигали костер и выливали полученную смесь на него. Костер не должен погаснуть, тогда под дровами будет осаждаться поташ. Он будет иметь красноватый оттенок из-за небольшого количества примесей.
Сегодня поташ получают при электролитическом взаимодействии карбоната магния в виде суспензии с раствором хлорида калия. Есть и другой способ. Для его осуществления нужно карбонизировать раствор гидроксида калия в электролитической ванне.
Применение поташа
Благодаря его щелочным свойствам, древние римляне использовали поташ для стирки одежды. При реакции с водой он образует щелочную среду, способную растворять жиры и выводить пятна. Сегодня применение карбоната калия гораздо шире.
Его используют в качестве пищевой добавки. Она носит название E501 и применяется как стабилизатор. Она помогает смешивать несмешивающиеся в природе вещества (вода и масло). Также E501 используется как регулятор кислотности. Она поддерживает в продукте определенное значение pH, водородного показателя. Учеными был доказан вред этой добавки для человека. Поташ провоцирует аллергические реакции и особенно опасен для больных астмой.
Щелочная природа поташа позволяет применять его в мыловаренной промышленности, а также для дезинфекции. Его добавляют в лекарства от экземы и других кожных болезней для многократного усиления эффекта. Этим порошком обрабатывают животноводческие фермы и конюшни.
Поташ
| Точность | Выборочно проверено |
Пота́ш, карбона́т ка́лия или углеки́слый калий (химическая формула K2CO3 — средняя соль калия и угольной кислоты, калийный аналог пищевой соды. Чистый карбонат калия выглядит как белый кристаллический порошок, хорошо растворимый в воде. Поташ малотоксичен, относится к III классу опасности химических соединений.
Содержание
Поташ в научной и научно-популярной литературе [ править ]
Много есть и других опытов, которыми то же подтверждается, напр, в воде распущенная сулема ни прозрачности, ни цвету оныя не переменяет. Но как только распущенный на влажном воздухе поташ влит будет, вода, прозрачность потеряв, померанцовый цвет на себя примет. Потом, как прильешь кислую материю, то есть купоросную или селитряную крепкую водку, цвет потеряется и прозрачность возвратится и на дне ничего подонков не сядет. Таким же образом опыты происходят, ежели другие соляные тела в воде распущены будут, разве только они от распущенного поташу не желты, но белы становятся. Откуду следует, что прозрачность тел не теряется от множества странной материи, в скважинах рассыпанной, но от ее густости. Подобным образом сандалом настоенная красная вода обращается в желтую, когда в оную крепкая водка влита будет, но от распущенного поташу переменяется опять в красную. Сухим розовым цветом настоенная вода от влитой кислой материи становится красна, от распущенного поташу ― зелена. И вообще известно, что цветы, которые от кислой материи происходят, от других кислых материй не переменяются, а которые от алкаличных рождаются, от кислых пропадают, равно как от кислых происшедшие, алкаличными изменяются. [1]
| Весною, прежде нежели лист древо распустит, точат из дерева приятный и лекарственный сок, из которого можно приготовлять вино и уксус. Сажа от жженых березовых дров употребляется в типографские чернила и живописцами. Зола для щелочения платья есть самая лучшая. Из нее ж добывают много поташу. [2] ― Образование тримэфилкарбинола из бутилена, приготовленного мной, удается также помощию серной кислоты. Крепкая серная кислота, отделяя при поглощении много теплоты, превращает бутилен в масло, имеющее высокую точку кипения, способное прямо соединяться с бромом и представляющее, конечно, полимеры высшего уплотнения; серная кислота, разведенная равным количеством воды, не поглощает бутилена почти вовсе, но в смеси 2-х объемов крепкой кислоты с 1 об. воды бутилен растворяется, почти не образуя масла, и из раствора, при разбавлении водой и перегонке и добавлении поташа к дестилляту, получается тримэфилкарбинол. ― Наоборот, из тримэфилкарбинола можно, действуя серной кислотой, приготовить бутилен. [3] Вот что происходит с ортоклазом в результате химического выветривания: ортоклаз превращается в каолин (разновидность глины), песок и поташ. Песок и глина идут на построение минерального костяка почвы, а калий, перешедший из ортоклаза в поташ, «раскрепощается», становится доступным для растений. Но не весь сразу. В почвенных водах молекулы К2СО3 диссоциируют. Часть ионов калия остается в почвенном растворе, который для растений служит источником питания. Но большая часть ионов калия поглощается коллоидными частицами почвы, откуда корням растений извлечь их довольно трудно. [4] Поташ в публицистике и мемуарах [ править ]Есть ли ободрить только самых соловозчиков к пережиганию помянутых соляных трав, то немалое количество соды можем получить с Эльтонского озера и с окружающей оное степи. Такое учреждение со времен может не только делать великое подспорье в казне, которая ежегодно на покупку соды тратится, но еще много будет служить к сбережению наших лесов, употребляемых на поташное дело: ибо сия щелочная соль почти на все потребы пригодна, на какие и поташ употребляется. [5] Ходя съ заводу на заводъ добралися до поташныхъ варницъ, которыя въ то время, по причинѣ замѣшательства главнокомандующаго, были остановлены. Всякъ знаетъ, какъ вывариваютъ поташъ: но можетъ быть не всякому у насъ извѣстно, какъ съ нимъ обходиться надобно. О поташѣ. Поташныя варницы принадлежатъ у насъ казнѣ, и имѣютъ разнаго званія правителей, надсмотрщиковъ, лѣсниковъ, и особенную присудственную контору, которая въ бытность нашу въ Арзамасѣ находилася. Для поташнаго употребленія отводятся цѣлыя палестины чернолѣсія, состоящаго по большой части изъ твердыхъ деревъ, какъ то илему, вязу, и прочая. Химики доказываютъ, что щелочная соль или поташъ раждается изъ сродной растѣніямъ кислой соли, когда она при зженіи чрезъ треніе съ возгараемымъ началомъ нѣкоторой части своей влажности лишается, и не прежде произойти можетъ, какъ по разрушеніи дѣйствующею силою огня всего прозябаемыхъ смѣшенія, отъ котораго не рѣдко находимъ различіе въ сродныхъ прозябеніямъ соляхъ; по чему никакой примѣтной разности въ поташѣ быть не можетъ, изъ какого бы онъ ни былъ полученъ растѣнія. Правда: нѣкоторые доказываютъ, что изъ разныхъ деревъ разная можетъ произойти щелочная соль; какъ покойный г. Профессоръ Гмелинъ въ сочиненіяхъ Императорской Академіи Наукъ въ пятой части пишетъ: но такая почти нечувствительная разность болѣе служитъ для любопытства, нежели для варенія поташу. Иное дѣло, когда одинъ поташъ предъ другимъ крѣпче примѣчается: да и сіе не отъ свойства дерева, но отъ разной поташа перечистки и каленія зависитъ. Теперь слѣдуетъ сказать: какое дерево для жженія золы на поташъ пригоднѣе? На сіе не столь удобно можно отвѣтствовать, какъ доказать сходство упорной щелочной соли всѣхъ прозябаемыхъ. На сіе не столь удобно можно отвѣтствовать, какъ доказать сходство упорной щелочной соли всѣхъ прозябаемыхъ. Сіе неоспоримо, что крѣпкое дерево при пережженіи дастъ больше золы, по тому что зола не иное что есть, какъ оставшіяся и огню противящіяся растѣнія начала, каковы суть земля и смѣсь изъ воды и земли составленная, что вообще называется солью. Но какъ твердость всѣхъ тѣлъ зависитъ отъ изобилія земли предъ другими тѣла началами, то и въ золѣ твердаго дерева будетъ больше земляныхъ частей; а земля сама собою никогда дать не можетъ соляныхъ частицъ: но онѣ единственно въ сокахъ прозябаемыхъ изобилуютъ. Я осмѣлюся сказать, что слабое дерево, кольми паче трава, которыя въ сравненіи съ твердыми тѣлами болѣе соками изобилуютъ, удобнѣе къ дѣланію поташа. Онѣ дадутъ меньше золы: но зола ихъ соотвѣтственно больше дастъ соли. Естьли кто не любопытствовалъ отвѣдывать золу разныхъ растѣній, то спроси у врачей, для чего они прописываютъ золу изъ бобовыхъ стеблей? Всякъ незараженный предразсужденіями будетъ отвѣтствовать, что зола бобовыхъ стеблей болѣе въ себѣ щелочной содержитъ соли. Онѣ дадутъ меньше золы: но зола ихъ соотвѣтственно больше дастъ соли. Естьли кто не любопытствовалъ отвѣдывать золу разныхъ растѣній, то спроси у врачей, для чего они прописываютъ золу изъ бобовыхъ стеблей? Всякъ незараженный предразсужденіями будетъ отвѣтствовать, что зола бобовыхъ стеблей болѣе въ себѣ щелочной содержитъ соли. Но положимъ, что крѣпкое дерево болѣе даетъ поташу: однако, должно смотрѣть и на то, что оно гораздо съ большею пользою на другія необходимости употреблено быть можетъ, что и подростъ его предъ слабымъ лѣсомъ гораздо болѣе требуетъ времени, а особливо, что не лишася той пользы, какую отечество отъ поташнаго получаетъ дѣла, можно пощадить уже во многихъ мѣстахъ обветшавшій лѣсъ. Валежникъ, о которомъ я говорилъ выше, удѣлитъ свою часть и на поташное дѣло; да при томъ онъ, для своей мозглости, только сотлѣвая, удобнѣе и полезнѣе къ перепеплыванію, нежели свѣжій лѣсъ. Кустарники и скоро выростающія дерева, какъ то вятлина, тальникъ, и проч. могутъ заступить второе мѣсто. [6] Мне особенно понравились мозаики на химическом заводе, стоящем на Мертвом море. На этом заводе производят поташ, используя в качестве сырья суперсоленую мертвоморскую воду. [7] Поташ в беллетристике и художественной прозе [ править ]Пообедав и выспавшись, Мовша заперся в сарае с Иоселем, Хацкелем и со мною. Я весьма удивился, когда он начал работать возле бочек. В середине был дёготь или поташ, а с краев оба дна отвинчивались, и там находились разные драгоценные товары, шёлковые материи, полотна, батисты, кружева, галантерейные вещи и т. п. Принесли жаровню, штемпели, черную и красную краски; растопили олово, и, пока я раздувал уголья, Мовша с товарищами начал клеймить и пломбировать товары, точно так как я впоследствии видал в таможнях. [8] Среди лесорасходных статей надо помянуть крестьянские ремесла, которыми держалась низовая Россия; вот цифры прежнего расточительства. Дерево издавна и во всех видах было товаром русского экспорта: выжигали поташ, тонна которого обходилась в тысячу кубометров ивы, вяза, липы. Гнали смолу и деготь, выпуская ценнейшие отходы в воздух, причем бересту покупали по пятиалтынному с пуда. В тысяча восемьсот пятьдесят пятом на Нижегородской ярмарке продано восемьсот пятьдесят тысяч пудов мочального товара, кроме лаптей, ― исконной обувки дореволюционного крестьянства. В общаге они питались пшенкой и маслинами, мешок с которыми сосед, любитель спелеологии, привез из Орджоникидзе: месяц отмачивали в поташе, окунали в рассол ветку лавра и сырое яйцо, чтобы всплыло по мере посола. [10] Разговор не вязался; я твердо намеревался отделаться от его околичностей и дядиных настояний одною вежливостью, и, возможно, успел бы в этом, если бы, перемежая сельских новостей жалобами, как плохо теперь идет поташ, торговец не заставил меня неосторожно заметить, сколь моему сочувствию мешает то, что я не знаю, каков поташ из себя, и не знаком с обстоятельствами, кои мешают ему хорошо ходить. Лицо гостя моего загорелось, он всплеснул мягкими руками; речь его полилась ― и получаса не прошло, как я, искренне проклинающий себя до седьмого колена и недоумевающий, как можно было человеку, хвалящемуся любовью к семейству Шанди, так глупо оступиться, ― я знал о перекалке шадрика все, что мне не было нужно о ней знать, из неиссякаемых уст человека, заклинавшего поверить, что поташ именно таков, каким он его изображает. [11] Поташ в поэзии [ править ]Но борется с вием-тленом Нам бы у вас пора бы Источники [ править ]См. также [ править ] |






