Биохимический анализ крови. Ферменты. Часть первая
Биохимический анализ крови. Ферменты. Часть первая
Что говорит биохимический анализ крови о ферментах и о жизнедеятельности нашего организма
Итак, в предыдущей статье мы выяснили, что по биохимическому анализу крови можно узнать обо всем, что творится в организме. Ну вот и откроем нашу книгу на главе «Ферменты». Они растворены в крови в мельчайших концентрациях, но почему определение именно их уровня иногда может стать решающим в постановке диагноза? Вообще, что это такое и какую роль они играют? Давайте разберемся.
Ферменты (энзимы) — это вещества белковой природы, которые ускоряют протекание тех или иных реакций обмена в организме в десятки, а то и сотни раз.
Без ферментов не обходится ни одна реакция. Причем каждый фермент способен воздействовать только на одну-единственную мишень, то есть для этой группы веществ характерна высокая специфичность. А еще он работает лишь в определенных условиях (кислая/щелочная среда, высокая/низкая температура). Каждый энзим состоит из так называемой белковой базы (апофермент) и активного центра (кофермент), который может иметь различное строение (ион, высоко/низкомолекулярный компонент). Собственно, именно активный центр и катализирует реакцию.
Так как вещество весьма специфично, то, само собой, у каждого фермента есть свой субстрат, который подходит ему, как замок ключу. Присоединяясь к субстрату, энзим при помощи активного центра «толкает» реакцию, после чего в итоге из субстрата образуется продукт, обладающий уже совершенно другими свойствами и необходимый организму для каких-либо следующих реакций.
А теперь представьте, что каждую минуту в вашем теле происходят миллионы биохимических взаимодействий… И во всех участвуют ферменты.
Есть ферменты, которые характерны для всех типов клеток и катализируют общие для них всех реакции. А есть ферменты, которые в наибольших количествах можно обнаружить только в определенных клетках определенных органов. Они и представляют диагностическую ценность, а, значит, ими и займемся. В первой части нашей «книги ферментов» мы поговорим о трансаминазах — отдельной и очень характерной группы ферментов.
Аланинаминотрансфераза (АлАТ, АЛТ)
Она относится к трансаминазам, то есть путем отщепления и переноса определенной аминокислоты (в данном случае аланина) превращает одну биологическую молекулу в другую.
Фермент производится внутри клеток, поэтому в норме в крови практически не определяется. Несмотря на то, что АЛТ есть и в клетках сердца, мышц, и в клетках почек, в больших количествах он синтезируется в печени, именно поэтому и представляя собой маркер острой клеточной патологии. Почему? При остром процессе клетки гибнут, а все, что было в их цитоплазме, выходит в кровеносное русло. Соответственно, мы и наблюдаем повышение концентрации АЛТ (и не только, но об этом позже), причем часто этот скачок очень значительный (в 5-10 раз).
Повышение АЛТ можно обнаружить уже за 1-4 недели до появления первых клинических признаков заболевания.
Норма : до 40 ед/л у мужчин, до 32 ед/л у женщин.
Повышение : может быть физиологическим (прием снотворных, оральных контрацептивов, эхинацеи, валерианы, нестероидных противовоспалительных средств; сильные физические нагрузки; у подростков в период активного роста), а может наблюдаться при заболеваниях, приводящих к разрушению клеток печени (острый гепатит, цирроз, рак печени, печеночные метастазы), при закупорке желчных протоков камнями (механическая или подпеченная желтуха), при введении гепатотоксичных препаратов (некоторые лекарства, отравление солями свинца), при массивных ожогах, при массивном инфаркте миокарда и повреждениях мышечной ткани. Также может наблюдаться у страдающих алкогольной зависимостью, жировым гепатозом или стеатозом (когда происходит перерождение печеночной ткани в жировую), у постоперационных больных.
Снижение : при крайне тяжелой степени цирроза в запущенной стадии, когда уже фактически не остается живых клеток, при дефиците витамина В6.
Аспартатаминотрансфераза (АсАТ, АСТ)
Еще один фермент из класса трансаминаз, теперь уже переносящий с молекулы на молекулу аспартат. Так же, как и АЛТ, он находится внутри клеток в цитоплазме и митохондриях, а при клеточной деструкции выделяется в кровь. Наибольшая активность АСТ зарегистрирована в печени, сердце, мышцах и почках.
Концентрация фермента в крови повышается в 5-10 раз при острых печеночных патологиях, в 4-5 раз при инфаркте миокарда. В последнем случае она сохраняется до 5 дней и затем должна снижаться. Если снижения не происходит или отмечается дальнейшее увеличение, это говорит о неблагоприятном для пациента прогнозе — расширении области некроза миокарда.
Норма : 15-31 ед/л для мужчин, 20-40 ед/л для женщин.
Снижение : крайняя степень цирроза, дефицит витамина В6.
Гамма-глутамилтрансфераза (гамма-глутамилтранспептидаза, ГГТ)
Очередной фермент из класса трансаминаз, изменяет биомолекулы благодаря переносу с одной на другую аминокислоты глутамина. В большой степени участвует в обмене жиров, отвечая за преобразование холестерина и триглицеридов. Это главный маркер застоя желчи.
ГГТ — также внутриклеточный фермент, и его повышение характерно для деструктивных клеточных процессов. В отличие от двух первых ферментов, наибольшее количество ГГТ содержится в органах желудочно-кишечного тракта: печени, поджелудочной железе и чуть меньше — в почках.
Норма : до 50 ед/л для мужчин, до 32 ед/л для женщин.
Повышение : при поражениях печени (острый/хронический гепатит, цирроз, алкогольная интоксикация, обтурация камнями желчных путей, злокачественные опухоли печени), при поражениях поджелудочной железы (острый/хронический панкреатит, сахарный диабет, панкреонекроз, рак), при поражениях почек (обострение гломерулонефрита и пиелонефрита), также может встречаться при инфекционном мононуклеозе, гипертиреозе, раке простаты, иногда отмечают при сердечной недостаточности из-за нарушения работы почек.
Снижение : при приеме оральных контрацептивов, эстрогенов, из-за низкой физической активности, вегетарианства, при гипотиреозе.
Показатели почек в биохимии

Когда определяют почечные показатели в биохимическом анализе крови?
Биохимические показатели почек рекомендуется определять в следующих случаях:
Динамическая оценка показателей почек в биохимическом анализе крови проводится при следующих патологиях и состояниях:
К тому же, показатели крови, отвечающие за почки, определяют при осложненном течении беременности — преэклампсия (повышенное давление в артериях, белок в моче) и плацентарная недостаточность.
Почечные показатели крови. Какие показатели указывают на заболевания почек?
Биохимические показатели работы почек включают в себя:
Нормальные показатели почек
Креатинин
Креатинин — это важный показатель крови при заболеваниях почек. Он является конечным продуктом азотистого обмена, а его концентрация напрямую зависит от объема мышечной ткани в организме. Поэтому физиологическая норма креатинина у женщин на порядок ниже, чем у мужчин. К тому же, больше, чем обычно, этого вещества содержится в плазме спортсменов.
По уровню креатинина в биохимическом анализе крови врачи могут выставить диагноз почечной недостаточности. Однако это не единственная причина, которая может привести к изменению этого параметра.
Повышенное содержание креатинина способно указывать на следующие состояния:
Дефицит креатинина часто встречается у вегетарианцев, у женщин в первой половине беременности и у пожилых людей.
Мочевина
Мочевина образуется в печени, а выводится почками. Поэтому по содержанию этого вещества можно делать выводы о состоянии этих двух органов. Повышенные показатели указывают на проблему почечного характера, которая может быть следствием:
Дефицит мочевины является признаком заболеваний печени. Уменьшается содержание этого вещества у беременных женщин и у людей, находящихся на безбелковой диете.
Мочевая кислота
Биохимический анализ крови для почек позволяет диагностировать подагру. В данном случае в плазме определяется повышенное содержание мочевой кислоты. Она образуется в печени вследствие распада пуринов и нуклеинов. Избыток мочевой кислоты приводит к образованию солей (уратов), которые начинают откладываться в суставах, вызывая безмикробное воспаление. У человека появляется боль, припухлость и покраснение в пораженной области.
Дефицит мочевой кислоты не имеет прогностического значения. В медицинской практике важно диагностировать избыточное содержание этого вещества в организме.
Где можно определить показатели работы почек?
Сдать анализы крови можно без предварительной записи ежедневно:
Для получения результатов анализов по электронной почте необходимо оставить письменное согласие на отправку у администраторов медицинского центра.
Функциональная биохимия почек и маркеры их повреждения
| Сайт: | Образовательный портал МБФ (ВолгГМУ) |
| Курс: | Клинико-лабораторная диагностика внутренних болезней |
| Книга: | Функциональная биохимия почек и маркеры их повреждения |
Оглавление
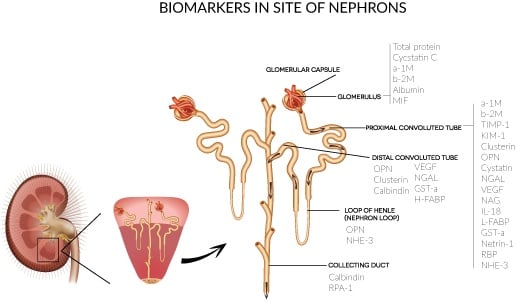
1. Локализация биомаркеров в нефроне
2. Острая почечная недостаточность
В 2004 г. в г. Виченце (Италия) экспертами трех нефрологических ассоциаций (Национального почечного фонда США (National Kidney Foundation, NKF), Американского общества нефрологов (American Society of Nephrology, ASN) и Международного общества нефрологов (ISN)) и Европейского общества интенсивной терапии (European Society of Intensive Care Medicine, ESICM) была впервые предложена концепция «острого повреждения почек» (ОПП, acute kidney injury (AKI)).
При этом ОПП рассматривалось как более широкое понятие, чем собственно острая почечная недостаточность (ОПН). Согласно заключению экспертов, диагноз «острое повреждение почек» может устанавливаться при быстром (в течение 48 часов) снижении функции почек, которое определяется как нарастание абсолютных значений концентрации креатинина в сыворотке крови на 26 мкмоль/л или более; относительном повышении концентрации сывороточного креатинина, равном или большем 50% (в 1,5 раза от базального уровня) или снижении объема мочи (диурез менее 0,5 мл/кг массы тела/ч в течение 6 часов)
Mehta R. L., Kellum J. A., Shah S. V. et al. Acute Kidney Injury Network: report of initiative to improve outcomes in acute kidney injury // Crit Care. 2007; 11 (2): R31.
3. Классификация биомаркеров ОПП
Классификация биомаркеров ОПП
I Топическая классификация
Альбумин, цистатин С сыворотки, альфа1-микроглобулин, бета2-микроглобулин и др.
2. Проксимальный каналец
NGAL, KIM-1, L-FABP, цистатин С мочи, IL-18 и др.
3. Дистальный каналец
4. Собирательная трубка
Калибиндин D28 5. Петля Генле Остеопонтин, NHE-3
II Патофизиологическая классификация
1. Биомаркеры функции почек
Креатинин, цистатин С сыворотки и др.
2. Биомаркеры оксидативного стресса
8(А2а)-изопростан, 4-ОН-2-ноненал и др.
3. Биомаркеры структурного и клеточного повреждения:
— факторы экзосомальной транскрипции АТФ3
4. Маркеры иммунного ответа
Иммуноглобулины, хемокины, компоненты комплемента
TGF- β 1, CTGF, Β ig-H3, Collagen type IV
6. Маркеры апоптоза
III. Клиническая классификация
1. Маркер в качестве фактора риска развития ОПП
2. Маркер, использующийся при скрининге ОПП
3. Диагностический маркер, указывающий на патогенетический вариант ОПП
4. Биомаркер, стратифицирующий тяжесть процесса
5. Маркер с высокой предиктивной значимостью
6. Маркер, характеризующий ответ на терапию
IV. Рабочая классификация
1. Белки, экспрессия которых повышается при ОПП
NGAL, L-FABP, KIM-1, IL-18
2. Функциональные маркеры
Цистатин С сыворотки
3. Низкомолекулярные белки мочи
Цистатин С мочи, альфа1-микроглобулин, бета2-микроглобулин
4. Внутриклеточные энзимы
4. Эпидемиология ОПП
В целом ОПП развивается у 7% всех госпитализированных пациентов, в том числе у 30% пациентов, находящихся в отделениях реанимации и интенсивной терапии (ОРИТ) [4].
Вероятность возникновения ОПП после кардиохирургических вмешательств достигает 9,5% [5, 6].
Последствия ОПП могут быть тяжелыми: у 50% пациентов, находившихся на остром гемодиализе, имел место летальный исход, а у 25% пациентов через три года после восстановления функции почек развивается терминальная хроническая почечная недостаточность. ОПП является причиной 4 млн смертей в год [7].
Смертность среди пациентов, находящихся в ОРИТ с послеоперационными ОПП и нуждающихся в экстренной заместительной почечной терапии, варьирует от 40% до 60% [8, 9].
Критерии, основанные на показателях концентрации сывороточного креатинина и количестве выделяемой мочи, не обеспечивают раннего обнаружения наступающего ОПП. Уровень креатинина повышается через 2–3 дня после наступления ОПП. Как утверждают Devarajan P. и соавт. [10], измерение сывороточного креатинина для выработки надежного терапевтического вмешательства при ОПП аналогично промедлению на 2–3 дня с началом терапии пациентов с инфарктом миокарда и острым нарушением мозгового кровообращения.
С другой стороны, Waikar S. S. и соавт. отметили, что снижение скорости клубочковой фильтрации (СКФ) не всегда наблюдается даже в случаях тяжелого паренхиматозного повреждения почек, в то же время редукция СКФ может встречаться в ситуациях без явной почечной патологии
Канальцевые ферменты
Регуляторные пептиды
Alanine Amino Peptidase
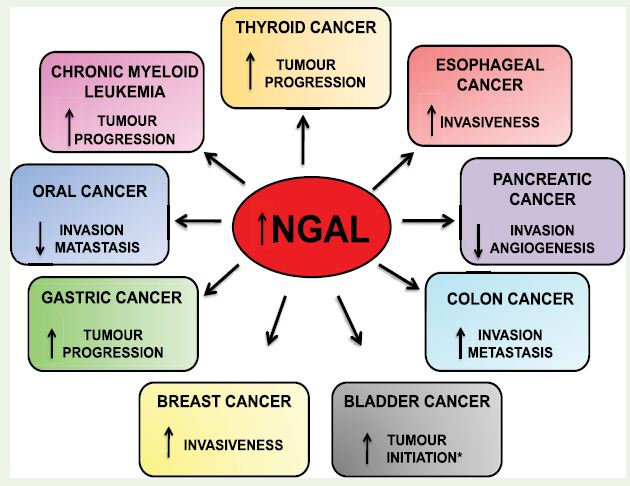
6. Липокалин-2 (NGAL)
Биологическая роль NGAL
NGAL «нормализует» поврежденные ткани за счет:
NGAL Образует комплексы с микробными сидерофорами ( железо переносящие белки животных и бактерий ), связывает железо, необходимое микробам и, тем самым, тормозит их рост 
При патологиях NGAL может стимулировать:
Липокалин-2 является одним из наиболее информативных биомаркеров ОПП. Первоначально NGAL был выделен из супернатанта активированных нейтрофилов человека и позднее был обнаружен в тубулярном эпителии почек. Липокалин-2 выходит в плазму крови из вторичных гранул активированных нейтрофилов, но синтезироваться он может в разных органах и в разных типах их клеток. Липокалин-2 является белком-компонентом острой фазы воспалительного ответа. Его основные функции заключаются в стимулировании пролиферации поврежденных клеток, в первую очередь, эпителиальных, а также в противодействии бактериальным инфекциям [12].
Одним из методов количественного определения липокалина-2 является хемилюминесцентный иммуноанализ на парамагнитных микрочастицах.
6.1. Особенности синтеза и экскреции липокалина-2
Повышение синтеза NGAL в клетках проксимальных канальцев вызывается нарушениями, связанными с ишемией почечной паренхимы и ее поражениями нефротоксическими соединениями.
Природа и источники NGAL в плазме крови и мочи во время AKI. Системное воспаление индуцирует синтез NGAL в экстраренальных тканях и высвобождение NGAL из нейтрофилов. Мочевые NGAL возрастают вследствие нарушение реабсорбции отфильтрованной мочи (понижающая регуляция Megalin-cubulin рецепторов в проксимальных канальцах), увеличение синтеза из нагруженных тубулярных клеткок в дистальной части нефрона и высвобождении при инфильтрации нейтрофилами. Нейтрофилы главным образом выделяют димерную форму (и в некоторой степени мономерную форму), в то время как канальцевые клетки в основном продуцируют мономерную форму и в некоторое количество NGAL, конъюгированного с ММР-9 (Гетеродимерный NGAL).