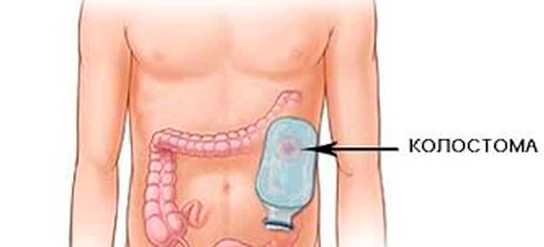
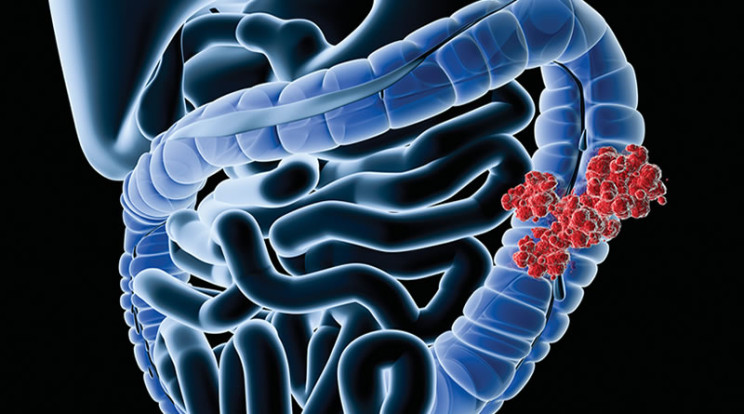
Стадии рака ободочной кишки
Ободочная кишка, состоящая из четырех отделов: восходящей, поперечной, нисходящей и сигмовидной кишки, занимает около 4/5 от длины толстой кишки. В любом из этих отделов может развиваться злокачественная опухоль.
Рак ободочной кишки обычно диагностируется в возрасте 50-75 лет, одинаково часто возникает как у мужчин, так и женщин. В половине случаев опухоль развивается в сигмовидной ободочной кишке, около 10-12% от всех злокачественных опухолей ободочной кишки приходится на восходящую часть, в 2% случаев злокачественное образование поражает сразу несколько отделов.
Задать вопросы и записаться на консультацию можно
по телефону: 222-10-87
или заполните форму ниже
Спасибо, ваш вопрос успешно отправлен, скоро мы с вами свяжемся!
Классификация
В зависимости от размеров первичной опухоли, степени ее прорастания, распространения на другие структуры организма, различают несколько стадий рака ободочной кишки. Установленная при первичном обследовании, стадия в дальнейшем не изменяется, даже если опухоль уменьшается или увеличивается. В течении рака ободочной кишки различают 4 стадии.
| Стадия | Характеристика опухоли |
|---|---|
| I | опухоль размером не более 1,5 см, локализована в пределах слизистого слоя |
| II | II A — размер опухоли превышает 1,5 см, раковые клетки распространяются на субсерозный слой; II B — клетки опухоли проникают в соседние структуры; III C — опухоль не более 1,5 см, но раковые клетки поражают близлежащие лимфоузлы; |
| III | III А — опухоль распространяется более, чем на половину окружности кишки, выходит за пределы кишечной стенки; II В — опухоль может быть любого размера, имеются множественные метастазы; |
| IV | процесс распространяется на отдаленные органы, независимо от размера первичной опухоли и степени прорастания кишечной стенки. |
Стадирование необходимо для выбора тактики лечения и составления прогноза. Для определения стадии проводится обследование, куда входят различные методы диагностики, позволяющие оценить локализацию патологического очага и степень распространения злокачественных клеток по организму. В нашей клинике пациентам доступны все современные и эффективные методы обследования: колоноскопия, томография, ультрасонография, различные исследования крови, в том числе на онкомаркеры и др.
Основные симптомы
На начальном этапе рака ободочной кишки какие-либо симптомы отсутствуют. Однако с ростом опухоли появляются различные признаки. На что стоит обратить внимание, чтобы распознать заболевание своевременно?
Стоит учитывать, что не бывает одинаковых пациентов с идентичными симптомами, появление признаков при раке ободочной кишки зависит от локализации опухоли. Например, болевой синдром чаще появляется при расположении опухоли в правых отделах кишечника. Отрыжка, дискомфорт в животе чаще беспокоит пациентов при опухоли поперечной ободочной кишки. Запоры, диарея, метеоризм, как правило, появляются в первую очередь при злокачественном образовании в левых отделах кишки. Сигмовидная кишка чаще дает о себе знать появлением слизи и крови в испражнениях. Поэтому при любом недомогании лучше обратиться к специалисту.
Однако существуют симптомы, которые появляются независимо от локализации опухоли. Необъяснимая слабость, потеря аппетита, резкое снижение веса, повышение температуры, которую сложно снижать — эти симптомы связаны с интоксикацией организма, что происходит при запущенной стадии рака любой локализации.
Осложнения
При отсутствии лечения существует риск развития осложнений. Опухоль, достигшая больших размеров, может перекрывать просвет кишки, становясь причиной кишечной непроходимости. В этом случае пациент нуждается в немедленной госпитализации. Помимо ухудшения состояния, существует риск некроза и развития перитонита, что представляет угрозу здоровью пациента.
Непрекращающееся кровотечение может стать причиной анемии, что также способно ухудшить состояние больного. При распространении метастазов в печень возможно нарушении оттока желчи и развитие желтухи. Одним из признаков тяжелой стадии рака также является скопление жидкости в брюшной полости — асцит. Подобные осложнения ухудшают прогноз при раке ободочной кишки.
Лечение
Основным методом лечения рака ободочной кишки является операция, цель которой — удаление опухоли. В ходе оперативного вмешательства вместе с опухолью удаляется часть приводящей и отводящей кишки, регионарные лимфатические узлы и окружающая клетчатка. Методика подбирается в зависимости от локализации опухоли. Существуют следующие виды оперативных вмешательств:
В том случае, если оперативное лечение противопоказано или не может быть проведено, проводится паллиативная операция, целью которой является устранение симптомов заболевания и облегчение состояния больного.
Как проводится операция
Операция выполняется в несколько этапов.
Постоянная колостома накладывается, если опухоль является неоперабельной. В таком случае проходимость кишки восстанавливается с использованием стента. Такая операция относится к паллиативным.
Мой подход к лечению пациентов с раком ободочной кишки
Я подбираю тактику лечения, учитывая результаты обследования, возраст пациента и наличие сопутствующих заболеваний. Если это возможно, я всегда отдаю предпочтение органосохраняющему и малоинвазивному лечению. При опухоли на ранней стадии может быть проведена резекция, при этом дистальный и проксимальный края резекции находятся на достаточном расстоянии от очага патологии, чтобы при микроскопическом исследовании отсутствовали опухолевые клетки; таким образом достигается радикальность операции.
Для диссекции на протяжении многих лет я использую технологию мезоколонэктомии по собственной оригинальной методике. Использование современных ультразвуковых ножниц и аппарата электротермического лигирования тканей «LigaSure» (США) позволяет провести быстро и бескровно мобилизацию кишки в правильном слое, без необходимости применения хирургических клипс и нитей.
При мобилизации правых отделов кишки для более безопасной диссекции тканей (вблизи печеночного изгиба, между фасцией Тольди и Герота) я использую оригинальный комбинированный латерально-медиальный доступ. Этот прием дает возможность безопасно выделить мочеточник и двенадцатиперстную кишку, после чего лигировать крупные сосуды, проходящие на этом участке кишки.
В большинстве случаев на этапе реконструкции я формирую анастомоз, что позволяет сохранить качество жизни пациента на прежнем уровне. При создании межкишечного соустья я использую сшивающие аппараты последнего поколения, их применение позволяет снизить количество таких осложнений после операции, как несостоятельность швов анастомоза или стриктура.
Удаление кишки, клетчатки, лимфоузлов проводится единым блоком. При этом удаляемые ткани предварительно помещаются в специальный пластиковый контейнер, что предупреждает попадание клеток опухоли на здоровые ткани, в противном случае высок риск рецидива. Весь биологический материал, удаленный в ходе операции, отправляется на гистологическое обследование — для верификации диагноза.
При проведении операции важным этапом является профилактика тромбоза и тромбоэмболии, для этого используется компрессионный трикотаж и управляемая интраоперационная прерывистая пневматическая компрессия SCD Response (Tyco Healthcare/Kendall).
Преимущества лапароскопии
В большинстве случаев я провожу операцию методом лапароскопии: все действия выполняются через несколько небольших проколов на передней брюшной стенке. Современное эндоскопическое оборудование, используемое в ходе операции, оснащено минивидеокамерой, что позволяет выполнять все действия точно и максимально бережно. Среди преимуществ лапароскопии также можно выделить:
Короткий период реабилитации позволяет пациентам в ближайшее время после операции приступить к химиотерапии, что важно для предотвращения рецидива. Кроме того, ранняя активизация пациента после лапароскопии рекомендована в целях предупреждения тромбоэмболии.
Прогноз
Продолжительность жизни больных после операции зависит от ряда факторов, основным из которых является своевременное начало лечения. Например, при опухоли 1-2 стадии выживаемость в течение первых пяти лет после лечения превышает 90%. Прогноз при раке ободочной кишки 3 стадии составляет около 30%. Ухудшает выживаемость наличие метастазирования в отдаленные органы, для пациентов с 4 стадией рака ободочной кишки прогноз неблагоприятный, показатель составляет не более 10%.
Впрочем, эти цифры весьма приблизительны. На эффективность лечения влияет тип опухоли, ее степень дифференцировки, а также наличие сопутствующих заболеваний. Кроме того, во многом излечение зависит от адекватности терапии. Существующие сегодня методы лечения, как хирургического, так и химиотерапевтического, позволяют добиться положительных результатов даже в тех случаях, которые еще недавно считались безнадежными. Но для этого обращаться за медицинской помощью следует в клинику, где есть современное оборудование и опытный персонал.
Лечением онкологических пациентов я занимаюсь на протяжении нескольких десятков лет. Я владею четырьмя узкими специализациями, одной из которых является колопроктология. Мною лично проведено более 300 хирургических вмешательств при заболеваниях ободочной кишки. Результаты обобщены в монографии «Малоинвазивная хирургия толстой кишки». Я также регулярно провожу семинары и мастер-классы, посвященные хирургическому лечению заболеваний кишечника, которые посещают специалисты клиник и центров, курсанты постдипломного образования.
Рак ободочной кишки
Что такое рак ободочной кишки?
Это злокачественная опухоль, которая входит в тройку лидеров среди других онкологических заболеваний по частоте возникновения и смертности во всем мире. Рак ободочной кишки берет начало из слизистой оболочки толстой кишки, он может распространяться на все слои кишечной стенки, поражать близлежащие органы и структуры.
Раком ободочной кишки чаще болеют мужчины. Наиболее часто данное заболевание диагностируется в возрасте от 50 до 75 лет, однако в последнее время чаще, чем раньше, оно выявляется и у молодых пациентов.
Причины и факторы риска развития
Среди факторов риска развития рака ободочной кишки выделяют: рацион питания с высоким содержанием жира, красного мяса и низким процентом клетчатки, употребление алкоголя, курение, низкую физическую активность, наличие сахарного диабета, хронических воспалительных заболеваний толстой кишки (неспецифический язвенный колит, болезнь Крона), наличие в семье случаев колоректального рака.
У 3-5% пациентов рак ободочной кишки связан с наличием наследственных синдромов (семейный аденоматоз толстой кишки и MUTYH-ассоциированный полипоз, синдром Линча).
Осложнения рака ободочной кишки
Наиболее часто рак ободочной кишки осложняется кишечной непроходимостью при перекрытии опухолью просвета кишки; также может развиваться кишечное кровотечение при травмировании опухоли, перфорация опухоли – разрыв стенки кишки в области опухоли. Отдаленные метастазы рака ободочной кишки могут нарушать работу соответствующих органов (печени, легких и т.д.).
Профилактика рака ободочной кишки
Профилактикой колоректального рака считается приверженность здоровому образу жизни, снижение в диете легкоусваиваемых углеводов и жиров, красного мяса. Физическая активность, в особенности занятия спортом на свежем воздухе, достаточное употребление фруктов и овощей способны профилактировать развите колоректального рака.
Рак ободочной кишки. Симптомы
Ранние формы рака ободочной кишки длительно не вызывают каких-либо симптомов; в большинстве случаев они выявляются при проведении колоноскопии у пациентов без каких-либо жалоб. По мере роста опухоли у пациента появляются и нарастают диспепсические явления (ухудшение аппетита, отрыжка, тошнота, иногда рвота, вздутие живота или метеоризм, чувство тяжести в эпигастральной области), расстройства стула, появляется слизь и кровь в каловых массах. У пациентов с поражением левых отделов кишечника нередко возникает кишечная непроходимость. Также пациенты жалуются на постоянную слабость и повышенную утомляемость, беспричинную потерю веса, характерна прогрессирующая железодефицитная анемия.
Нередко пациенты обращаются к врачу только после появления выраженных симптомов: следов крови и слизи в кале, длительных запоров, изменения вида кала, болевых ощущений и значительного ухудшения общего состояния.
Диагностика рака ободочной кишки
Золотым стандартом в диагностике заболеваний толстой кишки является колоноскопия. Исследование позволяет не только визуализировать опухоль, определить локализацию и размеры, макроскопический тип, оценить угрозу возникновения осложнений (перфорации, кровотечения), но и получить образцы ткани для гистологического исследования.
При выявлении рака ободочной кишки на колоноскопии назначают КТ грудной клетки и брюшной полости с контрастированием, чтобы исключить наличие метастазов опухоли.
В качестве дополнительных методов исследования могут быть выполнены: МРТ органов брюшной полости и малого таза с использованием контрастирования, в сложных случаях применяют ПЭТ-КТ – позитронно-эмиссионная томография.
Стадии и способы лечения рака ободочной кишки
Способы лечения рака ободочной кишки зависят от стадии процесса. Так, при 0 и 1 стадии возможно проведение малоинвазивной эндоскопической операции в ходе колоноскопии.
Стадия 2-3 требует удаления участка кишечника с опухолью и всех региональных лимфатических узлов. Способ выполнения такой операции определяет врач. Может быть использован открытый способ, лапароскопический или роботический метод. Для улучшения отдаленных результатов лечения иногда прибегают к предоперационной химиотерапии.
Если у пациента диагностирован рак ободочной кишки 3 стадии, то после операции такому пациенту назначают адъювантную химиотерапию – она позволяет снизить риск рецидива опухоли.
В случае 4 стадии стратегия лечения разрабатывается на мультидисциплинарном консилиуме с учетом локализации и распространения первичной опухоли и метастазов, сопутствующих заболеваний. Может применяться как химиотерапия, так и хирургическое лечение, или их комбинация.
Операции, выполняемые при раке ободочной кишки
Правосторонняя гемиколэктомия – используется при опухолях восходящей ободочной и слепой кишке, печеночного изгиба ободочной кишки. Хирург удаляет конечный участок тонкой и правую половину ободочной кишки.
Левосторонняя гемиколэктомия – требуется при поражении левых отделов ободочной кишки опухолями.
Резекция поперечно-ободочной кишки – выполняется редко при расположении опухоли в средней трети поперечной ободочной кишки. Чаще всего в подобных ситуациях прибегают к расширенной правосторонней гемиколэктомии или расширенной левосторонней гемиколэктомии.
Резекция сигмовидной кишки – удаление сигмовидной кишки с опухолью.
Если радикально удалить опухоль невозможно, то для профилактики развития осложнений выполняется паллиативная или симптоматическая операция (формирование отключающей кишечной стомы, стентирование толстой кишки, формирование обходного анастомоза и др.), которая помогает улучшить состояние пациента и дает возможность безопасно начать химиотерапию.
Химиотерапия
Для лекарственного лечения рака ободочной кишки сегодня используется современная химиотерапия, применяются таргетные и иммунотерапевтические препараты. В зависимости от стадии рака ободочной кишки, наличия или отсутствия определенных мутаций, сопутствующих хронических болезней, общего состояния здоровья пациента, они могут быть назначены как по отдельности, так и в комбинации.
Лечебные мероприятия после операции
После операции пациента переводят в отделение реанимации и интенсивной терапии, где врачи осуществляют контроль за жизненно-важными функциями (артериальное давление, насыщение крови кислородом, функция почек), а также проводят необходимую терапию. При благоприятном течении послеоперационного периода пациента переводят в палату стационара, где он получает дальнейшее лечение. Режим питания для пациента в послеоперационном периоде врач подбирает индивидуально, в зависимости от объема и характера вмешательства. Главная задача после операции – ранняя реабилитация пациента. Тактика последующего лечения после выписки определяется на основании результатов гистологического исследования на онкологическом консилиуме
Метастазы рака ободочной кишки
Метастазы могут быть региональными – в лимфатические узлы, собирающие лимфу от кишки, и отдаленные. Самой частой локализацией отдаленных метастазов при раке ободочной кишки являются печень и легкие. Реже метастазы могут поражать селезенку, надпочечники, кости, забрюшинные лимфатические узлы. Самыми сложным в лечении являются метастазы по брюшине – канцероматоз брюшины.
Важно помнить, что 4 стадия — это не приговор! Правильно выработанная тактика лечения позволяет добиться 15-летней выживаемости у 11% пациентов.
Прогноз заболевания
Прогноз заболевания во многом зависит от стадии. Пятилетняя выживаемость при начальной стадии рака ободочной кишки достигает 90%, а при продвинутых стадиях не превышает 30%.
Восстановление после операции
Все пациенты, перенесшие операцию по поводу рака ободочной кишки, остаются под наблюдением онколога, регулярно проходят плановые исследования для своевременного выявления прогрессирования заболевания и корректировки индивидуального плана лечения.
Преимущества обращения в Ильинскую больницу
В основу стратегии лечения больных раком ободочной кишки в Ильинской больнице положена концепция мультидисциплинарного комбинированного и комплексного подхода, сочетающего применение современных хирургических технологий с достижениями лучевой, лекарственной и иммунотерапии. Каждый клинический случай разбирается на онкологическом консилиуме (Tumor-board), в котором участвуют: химиотерапевт, хирург-онколог, врач лучевой диагностики, радиолог, онкопсихолог, врач-реабилитолог. Такое подход позволяет выработать наиболее эффективную персонализированную тактику лечения пациента, учесть все индивидуальные нюансы и добиться максимальной эффективности.
Рак ободочной кишки
Рак ободочной кишки является наиболее часто встречаемой патологией в онкологической практике и занимает третью позицию среди всех злокачественных раковых образований органов системы пищеварения. Как правило, заболевание поражает различные слои населения, преимущественно в возрастной категории старше 55-ти лет, независимо от половой принадлежности.
Ведущую роль в образовании атипичных клеток играют предраковые патологические процессы в органах системы пищеварения, а также употребляемая пища с низким содержанием клетчатки. К предраковым состояниям относятся полипы (полипоз), хронический неспецифический язвенный колит, дивертикулярная болезнь и болезнь Крона.
Что представляет собой рак ободочной кишки?
В большинстве случаев злокачественное новообразование образуется в результате трансформации полипов, возникших в толстой кишке. Таким образом, своевременное удаление полипов снижает вероятность развития онкологического заболевания и является хирургической профилактикой рака.
Опухоль ободочной кишки формируется в одном из ее отделов:
Несмотря на возможность формирования рака в любом из отделов ободочной кишки, частота поражения в каждом из участков значительно отличается. Так, в 50% случаев опухоль поражает сигмовидную кишку, более 20% приходится на слепую, 10% на поперечную ободочную и около 15% на участки физиологических изгибов кишки. И только в 2% случаях рак первоначально поражает несколько отделов ободочной кишки.
О заболевании
Распространение опухолевых клеток по организму происходит несколькими путями:
Гематогенные метастазы локализуются преимущественно в печени, иногда в легких.
Классификация рака ободочной кишки
Различают несколько клинических проявлений опухолевого процесса и их признаки:
Симптомы рака ободочной кишки
Первые симптомы патологического процесса практически отсутствуют, но при этом отмечается незначительное ухудшение общего самочувствия, снижение активности и аппетита. На ранних этапах развития болезни человек начинает прибавлять в весе.
Симптомы рака ободочной кишки полностью зависят от места расположения опухоли, размеров, степени распространения, наличия других заболеваний ЖКТ и возникающих осложнений.
Клинический комплекс проявляется ощущением болезненности и дискомфорта, запорами либо поносами, кровяными и слизистыми выделениями при опорожнении кишечника, ухудшением самочувствия.
Более подробная характеристика проявляющихся симптомов:
Фото рака ободочной кишки
Диагностика ракового заболевания ободочной кишки
Диагностика рака ободочной кишки состоит из комплекса мероприятий:
Методы лечения рака ободочной кишки
Основным методом лечения рака ободочной кишки является хирургический, иногда с проведением в послеоперационном периоде химиотерапии.
Метод оперативного лечения определяется после проведения соответствующих диагностических мероприятий для выявления степени распространения опухолевого процесса:
После проведения операции в течение первых 24 часов запрещается употреблять пищу, в это время проводится противошоковая терапия, а также мероприятия для устранения интоксикации и обезвоживания организма.
Начиная со второго дня больному разрешается принимать жидкую, полумягкую пищу и употреблять теплое питье. Со временем в дневной рацион включают такие блюда, как нежирные бульоны, протертые каши, пюре из овощей, омлет на пару, чаи на травяных отварах, различные соки и компоты из свежих либо замороженных фруктов и ягод.
Возможные последствия
Рак ободочной кишки — это серьезное заболевание, которое требует оперативного вмешательства. При отсутствии лечения на ранних стадиях существует риск развития осложнений:
Прогноз выживаемости
Прогноз при опухолях ободочной кишки во многом зависит от стадии патологического процесса, распространения атипических клеток на близлежащие органы, ткани и лимфатические узлы, а также от гистологической структуры злокачественного новообразования.
Лечебные мероприятия после операции
Лечение опухолевого процесса после операции продолжается с помощью химиотерапии.
Применение химиотерапии
Основными препаратами являются фторафур и 5-фторурацил. Большинство пациентов переносят лечение хорошо, реже возникают побочные эффект в виде тошноты, аллергических высыпаниях, рвоте и изменений анализа крови.
УЗИ органов брюшной полости и забрюшинного пространства
Что такое УЗИ органов брюшной полости и забрюшинного пространства?
Современная техника ультразвукового исследования (УЗИ) позволяет с высокой диагностической точностью оценить форму, размеры и расположение органов брюшной полости (печени, желчного пузыря, поджелудочной железы, селезенки и др.), выявить очаговые образования в них (рак печени, поджелудочной железы, метастазы опухолей, абсцессы, кисты, гематомы, аденомы и т. д.), оценить плотность и структуру паренхимы печени и поджелудочной железы при их диффузном поражении, диагностировать даже малые количества (100-200 мл) свободной жидкости в брюшной полости, выявить конкременты в желчевыводящих путях, оцепить изменения крупных сосудов, желчных протоков и т. п.
В последние годы ультразвуковое исследование широко применяется в клинике как метод, помогающий выбрать оптимальный доступ для проведения пункционной биопсии печени, дренирования брюшной полости и выполнения других манипуляций.
Жировая дистрофия печени (жировой гепатоз). Основным эхографическим признаком жировой дистрофии печени является усиление эхоструктуры печени в виде равномерного увеличения количества и размеров эхосигпалов. Это связано с отложением жира в печеночных дольках, расстояние между которыми и их размеры увеличиваются настолько, что ультразвуковые волны отражаются от них.
К числу важных, но менее специфичных признаков относятся увеличение размеров печени, увеличение нижнего угла левой доли более 45°, и четкость контуров печени и невозможность выявления воротной вены.
Эхографичсская картина при жировой дистрофии печени зависит от степени вовлечения в процесс печеночных клеток. При первой стадии заболевания печень несколько увеличена, край закруглен. Эхоструктура имеет пеструю картину, паренхима неравномерно мелкоочагово уплотнена. Это так называемый «островковый» вид поражения печени, который встречается и при гепатитах. При второй стадии печень значительно большего размера, нижний край закруглен, структура паренхимы мелкоочаговая, печень диффузно и равномерно уплотнена. При третьей стадии заболевания печень значительных размеров за счет увеличения обеих долей. Она имеет округлую форму. Структура паренхимы высокой плотности (эхогенности), портальные сосуды не кодируются.
Цирроз печени. Выделяют прямые и косвенные эхографические признаки цирроза печени. Диагноз цирроза печени считается достоверным, если при ультразвуковом исследовании выявляются 3 прямых или 2 прямых и 2 косвенных признака заболевания.
В большинстве случаев размеры печени увеличены, нередко преимущественно за счет левой доли печени. В конечной стадии заболевания при преобладании атрофических процессов размеры органа уменьшаются.
Характерно значительное закругление нижнего края печени и неровность ее контуров.
Эхоструктура печени существенно усиливается за счес появления более частых и крупных эхосигпалов, что связано со значительной перестройкой архитектоники печени, характерной для цирроза. При атрофической стадии количество и размер эхосигналов снижаются.
Наконец, важными признаками цирроза является снижение эластичности и звукопроводимости печени.
Косвенные эхографические признаки цирроза связаны преимущественно с развитием синдрома портальной гипертензии. Расширение селезеночной вены больше 10 мм и портальной вены больше 15 мм считают достоверными признаками повышения давления в системе v. porta.
Увеличение размеров селезенки и усиление ее эхоструктуры наблюдаются в 60-70% случаев цирроза печени, хотя этот признак не является специфичным только для портальной гипертензии.
Асцитическая жидкость и брюшной полости при ультразвуковом исследовании выглядит как эхонегативная структура, которая скапливается в боковых частях живота, в малом тазу или (при малых количествах жидкости) располагается вокруг печени. В этих случаях целесообразно исследование при перемене положения тела пациента (лежа и стоя).
«Застойная» печень. Во всех случаях застойной недостаточности кровообращения отмечают увеличение размеров печени и закругление ее краев. Патогпомопичпым признаком «застойной» печени является расширение нижней полой вены и печеночных всп, ветвление печеночных вен под углом близким к 90°. Характерно, что нижняя полая вена теряет способность изменять диаметр при дыхании: она вообще не сужается при вдохе пли сужается очень мало.
Очаговые изменения в печени
Ультразвуковое исследование печени при очаговых изменениях печени более информативно, чем при диффузных поражениях. При этом отмечаются локальное снижение или усиление эхоструктуры, диффузное или очаговое увеличение размеров печени и неровность ее контура с появлением выпуклости. Объемные очаговые процессы в печени могут вызывать сдавление желчных протоков с возникновением механической желтухи.
Наиболее частым признаком очаговых изменений печени является нарушение нормальной эхоструктуры печени. Различают несколько типов очаговых нарушений эхоструктуры:
Очаги, лишенные эхоструктуры (кисты печени, гематома, абсцесс печени, некротизированные опухоли).
Очаги со сниженной эхоструктурой (метастазы низкодифференцированного рака, саркома, злокачественная лимфома, гепатоцеллюлярный рак, аденома, гемангиома, абсцесс, гематома и др.).
Очаги с усиленной эхоструктурой (метастазы высокодифферепцированного рака, гепатома, аденома, гемангиома, рубцы, очаги обызвествления).
Таким образом, информативность ультразвукового исследования печени достаточно высока, особенно при очаговых поражениях органа. Тем не менее следует учитывать возможные ложноположитсльные и ложноотрицательные заключения. Поэтому при анализе и интерпретации результатов исследования необходимо учитывать клиническую картину заболевания в целом, а также данные других лабораторных и инструментальных методов исследования.
Важно знать:
Нормальная ультразвуковая картина, в том числе сагиттальные размеры печени по срединно-ключичной линии, не превышающие 12-15 см, не исключает наличия заболевания этого органа.
Диффузные или очаговые изменения эхоструктуры печени достоверно свидетельствуют в пользу ее патологии.
По ультразвуковой картине нельзя достоверно дифференцировать различные формы гепатита, начальные стадии жировой дистрофии и цирроза печени.
При диффузных изменениях печени окончательный диагноз следует верифицировать гистологически.
Для уточнения диагноза при очаговых изменениях в печени в большинстве случаев целесообразно проведение прицельной биопсии под эхографическим контролем для последующего цитологического и гистологического анализа.
Желчный пузырь и желчные протоки
Ультразвуковое исследование желчного пузыря и желчных протоков имеет определенные преимущества перед рентгенологическим исследованием (холецистографией, внутривенной холеграфией и др.), так как полностью исключает лучевую нагрузку на пациента, позволяет проводить исследование у детей и беременных женщин, а также при снижении функции печени и почек.
Наиболее общими показаниями к исследованию желчного пузыря и желчных протоков являются:
острый и хронический холецистит;
желчнокаменная болезнь;
желтуха;
опухоль;
водянка и эмпиема желчного пузыря;
состояние после холецистэктомии или других операций на желчевыводящих путях.
При исследовании желчного пузыря оценивают его положение, форму, величину, дыхательную подвижность, состояние наружных и внутренних контуров, толщину стенок, структуру стенки, дополнительные включения в полости желчного пузыря, эвакуаторную функцию органа.
При исследовании впепеченочных желчных протоков определяют их положение, диаметр, состояние стенок, наличие дополнительных включений в просвете.
В норме желчный пузырь выявляется как эхонегативиая структура па дорзалыюй поверхности правой доли печени. Дно желчного пузыря часто выступает из-под нижнего края печени па 1,0-1,5 см. Его длина не превышает 7-10 см, а ширина 3-4 см. Желчный пузырь имеет удлиненную грушевидную, овальную или округлую форму, четкий и ровный контур.
Острый холецистит. Характерными эхографическими признаками острого холецистита является утолщение стенки желчного пузыря более 4 мм. Его размеры могут оставаться нормальными или даже уменьшены, хотя чаще наблюдается небольшое увеличение желчного пузыря.
Эхоструктура желчного пузыря, в первую очередь его внутреннего контура, как правило, снижена. При флегмонозном холецистите внутренние и наружные контуры пузыря нечеткие. При присоединении перихолецистита стенка желчного пузыря имеет двойной контур с усилением эхоструктуры наружного и снижением эхоструктуры внутреннего контура. Появление полоски жидкости вокруг желчного пузыря указывает на наличие локального перитонита.
Хронический (бескаменный) холецистит. В период ремиссии хронического холецистита размеры желчного пузыря уменьшены или нормальные. Наиболее достоверными признаками являются утолщение стенки пузыря при одновременном ее уплотнении (усиление эхоструктуры) и наличие четких контуров. Это отличает эхографическую картину от таковой при остром холецистите.
Нередко изменяется форма желчного пузыря: появляются изгибы, втяжепия стенок и более выраженная деформация его стенок.
В то же время следует помнить, что диагноз хронического холецистита не может быть поставлен только на основании результатов ультразвукового исследования: необходимо обязательное клиническое подтверждение.
Желчнокаменная болезнь. Проблема желчнокаменной болезни (холелитиаза) занимает ведущее место в патологии желчного пузыря. Ультразвуковые признаки калькулсза желчного пузыря делятся на прямые и косвенные. К прямым признакам относят наличие в просвете желчного пузыря на фоне эхонегативной структуры желчи усиленного эхосигпала, соответствующего расположению камня. Размер сигнала несколько меньше истинного размера камня. При осмотре больного в горизонтальном положении камни располагаются преимущественно па дорзальной поверхности и в шейке желчного пузыря.
Одним из косвенных признаков калькулеза желчного пузыря является увеличение его размеров более 5 см в поперечнике и до 10 см и более в длину, а также утолщение его стенки и неровность контура.
Эхографическая картина при наличии камней во впепечепочпых желчных протоках напоминает таковую при калькулезе желчного пузыря. Камни размером более 3-4 мм в диаметре дают усиленный эхосигнал. Если диаметр камня превышает 5 мм, за его дорзальной стенкой определяется акустическая тень.
Камни небольших размеров при ультразвуковом исследовании обычно не выявляются. В этих случаях косвенным признаком калькулеза является расширение протока проксимальнее места его обтурации.
Дифференциальный диагноз механической и паренхиматозной желтух. Эхолокация оказалась одной из наиболее информативных и ценных методик дифференциальной диагностики обтурационной и паренхиматозной желтух. При этом следует иметь в виду, что одним из основных эхографических признаков механической желтухи является расширение желчных путей.
Дифференциальный диагноз строится на следующих принципах.
Если впутрипеченочные и внепечепочные протоки не расширены, а размеры желчного пузыря не увеличены, обтурациоппая причина желтухи вызывает сомнения. В этих случаях она, скорее всего, является следствием диффузных поражений печени (гепатит, цирроз печени и др.).
Если значительно расширены впутрипеченочные протоки, а желчный пузырь и внепечепочные протоки имеют нормальные размеры, причину желтухи следует усматривать в высокой обтурации, например на уровне общего печеночного протока.
Если значительно увеличены размеры вне- и внутрипеченочных желчных протоков, а также желчного пузыря, и эти размеры не изменяются при применении желчегонных средств, наиболее вероятной причиной желтухи является обтурация дистального отдела общего желчного протока («вколоченный» камень, рак сфинктера Одди, карцинома головки поджелудочной железы и т. д.). При этом следует иметь в виду, что сдавление общего желчного протока при опухоли головки поджелудочной железы нередко сопровождается симптомом Курвуазье (увеличением размеров желчного пузыря на фоне механической желтухи). При наличии камня в общем желчном протоке определяется расширение протоков, по желчный пузырь чаще не увеличен.
Ультразвуковое исследование поджелудочной железы
Эхография дает возможность визуализировать поджелудочную железу в разных проекциях и оценить ее состояние в динамике развития патологического процесса, хотя в связи с особенностями анатомического строения и расположения поджелудочной железы исследование сопряжено с определенными трудностями.
Показаниями для ультразвукового исследования поджелудочной железы являются:
любые рецидивирующие или длительно сохраняющиеся боли в эпигастралыюй области;
пальпируемое образование в эпигастралыюй области или болезненность при пальпации;
верифицированный острый или хронический панкреатит с целью своевременного выявления осложнений (образования кист, абсцесса, некроза);
подозрение на кисту, абсцесс, гематому, рак поджелудочной железы;
деформация задней стенки желудка при гастроскопии;
изменение формы и контуров петли двенадцатиперстной кишки при рентгенологическом исследовании.
Ультразвуковое исследование поджелудочной железы начинают в горизонтальном положении пациента сагиттальным сканированием. Датчик устанавливают продольно в эпигастральной области слева от срединной линии.
Исследование продолжают при поперечном расположении ультразвукового датчика, который постепенно перемещают книзу до визуализации селезеночной вены. При поперечном сканировании нередко удается визуализировать всю поджелудочную железу. При необходимости исследование; проводят и в других позициях: при положении пациента на правом и левом боку, в вертикальном положении.
При исследовании поджелудочной железы изучают се положение относительно «сосудов-ориентиров» и позвоночного столба, определяют форму, контуры и размеры органа, состояние панкреатического протока, эхоструктуру железы, выявляют наличие в ней очаговых изменений.
Поджелудочная железа располагается забрюшинно поперек задней брюшной стенки на уровне I и II поясничных позвонков. Хотя форма ее может варьировать, головка всегда является самой большой частью железы. Для практических целей следует учитывать, что размер головки свыше 35 мм, тела свыше 25 мм и хвоста больше 30 мм достоверно указывают па увеличение поджелудочной железы и связанную с этим патологию.
В норме эхоструктура поджелудочной железы по интенсивности напоминает эхоструктуру печени. Преобладают мелкие эхосигналы, которые равномерно распределяются по всей железе. С возрастом в связи с фибротизацией и отложением жира эхоструктура поджелудочной железы усиливается.
В норме диаметр вирсунгова протока не превышает 1,5-2 мм. После внутривенного введения секретина его диаметр увеличивается до 2,5-5 мм. При хроническом панкреатите нередко выявляют расширение панкреатического протока (до 2,5-3,5 мм). После введения секретина диаметр его просвета почти не изменяется, что является важным диагностическим критерием хронического панкреатита.
Селезенка: наиболее целесообразным ультразвуковое исследование этого органа является при подозрении на пороки развития (полное отсутствие, неправильное расположение, блуждающая селезенка, изменение формы, наличие добавочных селезенок), а также при повреждениях селезенки, которые встречаются в 22% случаев всех травм органов брюшной полости. Кроме того диагностируется увеличение селезенки при воспалительных ее поражениях и при заболеваниях печени, определяются кисты, кальцификаты, инфаркты, абсцессы, опухоли (гемангиомы, лимфангиомы, лимфомы, саркомы, метастатические поражения), изменения при системных заболеваниях крови (лейкозы).
Забрюшинное пространство: оценка лимфатических узлов.
Сосуды: оценка расположения магистральных и внутриорганных сосудов, их размеров, состояние просвета, скорости кровотока в них.
Как проходит процедура УЗИ органов брюшной полости и забрюшинного пространства?
Таким образом удастся визуализировать правую и левую доли печени, желчный пузырь, общий печеночный, общий желчный протоки, анатомические структуры, входящие в состав ворот печени, головку поджелудочной железы.
Исследование заканчивается сканированием брюшной полости для выявления свободной жидкости.
Как подготовиться к УЗИ органов брюшной полости и забрюшинного пространства?
За 3 дня до исследования пациенту рекомендуется исключить из питания молоко, черный хлеб, фрукты и овощи, сладкие соки и другие продукты, способствующие газообразованию в кишечнике. При склонности к метеоризму следует назначить ферментные препараты (фестал, панзинорм и др.) и адсорбенты (активированный уголь, пастой ромашки и др.).
Вечером накануне исследования и утром непосредственно перед исследованием ставят две очистительные клизмы. Впрочем, эта процедура не является обязательной при отсутствии у пациента метеоризма.
При необходимости экстренного ультразвукового исследования специальная подготовка желудочно-кишечного тракта не проводится.
Следует помнить, что ультразвуковое исследование органов брюшной полости целесообразно проводить не ранее, чем через 2 суток после рентгенологического исследования желудка с контрастированием или эзофагогастродуодепоскопии и через 3-5 дней после проведения лапароскопии или пиевмоперитопеума.
Какие нормальные показатели (расшифровка) УЗИ органов брюшной полости и забрюшинного пространства?
Анализ и интерпретация результатов исследований
Нормальная ультразвуковая картина печени
В норме контуры печени почти на всем протяжении четкие и ровные. Печень имеет гомогенное строение с равномерным одинаковым по интенсивности распределением сигналов, изображением эхоструктур (сосуды, связки, протоки). Постоянно лоцируется нижняя полая вена в виде лентообразного эхонегативного образования диаметром до 15 мм.
Портальная вена после ее образования из верхнебрыжечной и селезеночной вен впадает в ворота печени, которые лоцируются при поперечном и сагиттальном положении зонда. Виутрипсчеиочные протоки в норме прослеживаются с трудом, их просвет увеличивается от периферии к воротам печени. В отличие от вен внутрипеченочные протоки лишены стенок.
Таким образом, нормальная ультразвуковая картина печени характеризуется наличием мелких, неинтенсивных, относительно далеко расположенных друг от друга эхосигпалов, в результате чего между ними остаются эхонегативные пространства. Эхосигиалы гомогенны по размеру и равномерно распределены по всей печени. Портальные сосуды прослеживаются по периферии печени; эхоструктура их стенок более выражена, чем эхоструктура окружающей их паренхимы печени, звукопроводимость печени полностью сохранена; сагиттальный размер составляет 9-12 см; печень эластичная и имеет ровный, четкий контур.
Диффузные заболевания печени
К числу наиболее распространенных диффузных поражений печени относятся гепатиты (острые и хронические), жировая дистрофия и циррозы печени. Правильный диагноз при ультразвуковом исследовании зависит от целого ряда объективных и субъективных причин. К первым из них относят тип прибора, его чувствительность, разрешающую способность, наличие факторов, ухудшающих изображение (ожирение, газообразование в кишечнике и др.). Большое значение имеют опыт специалиста и тщательность проведения исследования. Наибольшие трудности представляет диагноз ранних стадий жировой дистрофии и цирроза печени.
При острых и хронических гепатитах эхограф и-ческая картина весьма неспецифичиа. Обычно определяется увеличение печени за счет одной или обеих долей, закругление ее краев. Эхоструктура часто нормальна, слабоэхогепна. Лишь при длительном течении заболевания эхоструктура печени становится «пестрой» и наблюдается чередование участков слабой и высокой эхогеиности. В некоторых случаях, в частности, при развитии портальной гипертен-зии, можно обнаружить увеличение селезенки и расширение селезеночной и портальной вены.
К каким докторам следует обращаться для консультаций по УЗИ органов брюшной полости и забрюшинного пространства?