Когда появляется иммунологическая память?
Человеческий эмбрион, находясь в утробе матери, не только взаимодействует с ее иммунными клетками, но и сам имеет различные популяции иммунных клеток, в том числе клеток памяти.
Автор
Редакторы
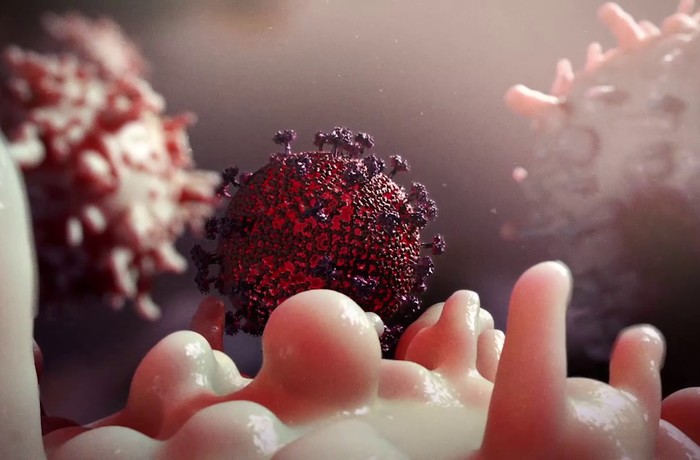
Когда B- и T-лимфоциты активируются в результате вторжения в организм какого-то патогенна, те из них, что способны распознавать антигены этого патогена, начинают размножаться, причем часть новых лимфоцитов не вступает непосредственно в схватку с врагом, а становится хранителем информации о его антигенах. Такие лимфоциты называют клетками памяти; они могут циркулировать в организме еще многие годы после столкновения с патогеном, и благодаря им при повторном заражении развивается молниеносный иммунный ответ, не оставляющий никаких шансов захватчику. Казалось бы, иммунные клетки памяти должны появляться в организме после рождения, когда он начинает сталкиваться с разнообразными бактериями и вирусами. Однако, как показало недавнее исследование, в кишечнике человеческого эмбриона имеется популяция CD4+ (то есть несущих на своей поверхности гликопротеин CD4) T-клеток, которые по молекулярным свойствам соответствуют клеткам памяти. Наша статья посвящена этому открытию.
О Т-клетках, обитающих в органах, не относящихся к иммунной системе, можно прочесть в статье «Т-лимфоциты: путешественники и домоседы» [1], а об особенностях иммунной системы новорожденных — в статье «Сказочка не для взрослых, или Об иммунитете новорожденных» [2].
Т-клетки были выявлены в кишечнике плода, небольшие их популяции также имеются в зародышевых лимфоузлах, тимусе и селезенке. Кроме того, CD4+ T-клетки, обладающие свойствами клеток памяти и эффекторных T-клеток, были обнаружены в крови, взятой из пуповины. Большая международная группа исследователей, провела всесторонний анализ T-клеток из кишечника человеческих эмбрионов и пришла к неожиданному выводу: в популяции кишечных T-клеток плода имеются CD4+ T-клетки памяти [3]! В состав исследовательской группы вошли и российские специалисты, работающие в Институте биоорганической химии и Сколковском институте науки и технологий: Софья Касацкая, Евгений Егоров, Марк Израэльсон, Ольга Британова и Дмитрий Чудаков. Как отмечает Софья, «лаборатория профессора Чудакова много лет сотрудничает с лабораторией Дэвида Прайса в Кардиффе по разным проектам, связанным с фундаментальными и медицинскими вопросами в иммунологии человека. Именно профессор Прайс решил позвать нас в этот проект, и так мы сделали для этой коллаборации подготовку ДНК-библиотек для высокопроизводительного секвенирования и провели анализ данных».
О проточной цитофлуориметрии, секвенировании ДНК и РНК, а также анализе индивидуальных репертуаров клеточных рецепторов можно прочесть в статьях на «Биомолекуле» [4–6].
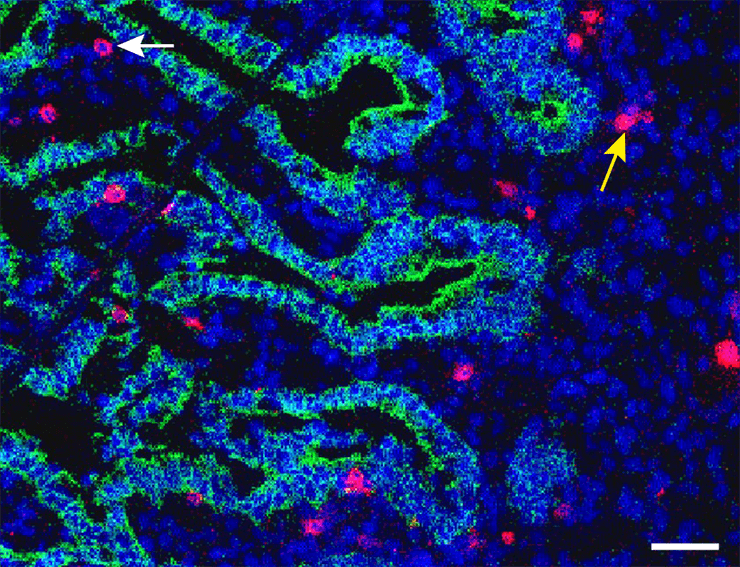
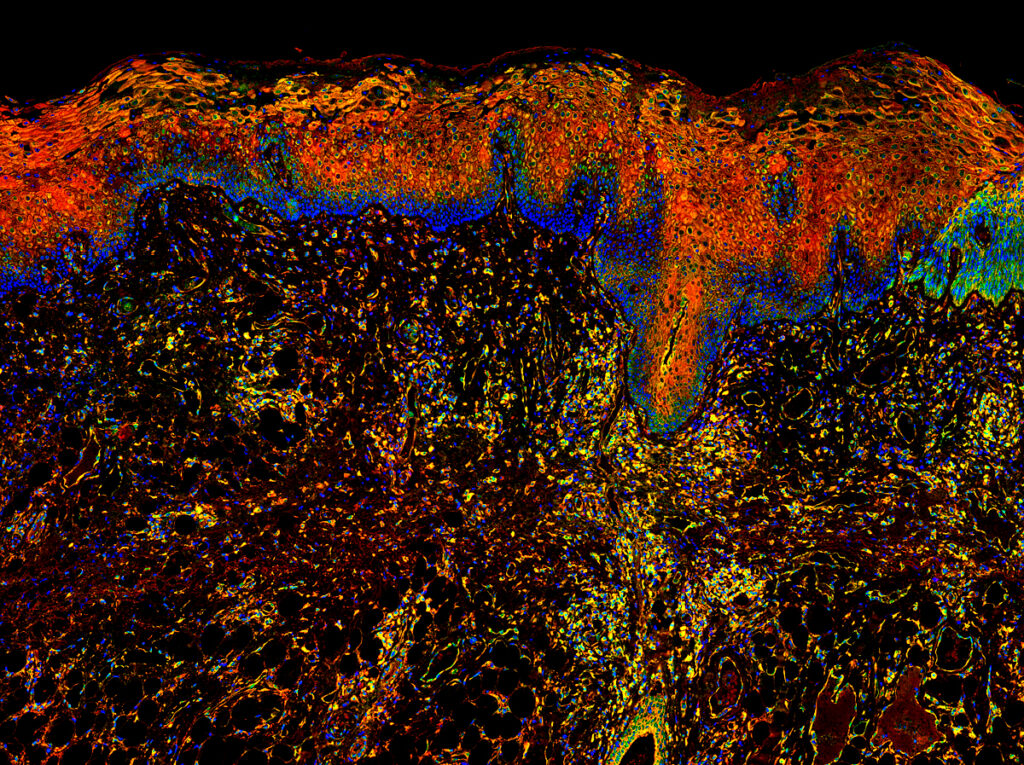
Конечно, Т-лимфоциты не находятся непосредственно в просвете кишки: они залегают в lamina propria (ресничном слизистом эпителии) (рис. 1); помимо лимфоидной ткани их можно найти в более глубоких слоях. В тонком кишечнике, клетки которого и исследовались в обсуждаемой работе, есть небольшие скопления лимфоцитов и В-клеточные фолликулы прямо под lamina propria, а также в более близком к поверхности (подслизистом) слое стенки кишечника.
Рисунок 1. Препарат тонкой кишки эмбриона. ДНК окрашена синим цветом, красным — CD3 (корецептор Т-клеток), зеленым — белок межклеточной адгезии E-кадгерин. Желтая стрелка указывает на наивные CD4+ T-лимфоциты, а белая — на CD4+ T-клетки памяти.
Всего выявили 22 группы Т-клеток, различающихся по экспрессии определенных белков-мáркеров; в их числе имеются наивные (то есть еще не сталкивавшиеся с антигенами) T-клетки и регуляторные T-клетки, а также T-клетки памяти. Среди них обнаружили CD4+ клетки памяти, в которых наблюдалась повышенная экспрессия белка Ki-67, служащего индикатором делящихся клеток. Кроме того, они секретировали провоспалительные цитокины интерферон-γ (INF-γ) и интерлейкин-2 (IL-2). Таким образом, исследователи показали, что разделение Т-клеток на наивные, регуляторные и клетки памяти, а также формирование обособленных популяций «оседлых» Т-клеток происходят очень рано — еще в период эмбрионального развития организма.
Стоит отметить, что популяция наивных Т-клеток в кишечнике плода гораздо больше популяции Т-клеток памяти, в то время как у взрослого человека бóльшая часть Т-клеток кишечника, напротив, приходится на клетки памяти. Ученые предполагают, что Т-клетки памяти плода формируются при локальном столкновении наивных T-клеток с чужеродными антигенами в зародышевых лимфоузлах, в которые мигрирующие из тимуса наивные Т-клетки заходят перед тем, как окончательно «осесть» в кишечнике. Антигенами, которые запускают образование эмбриональных T-клеток памяти, могут быть молекулы лейкоцитарных антигенов матери или фрагменты молекул патогенов, которые попали в амниотическую жидкость. Исследователи отмечают, что образование разнообразных иммунных клеток в кишечнике плода подготавливает его к столкновению с множеством бактерий, которое ждет его сразу же после рождения. Таким образом, формирование популяций специализированных иммунных клеток, в том числе и клеток памяти, начинается еще в период внутриутробного развития.
Иммунная память позволяет хорошо справляться с вирусами и бактериями, которые атаковали наш организм в прошлом. Благодаря этому мы приобретаем иммунитет к предыдущим инфекциям.
Его механизмы также являются основой эффективности профилактических прививок. Как появляется иммунная память? Какой иммунитет к болезни после вакцинации?
Клетки памяти иммунной системы
Термин «иммунная память» описывает способность иммунной системы быстро распознавать антиген, потенциально опасное вещество. С помощью этого механизма обнаруживается присутствие потенциально опасных злоумышленников, таких как патогенные вирусы и бактерии. Использование иммунологической памяти для борьбы с микробами возможно только тогда, когда одно и то же нашествие уже произошло.
Борясь с инфекцией, специализированные клетки иммунной системы запоминают антигены микробов. Благодаря этому организм способен эффективно его преодолевать при последующем контакте с патогенным фактором.
Иммунная память создается иммунной системой каждого человека на протяжении всей его жизни. Стимулами, инициирующими его развитие, являются ситуации воздействия различных факторов, потенциально опасных для здоровья. Побеждая их, иммунная система учится распознавать угрозу и бороться с ней соответствующим образом.
Иммунная память также является основой механизма действия иммунизации. По ходу лечения пациенту вводят антигены вирусов или бактерий в контролируемых условиях. Это позволяет иммунной системе научиться бороться с этими микробами. В результате прививок мы приобретаем искусственный иммунитет, который защищает нас от заражения определенными заболеваниями.
Термин «искусственный», относящийся к иммунитету, который возникает после введения вакцины, относится к самому процессу введения антигена пациенту. Достигнутая таким образом иммунологическая память предоставляет нашему организму «естественные» методы борьбы с угрозой.
Антигены и формирование иммунной памяти
Чрезвычайно важно, чтобы иммунная система распознавала определенные опасные вещества. Этот процесс позволяет отличить чужеродные клетки от тех, которые составляют наш организм. Таким образом, иммунные клетки узнают, что в организм проник вирус или бактерия.
Лимфоциты Т- и В-клетки обладают способностью распознавать ранее известные антигены. Благодаря этому они могут нейтрализовать их быстро и эффективно. Деятельность этих клеток является основой функционирования иммунной памяти.
Запоминание информации иммунной системой
Инфекция вызывает первичный иммунный ответ, направленный на борьбу с причиной заболевания. Когда микробное вторжение преодолевается, организм восстанавливается, но информация об этом событии остается в иммунной памяти.
Специализированные клетки, лимфоциты памяти, остаются в нашем теле, готовые дать отпор известному ранее врагу. Они быстро и эффективно реагируют на повторное заражение. Таким образом, они могут предотвратить развитие болезненного состояния.
Формирование иммунной памяти на клеточном уровне
После того, как инфекция побеждена, активно борющиеся клетки, участвующие в первичном иммунном ответе, уничтожаются. Однако небольшие количества антител, вырабатываемых в ответ на угрожающие антигены, остаются. Они являются элементом иммунной памяти и играют важную роль в защитном механизме в случае последующих инфекций того же микроорганизма.
Помимо антител, в организме остается небольшое количество Т- и В-клеток памяти. Они являются клеточным элементом иммунной памяти. Они сохраняюстся после заражения нашего организма, оставаясь в состоянии покоя. В случае очередной встречи с уже известным злоумышленником они могут немедленно отреагировать. Благодаря этому они способны устранить его до того, как начнется процесс болезни.
Ячейки памяти имеют долгий срок службы. Они остаются в организме даже через несколько десятков лет после заражения, обеспечивая иммунитет к болезни.
В-лимфоциты и иммунная память
После размножения В-лимфоциты дифференцируются в плазматические клетки и клетки памяти. Последние являются одним из клеточных компонентов иммунной памяти.
Т-лимфоциты и иммунная память
Т-лимфоциты созревают в тимусе, а затем перемещаются в лимфатические узлы и селезенку. Они ответственны за индукцию иммунного ответа клеточного типа. Их поверхность покрыта рецепторами иммуноглобулинов, которые действуют как антигенсвязывающие антитела.
Естественно приобретенный активный иммунитет
Естественно приобретенный активный иммунитет формируется в результате воздействия вторгающегося микроорганизма. Он создается после преодоления бактериальных и вирусных инфекций.
Как следствие действия патогена первоначально развивается первичный иммунный ответ. Этот процесс в конечном итоге приводит к иммунной памяти о микроорганизме, который вызвал иммунный ответ. Это естественный процесс нашего организма, который готовится к очередной борьбе с патогенными вирусами и бактериями.
Многие нарушения иммунной системы могут негативно повлиять на формирование приобретенного активного иммунитета. Мы можем перечислить здесь приобретенный или врожденный иммунодефицит. Применение иммуносупрессивных препаратов также нарушает этот процесс.
Искусственно приобретенный активный иммунитет
Искусственно приобретенный активный иммунитет вызывается иммунизацией. Во время них пациенту дают специально приготовленный антиген подходящего микроорганизма. Таким образом, вакцина стимулирует первичный ответ на антиген, не вызывая симптомов заболевания. В конечном итоге его принятие приводит к развитию иммунологической памяти относительно конкретного микроорганизма.
Эффективность прививок основана на имитации естественных инфекций. Благодаря этому механизму достигается развитие или усиление устойчивости организма к возбудителю. Результирующая иммунная память похожа на первое столкновение с реальной угрозой, такой как бактерии или вирусы.
Целью вакцинации является приобретение пациентом активного искусственного иммунитета. Его получение защищает от тяжелых заболеваний.
Важнейшим компонентом всех вакцин являются антигены. Это могут быть вирусы, бактерии или их продукты, такие как токсины, полисахариды или белки. Контакт с этими веществами позволяет сформировать иммунологическую память о патогенном микроорганизме.
Витамины для укрепления иммунной системы
Антигены в вакцинах могут быть в форме:
Живые, ослабленные вакцины против микробов вызывают сильную реакцию в организме. После их приема устойчивость к болезни возможна даже после однократного приема. Однако обычно их прием связан с более серьезными побочными эффектами, чем другие виды вакцинации.
Другие типы вакцин, которые содержат мертвые микроорганизмы или их ингредиенты, обеспечивают иммунитет после введения нескольких доз через соответствующие промежутки времени.
Введение антигена в организм стимулирует иммунные клетки к выработке соответствующих антител против него. В результате защитных процессов также образуются клетки иммунной памяти. Благодаря им возможен длительный эффект профилактической вакцинации.
Безопасность приобретения иммунной памяти с помощью вакцинации
Иммунитет, приобретенный против инфекционных заболеваний, полученный в результате иммунизации, аналогичен иммунитету, возникающему после инфекции. Эти два способа формирования иммунной памяти основаны на одних и тех же естественных механизмах иммунных реакций нашего организма.
Иммунный иммунитет, полученный путем вакцинации, называют «искусственным». Однако это название относится к методу контролируемого контакта с самим антигеном. Выученные в этом процессе методы борьбы с микробами полностью «естественны» для нашего организма. «Естественный» иммунитет приобретается через часто опасные инфекции. Заболевание инфекционным заболеванием иногда также связано с серьезными осложнениями. Побочные эффекты, возникающие в результате плановой вакцинации, в подавляющем большинстве случаев легкие.
Серьезные осложнения случаются крайне редко. Таким образом, формирование иммунной памяти с помощью вакцины намного безопаснее, чем приобретение ее посредством «естественной» инфекции.
Как устроен иммунитет: Объясняем по пунктам
Андрей Смирнов СПИД.ЦЕНТР
«Йогурт для укрепления иммунитета», «Иммуностимулирующие витамины», «Да простудился, наверное, иммунитет упал»… Мы слышим слово «иммунитет» так часто, что уже почти не задумываемся, как он устроен и работает. На уроках биологии нам рассказывали, что иммунитет защищает от микробов, но только ли этим ограничивается его функция и как именно он понимает, от кого нужно нас защищать? СПИД.ЦЕНТР объясняет, как устроена иммунная система.
Наш организм непрерывно меняется, но при этом очень «любит» постоянство и может нормально работать только при определенных параметрах своей внутренней среды. Например, нормальная температура тела колеблется между 36 и 37 градусами по Цельсию. Вспомните последнюю простуду и то, как плохо вы себя чувствовали, стоило температуре подняться всего на полградуса. Такая же ситуация и с другими показателями: артериальным давлением, рН крови, уровнем кислорода и глюкозы в крови и другими. Постоянство значений этих параметров называется гомеостазом, а поддержкой его стабильного уровня занимаются практически все органы и системы организма: сердце и сосуды поддерживают постоянное артериальное давление, легкие — уровень кислорода в крови, печень — уровень глюкозы и так далее.
Иммунная же система отвечает за генетический гомеостаз. Она помогает поддерживать постоянство генетического состава организма. То есть ее задача — уничтожать не только все чужеродные организмы и продукты их жизнедеятельности, проникающие извне (бактерии, вирусы, грибки, токсины и прочее), но также и клетки собственного организма, если «что-то пошло не так» и, например, они превратились в злокачественную опухоль, то есть стали генетически чужеродными.
Как клетки иммунной системы уничтожают «врагов»?
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
Иммунитет бывает врожденным (он же неспецифический) и приобретенным (он же адаптивный, или специфический). Врожденный иммунитет одинаков у всех людей и идентичным образом реагирует на любых «врагов». Реакция начинается немедленно после проникновения микроба в организм и не формирует иммунологическую память. То есть, если такой же микроб проникнет в организм снова, система неспецифического иммунитета его «не узнает» и будет реагировать «как обычно». Неспецифический иммунитет очень важен — он первым сигнализирует об опасности и немедленно начинает давать отпор проникшим микробам.
по теме
Мнение
«Иммунитет пациента с ВИЧ похож на иммунитет пожилого человека»
Однако эти реакции не могут защитить организм от серьезных инфекций, поэтому после неспецифического иммунитета в дело вступает приобретенный иммунитет. Здесь уже реакция организма индивидуальна для каждого «врага», поэтому «арсенал» специфического иммунитета у разных людей различается и зависит от того, с какими инфекциями человек сталкивался в жизни и какие прививки делал.
Специфическому иммунитету нужно время, чтобы изучить проникшую в организм инфекцию, поэтому реакции при первом контакте с инфекцией развиваются медленнее, зато работают гораздо эффективнее. Но самое главное, что, один раз уничтожив микроба, иммунная система «запоминает» его и в следующий раз при столкновении с таким же реагирует гораздо быстрее, часто уничтожая его еще до появления первых симптомов заболевания. Именно так работают прививки: когда в организм вводят ослабленных или убитых микробов, которые уже не могут вызвать заболевание, у иммунной системы есть время изучить их и запомнить, сформировать иммунологическую память. Поэтому, когда человек после вакцинации сталкивается с реальной инфекцией, иммунная система уже полностью готова дать отпор, и заболевание не начинается вообще или протекает гораздо легче.
Кто отвечает за работу различных видов иммунитета?
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.
Как клетки иммунной системы отличают «своих» от «чужих» и понимают, с кем нужно бороться?
В этом им помогает главный комплекс гистосовместимости первого типа (MHC-I). Это группа белков, которая располагается на поверхности каждой клетки нашего организма и уникальна для каждого человека. Это своего рода «паспорт» клетки, который позволяет иммунной системе понимать, что перед ней «свои». Если с клеткой организма происходит что-то нехорошее, например, она поражается вирусом или перерождается в опухолевую клетку, то конфигурация MHC-I меняется или же он исчезает вовсе. Натуральные киллеры и Т-киллеры умеют распознавать MHC-I рецептор, и как только они находят клетку с измененным или отсутствующим MHC-I, они ее убивают. Так работает клеточный иммунитет.
по теме
Эпидемия
Учёные выяснили, как вирусы обманывают иммунитет
Но у нас есть еще один вид иммунитета — гуморальный. Основными защитниками в этом случае являются антитела — специальные белки, синтезируемые B-лимфоцитами, которые связываются с чужеродными объектами (антигенами), будь то бактерия, вирусная частица или токсин, и нейтрализуют их. Для каждого вида антигена наш организм умеет синтезировать специальные, подходящие именно для этого антигена антитела. Молекулу каждого антитела, также их называют иммуноглобулинами, можно условно разделить на две части: Fc-участок, который одинаков у всех иммуноглобулинов, и Fab-участок, который уникален для каждого вида антител. Именно с помощью Fab-участка антитело «прилипает» к антигену, поэтому строение этого участка молекулы зависит от строения антигена.
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
Рассмотрим этот процесс на примере развития бактериальной инфекции. Например, вы поцарапали палец. При повреждении кожи в рану чаще всего попадают бактерии. При повреждении любой ткани организма сразу же запускается воспалительная реакция. Поврежденные клетки выделяют большое количество разных веществ — цитокинов, к которым очень чувствительны нейтрофилы и макрофаги. Реагируя на цитокины, они проникают через стенки капилляров, «приплывают» к месту повреждения и начинают поглощать и переваривать попавших в рану бактерий — так запускается неспецифический иммунитет, но до синтеза антител дело пока еще не дошло.
Расправляясь с бактериями, макрофаги выводят на свою поверхность разные их кусочки, чтобы познакомить Т-хелперов и B-лимфоцитов со строением этих бактерий. Этот процесс называется презентацией антигена. Т-хелпер и B-лимфоцит изучают кусочки переваренной бактерии и подбирают соответствующую структуру антитела так, чтобы потом оно хорошо «прилипало» к таким же бактериям. Так запускается специфический гуморальный иммунитет. Это довольно длительный процесс, поэтому при первом контакте с инфекцией организму может понадобиться до двух недель, чтобы подобрать структуру и начать синтезировать нужные антитела.
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
Иммунологическая память к коронавирусу SARS-CoV-2: пять компонентов иммунного ответа
Иммунологическая память к коронавирусу SARS-CoV-2: пять компонентов иммунного ответа
Как формируется и сколько держится иммунитет к коронавирусу. Вырабатывается ли и сколько сохраняется иммунная память при легком и бессимптомном COVID-19
Содержание
Иммунный ответ на SARS-CoV-2
CD4 + Т-клетки памяти (T-хелперы) помогают активировать патоген-специфические B-клетки памяти и секретируют сигнальные молекулы цитокины, включая IFNγ, для активации клеток врожденного иммунитета. CD8 + Т-клетки памяти (T-киллеры) могут убивать инфицированные вирусом клетки напрямую с помощью доставки молекул, разрушающих клетки. Клетки иммунной памяти помогают организму быстро избавиться от вируса, предотвращая болезнь и снижая вероятность передачи вируса.
Чтобы инфицировать клетки и размножаться, SARS-CoV-2 использует структуру на конце своего белка-шипа (S). Эта структура – рецептор-связывающий домен (RBD) – связывается с рецептором ACE2 клетки человека, и вирус проникает в клетку.
Большинство людей, инфицированных SARS-CoV-2, производят S- и RBD-специфические антитела при первичном иммунном ответе. RBD-специфические моноклональные антитела (полученные из копий одного B-лимфоцита) могут нейтрализовать вирус in vitro и in vivo.
Завершающая стадия развития В-лимфоцитов – плазматические клетки. Это основные клетки, вырабатывающие антитела в организме человека. Если специфические антитела к RBD экспрессируются долгоживущими плазматическими клетками (LLPC) или патоген-специфическими B-клетками памяти (MBC), вероятно, эти антитела смогут защитить от повторного заражения коронавирусом SARS-CoV-2.
Как работает противовирусный иммунитет
Организм умеет уничтожать патогены, с которыми сталкивался ранее. Эта способность называется приобретенным иммунитетом. Приобретенный иммунитет может убивать инфицированные вирусом клетки и генерировать защитную иммунологическую память. Именно она является основой стратегий вакцинации.
Для борьбы с вирусами и развития иммунологической памяти важны ответы Т-клеток и В-клеток. Попадая в клетку организма, вирусы берут на себя управление клеточными механизмами, чтобы создавать новые вирусные частицы и распространяться на здоровые клетки. Вирусные инфекции вызывают врожденные иммунные реакции, например, воспаление. Эти реакции активируют приобретенный иммунитет. Дендритные клетки захватывают вирусные белки и частицы и транспортируют их в лимфоидные органы – селезенку и лимфатические узлы. Там вирусные белки и частицы распознаются Т- и В-клетками. Клеточная (Т-клеточная) и гуморальная (В-клеточная) ветви приобретенного иммунитета работают вместе, обеспечивая вирус-специфическую защиту.
Механизм распознавания и устранения вируса
Как Т-клеточное распознавание вирусных пептидов, так и В-клеточное распознавание вирусных белков начинаются в лимфоидных тканях, где дендритные клетки представляют пептиды Т-клеткам, а В-клетки отбирают вирусные белки. Вместе они инициируют развитие эффекторных клеток для устранения вируса.
Величина ответов Т- и В-клеток определяется:
CD4 + Т-клетки также дифференцируются в фолликулярные Т-хелперы (Т FH ), которые необходимы для развития продуцирующих антитела В-клеток и поддерживают развитие В-клеток памяти. Т FH имеют решающее значение для формирования зародышевых центров в фолликулах периферических лимфоидных органов.
Антитела могут нейтрализовать вирусы, предотвращая проникновение в клетки или способствуя гибели инфицированных клеток. В результате скоординированного взаимодействия врожденного и приобретенного иммунитета пиковые реакции Т- и В-клеток приводят к снижению вирусной нагрузки и ослаблению воспаления, часто в течение одной недели после заражения.
T- и B-клетки памяти
После удаления вируса большинство эффекторных Т- и В-клеток погибают. Сохранившиеся Т-клетки становятся Т-клетками памяти. Сохранившиеся В-клетки генерируют либо долгоживущие плазматические клетки, продуцирующие антитела, либо становятся В-клетками памяти. Клетки памяти способны быстро реагировать на повторное заражение.
SARS-CoV-2-специфические CD4 + и CD8 + Т-клетки обнаруживаются в кровотоке как у активно инфицированных, так и у выздоровевших пациентов, что свидетельствует о потенциальной способности развития защитного клеточного иммунитета.
Т-клетки памяти бывают:
Т-клетки, расположенные в очагах инфекции, могут стать тканево-резидентными T-клетками памяти (TRM).
Что определяет эффективность приобретенного иммунного ответа
B-клетки переключаются с раннего синтеза антител класса M (IgM) на синтез антител IgG и IgA с более высоким сродством. Эти антитела обнаруживаются в сыворотке выздоравливающих пациентов с COVID-19.
Величина ранних ответов антител может свидетельствовать о тяжести инфекции, поскольку более высокие титры антител IgM и IgG ассоциированы с более тяжелым заболеванием. Как и в случае с другими вирусными инфекциями, общие титры антител к SARS-CoV-2 в сыворотке крови уменьшаются после излечения активной инфекции. Однако долгоживущие В-клетки памяти могут сохраняться и продуцировать циркулирующие вируснейтрализующие антитела. Недавнее исследование показало, что через 6-8 месяцев после начала заболевания COVID-19 нейтрализующие антитела против SARS-CoV-2 были обнаружены у 90% выздоровевших пациентов. Также важно отслеживать и сравнивать продолжительность реакции В-клеток памяти на естественную инфекцию SARS-CoV-2 и вакцины.
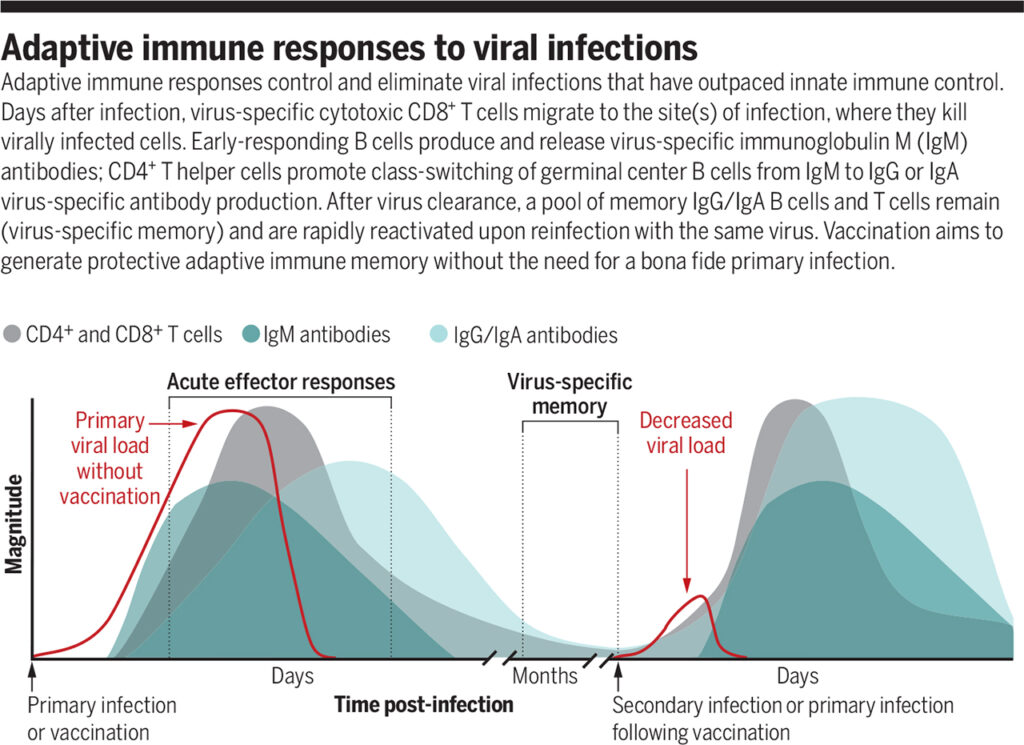
Приобретенный иммунный ответ на вирусные инфекции
Приобретенный иммунный ответ контролирует и устраняет вирусные инфекции, опередившие врожденный иммунный контроль. Через несколько дней после заражения вирус-специфические цитотоксические CD8 + Т-клетки мигрируют к месту инфекции, где убивают инфицированные вирусом клетки. В-клетки с ранним ответом продуцируют вирус-специфические антитела IgM. CD4 + Т-хелперные клетки способствуют переключению класса В-клеток зародышевого центра с IgM на IgG или выработке вирус-специфических антител IgA. После удаления вируса сохраняются B-клетки памяти IgG / IgA и Т-клетки памяти. Они быстро реактивируется при повторном заражении тем же вирусом. Вакцинация направлена на формирование защитной приобретенной иммунной памяти без необходимости в подлинной первичной инфекции.
Перекрестно-реактивные T- клетки и антитела
Пока неясно, могут ли уже существующие SARS-CoV-2-реактивные Т- и В-клетки способствовать улучшению исходов заболевания. Если они улучшают исход заболевания, то может быть желательно увеличить такие популяции Т- и В-клеток с помощью вакцинации.
Чем опасна чрезмерная активация T-клеток
Важно отслеживать степень инфицирования и воспаления, вызванного вирусами, включая SARS-CoV-2. Чрезмерные врожденные иммунные ответы, такие как гипервоспаление (повышенный уровень интерлейкина-6 (IL-6) и С-реактивного белка), могут способствовать выраженной активации Т-лимфоцитов, которая еще больше усиливает воспаление и тяжесть заболевания. Обширная активация Т-клеток во время COVID-19 может привести к лимфопении (уменьшению количества лимфоцитов), изменению дифференцировки и потере функции Т-клеток. Это может замедлить вирусный клиренс, продлить инфекцию и повысить заболеваемость.
Факторы, прогнозирующие тяжесть заболевания
Остается неясным, почему у некоторых инфицированных людей симптомы отсутствуют, тогда как у других наблюдается тяжелый COVID-19. Однако с тяжелым COVID-19 связаны:
Возможность выявления прогностических факторов будет увеличена за счет включения бессимптомных лиц, инфицированных SARS-CoV-2.
Опасные реакции приобретенного иммунитета на коронавирус SARS-CoV-2
Немецкие ученые обнаружили, что у активно инфицированных пациентов сильно мутировавшие рецепторы B-клеток и снижение клональной экспансии были связаны с более тяжелыми клиническими исходами, тогда как больший пул вирус-специфичных наивных В-клеток у пациентов коррелировал с развитием более эффективного противовирусного иммунного ответа.
Усиленная дифференцировка TH1, потеря TFH и связанное с этим отсутствие формирования зародышевого центра были недавно обнаружены при посмертном анализе лимфатических узлов и селезенки у пациентов, которые скончались в течение 10 дней с момента появления респираторных симптомов COVID-19. Измененные пропорции субпопуляций CD4 + Т-клеток периферической крови, статуса активации Т-лимфоцитов CD8 + и В-клеток также наблюдались у пациентов с тяжелым COVID-19. Углубленный анализ около 200 иммунных параметров показал, что тяжесть заболевания, включая тяжелое воспаление и органную недостаточность, коррелирует с общей лимфопенией, при этом оставшиеся лимфоциты: CD4 + и CD8 + эффекторные Т-клетки, клетки TFH и короткоживущие плазматические клетки, продуцирующие антитела – высокоактивированы и потенциально гиперактивированы.
T-клетки снижают тяжесть COVID-19
Нейтрализующие антитела, как правило, не связаны со снижением тяжести COVID-19. У нечеловекообразных приматов выработка нейтрализующих антител защищает от повторного заражения SARS-CoV-2 или SARS-CoV.
Введение нейтрализующих антител перед инфекцией имитирует повторное заражение. Оно эффективно ограничивает инфекцию верхних и нижних дыхательных путей, включая легкие, а также уменьшает симптомы коронавируса на животных моделях.
Введение нейтрализующих антител, проведенное после инфицирования у человека, оказывает более ограниченное воздействие на COVID-19. Это подтверждает значительную роль Т-клеток в контроле и очищении организма от SARS-CoV-2.
Исследования острых и выздоравливающих пациентов с COVID-19 показали, что Т-клеточные реакции связаны с уменьшением заболевания. Специфические для SARS-CoV-2 CD4 + и CD8 + Т-клетки могут играть важную роль для контроля и разрешения первичной инфекции SARS-CoV-2.
Для лучшего понимания стойкости защитного иммунитета против COVID-19, генерируемого первичной инфекцией SARS-CoV-2, важно дальнейшее комплексное изучение антител, B-клеток памяти, CD4 + и CD8 + Т-клеток памяти.
Не только антитела защищают от COVID-19
Хотя иммунологическая память является источником долгосрочного защитного иммунитета, прямые выводы о защитном иммунитете нельзя сделать на основе количественной оценки циркулирующих антител к SARS-CoV-2, B-клеток памяти, CD8 + и CD4 + T-клеток, поскольку механизмы защитного иммунитета против SARS-CoV-2 или COVID-19 у человека не определены. Тем не менее, можно сделать некоторые разумные интерпретации.
Антитела – единственный компонент иммунной памяти, который может обеспечить действительно стерилизующий иммунитет.
Исследования иммунизации на нечеловекообразных приматах показали, что циркулирующие титры нейтрализующих антител
200 могут обеспечить стерилизующий иммунитет верхних дыхательных путей против относительно высокой дозы вируса SARS-CoV-2, а нейтрализующие титры
3400 могут обеспечить стерилизующий иммунитет против очень высокой дозы вируса.
В то время как стерилизующий иммунитет против вирусов обеспечивают только нейтрализующие антитела с высоким титром, успешная защита от клинического заболевания или смерти может быть достигнута с помощью нескольких других сценариев адаптивной иммунной памяти.
CD4 + и CD8 + T-клетки памяти, а также B-клетки памяти, продуцирующие нейтрализующие RBD-антитела, могут ограничивать SARS-CoV-2 в верхних дыхательных путях и ротовой полости и минимизировать тяжесть COVID-19 до обычной простуды или бессимптомного заболевания.
У человека SARS-CoV-2-специфические CD4 + Т-клетки и CD8 + T-клетки связаны с уменьшением тяжести COVID-19 при продолжающейся инфекции SARS-CoV-2, а быстрое образование антител связано со значительным снижением вирусной нагрузки при остром заболевании в течение 14 дней. Эти факты согласуются с гипотезой о том, что Т-клетки и В-клетки памяти могут существенно ограничивать распространение SARS-CoV-2 и / или вирусную нагрузку, что приводит к значительному снижению тяжести заболевания COVID-19. Вероятность таких исходов тесно связана с кинетикой инфекции, поскольку ответы B- и Т-клеток памяти могут занять 3-5 дней, чтобы успешно отреагировать на инфекцию.
Учитывая относительно медленное течение тяжелого COVID-19 у людей, существует большое окно времени для того, чтобы иммунная память могла внести значимый вклад в защитный иммунитет против пневмонии, тяжелого или смертельного повторного COVID-19. Наличие нейтрализующих антител во время воздействия SARS-CoV-2 притупило бы размер первоначальной инфекции и могло бы внести дополнительный вклад в ограничение тяжести COVID-19.
T-клетки обеспечивают иммунитет, если нет антител к коронавирусу
Выводы
У потенциальных доноров плазмы с неопределяемыми антителами против белка S1 SARS-CoV-2 ответ Т-клеток на мембранный белок M был сильнее, чем на белок S1. Возможно, Т-клетки этих доноров предпочтительно нацеливаются на пептиды, участвующие в сборке вирусных частиц, а не в связывании вируса с клеткой. Однако эта гипотеза нуждается в подтверждении.
Ответы на пептиды S1 / S2 были сильнее, чем на белок S1, возможно, потому, что фрагменты макромолекулы антигена S2 вызывали более сильный иммунный ответ.
Интересно, что различия между участниками с соотношением антител 3, по-видимому, более выражены после стимуляции белком S1, чем пептидами S1 / S2. Таким образом, помимо белка М, белок S2 может быть дополнительной мишенью для Т-клеточных ответов, особенно у участников с неопределяемыми Т- и В-клеточными ответами против белка S1.
Обнаружение того, что ответ Т-клеток на белок S1, который является наиболее специфичным для SARS-CoV-2, был относительно низким, поднимает вопрос о потенциальной перекрестной реактивности после стимуляции пептидами S1 / S2 или М.
Перекрестная реактивность ранее наблюдалась для антител к SARS-CoV-1 и SARS-CoV-2. Точно так же могут возникать перекрестно-реактивные к SARS-CoV-2 Т-клетки из-за контакта с распространенными коронавирусами. Это может повлиять на специфичность тестов ELISpot. Тем не менее, недавняя подтвержденная ПЦР инфекция SARS-CoV-2 могла привести к тому, что частота реактивных к SARS-CoV-2 Т-клеток была выше у потенциальных доноров плазмы, чем у тех, кто перенес другие распространенные коронавирусы. Кроме того, перекрестно-реактивные Т-клетки могут защищать от инфекции SARS-CoV-2, особенно детей и молодых людей с частыми социальными контактами. Исследование Braun et al. показало, что у 34% здоровых доноров плазмы есть ранее существовавшие SARS-CoV-2 S-перекрестно-реактивные CD4+ Т-клетки, а исследование Grifoni et al. обнаружило перекрестно-реактивные Т-клетки у 40% –60% лиц, не подвергавшихся воздействию коронавируса SARS-CoV-2. Однако из-за возможности того, что перекрестная реактивность мешает анализам ELISpot, ученые проверили Т-клеточные ответы в группе отрицательного контроля. Ответы были отрицательными.
Клеточный иммунитет к любому из антигенов SARS-CoV-2 был обнаружен у 7 из 9 (78%) участников, у которых соотношение антител было 3 имели определяемый клеточный иммунитет. Учитывая всех потенциальных доноров плазмы с подтвержденной ПЦР инфекцией SARS-CoV-2 (также с соотношением антител 1,1–3), 22 из 28 (79%) доноров имели T-клеточный иммунитет.
Таким образом, Т-клеточный иммунитет против SARS-CoV-2 наблюдался у большинства участников, положительных по ПЦР на SARS-CoV-2, с неопределяемыми антителами IgG к белку S1. В этой группе Т-клеточный иммунитет был сильнее направлен против белка М, чем против белка S1.
Защищает ли Т-клеточный иммунитет от повторного заражения коронавирусом
Отсутствие антител IgG к SARS-CoV-2 не означает, что человек не болел коронавирусом. Оценка клеточного иммунитета может дополнить данные о гуморальном ответе. Предыдущие исследования продемонстрировали, что величина ответа антител на SARS-CoV-2 зависит от продолжительности и силы воздействия вируса. Отсутствие устойчивых системных ответов IgG может указывать на легкую и временную инфекцию SARS-CoV-2, которая была эффективно устранена, например, врожденной иммунной системой. Однако необходимо выяснить, привел ли этот иммунный ответ к защитному иммунитету от коронавируса.
Chandrashekar et al. наблюдали почти полную защиту у 9 макак-резусов после инфекции SARS-CoV-2. После первоначального обезвреживания вируса при повторном заражении животные показали снижение средней вирусной нагрузки по сравнению с первичной инфекцией и устойчивый гуморальный и клеточный иммунный ответ. Deng et al. сообщили, что при повторном заражении SARS-CoV-2 у 4 макак-резусов наблюдалось временное повышение температуры тела, однако без вирусной нагрузки. Kirkcaldy et al. сообщили об ограниченных доказательствах повторного заражения среди перенесших COVID-19. Сингапурское исследование показало, что Т-клетки, специфичные для SARS-CoV-2, выявлялись у большинства выздоровевших пациентов. Данные о предыдущем коронавирусе SARS-CoV-1 показали, что клеточный иммунитет выявлялся в течение более 17 лет после заражения. Ученые Швеции и Франции наблюдали Т-клеточный ответ против SARS-CoV-2 у пациентов без антител к коронавирусу.
Данные IFN-γ ELISpot, полученные в среднем через 2 месяца после появления симптомов SARS-CoV-2, показывают, что 79% участников имели определяемый Т-клеточный иммунитет, что хорошо согласуется с предыдущими данными о структурно родственном коронавирусе SARS-CoV-1. Это означает, что у выздоравливающих пациентов с неопределяемым IgG к SARS-CoV-2 иммунитет могут обеспечивать Т-клетки.
Неоднородность иммунной памяти к SARS-CoV-2 и риск повторного заражения
Американские ученые исследовали иммунную память у 185 человек в возрасте от 18 до 81 года с бессимптомным, легким, умеренным и тяжелым COVID-19. У большинства пациентов был легкий случай COVID-19, не требующий госпитализации. 92% участников исследования никогда не были госпитализированы из-за COVID-19. 7% участников были госпитализированы, некоторым из них потребовалось лечение в отделении интенсивной терапии. Это соответствует распределению тяжести заболевания COVID-19 в США. Большинство участников (97%) сообщили о симптоматическом заболевании. Большинство участников сдали образец крови один раз между 6 и 240 днями после появления симптомов. 41 участник сдал образец крови более чем через 6 месяцев после появления симптомов. 38 участников предоставили 2-4 повторных образца крови в течение нескольких месяцев.
Особенности иммунной памяти к SARS-CoV-2:
Таким образом, неоднородность иммунной памяти к SARS-CoV-2 не связана с полом или тяжестью заболевания COVID-19.
Величина ответа антител против SARS-CoV-2 очень неоднородна у разных людей. Разнородные исходные реакции антител не сводятся в однородную циркулирующую память антител. Эта неоднородность является главной особенностью иммунной памяти к SARS-CoV-2. Для антител ответы охватывают
Источник неоднородности иммунной памяти к SARS-CoV-2 неизвестен и заслуживает дальнейшего изучения. Возможно, такая неоднородность является результатом низкой кумулятивной вирусной нагрузки, что приводит к очень незначительной или преходящей инфекции, которая вызывает слабый адаптивный иммунный ответ.
В результате неоднородности иммунного ответа можно ожидать, что, по крайней мере, часть переболевших SARS-CoV-2 с особенно низкой иммунной памятью будет относительно быстро восприимчива к повторному заражению.
Сколько держится иммунитет к коронавирусу после естественного течения заболевания?
Ученые предположили, что в защитном иммунитете важную роль играют 5 компонентов: RBD IgG, RBD IgA, RBD B-клетки памяти, SARS-CoV-2-специфические CD8 + и CD4 + Т-клетки.
Результаты исследования на 185 пациентах показали, что каждый компонент иммунной памяти к SARS-CoV-2 демонстрирует различную кинетику:
В-клеточная память о некоторых других инфекциях долговечна: 60+ лет после вакцинации против оспы, 90+ лет после заражения гриппом.
Период полураспада Т-клеток памяти, наблюдаемый в течение 6+ месяцев после появления симптомов в этом исследовании (
166 – 271 дней для CD8 + и
96 – 174 дней для CD4 + Т-клеток), сопоставим с 123-дневным периодом полураспада для CD8 + T-клеток памяти после иммунизации против желтой лихорадки. Период полураспада CD4 + Т-клеток памяти к оспе –
10 лет. Известен случай обнаружения Т-клетки к SARS-CoV через 17 лет после первоначального заражения. Эти данные показывают, что память Т-клеток может достигнуть более стабильного плато или более медленной фазы распада позже, чем в первые 6 месяцев после заражения.
Иммунная память, состоящая, по крайней мере, из трех иммунологических компонентов, была измерена у
90% субъектов через ≥ 5 месяцев после появления симптомов. Это указывает на то, что устойчивый иммунитет против повторного COVID-19 возможен у большинства людей.
Сохраняется ли иммунитет к SARS-CoV-2 после COVID-19 в легкой форме?
Первая волна иммунного ответа – короткоживущие малоэффективные плазмобласты, секретирующие антитела. Далее организм генерирует высокоэффективные B-клетки памяти (MBC) и долгоживущие плазматические клетки (LLPC), секретирующие антитела. LLPC могут поддерживать определяемые титры сывороточных антител от месяцев до многих лет, в зависимости от конкретной вирусной инфекции. Очень важно отличать первую волну убывающих антител, производных от плазмобластов, от более поздней волны устойчивых антител, производных от LLPC, которые могут нейтрализовать последующие инфекции, потенциально на всю жизнь.
Популяции активированных клеток врожденного и адаптивного иммунитета увеличиваются в крови во время первичного ответа на инфекцию SARS-CoV-2. Когда острая вирусная инфекция проходит, большинство этих воспалительных клеток либо умирают, либо становятся клетками памяти.
Ученые Вашингтонского университета (Сиэтл, Вашингтон, США) оценили иммунные ответы у пациентов с легкой формой COVID-19 через один и три месяца после появления симптомов.
Чтобы определить, образуются ли клетки иммунной памяти после COVID-19 с легкими симптомами, ученые собрали плазму и мононуклеарные клетки периферической крови у 15 человек, вылечившихся от COVID-19. Первый образец крови был взят через ≥ 20 дней после положительного результата ПЦР-теста на SARS-CoV-2 и в среднем через 35,5 дней после появления симптомов. Вирусная нагрузка снижается примерно через 8 дней после появления симптомов, поэтому в этот момент времени будет сокращаться первичный иммунный ответ и формироваться ранняя иммунная память. Второй анализ крови собрали в среднем через 86 дней после появления симптомов, чтобы оценить количество и качество клеток иммунной памяти.
Исследование показало, что легкий COVID-19 индуцирует стойкие нейтрализующие антитела IgG к SARS-CoV-2. В течение, по крайней мере, 3 месяцев после появления симптомов у участников присутствовали LLPC, поддерживающие на обнаруживаемом уровне нейтрализующие антитела S и RBD IgG против SARS-CoV-2.
Инфекция SARS-CoV-2 индуцирует устойчивые функциональные S-реактивные CD4 + Т-клетки памяти. CD4 + Т-клетки памяти продуцируют цитокины в течение нескольких часов после активации, тогда как наивным Т-клеткам требуется несколько дней. CD4 + Т-клетки памяти, специфические для SARS-CoV-2, сохраняют способность оказывать помощь В-клеткам даже через три месяца после появления симптомов.
RBD-специфические B-клетки памяти, индуцированные инфекцией SARS-CoV-2, способны продуцировать нейтрализующие антитела против вируса и могут способствовать защите от повторного заражения SARS-CoV-2.
Исследование продемонстрировало повышенный уровень антител RBD IgG, которые образуются и сохраняются в течение как минимум 3 месяцев после заражения SARS-CoV-2.
Иммунная память к SARS-CoV-2 формируется и сохраняется после легкой формы COVID-19, по крайней мере, 3 месяца. Т-клетки памяти обладают признаками защитного противовирусного иммунитета. В то время как антитела выявляют вклад долгоживущих плазматических клеток (LLPC), функциональная вирус-специфическая память B- и T-лимфоцитов также может быть ключом к защитной иммунной памяти.
Иммунитет к SARS-CoV-2 при бессимптомной коронавирусной инфекции
Несмотря на способность бессимптомных людей, избавившихся от SARS-CoV-2, эффективно контролировать инфекцию, была выдвинута гипотеза о снижении у них противовирусного адаптивного иммунного ответа. Эта гипотеза подтверждается в основном измерениями специфических антител к SARS-CoV-2 и количества В-клеток.
Антитела и Т-клетки действуют вместе, чтобы уменьшить распространение вируса в организме и уничтожить патоген. Однако защитный иммунный ответ может также запускать патологические процессы, характеризующиеся локализованными или системными воспалительными реакциями. Воспаление и повреждение тканей могут быть результатом уничтожения инфицированных клеток вирус-специфическими антителами и Т-клетками или высвобождения медиаторов воспаления, продуцируемых инфицированными клетками и активированными миелоидными клетками. В тяжелых случаях системные высокие уровни воспалительных цитокинов и активированных моноцитов сосуществуют с вирус-специфическими антителами и Т-клетками. Таким образом, остается открытым вопрос о том, вызывают ли вирус-специфические антитела и Т-клетки преимущественно защиту или повреждение.
Эффективность вирус-специфических Т-клеток в устранении патогенов зависит от тонкого баланса между их противовирусными и воспалительными свойствами. Т-клетки, специфические для SARS-CoV-2, у людей, избавившихся от инфекции SARS-CoV-2 без симптомов, могут проявлять непатологические, но защитные характеристики.
Сингапурские ученые сравнили количество и функцию Т-лимфоцитов, специфических для SARS-CoV-2, в группе бессимптомных лиц (85 человек) и пациентов с симптомами COVID-19 (76 человек) в разные моменты времени после образования антител. Участники были отобраны среди рабочих, которые проживали в густонаселенных общежитиях и сдавали кровь при приеме на работу.
Ученые количественно оценили Т-клетки, реактивные к вирусным белкам: N (нуклеокапсид), S (белок-шип) и M (мембрана вируса), и измерили величину секреции цитокинов: IL-2, IFN-γ, IL-4, IL-6, IL-1β, TNF-α и IL-10 в цельной крови после активации Т-клеток SARS-CoV-2.
Исследование показало, что:
Общая величина ответа Т-клеток против различных структурных белков одинакова как у бессимптомных лиц, так и у пациентов с COVID-19. Т-клетки, индуцированные бессимптомной инфекцией, по-видимому, секретируют большее количество IFN-γ и IL-2 и вызывают более скоординированное производство провоспалительных и регуляторных цитокинов, чем Т-клетки пациентов с симптомами COVID-19.
Таким образом, способность создавать значительный вирус-специфический Т-клеточный ответ не обязательно связана с серьезностью симптомов. Бессимптомные люди, инфицированные SARS-CoV-2, не характеризуются слабым противовирусным иммунитетом. Напротив, у них возникает устойчивый и высокофункциональный вирусоспецифический клеточный иммунный ответ, который защищает организм и не вызывает каких-либо явных патологий.