Что такое фцс в медицине
Исследование «всего тела» заключается в сканировании пациента от уха до верхней трети бедра. Т.е. в область исследования будут включены голова (частично, от козелка уха, без захвата головного мозга), шея, органы грудной полости, брюшной полости, малого таза и костная система (без верхних и нижних конечностей).
Сканирование нижних конечностей проводится за дополнительную плату.
Вопрос №2. Что такое радиофармпрепарат?
Радиофармпрепарат (РФП) – это соединение, состоящее из специального вещества и радионуклида (изотопа, радионуклидной метки). Специальное вещество отвечает за то, в каком органе накопится РФП, а радионуклидная метка позволяет врачу-диагносту увидеть это накопление на изображении.
В настоящее время для производства РФП используется очень широкий спектр как специальных веществ, так и радионуклидных меток. Во всем мире самым часто используемым у онкологических больных соединением специального вещества и радионуклидной метки является 18 F-фтордезоксиглюкоза ( 18 F-ФДГ). В данном соединении 18 F выполняет функцию радионуклидной метки, ФДГ – специального вещества.
Вопрос №3. Что такое физиологическое накопление РФП?
Физиологическое накопление (гиперфиксация) РФП – это повышенное накопление РФП, определяющееся в различных органах и системах в норме.
Физиологическое накопление наблюдается при исследованиях со всеми РФП: 18 F-ФДГ, 11 С-холином, 11 С-метионином, 68 Ga-ПСМА и т.д. В зависимости от типа РФП меняется лишь местоположение физиологической гиперфиксации. Например, при ПЭТ и ПЭТ/КТ с самой часто используемой 18 F-ФДГ физиологическое накопление РФП определяется в коре головного мозга, ротоглотке, носоглотке, мышцах гортаноглотки, миокарде левого желудочка, чашечно-лоханочных системах почек, фрагментарно по ходу петель толстой кишки, мочевом пузыре.
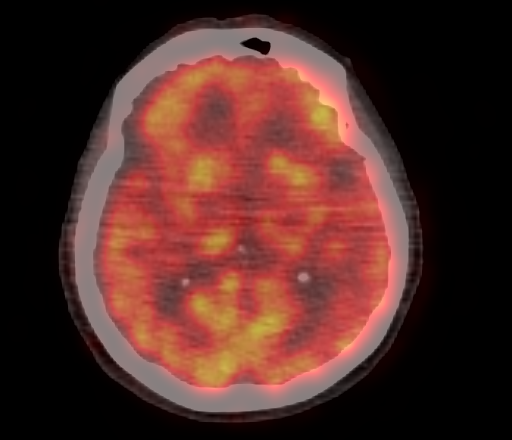 |  |
| Физиологическое накопление 18 F-ФДГ в коре головного мозга. | |
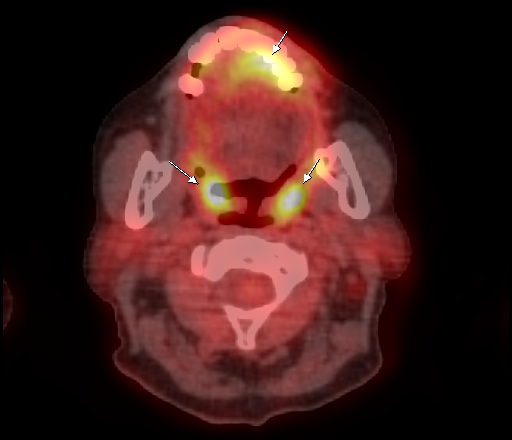 | 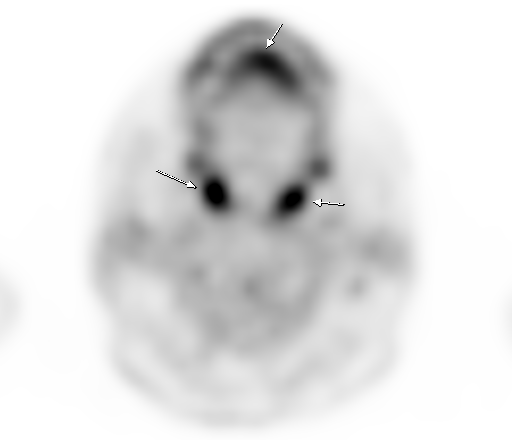 |
| Физиологическое накопление 18 F-ФДГ в ротоглотке. | |
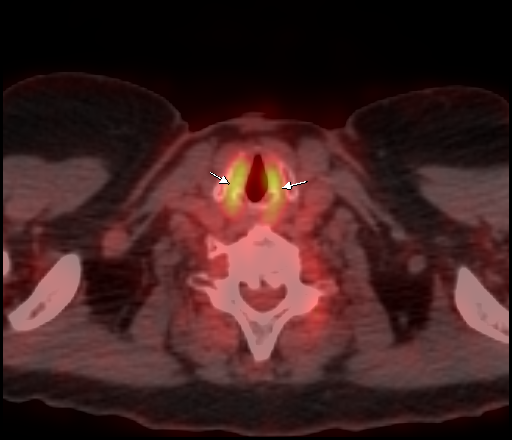 | 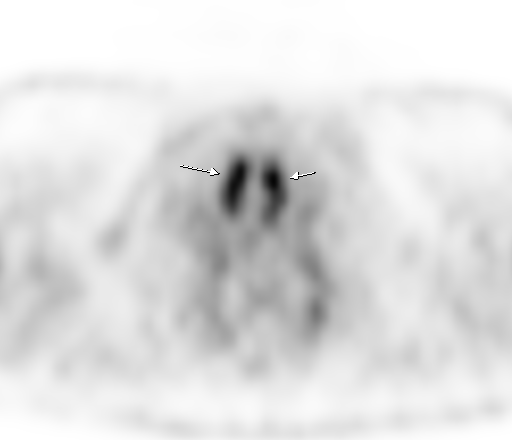 |
| Физиологическое накопление 18 F-ФДГ в мышцах гортаноглотки. | |
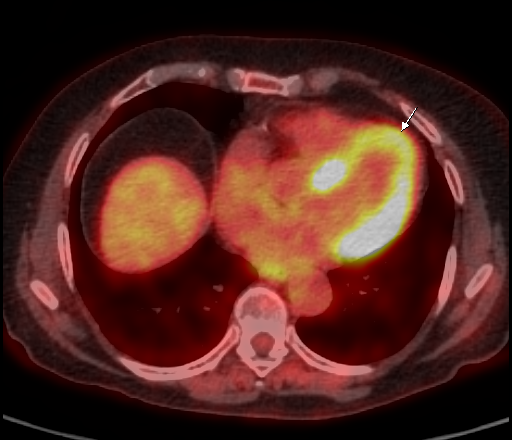 | 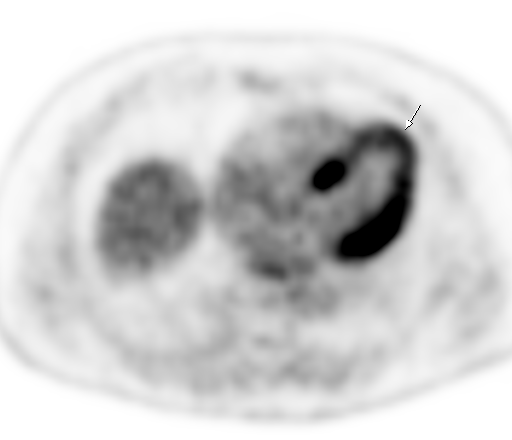 |
| Физиологическое накопление 18 F-ФДГ в миокарде левого желудочка. | |
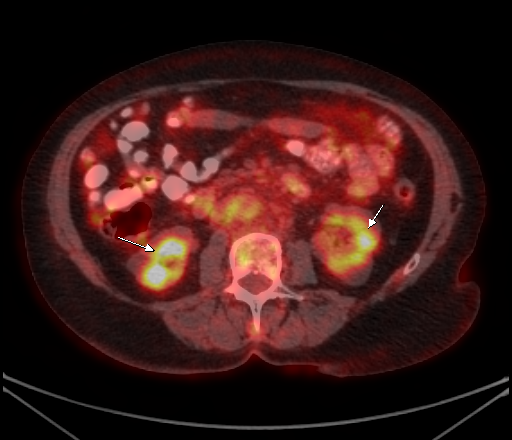 | 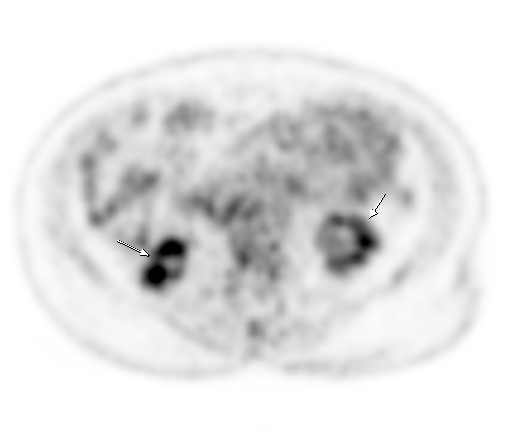 |
| Физиологическое накопление 18 F-ФДГ в чашечно-лоханочных системах почек. | |
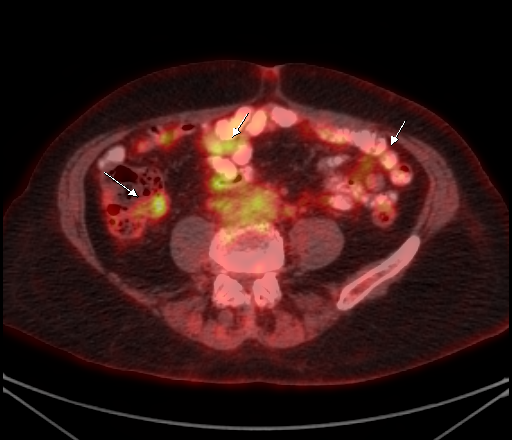 | 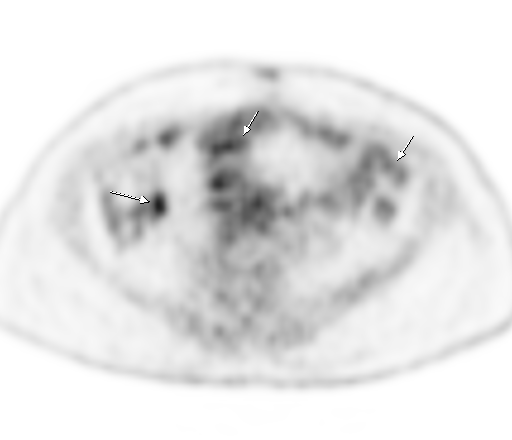 |
| Физиологическое накопление 18 F-ФДГ по ходу петель толстой кишки. | |
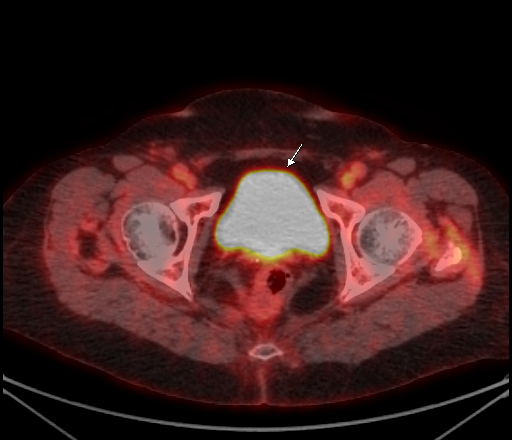 | 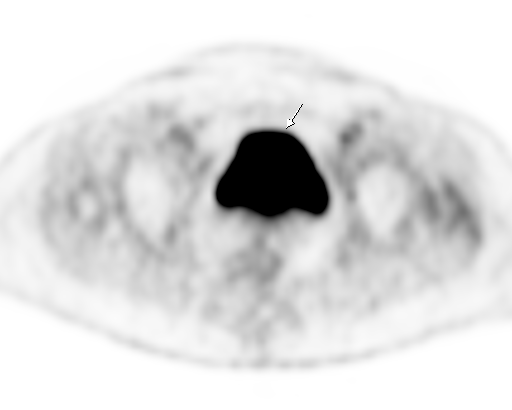 |
| Физиологическое накопление 18 F-ФДГ в мочевом пузыре. | |
Вопрос №4. Что такое патологическое накопление РФП?
Патологическое накопление РФП – это повышенное накопление РФП в органах и тканях, регистрирующееся при заболеваниях, чаще всего в злокачественных опухолях.
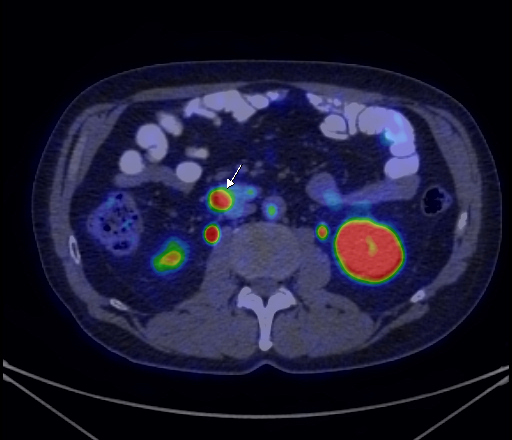 |
| Данные ПЭТ/КТ с 68 Ga-DOTA-TATE у пациента с нейроэндокринной опухолью тощей кишки. В проекции злокачественной опухоли, расположенной в тощей кишке, определяется очаг патологической гиперфиксации РФП. |
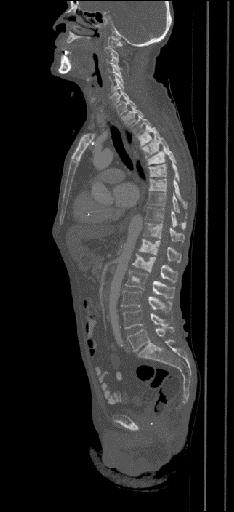 | 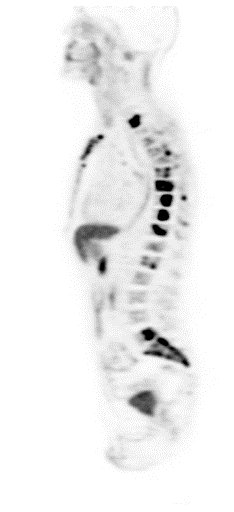 | 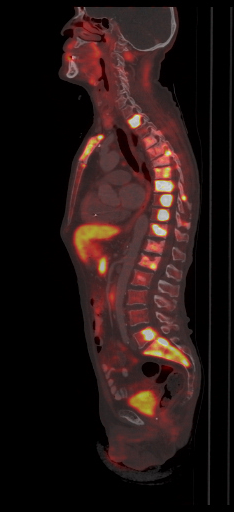 |
| Данные ПЭТ/КТ с 11 С-холином у пациента с раком предстательной железы. Состояние после простатэктомии. В костях скелета визуализируются множественные очаги патологического накопления РФП (метастазы). | ||
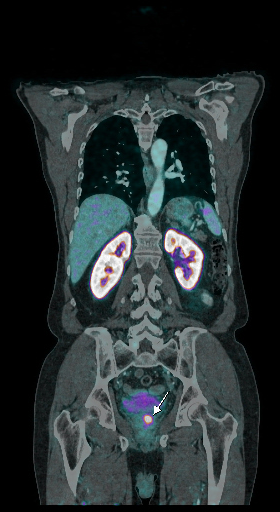 | 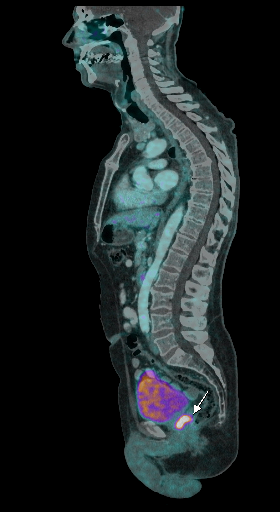 | 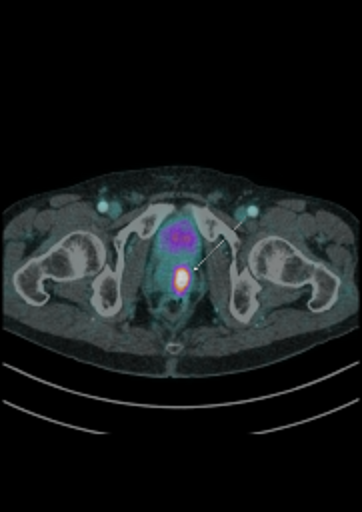 |
| Данные ПЭТ/КТ с 68 Ga-ПСМА у пациента с местным рецидивом рака предстательной железы. Состояние после лучевой терапии. В левых отделах предстательной железы определяется очаг патологического накопления РФП. | ||
Вопрос №5. Что такое метаболически активное и метаболически неактивное образование?
Метаболически неактивное образование – это образование, которое не накопило РФП. Чаще всего отсутствие повышенного накопления РФП в опухоли свидетельствует о ее доброкачественной природе.
Метаболически активное образование – это образование, в котором накопился РФП в повышенном количестве. Повышенное накопление РФП в опухоли чаще всего свидетельствует о ее злокачественном характере.
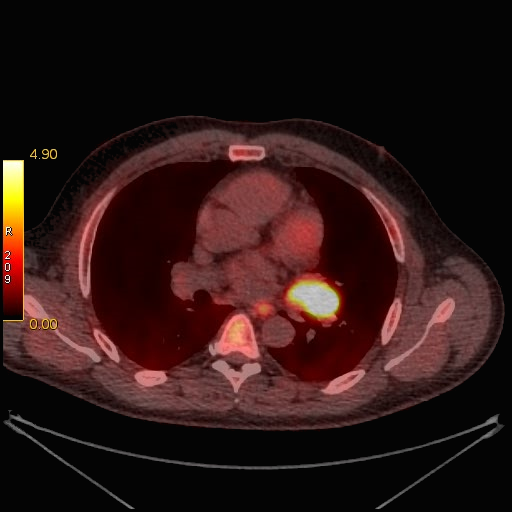 |
| Данные ПЭТ/КТ с 11 С-метионином у больного с метаболически активным образованием корня левого легкого (типичный карциноид). |
Вопрос №6. Что такое SUV?
SUV (Standardized Uptake Value, стандартизированный уровень захвата) – это величина, отражающая интенсивность накопления РФП в зоне интереса, например, в опухоли.
Показатель SUV рассчитывается программным комплексом автоматически и измеряется в различных единицах. В нашем Центре, как и в большинстве отечественных и зарубежных медицинских учреждений, где проводится позитронная эмиссионная томография, в качестве единиц измерения показателя SUV принято использовать г/мл (g/ml).
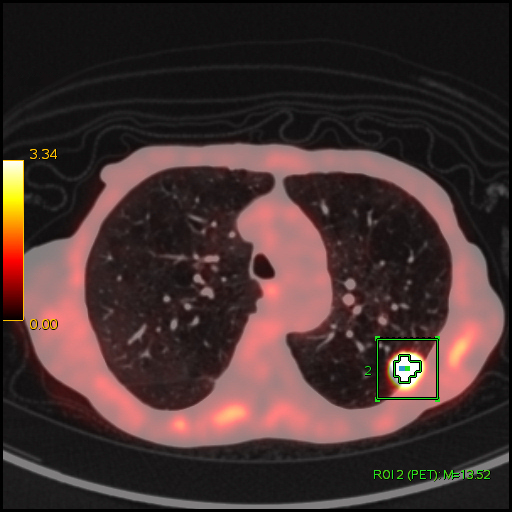 |
| Данные ПЭТ/КТ с 18 F-ФДГ. Оконтуривание метаболически активной злокачественной опухоли левого легкого для измерения показателя SUV. В данном случае величина SUV в опухоли определяется на уровне 13,52 g/ml. |
Вопрос №7. Для чего используется величина SUV?
Величина SUV в основном используется для оценки ответа злокачественной опухоли на проведенное лечение. Важно подчеркнуть, что в ряде клинических ситуаций показатель SUV в опухоли является единственным критерием, позволяющим оперативно получить информацию о чувствительности образования к только что начатой терапии.
Если опухоль чувствительна к лечению, то уровень SUV в ней при повторном ПЭТ-исследовании будет снижаться, если нечувствительна или малочувствительна (резистентна, устойчива) – значение SUV останется без изменений или увеличится. Следует помнить, что своевременная диагностика устойчивости опухоли к лечению позволит скорректировать план лечения, а в некоторых случаях и радикально его изменить.
Как уже было сказано выше, для оценки эффективности терапии врач-радиолог оценивает динамику показателя SUV до и после лечения.
Существует четыре варианта метаболического ответа опухоли на проведенное лечение:
Результаты ПЭТ с 18 F-ФДГ у пациента с диффузной В-клеточной крупноклеточной лимфомой до лечения (а), после 2 курса ПХТ (б) и через 13 месяцев после окончания терапии (в).
а – до лечения в средостении визуализируется массивное метаболически активное образование с уровнем SUV=12,6;
б – после 4 курса ПХТ отмечается значительное уменьшение метаболического объема опухоли и снижение показателя SUV до 3,4 (достигнут частичный метаболический ответ, т.е. опухоль чувствительна к выбранной ПХТ);
в – через 13 месяцев после окончания ПХТ очагов патологической гиперфиксации РФП в проекции органов средостения не обнаружено (достигнут полный метаболический ответ).
Гипервентиляционный синдром и дисфункциональное дыхание
Клинические особенности, диагностические критерии гипервентиляционного синдрома (ГВС) и дисфункционального дыхания (ДД) недостаточно знакомы широкому кругу врачей [1, 2, 3]. К одной из исторических вех, связанной с понятиями о функциональных нарушениях
Клинические особенности, диагностические критерии гипервентиляционного синдрома (ГВС) и дисфункционального дыхания (ДД) недостаточно знакомы широкому кругу врачей [1, 2, 3]. К одной из исторических вех, связанной с понятиями о функциональных нарушениях дыхания, относят 1871 год, когда Да Коста (Da Costa Jacob, 1833–1900), американский врач, принимавший участие в Гражданской войне США, применил термин «гипервентиляционый синдром» (ГВС) у пациентов с так называемым «солдатским сердцем». С тех пор для характеристики дыхательных расстройств предлагались различные альтернативные определения: «дыхательный невроз», «нейрореспираторная дистония», «респираторный синдром», «респираторная дискинезия», «идиопатическая гипервентиляция», «нейрореспираторный синдром», «неустойчивое дыхание» и др. Однако указанные термины не получили широкого признания. Они являются достаточно общими и не отражают особенностей нарушений дыхания у конкретного больного [4]. Перечисленные определения нередко связывают с понятием «непонятная одышка» (unexplained dyspnea).
ГВС встречается в 6–11% от числа пациентов общей практики. Соотношение мужчин и женщин составляет 1:4, 1:5; чаще наблюдается в 30–40 лет, но возможно развитие в других возрастных группах, включая детей и пожилых. L. Lum (1987) подчеркивал, что «каждый врач в течение недели может встретить хотя бы одного больного с ГВС». Врачи различных специальностей — невропатологи, кардиологи, пульмонологи, психиатры — могут наблюдать у своих пациентов явления гипервентиляции. Острое течение ГВС встречается значительно реже, чем хроническое, и составляет лишь 1–2% от общего числа больных [2, 6, 7].
Причины развития ГВС довольно многочисленны. Это неврологические и психические расстройства, вегетативные нарушения, болезни органов дыхания, некоторые заболевания сердечно-сосудистой системы, органов пищеварения, экзогенные и эндогенные интоксикации, лекарственные средства (салицилаты, метилксантины, β-агонисты, прогестерон) и др. Считается, что в 5% случаев ГВС имеет только органическую природу, в 60% случаев — только психогенную, в остальных — комбинации этих причин [6].
Важной особенностью развития ГВС является то обстоятельство, что если причины, являющиеся триггерными, устраняются, то гипервентиляция, которая уже не соответствует требованиям конкретной ситуации, сохраняется, сохраняется и гипокапния. Происходит стабилизация гипокапнических нарушений газообмена и формируется «порочный круг» ГВС, который начинает циркулировать автономно, и симптомы могут персистировать достаточно долго — феномен «махового колеса». Эти изменения реакции дыхания указывают на уязвимую систему контроля дыхания, которая не способна поддержать нормальное парциальное давление углекислого газа в крови (РСО2) и кислотно-щелочной гомеостаз [8, 9, 10, 11].
В основе развития клинических проявлений ГВС лежат гипокапнические нарушения газообмена [2, 3, 10]. Среди множества клинических проявлений ГВС одышка является ведущей жалобой и встречается практически в 100% случаев. Одышка может быть единственным клиническим проявлением, но чаще сочетается с другими симптомами.
Основные клинические проявления ГВС
Респираторные: одышка, вздохи, зевота, сухой кашель.
Общие: снижение трудоспособности, слабость, утомляемость, субфебрилитет.
Кардиальные: кардиалгия, экстрасистолия, тахикардия.
Психоэмоциональные: тревога, беспокойство, бессонница.
Гастроэнтерологические: дисфагия, боли в эпигастрии, сухость во рту, аэрофагия, запоры.
Неврологические: головокружение, обмороки, парестезии, тетания (редко).
Мышечные: мышечная боль, тремор.
Диагностика ГВС в первую очередь опирается на знание врачей самых различных специальностей об особенностях клинической картины ГВС. ГВС должен устанавливаться только после проведения дифференциальной диагностики с другими заболеваниями, протекающими с синдромом одышки. Полиморфизм клинических проявлений ГВС вызывает диагностические проблемы. Назначаются многочисленные обследования, дорогостоящие, ненужные, а иногда и опасные для больного. L. Lum (1987), обсуждая диагностические проблемы, называет среди врачебных ошибок бесполезные абдоминальные операции, операции на позвоночнике и других органах, инвазивные исследования, проводимые не без риска, и, что еще хуже, такие диагнозы, как эпилепсия и инфаркт миокарда. Взаимосвязи гипокапнии и ассоциированных с ней симптомов являются чрезвычайно сложными. Многие врачи при регистрации у больных низких значений РСО2 автоматически устанавливают диагноз ГВС, что является неправильным. Известно, что явления гипокапнии могут быть у больных рестриктивными легочными процессами, при лихорадочных состояниях, сердечной патологии, однако при этом «классических» гипокапнических жалоб может и не быть. И наоборот, так называемые гипокапнические жалобы, например тревога, одышка, парестезии и др., встречаются у пациентов с нормокапнией.
В практической медицине больной с ГВС — это пациент, предъявляющий жалобы на одышку, которая не соответствует данным объективного осмотра, показателям клинико-инструментальных исследований дыхания, с диспропорциональной, непонятной одышкой, субъективное восприятие которой является довольно тягостным. К сожалению, при отсутствии достоверных объяснений одышки больные обычно направляются для консультаций в различные лечебные учреждения. В конечном итоге они и формируют основной контингент альтернативной медицины, различных псевдоспециалистов «по тренировке правильного дыхания».
Исследование функции внешнего дыхания, имеющее важное значение в дифференциальной диагностике одышки, не помогает в верификации функциональных нарушений дыхания. Основным подтверждением ГВС служит выявление гипокапнических нарушений газообмена. Снижение РСО2 — прямое свидетельство альвеолярной гипервентиляции. Однако исходная гипокапния у больных с ГВС встречается не так часто. Поэтому в тех случаях, когда у пациента с предположительным ГВС в условиях покоя определяются нормальные значения углекислоты, рекомендуется определение изменений уровня СО2 при различных провокационных тестах. К «золотому стандарту» диагностики ГВС относят пробу с произвольной гипервентиляцией.
Департаментом пульмонологии университета г. Наймиген (Голландия) разработан Наймигенский опросник (Nijmegen questionnaire) для выявления физиологических показателей дизрегуляции вентиляции, сопоставимых с ГВС (табл.). Анкета содержит 16 пунктов, которые оцениваются по 5-балльной шкале (0 — никогда, 4 — очень часто). Минимальные и максимальные достижимые числа — 0 и 64 соответственно.
Данный опросник нашел свое применение прежде всего для скрининг-диагностики ГВС. Существует положение, согласно которому использование данного опросника позволяет корректно предсказывать ГВС в 90% от всех случаев [2, 12].
В последние годы в клиническую практику начинает внедряться понятие «дисфункциональное дыхание» (ДД). Приоритет внедрения термина принадлежит Ван Диксхорну (J. van Dixhoorn), который привел его в работе Hyperventilation and dysfunctional breathing (1997). Основанием для этого явилось понимание, что при функциональных нарушениях дыхания возможны различные изменения паттерна дыхания и значений РCO2, а не только гипокапнические расстройства, характерные для ГВС. ДД может проявляться также быстрым, аритмичным, поверхностным дыханием, частыми вздохами, преобладанием грудного типа дыхания.
Одной из сложных и дискуссионных проблем в пульмонологии является понимание взаимоотношений ГВС, ДД и бронхиальной астмы (БА) [15–18]. С. И. Овчаренко и др. (2002) у 22 из 80 больных БА выявили нарушения дыхания, соответствующие критериям ГВС. Сведений относительно встречаемости дисфункциональных нарушений дыхания при астме немного. Установлено, что среди лиц с диагнозом БА и по крайней мере с одним предписанием антиастматического препарата 29% имеют клинические признаки ДД [19]. Указывается, что ДД может усиливать симптомы БА и приводить к избыточному назначению лекарств.
Достаточно сложным является понимание механизмов развития дисфункциональных расстройств дыхания при БА; существует ряд предположений. К достаточно обоснованным факторам развития гипервентиляции относят тревожные расстройства. Использование больными бронходилататоров (β-2-агонисты, теофиллин), которые обладают эффектами стимуляции дыхания, также относят к факторам развития гипервентиляции. Обсуждается роль изменений перцепции одышки при БА. Анализ существующих проблем взаимосвязи ДД и БА провел M. Morgan (2002), представив следующие ключевые положения:
В зависимости от установления особенностей ДД должна осуществляться и программа лечения больных. При выявлении ГВС релаксирующие методы дыхательной гимнастики проводятся под руководством опытных инструкторов, назначаются β-адреноблокаторы, бензодиазепины [5, 22, 23]. При явлениях гиповентиляции — массаж дыхательных мышц, использование дыхательных тренажеров. Выявление ГВС при БА указывает на необходимость применения методов коррекции функциональных нарушений дыхания. Релаксирующие дыхательные упражнения за счет неспецифических механизмов дыхательного тренинга улучшают качество жизни у этих больных.
По вопросам литературы обращайтесь в редакцию.
В. Н. Абросимов, доктор медицинских наук, профессор
Рязанский ГМУ им. акад. И. П. Павлова, Рязань
Нарушение ритма сердца и проводимости (аритмии сердца)
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Практически у 80% пациентов с ишемической болезнью сердца регистрируются аритмии различного характера и до 65% из них угрожают жизни. НРС могут быть самостоятельными или являться осложнением заболеваний сердечно-сосудистой системы и других органов и систем
С учетом частоты сердечных сокращений их можно подразделить на две большие группы:
1. Брадиаритмии:
2. Тахиаритмии:
Важно отличать нарушения ритма сердца, вызванные органическим (необратимым) поражением миокарда, и функциональные нарушения. Как правило, функциональные нарушения встречаются при здоровом сердце и могут быть вызваны психогенными, рефлекторными и гуморальными расстройствами. Функциональные нарушения ритма сердца встречаются достаточно часто, важно выявить и исключить вызывающие их причины, что позволит избавить человека от аритмии.
Органические нарушения возникают при: коронарной ишемии, гемодинамических пороках сердца и крупных сосудов, сердечной недостаточности, гипертонии. Они могут появляться при токсическом воздействии (медикаментозных препаратов, алкоголя и др.) или инфекционно токсическом (ревматизм, вирусные инфекции, миокардиты различной этиологии и др.), гормональных сдвигах. Аритмии бывают врожденные (синдром WPW, врожденная АВ блокада и др.) и приобретенными, вызванные внешними воздействиями (миокардит,операции и травмы сердца и др.).
Основные симптомы (проявления аритмий)
Брадиаритмии:
Тахиаритмии:
Обычно диагностика аритмий осуществляется врачом поликлиники, кардиологом или врачом скорой помощи. Имеет значение сбор анамнеза, физикальное обследование, и различные инструментально-диагностические методы. Наиболее важным является регистрация НРС на ЭКГ (для предъявления аритмологу).
На сегодняшний день в специализированных или многопрофильных клиниках пациентов консультирует врач кардиохирург-аритмолог и определяет необходимость и возможность эндоваскулярного интервенционного (малотравматичного) лечения нарушения ритма сердца. В нашей Клинике есть все необходимые ресурсы для диагностики и лечения аритмий
К методам диагностики нарушения ритма сердца относят:
Тилт-тест – проба с пассивным ортостазом. Проводится на специальном поворотном столе. Позволят выявить или исключить связь между развитием обморочных состояний и нарушениями сердечного ритма.
Лечение аритмий: хирургическая коррекция нарушений ритма сердца
В нашей Клинике выбор способа лечения нарушения ритма сердца осуществляется специа-листом с учетом клинической картины заболевания, данных инструментально-диагностических исследований и рекомендаций Российского кардиологического обще-ства, Всероссийского научного общества аритмологов.
Самостоятельный прием препаратов, самолечение различными методами является крайне не желательным и не безопасным, если неизвестен и не учитывается характер, механизм и причина аритмии.
Существует несколько способов лечения нарушения ритма сердца:
Операция выполняется под местной анестезией в условиях рентгеноперационной длительностью до 40-55 минут.
Эффективным и радикальным методом лечения тахиаритмий является катетерная аблация (деструкция) очага аритмии. Операция, в среднем, длится не более 1 часа, и через сутки пациент может быть выписан из стационара.
Что такое фцс в медицине
Понятие пациент-ориентированного подхода появилось достаточно недавно. Безусловно, данный подход произрастает из недр клиент-ориентированного подхода, только с той разницей, что в данном случае клиентом (конечным потребителем) является пациент (клиент медицинской организации), а услуга является медицинской. Это вносит в формирование подхода существенные особенности. Приравнивать клиент-ориентированный подход к пациент-ориентированному, конечно, нельзя, хотя стоит заметить, что принципы формирования их, безусловно, едины. Формируя услугу и выводя ее на рынок, необходимо понимать, что ключевым будет конгруэнтность покупательской (потребительской) способности и предлагаемой модели услуг [1]. Продукт (услуга) должен прежде всего соответствовать ожиданиям потребителя. Необходимо выстраивать гибкую систему взаимодействия (работы) с клиентами и своевременно менять условия предоставления услуг в случае изменения потребностей и желаний конечного потребителя. Создание комфортных эмоционально-психологических условий и соучастие в поиске решений для клиента – это базовые принципы наряду со стремлением постоянно совершенствоваться и изменяться к лучшему в отношении производства продукта (услуги) [2]. Особенности пациент-ориентированного подхода заключаются в том, что на основе клиент-ориентированности необходимо создать инновационный подход к планированию, проведению, оценке и контролю медицинской помощи, которая базируется на партнерских и взаимовыгодных принципах сотрудничества между пациентом и его ближайшим окружением (семья) с медицинской организацией в лице административного, врачебного, сестринского и обеспечивающего персонала [3; 4].
Принципы пациент-ориентированного подхода
1. Первый принцип пациент-ориентированности заключается в уважении потребительских ценностей, потребностей и предпочтений. Рассматривая принцип «уважительного отношения к пациенту», можно говорить, что данный аспект отражается в обеспечении прав граждан в сфере оказания медицинской помощи. Помимо этого, ставится во главу угла приоритет интересов пациента.
2. Второй принцип – целостность, логичность и преемственность лечебно-диагностического процесса. Надо понимать, что пациенты в данном аспекте являются уязвимым звеном. Болезнь, которая снижает качество жизни пациента, окрашивает в негативные краски психоэмоциональный фон настроения. Пациент, видя согласованность действий со стороны медицинских работников, вселяет в себя надежду на скорейшее выздоровление.
3. Третий принцип – информированность пациента обо всех деталях лечебно-диагностического процесса, о ходе медико-социальной реабилитации и т.д. Этот принцип достаточно широкий и охватывает много аспектов. Так, пациент по желанию должен иметь доступ к информации о своем заболевании, о клиническом состоянии, о вариантах лечения, а также о методах профилактики.
4. Четвертый принцип – создание комфортных условий пребывания пациента в процессе оказания ему медицинской помощи на всех этапах: в амбулаторно-поликлиническом учреждении, в стационаре, в отделениях реабилитации и т.д.
5. Пятый принцип – обеспечение эмоциональной поддержки в отношении пациента. В реализации данного принципа медицинский работник должен учитывать такие факторы, как обеспокоенность пациента по поводу своего состояния, а также исхода заболевания. Надо учитывать, что пациенты могут испытывать тревогу из-за возможных последствий болезни (инвалидизация, финансовая несостоятельность, потеря работы, проблемы в семье).
6. Шестой принцип – создание условий общения пациента с его ближайшим окружением. Следует уделять внимание уровню субъективного комфорта пациента, по возможности обеспечивать всестороннюю поддержку, не ограничивать его в общении с родственниками, коллегами, друзьями.
7. Седьмой принцип – обеспечение непрерывности лечебного процесса, а также оправдание ожиданий в части его видоизменения со временем. Для обеспечения этого принципа прежде всего надо доносить подробную информацию о лекарственных препаратах, ограничениях, диетах в доступной для пациента форме.
8. Восьмой принцип является базовым и формирующим все предыдущие принципы. Он заключается в надлежащем обеспечении доступности медицинской помощи для потенциального пациента. Это физическая доступность к медицинской организации, наличие общественного транспорта, возможность беспрепятственной записи на прием к врачу, возможность выбора врача, методики лечения.
Внедрение пациент-ориентированного подхода
Один из первых шагов во внедрении пациент-ориентированного подхода при оказании медицинской помощи населению – это необходимость знать мнение пациентов о качестве и доступности оказываемых им медицинских услуг [8]. Самый простой способ – это опрос пациентов «на выходе». Прежде всего, необходимо поменять модель взаимодействия в структуре взаимодействия с пациентом как конечным и ключевым потребителем медицинской услуги [9; 10]. Необходимо задавать вопрос «Что бы Вы хотели улучшить в работе медицинской организации?», а не «Что случилось у Вас при посещении медицинской организации?». При этом надо понимать, что отслеживание настроений и ожиданий пациентов ложится не на плечи медицинских работников (врачебный и/или средний медицинский персонал), а на обеспечивающий персонал по данному направлению. Медицинский персонал обеспечивает основной поток ценностей организации, и пациент-ориентированность в их отношении лежит в области этики и деонтологии медицинской деятельности, степени эмпатии и т.д. [11].
Можно говорить о трёхуровневой системе (структуре) пациент-ориентированного здравоохранения. На микроуровне ключевым является модель взаимоотношений «врач – пациент», на среднем уровне – «медицинская организация – пациент», на макроуровне – «национальная система здравоохранения – пациент». При этом в сбалансированной системе здравоохранения основой в этой структуре является модель «врач – пациент». Она является «материнской платформой» (базовым неделимым элементом) для формирования модели «медицинская организация – пациент». В свою очередь, модель «медицинская организация – пациент» является базовым элементом для модели макроуровня [12]. В несбалансированной системе здравоохранения одна из моделей может преобладать на фоне деградации других моделей. Так, например, при гипертрофии модели «врач – пациент», которая преобладает в кризисные ситуации (при разрушении национальной системы здравоохранения), формируется частный децентрализованный сектор медицинских организаций. При увеличении роли государства и централизации системы здравоохранения, бюрократизации и формализации лечебно-диагностического процесса происходит деградация модели «врач – пациент». При этом при увеличении доли государства в формировании национальной системы здравоохранения, при отсутствии эффективных инструментов управления (процессно-ориентированный подход в управлении медицинской организацией, внедрение бережливых технологий на рабочих местах) и контроля (независимые профессиональные союзы, ассоциации и т.д.), происходит монополизация рынка медицинских слуг и уничтожение конкурентных взаимоотношений [13]. Отсутствие конкуренции на рынке медицинских услуг пагубно сказывается как для медицинских работников, так в итоге и для пациентов. Для медицинского персонала в данной ситуации ключевым критерием профессиональной состоятельности становится не уровень и широта компетенций, а лояльность к работодателю. Для пациентов – это прежде всего падение качества медицинских услуг [14; 15].
Внедрению пациент-ориентированного подхода в оказании медицинских услуг могут препятствовать ряд факторов. Прежде всего, это система профессиональной организации труда медицинских работников. Здесь одним из ключевых факторов является негибкая система оплаты труда. В настоящее время, несмотря на введение эффективных критериев оценки труда сотрудников, утвержденная система, по сути, не учитывает качества оказываемых медицинских услуг (за исключением формальных критериев). Привязка количества обслуживаемых пациентов к оценке качества оказанных услуг и уровню оплаты труда является не эффективной в долгосрочной перспективе [16]. Такой подход может привести в формальной оценке труда медицинских работников без корреляции с показателями здоровья обслуживаемого населения. Зачастую врач может стремиться (если речь идет о корреляции между уровнем оплаты труда и количеством пациентов) к увеличению базы пациентов. Тем самым сокращается время, затрачиваемое на каждого пациента в отдельности. Такой подход неминуемо приведет к падению качества медицинских услуг, профессиональному выгоранию и деградации модели «врач – пациент» [17].
Одним из примеров привязки уровня оплаты врача к количеству пациентов могут служить данные социологического опроса медицинских сотрудников, проведённого Ernst&Young Russia в 20 тыс. медицинских организациях государственного и частного сектора в 2015 г. Так, более 45 % организаций сообщили о том, что уровень оплаты труда сотрудников зависит напрямую от выполнения плана по количеству пациентов. В этих организациях введена прогрессивная шкала заработной платы в зависимости от суммы выручки организации. В то же время 55 % опрошенных заявили, что их цель – это эффективное лечение пациентов, и считают привязку размера зарплаты к прибыли организации пагубной. По мнению А.З. Столпнера, привязка заработной платы врача к выручке может повлиять на необоснованные с медицинской точки зрения назначения (лечебно-диагностические процедуры и т.д.). По его мнению, практика доплаты за дополнительные назначения врачу широко распространена в настоящее время в столичных медицинских организациях. Он настаивает на том, что упор на качество лечения заставляет пациента возвращаться именно в эту клинику и приводить туда своих родственников и знакомых, тем самым повышая уровень доверия к медицинской организации. Стоит заметить, что в данном подходе главная цель – это повышение уровня доверия к бренду (brand loyalty) [14].
По мнению James Alan Robinson, профессора University of Chicago, одного из ведущих специалистов в области политики и менеджмента в сфере здравоохранения, все три существующие модели оплаты труда в системе здравоохранения (оплата за отдельно взятые услуги, подушевое финансирование, фиксированные ставки оплаты труда) не являются совершенными. Он заявляет, что «оплата за услуги поощряет оказание нецелесообразных услуг, мошенническое накручивание посещений и процедур и бесконечное перенаправление пациентов от одного специалиста к другому», «подушевая оплата поощряет отказ в предоставлении нужных услуг, отказ от хронических больных и сужение объема работы при отбрасывании пациентов, требующих много времени», «окладная система подрывает продуктивность, поощряет отдых на рабочем месте и насаждает бюрократическую ментальность, в которой любая процедура – еще чья-то проблема» [18; 19].
Комплаентность и лояльность пациентов
Ключевой базовый принцип пациент-ориентированного подхода – это повышение комплаентности (patient compliance) и лояльности пациентов (patient loyalty). В данном аспекте стоит различать эти два понятия, хотя с лингвистической точки зрения они, безусловно, являются синонимичными. Разделение этих понятий при формировании пациент-ориентированного подхода необходимо ввиду различной функциональной значимости (нагрузки) этих определений. Приверженность к следованию назначенного лечения (adherence to therapy), а также выполнению требований врача по соблюдению лечебно-охранительного режима отражает личное отношение в системе «врач – пациент». Но этот фактор определяется уровнем доверия пациента к компетенции врача, его уровню профессиональной подготовки (квалификации). По мнению I.E. Leppik, категория «приверженности» включает в себя несколько компонентов: поведенческий компонент (пациента), его нацеленность на результат, а также степень возможности (условий) выполнения назначений. На практике уровень «приверженности» обычно измеряется правильностью или неправильностью выполнения медикаментозных назначений (следование назначенным дозам, соблюдение временного интервала и т.д.). Если пациент принимает лекарственное средство в дозе, составляющей 80–120 % от назначения, то уровень «приверженности» можно расценивать как высокий. Помимо прямых оценок «приверженности», существуют и косвенные (непрямые) методы определения уровня данного показателя. К ним можно отнести количество использованных/оставшихся таблеток, анкетирование, проверку записей (дневников) пациентов и т.д. [20].
Что касается «лояльности» пациента, то целесообразнее ее рассматривать в модели «медицинская организация – пациент». Данный показатель отражает как степень доверия пациента к конкретной медицинской организации (к юридическому лицу, к учреждению), так и к системе оказания медицинской помощи в целом. Например, доверие к частной или государственной системе здравоохранения или к системе «платной» или «бесплатной» медицины. Так, согласно данным агентства BusinesStat, в 2019 г. более 27,0 % жителей Москвы и Московской области обращались за услугами частных медицинских организаций. Высокий показатель ( %) обращаемости в коммерческие клиники на фоне развитой сети государственных учреждений здравоохранения говорит прежде всего о степени доверия респондентов. Ключевыми причинами явились в 35,2 % случаев – высокая профессиональная составляющая врачей, по мнению респондентов, в 34,5 % – высокая результативность назначенных схем и процедур. При этом 56,4 % опрошенных шли на прием к конкретному врачу (фактор приверженности модели «врач – пациент»). На фактор приверженности в модели «медицинская организация – пациент», по мнению 21,4 % респондентов, повлиял хороший уровень организации медицинской помощи (оперативность, полнота охвата и т.д.). Помимо медицинских организаций, в круг субъектов мотивационной модели «медицинская организация – пациент» может быть включена и страховая компания. Но этот аспект играет роль исключительно в частном секторе. Что касается государственного сектора здравоохранения, согласно опросу, доверие к врачу (42,4 %) значительно ниже, чем доверие к медицинской организации (76,9 %) в целом (или к системе государственного здравоохранения). Это обусловлено главным образом тем, что наряду с признанием низкой квалификации врачей в госсекторе, респондентами осознается «всеобщий» охват государственных гарантий в системе ОМС и возможность «получить» дорогостоящие методы лечения и обследования при наличии показаний. Омрачает эту картину, по мнению 79,9 % респондентов, высокий уровень «бюрократизации» государственной система оказания медицинской помощи. В то же время в частном секторе доверие к врачу значительно выше, чем к коммерческой организации в целом. Это обусловлено тем, что большинство опрошенных (65,5 %) считают, что руководство таких организаций ставит цель получения прибыли на порядок выше, чем оказание качественной медицинской помощи [16].
При формировании пациент-ориентированного управления в медицинской организации необходимо руководствоваться в принятии решений прежде всего интересами пациента (клиента). Главной целью является повышение уровня доверия пациента к врачу и к медицинской организации в целом. Взаимодействие в данной системе осуществляется на взаимовыгодных условиях и партнёрских отношениях, что должно отражаться на планировании и реализации медицинских услуг населению. Для оценки деятельности медицинской организации и системы здравоохранения в целом необходимо учитывать мнение граждан о системе контроля качества медицинских услуг и результативности/эффективности менеджмента [20; 21]. Учредитель медицинской организации должен регулярно инициировать проведение независимого опроса прикрепленных пациентов, что должно стать основой для планирования объема и вида медицинских услуг. Внедрение пациент-ориентированного подхода при надлежащей имплементации ведет, прежде всего, к повышению обращаемости населения, приверженности к лечению, что, в свою очередь, отразится на показателях выявляемости заболеваний, длительности ремиссий, снижения уровня заболеваемости, а также на более широком охвате населения профилактическими мероприятиями [22].
