Наверное, многие слышали термин «очищение крови». Нозачем, как иотчего еечистить— вопрос неочевидный. Попробуем разобраться вместе. Воснове этой инновационной области медицины лечит наука трансфузиология— изучающая воздействие накровь или еекомпоненты сцелью лечения различных заболеваний. Кстати, экспериментировать спереливанием крови медики начали еще в17веке, пробуя переливать кровь отживотного кживотному иотживотного кчеловеку. Нолишь в19веке трансфузиология начинает широко применяться вмедицине. Пионером трансфузиологии считают Джеймса Бланделла, британского акушера, который провел первое удачное переливание человеческой крови пациентке спослеродовым кровотечением. Когда-то переливание крови применяли исключительно для спасения жизни, носегодня все чаще ичаще мыслышим очудодейственных методах лечения серьезных аутоиммунных заболеваний методами очищения крови— по-научному, эта область медицины называется экстракорпоральной гемокоррекцией (потому что очищение крови происходит вне организма человека) или гравитационной хирургией крови. Вторая область применения этих высокотехнологических методов— радикальное омоложение организма. Вовремя процедур гемокоррекции специальный аппарат разделяет кровь наклетки иплазму. Плазма крови проходит через специальный фильтр, вкотором остаются болезнетворные вещества ивирусы. Затем «очищенная» плазма соединяется склетками крови ивозвращается пациенту.
Например, при лечении аутоимунных заболеваний изплазмы производится удаление аутоантител, циркулирующих иммунных комплексов, провоспалительных цитокинов иряда других веществ, поражающих собственные ткани. Улучшение качества жизни наступает вследствие быстрого купирования обострения иоптимизации течения аутоиммунного процесса: снижение частоты иинтенсивности обострений.
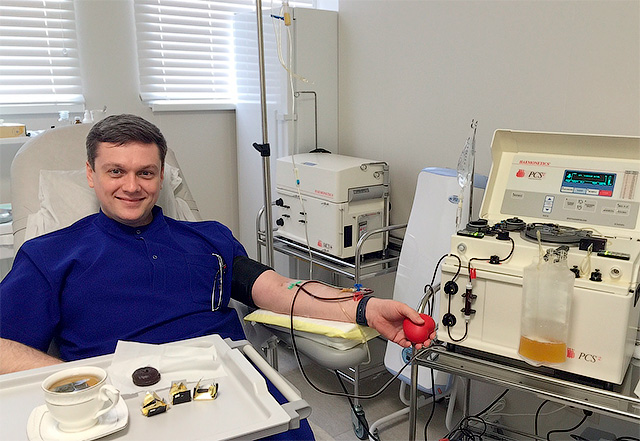
Для пациента важно, что процедуры гемокоррекции абсолютно комфортны. Вовремя сеанса ввену пациента вводится игла. Онсидит вкресле иможет вэто время читать журналы, книги, разговаривать потелефону, смотреть телевизор, слушать музыку ит.д. После завершения процедуры пациент покидает кабинет сзабинтованной рукой; повязку обычно необходимо держать неменее 6часов. Количество ипериодичность процедур определяет врач всоответствии споказаниями. Безопасность гравитационной хирургии позволяет лечить пациентов ослабленных, пожилых — в любых случаях, когда традиционное лечение медикаментами не приносит желаемого результата или противопоказано из-за осложнений.
Пять важных фактов о гемокоррекции, если Вы впервые услышали об этом методе:
Чурсин В.В. Трансфузионная терапия при острой массивной кровопотере (методические рекомендации)
Информация
Список сокращений
Введение
Тактика интенсивной терапии при острой массивной кровопотере
Всё это верно при единственном условии – достаточный газообмен в лёгких. Это, в свою очередь, при корректной ИВЛ и отсутствии органических поражений лёгких, будет зависеть только от перфузии лёгких.
Таким образом, всё зацикливается на достаточной перфузии в малом и большом кругах кровообращения. От чего же зависит перфузия? Основных фактора два: производительность сердца и сосудистый тонус.
Механизм компенсации острой кровопотери общеизвестен: при уменьшении ОЦК происходит, в первую очередь, уменьшение ёмкости венозной системы (1 этап), что поддерживает преднагрузку на достаточном уровне. Далее, при увеличении концентрации катехоламинов, спазмируются артериолы (2 этап) и развивается централизация кровообращения (3 этап), характеризующаяся генерализованным спазмом сосудов, за исключением сосудов мозга и лёгких, а также коронарных артерий.
Если в этот момент не помочь организму, то защитная реакция переходит в патологическую. Причин тому несколько: резко повышается нагрузка на миокард вследствие увеличения постнагрузки, развивается ишемия в органах и тканях, принесённых в жертву ради спасения мозга, нарушается гуморальная регуляция из-за метаболической интоксикации и выброса биологически активных веществ из повреждённых и ишемизированных тканей и т.д. В итоге, организм, спасая одно, губит всё.
Коагулопатии
Гемостатики
Этамзилат (Дицинон). Препарат увеличивает образование в стенках капилляров мукополисахаридов большой молекулярной массы и повышает устойчивость капилляров, нормализует их проницаемость при патологических процессах, улучшает микроциркуляцию. снижает время кровотечения. Стимулирует физиологические механизмы свертывающей системы крови, уменьшая время кровотечения и увеличивая чиcло тромбоцитов, их активность и период жизни в кровяном русле. Его действие проявляется в значительном статистическом уменьшении времени кровотечения, а также в умеренном увеличении числа тромбоцитов. Оказывает гемостатическое действие, которое обусловлено активацией формирования тромбопластина в месте повреждения мелких сосудов.
Препарат стимулирует образование фактора свертывания крови III, нормализует адгезию тромбоцитов. Препарат не влияет на протромбиновое время, не обладает гиперкоагуляционными свойствами и не способствует образованию тромбов.
Транексамовая кислота относится к синтетическим ингибиторам фибринолиза и, вследствие своего структурного сходства с лизином, способна по конкурентному типу блокировать процесс активации плазминогена, предупреждая лизис тромба в зоне повреждения сосуда. Следовательно, этот препарат, как и другие ингибиторы фибринолиза теоретически целесообразно использовать для остановки кровотечения, связанного с первичной системной или местной активацией фибринолиза.
На практике, однако, выполнение этого правила представляет серьезную проблему, поскольку предполагает необходимость лабораторно и визуально подтвердить показания к назначению препарата и исключить другие возможные причины кровотечения. Более того, при диссеминированном сосудистом свертывании крови или в случае массивного кровотечения, вызвавшего системное повышение гемостатического потенциала в комплексе с гиповолемией и гиподинамией кровообращения, целенаправленное стремление блокировать фибринолиз может оказаться опасным, а введение ингибиторов – усилить нарушения микроциркуляции и ишемию внутренних органов, повысить риск артериальных и венозных тромбозов. Такая точка зрения хорошо известна. Она основана на современных представлениях о механизмах тромбообразования и фибринолиза, и, в целом, является ответом на вопрос о том, почему, несмотря на явный гемостатический эффект введения ингибиторов фибринолиза, во многих клинических ситуациях использование этих препаратов в плановой хирургии остается довольном редким явлением.
Другой целью систематического обзора, выполненного ассоциацией Кохрана было сравнительное изучение эффективности трех наиболее широко используемых в мировой клинической практике ингибиторов фибринолиза: апротинина, эпсилон-аминокапроновой кислоты и транексамовой кислоты. В сравнительных исследованиях этих препаратов некоторые преимущества были отмечены у апротинина, однако статистически значимыми они оказались только для определенной группы кардиохирургических больных с высоким риском. В остальных областях хирургии достоверных отличий по эффективности ТСК и апротинина не выявлено, при этом, однако установлено, что по антифибринолитической активности транексамовая кислота значительно превосходит эпсилон-аминокапроновую кислоту.
Таким образом, учитывая отличия в стоимости препаратов, по показателю «цена – эффект» использование ТСК во многих клинических ситуациях может быть наиболее перспективным. Например, это может касаться операции тотального протезирования коленного сустава – вмешательства, при котором целесообразность применения ТСК можно считать наиболее обоснованным.
Алгоритм проведения гемотрансфузии
Правила клинического использования донорской крови и (или)ее компонентов.
Трудноопределимые группы крови
Неспецифическая агглютинация наблюдается при аутоиммунной гемолитической анемии и других аутоиммунных заболеваниях, сопровождающихся адсорбцией аутоантител на эритроцитах, при гемолитической болезни новорожденных, эритроциты которых нагружены аллоантителами матери.
Кровяные химеры. Кровяными химерами называют одновременное пребывание в кровяном русле двух популяций эритроцитов, отличающихся по группе крови и другим антигенам.
Трансфузионные химеры возникают в результате многократного переливания эритроцитной массы или взвеси группы 0 (I) реципиентам другой группы. Истинные химеры встречаются у гетерозиготных близнецов, а также после пересадки аллогенного костного мозга.
Другие особенности. Определение группы крови АВ0 и резус принадлежности может быть затруднено у больных в связи с изменением свойств эритроцитов при различных патологических состояниях (у больных циррозом печени, при ожогах, сепсисе).
Проба на совместимость на плоскости при комнатной температуре
для проведения проб на индивидуальную совместимось используется кровь ( сыворотка) больного, взятая перед трансфузией или не более чем за 24 часа, при условии хранения при температуре +4+2°С.
Проба на совместимость с применением 33%полиглюкина
В пробирку вносят 2 капли (0, 1 мл) сыворотки реципиента 1 каплю (0, 05) мл эритроцитов донора и добавляют 1 каплю (0, 1 мл) 33% полиглюкина.
Пробирку наклоняют до горизонтального положения, слегка потряхивая, затем медленно вращают таким образом, чтобы содержимое ее растеклось по стенкам тонким слоем. Контакт эритроцитов с сывороткой больного при вращении пробирки следует продолжать не менее 3 мин.
Результат учитывают, просматривая пробирки на свет невооруженным глазом или через лупу. Агглютинация эритроцитов свидетельствует о том, что кровь реципиента и донора несовместимы, отсутствие агглютинации является показателем совместимости крови донора и реципиента.
Ошибочный порядок расположения реагентов.
Температурные условия (определение группы крови производят при температуре не ниже 15°Си не выше 25°С)
Соотношение реагентов и исследуемых эритроцитов.
Продолжительность наблюдения. (позволяет выявить слабый агглютиноген А_2, характеризующийся замедленной агглютинацией)
Биологическую пробу проводят независимо от объема гемотрансфузионной среды и скорости ее введения.
При необходимости переливания нескольких доз компонентов крови биологическую пробу проводят перед началом переливания каждой новой дозы.
в течение 3 мин наблюдают за реципиентом, контролируя у него пульс, дыхание, артериальное давление, общее состояние, цвет кожи, измеряют температуру тела
такую процедуру повторяют еще дважды. Появление в этот период даже одного из таких клинических симптомов, как озноб, боли в пояснице, чувство жара и стеснения в груди, головной боли, тошноты или рвоты, требует немедленного прекращения трансфузии и отказа от переливания данной трансфузионной среды.
Экстренность трансфузии компонентов крови не освобождает от выполнения биологической пробы.
Врач, проводящий переливание компонентов крови обязан:
1.Определить показания для проведения гемотрансфузионной терапии с учетом противопоказаний.
2. Получить информированное добровольное согласие реципиента или его законного представителя на проведение гемотрансфузионной терапии по установленной форме.
3. Провести первичное определение групповой принадлежности крови больного по системе АВО.
КАТЕГОРИЧЕСКИ ЗАПРЕЩАЕТСЯ ИСПОЛЬЗОВАТЬ ДАННЫЕ О ГРУППОВОЙ ПРИНАДЛЕЖНОСТИ ПО СИСТЕМАМ АВО И РЕЗУС ИЗ ПАСПОРТА, ПРЕДШЕДСТВУЮЩЕЙ ИСТОРИИ БОЛЕЗНИ И ДРУГИХ ДОКУМЕНТОВ.
4. Внести в направление в клинико-диагностическую лабораторию (форма № 207/у), сведения о результате определения группы крови по системе АВО, серии диагностикумов, трансфузионный и акушерско-гинекологический анамнез. Подписать направление
5. Ознакомиться с заключением клинико-диагностической лаборатории. Перенести данные о групповой и резус-принадлежности больного на лицевую часть медицинской карты стационарного больного с указанием даты анализа и своей фамилии.
6. Оформить предтрансфузионный эпикриз.
7. Провести макроскопическую оценку лабораторного желатина и диагностикумов.
8. Провести макроскопическую оценку каждой дозы гемотрансфузионной среды.
9. Повторно непосредственно перед трансфузией определить группу крови реципиента по системе АВО
10. Определить группу крови по системе АВО с эритроцитсодержащей средой.
11. Проконтролировать соответствие паспортных данных.
12. Провести пробу на совместимость крови реципиента и крови донора (гемотрансфузионной среды) по системам АВО и резус.
13. Зафиксировать результат изосерологических исследований в протоколе операции переливания крови.
ПРОБЫ НА ИНДИВИДУАЛЬНУЮ СОВМЕСТИМОСТЬ ПО СИСТЕМЕ АВО И РЕЗУС НЕ ЗАМЕНЯЮТ ДРУГ ДРУГА.
ПРОВОДЯТСЯ ВО ВСЕХ СЛУЧАЯХ С ОБРАЗЦАМИ КРОВИ ИЗ КАЖДОГО КОНТЕЙНЕРА.
ОБЯЗАТЕЛЬНЫ, ДАЖЕ ЕСЛИ ЭРИТРОЦИТНАЯ МАССА ИЛИ ВЗВЕСЬ ПОДОБРАНЫ РЕЦИПИЕНТУ ИНДИВИДУАЛЬНО В СПЕЦИАЛИЗИРОВАННОЙ ЛАБОРАТОРИИ.
14. Провести биологическую пробу. Зафиксировать её результат в протоколе операции переливания крови.
15. Контролировать состояние реципиента, темп введения трансфузионной среды.
16. При изменении состояния больного в первую очередь исключить посттрансфузионное осложнение.
17. Оценить показатели артериального давления, пульса, результаты термометрии.
18. Зарегистрировать гемотрансфузию:
•в дневнике наблюдений медицинской карты стационарного больного;
•в журнале регистрации переливаний крови и её компонентов (форма № 009/у) ;
•заполнить протокол гемотрансфузии
19. Провести макрооценку первой порции мочи.
20. Назначить клинические анализы крови и мочи на следующие сутки после гемотрансфузии.
21. Провести оценку суточного диуреза, водного баланса, результатов анализов мочи и крови.
22. Наблюдать за больным с отражением результатов наблюдения в дневнике истории болезни. При изменении клинической симптоматики и лабораторных показателей до выписки больного из стационара в первую очередь исключить посттрансфузионное осложнение.
Осложнения
-Иммунные осложнения ( острый гемолиз, гипертермическая негемолитическая реакция, анафилактический шок, некардиогенный отек легких)
-Неиммунные осложнения (острый гемолиз, бактериальный шок, ОССН, отек легких)
-Непосредственные осложнения (аллоиммунизация антигенами эритроцитов, лейкоцитов, тромбоцитов или плазменными белками, гемолиз, реакция >, посттрансфузионная пурпура)
-Иммунные ( гемолиз, Реакция «трансплантат против хозяина», Посттрансфузионная пурпура, Аллоиммунизация антигенами эритроцитов, лейкоцитов, тромбоцитов или плазменными белками
А. Г. Румянцев, В. А. Аграненко. Клиническая трансфузиология-М.: ГЭОТАР МЕДИЦИНА, 1997.
Е. Б. Жибурт. Трансфузиология-С.: ПИТЕР, 2002.
Рагимов А. А. Трансфузиология. Национальное руководство-М.: ГЭОТАР Медиа, 2012.
Алгоритмы исследования антигенов эритроцитов и антиэритроцитарных антител в сложнодиагностируемых случаях. Методические рекомендации N 99/181 (утв. Минздравом России 17. 05. 2000)
Приказ Минздрава России от 25. 11. 2002 N363 » Об утверждении Инструкции по применению компонентов крови»
Приказ Минздрава России от 02. 04. 2013 N183н » Об утверждении правил клинического использования донорской крови и (или) ее компонентов»
Что такое эксфузия крови
Обменное переливание крови выполняют через две вены (обычно на локтевом сгибе или любую доступную) больного: через одну вену кровь реципиента эксфузируется, а через другую параллельно вливается донорская кровь со скоростью 50—100 мл/мин. Число кровопусканий и темп эксфузии устанавливаются индивидуально для каждого конкретного больного, в зависимости от исходного состояния больного и уровня АД во время операции.
Процедуру ОПК нельзя рассматривать только как простое замещение «плохой» крови некоторым объемом «хорошей». При ОПК сочетаются как минимум два эффекта — заместительный и дезинтоксикационный. ОПК уменьшает степень интоксикации, способствует нормализации гемостаза, микроциркуляции, улучшает иммунологический статус реципиента.
При обменном переливании крови из кровотока удаляются крупномолекулярные соединения, такие как гемоглобин и миоглобин. Для достижения дезинтоксикационного эффекта, как правило, достаточно переливания 2—3 л донорской крови, т. е. замещения до 1/3 ОЦК. В ряде случаев вместо обменного переливания в последние годы используют адекватные методы селективного гемафереза.
Цельная консервированная аутокровь
В связи с постоянным уменьшением числа донорских кадров, а также с увеличением количества инфицированных доноров Службе крови все труднее удовлетворять в полной мере запросы клиник в компонентах и препарах донорской крови. В особенности это касается больных с редкими группами крови и изосенсибилизированных реципиентов.
Переливая собственную кровь больного (аутокровь), можно во многом разрешить проблему компенсации операционной кровопотери, исключить опасность гемотрансфузионных реакций и осложнений, перенос инфекционных заболеваний, таких как гепатит, сифилис, СПИД и др., сопутсвующих гемотрансфузиям компонентов донорской крови.
Аутогемотрансфузия — значительно более безопасный метод, чем переливание донорской крови или ее компонентов. Этот простой метод позволяет сократить объемы использования донорской крови, а при ряде операций и обходиться без них.
Аутокровь консервированная. Предоперационная заготовка крови — аутокрови больного (техническое исполнение) практически ничем не отличается от заготовки ее у донора крови. Основная особенность — забор крови у больного необходимо осуществлять с учетом заболеваний пациента, возможных осложнений, которые может справоцировать процедура.
В случае предоперационной заготовки крови у больного однократно либо в течение нескольких недель до хирургического вмешательства эксфузируют кровь, разделяют на компоненты, хранят и затем используют во время операции или в ближайшем послеоперационном периоде.
Последняя кроводача берется не менее чем за 3—4 дня до оперативного вмешательства.
Если до операции достаточно времени (2—3 недели), то заготовку аугокомпонентов (или аутокрови) можно осуществлять «методом эксфузии-аутогемотрансфузии» или «ступенчатым методом». Забранная консервированная кровь или ее соответствующий компонент через 5—7 дней возвращается больному и забирается новая порция крови, превосходящая первую на одну дозу. Этот метод позволяет заготовить достаточный объем аутоплазмы, аутоэритроцитов, а в некоторых случаях (за 3—5 дней до операции) и аутотромбоконцентрат.
Аутокровь консервированная, фильтрованная. Если появляется необходимость трансфузии крови или аутоэритроцитной массы в сроки, превышающие 2—3 дня после заготовки, рекомендуется профильтровать кровь через лейкофильтры.
Метод аутотрансфузий целесообразно применять во всех случаях, когда показана трансфузия компонентов крови для возмещения кровопотери и отсутствуют противопоказания для эксфузии крови у данного больного.
Наиболее часто метод аутогемотрансфузии применяют:
• при отсутствии крови, эритроцитной массы массы необходимой групповой принадлежности или при наличии редкой группы крови у больного;
• при невозможности подбора совместимой гемотрансфузионной среды;
• при проведении хирургических операций с гемодилюцией;
• при наличии в анамнезе больного посттрансфузионных реакций и осложнений;
• при наличии у больного противопоказаний к трансфузиям гомологичной крови (нарушения функции печени, почек и др.).
Почему ВОЗ призвала перестать переливать плазму крови для лечения COVID-19
Иммунолог Крючков объяснил, почему не стоит переливать плазму крови для лечения COVID
Фото, видео: Depositphotos / sudok1; 5-tv.ru
Переливание плазмы крови переболевших COVID-19 стали использовать для лечения заболевания, но ВОЗ заявили о несостоятельности этого метода. Иммунолог Николай Крючков объяснил, почему это не работает.
Женевская штаб-квартира Всемирной организации здравоохранения сделала заявление, в котором призвала отказаться от переливании плазмы крови переболевших для лечения COVID-19 — согласно позиции организации, такой метод не улучшает выживание и не снижает потребность в искусственной вентиляции легких. А ведь на бумаге идея выглядит отличной — но, к сожалению, иногда то, что работает в теории, на практике оказывается несостоятельным.
Иммунолог Николай Крючков объяснил 5-tv.ru позицию ВОЗ — несмотря на то, что переливание плазмы действительно может помочь при некоторых других заболеваниях, для лечения коронавируса этот метод использовать вряд ли стоит.
«Логика применения такого метода лечения — она проста: человек переболевает коронавирусной инфекцией, у него вырабатываются антитела. Соответственно, такой человек после заболевания, уже выздоровев, естественно, идет сдает кровь, выделяется фракция плазмы, содержащая эти антитела, и, соответственно, тем людям, которым бы не помешали сейчас эти антитела, вводим этот препарат — эту плазму с антителами, и эти антитела сразу же начинают активно работать против вируса», — объяснил иммунолог.
Но это в теории — на практике такой метод лечения очень сложно стандартизировать, он достаточно дорог, а эффективность его минимальна. С учетом всех затрат — переливание плазмы просто не имеет смысла.
На самом деле, в медицине есть много теоретических методов, которые должны бы прекрасно работать — но по тем или иным причинам не работают. Например, иногда препарат, который прекрасно борется с вирусом или бактерией в пробирке, в организме человека или животного это делать перестает — потому что организм подавляет его действие или его невозможно доставить к нужному органу в необходимой концентрации. При этом, даже для разных заболеваний один и тот же метод вполне может показывать разную эффективность — переливание плазмы крови практикуется для лечения бешенства и столбняка.
«При некоторых заболеваниях в остром периоде это работает — равно как работают антитела, например, антирабические, антистолбнячные — это прекрасно работающие методы, давние, старые и так далее», — уточнил эксперт.
Но к коронавирусу, повторил эксперт, это не относится — тратить ресурсы на переливание плазмы просто нерационально.
Именно поэтому важно проводить исследования — клинические на животных и людях, эпидемиологические, пост-маркетинговые, пост-регистрационные и прочие. Все эти исследования помогут понять, как препарат работает у разных людей, есть ли у него побочные эффекты и как безопаснее его использовать.
«Те исследования, которые на сегодняшний день с плазмой переболевших — реконвалесцентов так называемых провели не показали сколько-нибудь значимую эффективность клиническую. Да, может быть, у определенных подгрупп людей, в определенных условиях это может работать — мы этого не исключаем. Просто как рутинный, массовый метод, для большинства людей, он абсолютно не подходит. Это было понятно уже давно — никакой тут особой новости нет. Просто сейчас в связи с тем, что где-то такая практика — и в России, кстати, тоже — распространена, ВОЗ просто разъяснила свою точку зрения», — подытожил Крючков.