Аденовирусная инфекция
Аденовирусная инфекция – острый вирусный инфекционный процесс, сопровождающийся поражением дыхательных путей, глаз, лимфоидной ткани, пищеварительного тракта. Признаками аденовирусной инфекции служат умеренная интоксикация, лихорадка, ринорея, осиплость голоса, кашель, гиперемия конъюнктивы, слизистое отделяемое из глаз, нарушение функции кишечника. Кроме клинических проявлений, при постановке диагноза применяются серологические и вирусологические методы исследования. Терапия аденовирусной инфекции проводится противовирусными препаратами (внутрь и местно), иммуномодуляторами и иммуностимуляторами, симптоматическими средствами.
МКБ-10
Общие сведения
Аденовирусная инфекция – заболевание из группы ОРВИ, вызываемое аденовирусом и характеризующееся развитием ринофарингита, ларинготрахеобронхита, конъюнктивита, лимфаденопатии, диспепсического синдрома. В общей структуре острых респираторных заболеваний аденовирусная инфекция составляет около 20%.
Наибольшую восприимчивость к аденовирусам демонстрируют дети от 6 месяцев до 3-х лет. Считается, что в дошкольном возрасте практически все дети переносят один или несколько эпизодов аденовирусной инфекции. Спорадические случаи аденовирусной инфекции регистрируются круглогодично; в холодное время года заболеваемость носит характер эпидемических вспышек. Пристальное внимание к аденовирусной инфекции приковано со стороны инфекционных болезней, педиатрии, отоларингологии, офтальмологии.
Причины
В настоящее время известно более 30 сероваров вирусов семейства Adenoviridae, вызывающих заболевание человека. Наиболее частой причиной вспышек аденовирусной инфекции у взрослых выступают 3, 4, 7, 14 и 21 серотипы. Серовары типов 1, 2, 5, 6 обычно поражают детей-дошкольников. Возбудителями фарингоконъюнктивальной лихорадки и аденовирусного конъюнктивита в большинстве случаев служат серотипы 3, 4, 7.
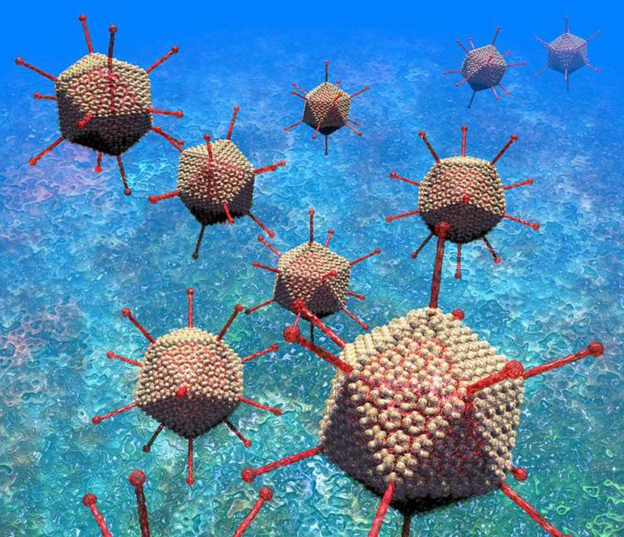
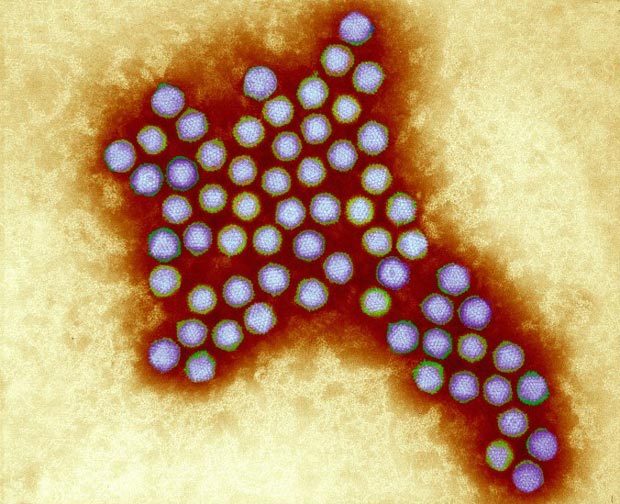
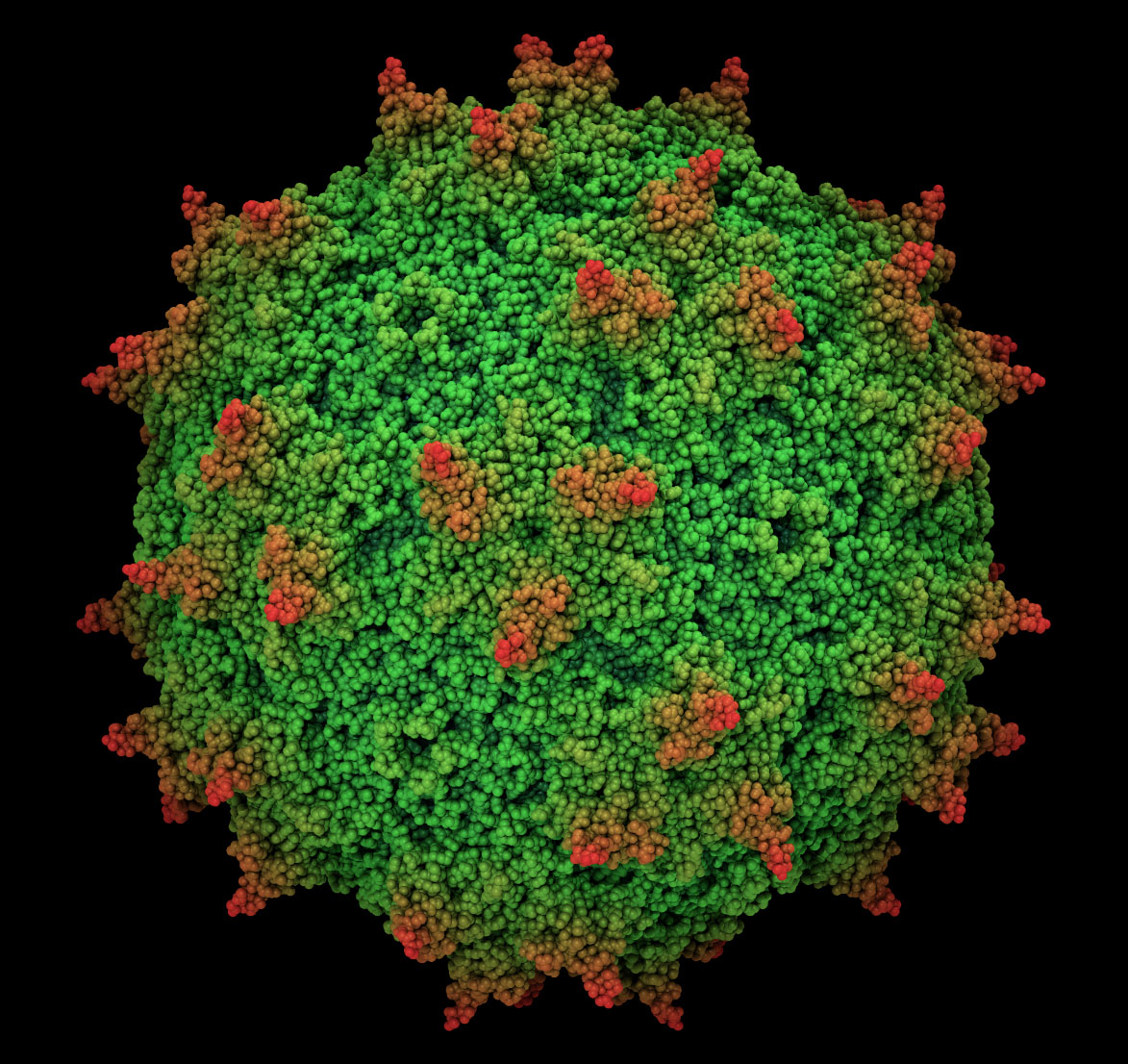
Вирионы возбудителя содержат двухцепочечную ДНК, имеют диаметр 70-90 нм и три антигена (группоспецифический А-антиген; определяющий токсические свойства аденовируса В-антиген и типоспецифический С-антиген). Аденовирусы относительно устойчивы во внешней среде: при обычных условиях сохраняются в течение 2-х недель, хорошо переносят низкие температуры и высушивание. Вместе с тем, возбудитель аденовирусной инфекции инактивируется при воздействии ультрафиолетовых лучей и хлорсодержащих дезинфектантов.
Источником аденовирусной инфекции также могут являться вирусоносители, пациенты с бессимптомными и стертыми формами болезни. Иммунитет после перенесенной инфекции типоспецифический, поэтому возможны повторные заболевания, вызванные другим серотипом вируса. Встречается внутрибольничное инфицирование, в т. ч. при проведении парентеральных лечебных процедур.
Патогенез
Аденовирус может проникать в организм через слизистые верхних дыхательных путей, кишечника или конъюнктиву. Репродукция вируса протекает в эпителиальных клетках, регионарных лимфатических узлах и лимфоидных образованиях кишечника, что по времени совпадает с инкубационным периодом аденовирусной инфекции. После гибели пораженных клеток вирусные частицы высвобождаются и проникают в кровь, вызывая вирусемию.
Изменения развиваются в оболочке носа, миндалин, задней стенки глотки, конъюнктивы; воспаление сопровождается выраженным экссудативным компонентом, что обусловливает появление серозного отделяемого из полости носа и конъюнктивы. Вирусемия может приводить к вовлечению в патологический процесс бронхов, пищеварительного тракта, почек, печени, селезенки.
Симптомы аденовирусной инфекции
Основными клиническими синдромами, форму которых может принимать данная инфекция, служат катар дыхательных путей (ринофарингит, тонзиллофарингит, ларинготрахеобронхит), фарингоконъюнктивальная лихорадка, острый конъюнктивит и кератоконъюнктивит, диарейный синдром. Течение аденовирусной инфекции может быть легким, среднетяжелым и тяжелым; неосложненным и осложненным.
Инкубационный период при аденовирусной инфекции длится 2-12 дней (чаще 5-7 дней), вслед за чем следует манифестный период с последовательным появлением симптомов. Ранними признаками служат повышение температуры тела до 38-39 °С и умеренно выраженные симптомы интоксикации (вялость, ухудшение аппетита, мышечные и суставные боли).
Поражение дыхательных путей
Катаральные изменения в верхних дыхательных путях возникают одновременно с лихорадкой. Появляются серозные выделения из носа, которые затем становятся слизисто-гнойными; затрудняется носовое дыхание. Отмечается умеренная гиперемия и отечность слизистой оболочки задней стенки глотки, точечный белесоватый налет на миндалинах. При аденовирусной инфекции возникает реакция со стороны подчелюстных и шейных лимфоузлов. В случае развития ларинготрахеобронхита появляется осиплость голоса, сухой лающий кашель, возможна одышка, развитие ларингоспазма.
Поражение конъюнктивы
Поражение конъюнктивы при аденовирусной инфекции может протекать по типу катарального, фолликулярного или пленчатого конъюнктивита. Обычно в патологический процесс глаза вовлекаются поочередно. Беспокоит резь, жжение, слезотечение, ощущение присутствия инородного тела в глазу. При осмотре выявляется умеренное покраснение и отек кожи век, гиперемия и зернистость конъюнктивы, инъецированность склер, иногда – наличие плотной серовато-белой пленки на конъюнктиве. На второй неделе заболевания к конъюнктивиту могут присоединяться признаки кератита.
Кишечная форма
Если аденовирусная инфекция протекает в кишечной форме, возникают приступообразные боли в околопупочной и правой подвздошной области, лихорадка, диарея, рвота, мезентериальный лимфаденит. При выраженном болевом синдроме клиника напоминает острый аппендицит. Лихорадка при аденовирусной инфекции длится 1-2 недели и может носить волнообразный характер. Признаки ринита и конъюнктивита стихают через 7-14 дней, катара верхних дыхательных путей – через 14-21 день.
Осложнения
При тяжелой форме заболевания поражаются паренхиматозные органы; может возникать менингоэнцефалит. У детей первого года жизни нередко развивается аденовирусная пневмония и выраженная дыхательная недостаточность. Осложненное течение аденовирусной инфекции обычно связано с наслоением вторичной инфекции; наиболее частыми осложнениями заболевания служат синусит, средний отит, бактериальная пневмония.
Диагностика
Распознавание аденовирусной инфекции обычно производится на основании клинических данных: лихорадки, катара дыхательных путей, конъюнктивита, полиаденита, последовательного развития симптомов. Методами экспресс-диагностики аденовирусной инфекции служит реакция иммунофлюоресценции и иммунная электронная микроскопия. Ретроспективное подтверждение этиологического диагноза проводится методами ИФА, РТГА, РСК. Вирусологическая диагностика предполагает выделение аденовируса из носоглоточных смывов, соскоба с конъюнктивы и фекалий больного, однако ввиду сложности и длительности редко используется в клинической практике.
Дифференциальная диагностика
Дифференциальную диагностику различных клинических форм аденовирусной инфекции проводят с гриппом, другими ОРВИ, дифтерией глотки и глаз, инфекционным мононуклеозом, микоплазменной инфекцией, иерсиниозом. С этой целью, а также для назначения местного этиотропного лечения пациенты нуждаются в консультации офтальмолога и отоларинголога.
Лечение аденовирусной инфекции
Общая этиотропная терапия проводится препаратами антивирусного действия (умифеновир, рибавирин, препарат из антител к гамма-интерферону человека). Местная терапия аденовирусной инфекции включает: инстилляции глазных капель (раствора дезоксирибонуклеазы или сульфацила натрия), аппликации ацикловира в виде глазной мази за веко, интраназальное применение оксалиновой мази, эндоназальную и эндофарингеальную инстилляцию интерферона. Проводится симптоматическая и посиндромная терапия: ингаляции, прием жаропонижающих, противокашлевых и отхаркивающих препаратов, витаминов. При аденовирусной инфекции, отягощенной бактериальными осложнениями, назначаются антибиотики.
Прогноз и профилактика
Неосложненные формы аденовирусной инфекции оканчиваются благоприятно. Смертельные исходы могут отмечаться у детей раннего возраста в связи с возникновением тяжелых бактериальных осложнений. Профилактика аналогична предупреждению других ОРВИ. В периоды эпидемических вспышек показана изоляция больных; проведение текущей дезинфекции, проветривания и УФО помещений; назначение интерферона лицам, подвергшимся риску заражения. Специфическая вакцинация против аденовирусной инфекции пока не разработана.
Что такое аденовирус
Что если вам скажут, будто одна и та же группа вирусов может вызывать все на свете заболевания, – от банальной простуды до инфекций мочевого пузыря? Несколько странно, не так ли? И определенно это не та новость, которую хотелось бы услышать в преддверии гриппозно-простудного сезона (за что просим прощения).
Однако это соответствует действительности: представители группы патогенов, называемых аденовирусами, в некоторых случаях могут быть смертельно опасны. Корреспондент сайта « Health » обратился к эксперту в области инфекционных болезней за разъяснениями вопросов о том, что в сущности представляют собой аденовирусы, какие симптомы они могут вызывать и как можно вылечиться.
И вот что необходимо знать.
Согласно информационным материалам Центров по контролю и профилактике заболеваний (CDC), аденовирусами называют группу обычных вирусов, способных вызывать широкий спектр заболеваний, включая обычную простуду, желудочный грипп, ангину, бронхит, диарею, эпидемический конъюнктивит, лихорадку, – словом, все заболевания, протекающие с умеренно выраженной симптоматикой и, как правило, поддающиеся лечению в домашних условиях. Однако некоторые штаммы аденовирусов приводят к более серьезным проблемам, например, к инфекциям мочевых путей или воспалению легких.
Поскольку аденовирусы чрезвычайно разнообразны, вызываемая ими симптоматика также варьирует очень широко. В основном, развиваются респираторные заболевания и конъюнктивиты. Это означает, что именно аденовирусы «виновны» в большинстве регистрируемых случаев кашля, хрипов и зудящих красных глаз.
Отличие аденовирусов от прочих вирусов (например, от вируса гриппа) заключается в том, что первые не обязательно предпочитают холодное время года. «Аденовирусные инфекции наблюдаются круглогодично, – говорит Фрэнк Эспер, доктор медицины, педиатр, специализирующийся на инфекционных болезнях в Кливлендской клинике. – Лето нравится аденовирусу не меньше, чем зима».
Наиболее типичный путь распространения аденовирусной инфекции – через прямой контакт, например, прикосновение, кашель, чихание, рукопожатие, или же через прикосновение к зараженной поверхности с последующим касанием собственного рта, носа, глаз. Реже аденовирусы распространяются через инфицированный кал (при смене подгузника больному ребенку, например) или через воду (в общественных бассейнах и т.п.).
«Могут ли аденовирусы представлять опасность для жизни? – В некоторых случаях, да. Восемнадцатилетняя студентка колледжа при Университете Мэриленда умерла от аденовирусной инфекции во время эпидемической вспышки 2018 года, когда заболело 40 студентов и 15 из них пришлось госпитализировать».
«Как правило, – продолжает доктор Эспер, – под угрозой оказываются лица с ослабленной иммунной системой. Если у вас практически нет иммунитета, тогда аденовирус становится действительно серьезной проблемой».
Именно это случилось с погибшей девушкой, которая, как сообщает « Washington Post «, страдала и боролась с болезнью Крона, – разновидностью хронического кишечного воспаления, – постоянно принимая поддерживающие препараты в связи с данным заболеванием (определенные группы медикаментов, – используемые, в частности, для контроля болезни Крона и лечения рака, – в индивидуальных случаях могут стать причиной иммунодефицитного состояния).
Впрочем, аденовирусы могут становиться опасными даже для лиц с нормально функционирующей иммунной системой. Случится это или нет, зависит от конкретных осложнений аденовирусной инфекции. «Скажем, вирусный миокардит, т.е. воспаление сердечной мышцы, – объясняет доктор Эспер, – может развиться и у иммунокомпетентного человека, и это осложнение может стать фатальным».
«Существует ли лечение от аденовирусов? – Нет, специфическая терапия аденовирусных инфекций пока не разработана, и применяемые в этих случаях безрецептурные лекарства служат лишь для облегчения симптоматики (т.е. для устранения болей или лихорадки, снижения температуры и т.д.)».
В связи с этим приходится повторять, что лучшим средством против аденовирусных инфекций является их профилактика. Это означает частую и тщательную гигиену рук, исключение случаев употребления пищи или напитков из общей с контагиозным человеком посуды, и избегание любых людей, кто открыто кашляет или чихает (возможно, стоило бы им напомнить: хотя бы используйте локоть, пожалуйста).
В экстремальных случаях применяется препарат под названием цидофовир, но, опять же, его назначают крайне редко. По словам Ф.Эспера, «препарат очень токсичен, он сам по себе может стать причиной тяжелого состояния, например, почечной недостаточности. Обычно мы воздерживаемся от этиотропного лечения аденовирусов и прибегаем к выжидательной тактике. Больной должен быть в очень тяжелом состоянии, чтобы пришлось назначать эти медикаменты».
В общем и целом, для здорового человека аденовирусы не должны составлять особую проблему, – тем не менее, будет разумным соблюдать все меры предосторожности и, если вы все же заболели, защитить близких людей с помощью санитарно-гигиенического режима.
Что такое человеческий аденовирус
Аденовирусная инфекция — группа острых вирусных заболеваний, проявляющихся поражением слизистых оболочек дыхательных путей, глаз, кишечника и лимфоидной ткани преимущественно у детей и лиц молодого возраста.
Дети чаще болеют аденовирусной инфекцией, чем взрослые. Большинство детей переболеют, по крайней мере, одним типом аденовирусной инфекции к тому времени, когда им исполнится 10 лет.
Возбудители инфекции — аденовирусы.
Источник инфекции — больной человек или вирусоноситель.
Инфекция передается воздушно-капельным, пищевым, контактно-бытовым путями. Возможно внутриутробное инфицирование плода.
Вирусы распространены в местах с организованными группами детей (детские сады, школы и летние лагеря).
Инфекция распространяется при кашле или чихании. Капли, содержащие вирус, разлетаются по воздуху и приземляются на поверхности.
Аденовирусы чрезвычайно устойчивы в окружающей среде. При комнатной температуре сохраняют жизнеспособность до 2 недель, на предметах обихода в высушенном виде – более 8 дней. К низким температурам высокоустойчивы, однако, при 60 0 С инактивируются в течение 2 минут.
Аденовирусная инфекция быстро распространяется среди детей, дети часто касаются руками лица, берут пальцы в рот, игрушки.
Аденовирусная инфекция обычно протекает без осложнений, симптомы проходят через несколько дней. Но клиническая картина может быть более серьезной у людей со слабой иммунной системой, особенно у детей.
Аденовирусная инфекция характеризуется многообразием клинических проявлений.
лихорадка длительностью от 2-3 дней до 2 недель
Ученый из МФТИ раскрыл процесс создания вакцины от коронавируса
Как создают вакцину от коронавируса?
Об эксперте: Павел Волчков — кандидат биологических наук, вирусолог, генетик, заведующий Лабораторией геномной инженерии Московского физико-технического института (МФТИ).
Существует много разных подходов к созданию вакцины от COVID-19. Она может быть вирусной, инактивированной, векторной, на основе нуклеиновых кислот. Какая из них окажется самой эффективной — пока никто точно не знает. Если вы разработчик, то можете выбрать любую и принять участие в большой мировой гонке по созданию долгожданной прививки. А можете, как ученые из МФТИ, сознательно отказаться от возможных бенефитов и неспешно заняться разработкой экспериментальной вакцины нового типа.
Одни из самых популярных на сегодняшний день — это рекомбинантные или векторные вакцины. Они изготавливаются на основе вирусов-носителей или вирусных векторов. Как это работает? Вы берете какие-то вирусные частицы, «вычищаете» из них все патогенные составляющие и на их место вставляете нужные вам элементы — генетический материал вируса, против которого изготавливается вакцина. По такому принципу была создана прививка от вирусного гепатита B или ротавирусной инфекции. И по такому же принципу сегодня многие разработчики создают вакцину от COVID-19. В частности, в России векторную вакцину от коронавируса разработали в НИИ эпидемиологии и микробиологии имени Н.Ф. Гамалеи.
Павел Волчков:
«Чем хорош вирусный вектор? Он способен инфицировать клетки только один раз и не может размножаться в организме человека дальше. Такая особенность делает рекомбинантные вакцины довольно безопасными. При этом в качестве вирусного вектора можно использовать буквально любой вирус из библиотеки человеческих патогенов. Выбор зависит от того, для какого заболевания вы изготавливаете вакцину. Потому что одни вирусы лучше заражают мышцы, другие — легкие, третьи — центральную нервную систему. Например, та же вакцина Центра Гамалеи выполнена на аденовирусном векторе».
Аденовирусы — ДНК-вирусы. Относятся к группе острых респираторных вирусных инфекций (ОРВИ) и характеризуются поражением слизистых оболочек верхних дыхательных путей, конъюнктив, лимфоидной ткани. Большинство аденовирусных инфекций представляют собой легкую форму инфицирования. Существует семь видов аденовирусов человека (от А до G) и 57 серотипов. Подразделение на серотипы связано с различными способами заражения.
В качестве векторов для вакцин, аденовирусы применяются довольно давно. Эти вирусы хорошо изучены. Согласно данным сайта ClinicalTrials.gov, клинические испытания на людях успешно прошли или проходят более сотни различных вакцин на основе аденовирусных векторов.
Среди главных преимуществ этих вирусов — их естественный механизм взаимодействия с клетками человека. Они способны обеспечивать довольно длительную экспрессию антигена, а это успешно активирует врожденный иммунный ответ.
Антигены — это любые вещества, содержащиеся в микроорганизмах и других клетках (или выделяемые ими), которые несут в себе признаки генетически чужеродной информации, и которые потенциально могут быть распознаны иммунной системой организма.
Павел Волчков:
«При всех плюсах, у аденовирусов есть и ряд минусов. Первое — они обладают провоспалительным эффектом. То есть могут чрезмерно драйвить иммунную систему. Проще говоря — вызывать сильный иммунный ответ. Это один из возможных побочных эффектов вообще всех аденовирусных вакцин. Но есть еще один нюанс. Большинство аденовирусов — это естественные патогены человека. Многие из нас сталкивались в течение жизни с аденовирусными инфекциями. А что это значит? Что в крови у таких людей уже есть нейтрализирующие антитела к этому вирусу. Они могут связываться с компонентами вакцины и блокировать ее действие. Поэтому для некоторых из нас такая вакцина будет совершенно неэффективна».
Вакцина МФТИ: в чем инновация?
Поскольку у аденовирусных векторов есть существенные недостатки, ученые из МФТИ выбрали другие вирусы в качестве вектора — аденоассоциированные вирусы. Что любопытно, раньше никто в мире не использовал их в таком качестве.
Аденоассоциированные вирусы — мелкие ДНК-содержащие вирусы. Размер частиц 22-24 нм. Размножаются только в присутствии аденовирусов. Способны инфицировать клетки человека и некоторых других приматов. Аденоассоциированный вирус, по-видимому, не вызывает заболеваний у человека, поэтому провоцирует слабый иммунный ответ.
Один из плюсов аденоассоциированных вирусов — они давно и успешно используются в генной терапии. Сегодня зарегистрировано несколько лекарственных средств на их основе. Одно из самых нашумевших — Luxturna. Это первое генное лекарство, созданное для лечения наследственной слепоты, вызванной мутацией гена RPE65.
По аденоассоциированным вирусам также накоплена внушительная клиническая база. На сайте ClinicalTrials.gov можно увидеть, в каком количестве клинических экспериментов аденоассоциированные вирусы уже приняли участие. Это несколько сотен доклинических исследований и порядка 50 клинических экспериментов. Носитель хорошо охарактеризован и, что еще важнее, показана его безопасность. Все это делает аденоассоциированные вирусы весьма привлекательным кандидатом для создания вирусных векторов не только для генной терапии, но и для вакцин, уверены в Лаборатории геномной инженерии МФТИ.
Еще одной веской причиной создать вакцину на аденоассоциированном векторе стало то, что ученые из МФТИ уже давно придумывают, модифицируют и создают аденоассоциированные вирусы. На сегодняшний день в библиотеке МФТИ их более миллиона. Все они имеют разную специфичность и разные свойства. Что важно, к этим вирусам у человека не может быть иммунного ответа, который бы снизил эффективность вакцины. Поскольку все они созданы искусственно.
Павел Волчков:
«Мы с самого начала понимали, что сможем не только разработать вакцину, но и масштабировать ее производство. То есть произвести столько доз, сколько потребуется или столько, сколько захотим. В мире существует огромное количество аутсорсинговых компаний, которые по GMP сделают вам любое количество доз препарата.
Good Manufacturing Practice (GMP) — правила, которые устанавливают требования к организации производства и контроля качества лекарственных средств для медицинского и ветеринарного применения.
Поэтому с самого начала у нас было четкое понимание, что проблем с производством не будет. Как и проблем с лицензией на вирусный носитель. Это качественно отличает нашу лабораторию от многих других разработчиков вакцин в Российской Федерации. В современном мире все технологии так или иначе кому-то принадлежат, и аденовирусы, и прочие системы векторной доставки, аденоассоциированные в том числе. Живя по правилам свободного рынка, вы не можете просто взять и сделать вакцину на основе любого понравившегося вектора. Вы должны иметь разрешение от компании, которая обладает правами на технологию, либо владеет непосредственно интеллектуальной собственностью в области этого вектора. И тут у нас все хорошо — мы как раз владеем патентом по разработке аденоассоциированных вирусов. Нам не нужно просить ни у кого лицензию на производство данной вакцины, поскольку мы используем собственные же аденоассоциированные вирусы».
Вакцина МФТИ будет эффективна против разных штаммов SARS-CoV-2
Изначально ученые хотели разработать вакцину, которая бы вырабатывала иммунитет практически ко всем поверхностным белкам вируса SARS-CoV-2. А не только к S-белку, как это делают большинство разработчиков вакцин по всему миру (включая НИИ им. Гамалеи). Но в итоге разработчики остановились на конечном числе компонентов. Ими стали S-белок, Е-белок и М-белок.
Павел Волчков:
«По сути мы воплощаем идею совершенно нового типа вакцин — так называемых поливалентных вакцин. Это когда в одном препарате сразу несколько вирусных компонентов. Такой подход кажется нам крайне эффективным применительно к SARS-CoV-2. Ведь на самом деле это не один какой-то конкретный вирус, который распространился по планете. Если мы начнем секвенировать разные изоляты коронавируса, то они все будут отличаться друг от друга. Либо на одну аминокислотную замену, либо на несколько. Поливалентная вакцина как раз направлена на то, чтобы вырабатывать иммунный ответ не к одному поверхностному белку вируса, а сразу к нескольким. В том числе к консервативным поверхностным белкам, которые меньше остальных подвержены мутациям. Так наша вакцина поможет сформировать иммунитет к разным штаммам вируса SARS-CoV-2».
Если текущая разработка покажет свою эффективность и безопасность, ученые планируют пойти еще дальше и разработать вакцину, которая будет содержать не только различные компоненты SARS-CoV-2, но еще и вируса гриппа или других сезонных респираторных вирусов. То есть объединить в одной вакцине генетический материал от самых разных сезонных патогенов. По мнению ученых из МФТИ, такие ассемблированные, поливалентные вакцины могли бы готовить людей каждый сезон к новому остро-респираторному вирусному нашествию.
Что касается текущей разработки (вакцины от COVID-19), то на данный момент ее разработка завершена. Впереди подготовка к доклиническим испытаниям на китайских хомяках и приматах. Если они пройдут успешно, вакцину ожидают испытаниях на людях. Но торопиться и участвовать в текущей «вакцинной» гонке разработчики из МФТИ не собираются.
Павел Волчков:
«Дело в том, что в нашей вакцине слишком много новых компонентов. Несмотря на то, что аденоассоциированные вирусы используются в генной терапии, для создания вакцин их еще никто не применял. Спешка или сокращение сроков проведения доклинических и клинических исследований может обернуться ошибкой и поставить крест на такой многообещающей и перспективной платформе. Но это не значит, что сейчас мы создаем вакцину, что называется «в стол». Во-первых, когда она будет испытана, мы сможем ее продавать другим нуждающимся странам. Во-вторых, наша основная цель — получить опыт по созданию быстрых вакцин, который мы планируем применять в будущем. Как научная лаборатория мы можем проводить такие эксперименты — создавать платформу для вакцин совершенно нового типа. И если у нас все получится, то в следующий раз, когда в мире появится новость о новой вспышке заболевания, мы будем готовы пройти весь путь создания препарата гораздо быстрее, чем мы проходим его сейчас».
Массовая вакцинация от COVID-19 может не понадобиться?
Павел Волчков уверен, что сама по себе гонка по созданию вакцин от короновируса уже не имеет смысла. Он уверен, что к тому моменту, когда российские вакцины будут испытаны и наработаны для массовой вакцинации населения, потребность в них может отпасть. Ученый считает, что уже к осени мы все, так или иначе, переболеем COVID-19 и получим естественный иммунитет.
У этой оптимистичной гипотезы есть основания. Не так давно шведские ученые провели исследование и померяли иммунитет в шведской популяции. Измерялся и гуморальный иммунитет (то есть антитела в крови), и клеточный иммунитет. А именно Т-лимфоциты — так называемые клетки иммунной памяти, которые при повторной встрече с инфекцией «просыпаются» и активизируют иммунный ответ.
Исследование показало, что лишь у небольшой части шведов в крови присутствовали антитела, но примерно треть граждан имела ту самую клеточную память. Это говорит о том, что существенная часть популяции шведов в той или иной форме переболела COVID-19 или имела непродолжительный контакт с вирусом. В последнем случае большой продукции антител не происходит, но благодаря Т-лимфоцитам формируется иммунологическая память к COVID-19.
Павел Волчков:
«Согласно московской статистике, антитела к коронавирусу были определены в крови примерно у 20% жителей столицы. А это около 2 млн человек. Следуя логике шведского исследования, которому у меня лично нет причин не доверять, то скорее всего еще у 20% (а может и у 40% или даже 50-60%) людей уже есть клеточный иммунитет к COVID-19. Эти люди контактировали с небольшими дозами вируса, их иммунная система его детектировала и сформировала клетки памяти. Фактически, половина населения столицы естественным образом получила живую вакцину от COVID-19. Что примечательно, иммунитет, полученный в результате натуральной инфекции, оказывается более стойким, чем от гипотетической вакцины. Потому что в таком случае, иммунная система знакомится с полноценным вирусом (со всеми поверхностными белками), а не с его редуцированной версией, как это происходит при вакцинации. Я думаю, что такая ситуация с клеточным иммунитетом к COVID-19 обстоит не только в Москве, а во многих российских городах. То есть огромное количестве людей по всей России на самом деле уже имеет иммунитет к коронавирусной инфекции».